工艺流程题的解法探究
工艺流程题的解法探究
山东王洪印工艺流程题以“先进生产工艺”或“实验操作流程”为情境,以元素化合物知识为框架,要求学生能够将文字表述、框图描述中的新信息进行吸收、整合、分析,准确地提取出实质性的内容,要求学生会从化学视角分析和解决实际问题。由于流程题为考查化学核心知识提供了广阔的情景空间,能有效地考查学生的阅读能力、资料的收集处理能力和迁移推理能力,因此近几年工艺流程题逐渐成为中考化学的热点。
一、解题策略
一道完整的工艺流程题包括题头、流程图和问题三部分。题头部分一般是简单介绍该工艺生产的原材料或实验背景、资料信息等,流程图部分主要用框图形式将原料到产品的主要生产工艺流程或实验操作流程及其主要现象表示出来,问题部分主要是根据生产或实验过程中涉及的化学知识设计成系列问题,从而构成一道完整的化学试题。此类试题主要包括物质制取、物质含量测定、物质回收、物质分离和提纯以及物质成分探究的流程问题等类型。不管哪种类型的流程题,一般都是从以下三个方面进行分析和思考:
第一,通读试题,提取信息。通过阅读试题明确其中蕴含的相关信息,把它们提取出来,提取的信息主要包括物质反应的化学方程式、物质的稳定性、物质的溶解性、实验操作步骤、实验过程中需注意的问题等。
第二,分析流程,弄清作用。首先对比分析工艺生产流程示意图或实验操作流程图中的第一种物质(或第一个方框中所提供的信息)与最后一种物质(或最后一个方框中所提供的信息),从对比分析中找出它们之间的相互关系,明确:生产或实验流程中原料(药品)转化为产品(生成物即目标物质)的过程中依次进行了什么反应;每一步除目标物质外还产生了什么杂质或副产物;杂质是否要除去,采用什么操作方法除去等。
第三,看清问题,准确解答。这一步很关键,历年中考评卷分析都反应学生的简述能力比较差,特别是化学用语的表述存在很大的偏差。所以答题时要看清问题,不能答非所问,要注意语言表达的科学性,如物质的表示是用化学式还是用名称,书写出来的化学方程式是否进行了配平,让填写的是实验操作名称还是具体操作步骤等。
二、典例分析
1.生产工艺的流程问题
例1(2014·泰安)海洋是人类宝贵的自然资源,海水“制碱”体现了化学科学在改造物质中的智慧。下图是某厂生产纯碱的工艺流程图:
请完成下列问题。
(1)该厂最终产品有(填物质名称)。
(2)流程Ⅰ中为了除去杂质,加入了过量BaCl2溶液、NaOH溶液和Na2CO3溶液,下列说法正确的是(填字母)。
A.加入3种物质的顺序不能调整
B.加入3种溶液将粗盐水中的SO2-4、Mg2+、Ca2+转化为沉淀
C.按流程Ⅰ所加溶液的顺序除杂,过滤后得4种沉淀
(3)在流程Ⅱ中,如果加入氨气不是为了生产氯化铵,那么氨气在制碱过程中的作用是。
(4)写出流程Ⅲ中发生反应的化学方程式:。
解析:(1)除去氯化钙、氯化镁、硫酸钠后,再进行氨化、碳酸化,生成碳酸氢钠和氯化铵,由于相同条件下碳酸氢钠的溶解度小于氯化铵的溶解度,因此碳酸氢钠析出,加热碳酸氢钠可以得到碳酸钠,通过降温结晶可以得到氯化铵,因此该厂最终产品有碳酸钠和氯化铵。(2)加入3种溶液的顺序可以调整,如先加入过量的氢氧化钠溶液除去氯化镁,再加入过量的氯化钡溶液除去硫酸钠,最后加入过量的碳酸钠溶液除去氯化钙和过量的氯化钡,选项A说法不正确;加入3种溶液能够将粗盐水中的SO2-4、Mg2+、Ca2+转化为沉淀硫酸钡、氢氧化镁和碳酸钙,选项B说法正确;按流程Ⅰ所加溶液的顺序除杂,过滤后得到4种沉淀,它们是硫酸钡、氢氧化镁、碳酸钙和碳酸钡,选项C说法正确。(3)在流程Ⅱ中,如果加入氨气不是为了生产氯化铵,则氨气在制碱过程中的作用是使溶液显碱性,有利于吸收二氧化碳。(4)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式,碳酸氢钠受热分解的化学方程式为2NaHCO3△Na2CO3+H2O+CO2↑。
答案:(1)碳酸钠和氯化铵(2)BC(3)使溶液显碱性,有利于二氧化碳的吸收(4)2NaHCO3△Na2CO3+H2O+CO2↑
2.物质制取的流程问题
例2(2014·扬州)过氧化钙(CaO2)是一种对环境友好的多功能无机化合物,通常有两种制备方法。
已知:温度过高过氧化物会分解生成氧化物和氧气。
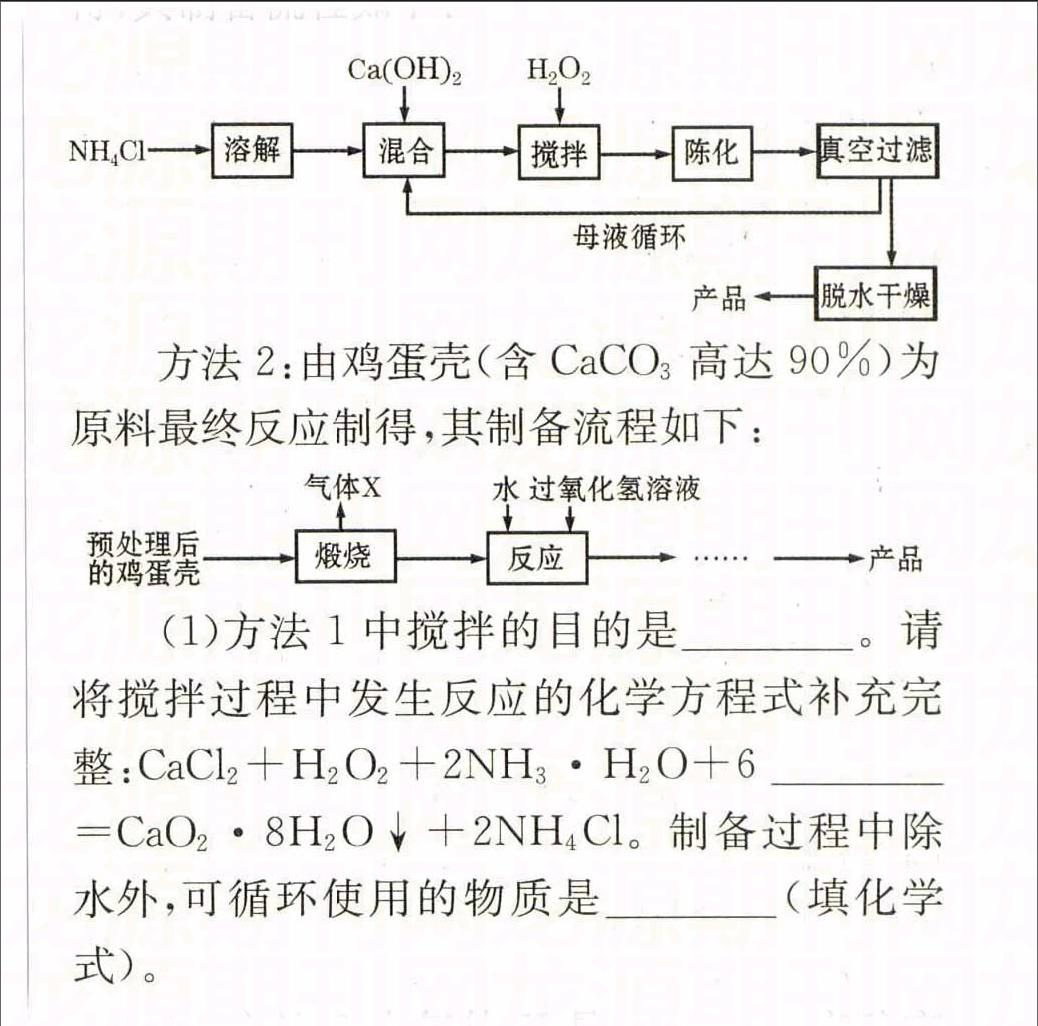
方法1:由Ca(OH)2为原料最终反应制得,其制备流程如下:
方法2:由鸡蛋壳(含CaCO3高达90%)为原料最终反应制得,其制备流程如下:
(1)方法1中搅拌的目的是。请将搅拌过程中发生反应的化学方程式补充完整:CaCl2+H2O2+2NH3·H2O+6=CaO2·8H2O↓+2NH4Cl。制备过程中除水外,可循环使用的物质是(填化学式)。
(2)方法2中气体X是,实验室常用溶液来吸收。煅烧后的反应是化合反应,也能生成CaO2·8H2O,反应的化学方程式为。该反应需控制温度在0~2℃,可将反应器放置在中,获得的CaO2产品中主要含有的固体杂质是(填化学式)。
(3)这两种制法均要求在低温下进行(除煅烧外),温度过高除了防止氨水挥发外,还能。
(4)“绿色化学”一般是指反应物的原子全部转化为期望的最终产物,则上述两种方法中生成CaO2·8H2O的反应符合“绿色化学”的是(填“方法1”或“方法2”)。
解析:(1)搅拌的目的是使反应充分,提高原料利用率;根据反应前后原子的个数不变,反应前缺少12个氢原子和6个氧原子,所以需要填写的化学式为H2O;制备过程中除水外,可循环使用的物质是NH4Cl。(2)CaCO3煅烧生成CaO和CO2,所以气体X为CO2,实验室中常用NaOH溶液吸收CO2;煅烧后反应的反应物是CaO、H2O2和H2O,生成物是CaO2·8H2O,根据化学方程式的书写步骤可写出化学方程式;冰水混合物的温度是0℃,反应需控制温度在0~2℃,所以可将反应器放置在冰水中;因为CaO会和H2O反应生成Ca(OH)2,所以获得的CaO2产品中主要含有的固体杂质是Ca(OH)2。(3)因为温度过高过氧化物会分解生成氧化物和氧气,所以制备过程中温度较低除了能防止氨水挥发外,还能防止CaO2分解。(4)方法2发生的是化合反应,反应物的原子全部转化为了期望的最终产物,所以符合“绿色化学”的理念。
答案:(1)使反应充分,提高原料利用率H2ONH4Cl(2)CO2NaOHCaO+H2O2+7H2O=CaO2·8H2O冰水Ca(OH)2(3)防止CaO2分解(4)方法2
3.物质回收的流程问题
例3(2014·呼和浩特)有一种工业废水,其中含有大量的硫酸亚铁、少量硫酸铜和污泥。某同学设计了一个既经济又合理的实验方案,制备硫酸亚铁晶体(FeSO4·7H2O)并回收铜。方案流程如下:
【查阅资料】FeSO4·7H2O受热易分解。
回答下列问题。
(1)步骤①中用到的玻璃仪器有烧杯、漏斗和。
(2)步骤②中需加入的物质是,目的是。
(3)步骤③中发生反应的化学方程式是。
(4)步骤④的操作是蒸发浓缩、、过滤。
解析:过滤分离不溶性固体与液体,将废水中的污泥与溶液用过滤法分离,得溶液1(硫酸铜和硫酸亚铁的混合液);加入过量的铁将硫酸铜中的铜全部置换出来,过滤得到铜和铁的混合物以及滤液硫酸亚铁;然后在固体混合物中加入适量稀硫酸,稀硫酸与铁反应生成硫酸亚铁溶液;最后将硫酸亚铁溶液蒸发结晶,即得硫酸亚铁晶体。
答案:(1)玻璃棒(2)过量的铁在硫酸铜与硫酸亚铁的混合溶液中回收铜,同时得到硫酸亚铁溶液(3)Fe+H2SO4=FeSO4+H2↑(4)冷却结晶
4.物质成分探究的流程问题
例4(2014·湖州)为增加拉面的韧性,制作过程中添加了用蓬草烧制而成的草灰,即蓬灰,蓬灰中的主要成分是什么呢?科学兴趣小组猜想蓬灰的主要成分可能是K2CO3,小组成员分甲、乙两组进行部分探究。
甲组实验:
乙组实验:
实验过程中的操作A的名称是,你认为(填“甲”或“乙”)组的实验比较理想。
解析:把不溶于液体的固体和液体分离的操作是过滤。蓬灰的成分是不是K2CO3,检验组成中是否含有碳酸根离子即可。可先向滤液中加稀盐酸,再把生成的气体通入澄清石灰水中,观察溶液是否变浑浊。向滤液中加入氯化钡产生白色沉淀现象,滤液中还可能含有硫酸根离子。
答案:过滤乙