流行性出血热、腺垂体功能减退、肾功能不全
周 岩 程 震 刘志红
·临床集锦·
流行性出血热、腺垂体功能减退、肾功能不全
周 岩 程 震 刘志红
51岁男性患者,流行性出血热后肾功能不全6年,肾活检示肾小球系膜增生性病变,免疫荧光染色阴性,完善检查发现甲状腺功能降低(甲减),考虑肾功能不全为甲减所致,进一步寻找甲减的原因,腺垂体功能减退,最后诊断为腺垂体功能减退症(继发于流行性出血热)、继发性甲状腺功能减退、甲状腺功能减退相关性肾损害,经补充激素后肾功能改善。
腺垂体 甲状腺功能减退 激素 肾功能不全
病历摘要
现病史 51岁男性患者,因“流行性出血热后血清肌酐(SCr)升高6年”于2014-07-18入院。
2008年患者无明显诱因出现高热,最高40.0℃,伴纳差、乏力,无明显疼痛,后逐渐出现无尿,血液及血压变化不详,诊断为流行性出血热,予输液及血液透析3次后尿量恢复,体温正常。住院期间高热时曾出现意识模糊,全身散在出血点,随着疾病好转意识恢复,出血点消退。出院后半年逐渐出现乏力、怕冷、反应迟钝、记忆力减退、口齿不清,未进一步诊治;定期复查SCr 100~150 μmol/L,尿常规正常,不规律口服中成药治疗。2014年6月患者自觉四肢乏力、活动后气短,无胸闷、夜间可平卧,无发热,无明显肌肉酸痛、关节痛,食欲可,尿色、尿量正常,进一步诊治。
既往史及个人史 6年前流行性出血热(EHF)肾损害时有输血史,无输血反应;婚育史及家族史无特殊。
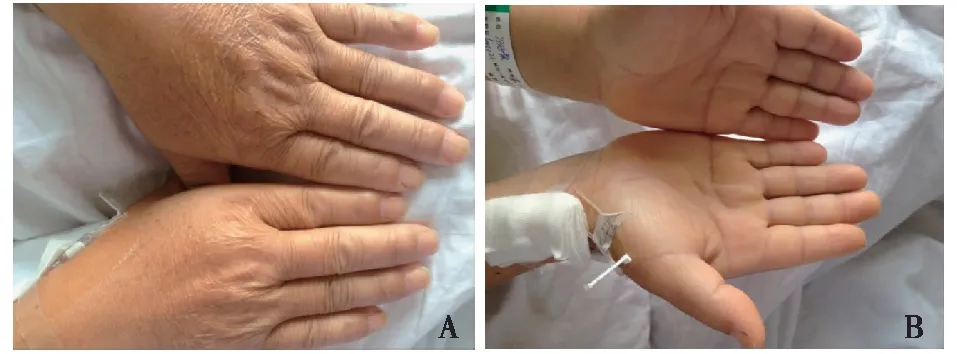
图1 A、B.患者双手背及手掌表现:皮肤干燥,少光泽
体格检查 体温36.2℃,脉搏60次/min,血压137/89 mmHg(18.26/11.86 kPa),皮肤干燥、粗糙(图1),眉毛稀疏,腋毛脱落,阴毛稀疏。眼睑水肿,甲状腺未触及肿大及块,心肺腹未及异常,双肾无叩击痛,双下肢无水肿。神经系统查体:神清,反应迟钝、口齿不清,双侧瞳孔等大等圆,对光反射灵敏,鼻唇沟、口角对称,皱眉、闭眼、鼓腮均正常。指鼻试验、轮替试验准确,四肢感觉对称,肱二头肌反射、左腿膝反射正常,右侧膝反射减弱,Hoffmann征、Babinski’s征阴性、脑膜刺激征阴性。
实验室检查
尿液 尿常规蛋白、隐血均阴性,尿蛋白定量0.17 g/24h,尿微量白蛋白 9.6 mg/24h,尿沉渣红细胞计数 1.0万/ml,白细胞0~1/HP,管型定型阴性,尿渗量386 mOsm/(kg·H2O),尿NAG 2.0 U/(g·Cr),视黄醇结合蛋白(RBP)0.1 mg/L,溶菌酶<0.5 mg/L。
血液
血常规 血红蛋白(Hb) 124 g/L,白细胞计数5.4×109/L,N/L 47.89/43.3,血小板172×109/L,C反应蛋白3.5 mg/L。
血生化 白蛋白46.2 g/L,球蛋白33.4 g/L,尿素5.0 mmol/L,SCr 135 μmol/L,尿酸241 μmol/L,胱抑素C 1.36 mg/L,谷丙转氨酶21 U/L,谷草转氨酶41 U/L,胆碱酯酶9.5 KU/L,肌酸激酶959 U/L,肌酸激酶MB同工酶17.0 U/L,钾3.9 mmol/L,钠143 mmol/L,氯105 mmol/L,总胆固醇7.33 mmol/L,三酰甘油9.56 mmol/L,高密度脂蛋白胆固醇0.86 mmol/L,低密度脂蛋白胆固醇1.28 mmol/L,乳酸脱氢酶771.0 U/L,脂肪酶100.0 U/L,肌红蛋白179.2 ng/ml,钠143.0 mmol/L,总二氧化碳30.0 mmol/L。空腹血糖5.91 mmol/L,餐后2h血糖8.9 mmol/L。估算的肾小球滤过率(eGFR)46.34 ml/(min·1.73m2)(CKD-EPI公式)[1]。肌钙蛋白Ⅰ 0.01 ng/ml,肌钙蛋白T 0.009 ng/ml。
免疫 抗核抗体(ANA)、抗dsDNA阴性,补体C3、C4正常。抗核抗体谱均阴性。抗链球菌溶血素“O” 90.3 IU/ml,IgA 2.620 g/L,IgE 137.0 IU/ml,IgG 15.900 g/L,IgM 2.470 g/L,类风湿因子23.7 IU/ml。外周血淋巴细胞亚群CD3+1 505个/ml,CD4+836个/ml,CD8+542个/ml。
甲状腺功能及相关抗体 抗甲状腺球蛋白抗体0.7 IU/ml,甲状腺微粒体抗体0.7 IU/ml,甲状腺过氧化物酶抗体4.0 IU/ml,促甲状腺激素受体抗体16.9 IU/ml。全段甲状旁腺激素(iPTH)64.8 pg/ml。
垂体与性激素测定 硫酸脱氢表雄酮(DHEA)0 mmol/L(正常值<5 mmol/L),皮质醇(8:00) 0.01 mmol/L(正常值 0.17~0.44 mmol/L),生长激素(GH) 0 mg/L(0~6 mg/L),催乳素(PRL)18.7 mIU/L(正常值95.4~400 mIU/L),睾酮(T)0.10 nmol/L(正常值9.4~37 nmol/L),促肾上腺皮质激素(8:00~10:00)12.64 pg/ml(正常值6~40 pg/ml),雌二醇(男)46.00 pmol/L(正常值58.6~194.2 pmol/L),卵泡刺激素(FSH)(男)0.3 IU/L(正常值1~5.5 IU/L),黄体生成素(男)0 IU/L(正常值1~6.3 IU/L)。
其他
肾脏B超 左97 mm×42 mm×48 mm,右93 mm×41 mm×46 mmm,左肾中上极见一点状强回声,未见后声影。
垂体MRI 空泡蝶鞍,双侧基底节区多发腔隙性脑梗塞(图2)。
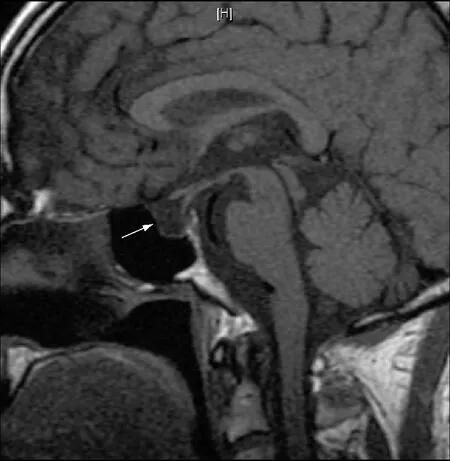
图2 头颅MRI:空泡蝶鞍(↑)
心电图 窦性心律,低电压趋势。
甲状腺及肝胆胰脾超声 未见异常。
胸部CT 双侧胸腔积液;心包积液。
肾活检
光镜 10个肾小球中4个球性废弃。余肾小球系膜区节段轻度增宽,系膜基质增多(图3A),毛细血管袢开放好,肾小球囊壁节段增厚。PASM-Masson:阴性。肾小管间质慢性病变,髓质区间质增宽纤维化++~+++。小叶间动脉弹力层增厚、分层,小动脉管壁增厚,管腔狭窄(图3B)。
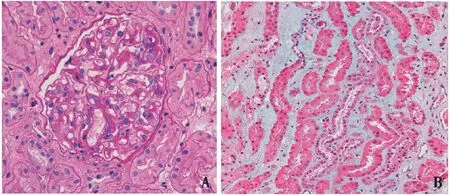
图3 A:肾小球系膜增生性病变(PAS,×400);B:肾间质区域增宽、纤维化(Masson三色,×200)
免疫荧光 IgG、IgA、IgM、C3、C1q均阴性。
诊疗分析 患者为中年男性,病程长,病史特点:(1)既往EHF病史,病愈后肾功能未完全恢复正常;(2)病程6年余,肾功能相对稳定,尿检(无蛋白尿及血尿)及临床特点不支持肾小球疾病所致肾功能损害;(3)入院后发现甲状腺功能减退(甲减)、腺垂体功能减退、空泡蝶鞍。该患者需与以下疾病相鉴别。
EHF肾损害 EHF多数预后良好,肾功能一般均可完全恢复[2];但不排除少数患者肾功能未完全恢复的可能性。
慢性间质性肾炎(CIN) 本例患者慢性肾衰竭伴尿液浓缩功能减退,无明显的蛋白尿、血尿,需考虑CIN,本例患者无长期用药史、无毒物接触史,自身免疫相关检查无异常;尿NAG、RBP、溶菌酶、尿
糖等肾小管损伤指标均正常,不支持CIN。
横纹肌溶解 患者血生化提示肌酶、肌红蛋白显著升高,肾功能不全;但患者6年病程中,病程中无明显肌痛,无肌肉损伤的明确诱因;无肌红蛋白尿,尿常规隐血阴性,肾小管损伤标记物均正常,不支持横纹肌溶解所致急性肾损伤(AKI)。
甲减相关肾损害 其特征为持续的肾功能不全但尿检轻微,血生化可有肌酶、胆固醇的升高,在补充甲状腺素后肾功能可恢复,本例患者甲减多年,在补充甲状腺素后肾功能改善。
根据上述特点,考虑为EHF所致的腺垂体功能减退继而出现甲减、肾功能不全,治疗上予激素替代治疗(泼尼松7.5 mg/d服用2周后加用优甲乐25 μg/d),患者乏力、意识淡漠较前缓解。出院1月后复查SCr 133.5 μmol/L;2014-10-24末次随访时,患者乏力、精神萎靡、怕冷、反应迟钝、记忆力减退、口齿不清等情况明显改善,SCr降至 115.8 μmol/L,eGFR升高,总胆固醇 5.44 mmol/L,三酰甘油1.94 mmol/L(表1),继续优甲乐及保肾片治疗。
最后诊断 腺垂体功能减退症(继发于EHF);继发性甲减;甲减相关性肾损害。
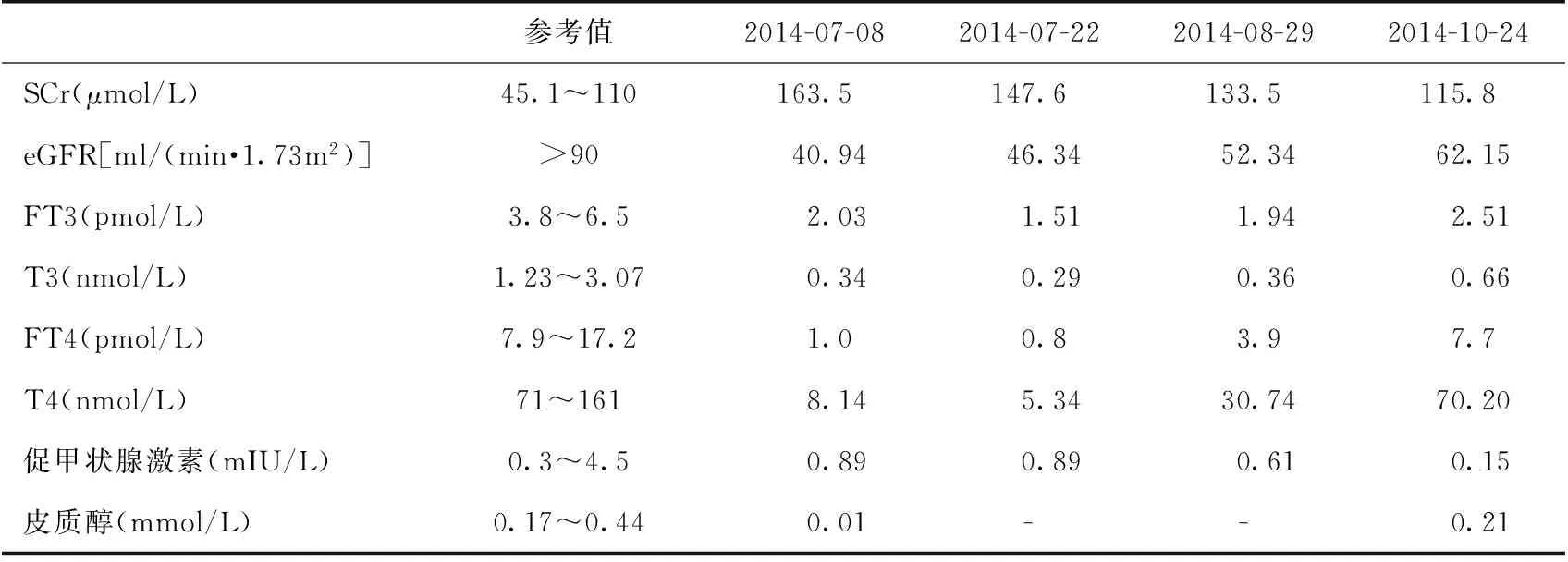
表1 肾功能、甲状腺功能的变化
SCr:血清肌酐;eGFR:估算的肾小球滤过率;T3:三碘甲腺原氨酸;FT3:游离T3 ;T4:四碘甲状腺原氨酸:FT4:游离T4
讨 论
本例为中年男性患者,慢性起病;肾脏方面表现为慢性肾功能不全,无蛋白尿及血尿,双肾体积大小正常。既往确诊EHF肾损害,并行血液净化治疗;肾外表现为乏力、怕冷、反应迟钝、口齿不清等;血生化检查提示乳酸脱氢酶、肌酸激酶和总胆固醇升高。完善检查提示甲状腺功能降低,考虑肾功能不全可能为甲减所致。进一步寻找甲减的原因,发现腺垂功能减退,最后诊断为继发于EHF的腺垂体功能减退症,继发性甲减,甲减相关性肾损害。经激素替代治疗后,患者临床症状及肾功能均明显改善。
甲状腺激素可影响全身的所有器官、系统,并可影响肾脏发育和生长、血流动力学、水盐平衡[3]及GFR[4]。甲减可导致AKI或慢性肾脏病(CKD),其主要临床特点是尿常规通常阴性,肾小管功能基本正常,双肾大小正常,肾活检病理改变较轻,多为轻度肾小球系膜增生性改变,后期可出现肾间质纤维化。甲减相关的肾功能不全的多数患者在补充甲状腺素后肾功能可明显改善[5]。甲减相关肾损害的机制主要由于血流动力学的改变导致肾脏缺血、灌注减少[6],FT3<3 pg/ml 与CKD的发生率明显相关[7]。甲状腺激素减少后可导致心肌收缩力降低和心率变慢,也可通过降低NO合成酶的活性,增加全身血管抵抗,降低肾素-血管紧张素-醛固酮系统活性,导致Na重吸收减少,心输出量减少导致肾灌注不足[3]。甲减导致的肾损害有较多个案报道[8,9],Makino等[10]报道1例缺血性肾脏病患者因甲减SCr由282.9 μmol/L升至627.6 μmol/L,经甲状腺素替代治疗,SCr降至159.1 μmol/L。Shin等[11]观察113例合并亚临床甲减的CKD患者,予激素替代治疗可延缓eGFR下降速率,从而延缓进入终末期肾病(ESRD)的进程。Kim等[12]报道127例甲状腺功能正常和41例亚临床甲减的患者,51.2%的甲状腺功能自发恢复正常的患者的eGFR的下降速度与甲状腺功能正常的患者相似,而未自发恢复正常的患者的eGFR下降速度明显快于恢复的患者和甲状腺功能正常的患者。Hataya等[13]报道一组CKD合并甲减患者在补充甲状腺素后eGFR较基础值提高了近30%[(47.5±7.7) ml/(min·1.73m2)vs(62.1±9.5) ml/(min·1.73 m2),P<0.01]。此外,甲减患者常见肌酸激酶升高,极少数可出现横纹肌溶解综合症,导致肾功能不全(出现少尿甚至无尿,肌痛伴血肌红蛋白明显升高)[14],本例的临床表现明显与此不符。
甲减病因复杂,以原发性甲状腺疾病多见,包括慢性淋巴细胞性甲状腺炎、甲状腺手术切除、Graves病晚期、抗甲状腺药物过量等。继发性甲减(也称垂体性甲减),常见于肿瘤、手术、放疗或产后垂体坏死等。下丘脑性甲减等其他类型均少见。本例患者的甲状腺功能提示甲减,但促甲状腺激素(TSH)正常,提示垂体不能有效分泌TSH,考虑为垂体性或下丘脑性甲减,进一步完善垂体相关的多种激素提示均不同程度的缺乏,诊断腺垂体功能减退症明确。
任何原因引起的垂体前叶激素分泌不足所导致的一系列临床表现称为垂体前叶功能减退症,该病又分为原发性和继发性两类,前者是由于垂体分泌细胞破坏所致,后者是由于下丘脑病变导致垂体缺乏刺激所致,临床上以前者多见。
腺垂体功能减退的原因:(1)垂体及其附近肿瘤压迫或浸润;包括垂体瘤、鞍旁或鞍上肿瘤或恶性肿瘤转移、浸润等;(2)垂体缺血性坏死:如产后大出血(Sheehan综合征)、糖尿病血管病变、动脉粥样硬化、子痫等;(3)垂体手术、创伤或垂体卒中;(4)各种颅内感染或炎症;(5)空泡蝶鞍;(6)其他:如慢性肾衰竭可出现促性腺激素释放激素(GnRH)和TSH分泌低下等。
汉坦病毒感染引起EHF是我国广泛流行的自然疫源性疾病,基本病理改变是全身小血管和毛细血管广泛性损伤[15]。表现为渗出、充血、出血及部分组织坏死的改变,脑垂体是最易受损器官之一,垂体血管的损伤可致垂体缺血或急性出血、甚至局部坏死,坏死区可凝集成块,垂体功能受损,导致垂体性甲减,由于腺垂体被广泛破坏,表现为垂体多种激素[GH、TSH、促黄体生成素(LH)、FSH、PRL等]同时缺乏。TSH分泌减少,从而血T3、T4 降低,出现继发性甲状腺功能低下,促性腺激素分泌减少,导致性征的改变。严重出血和长时间休克常为并发症促发因素[16]。Stojanovic等[17]随访观察年龄在(35.8±1.3)岁的60例EHF患者(3.7±0.5)年,其中有8例(13.3%)合并严重的生长激素低下,5例有多种垂体激素功能不全,5例(8.3%)有甲状腺轴功能缺陷,6例(10%)存在下丘脑-垂体-肾上腺轴功能缺陷,11例(18.3%)有内分泌缺陷。Hautala等[18]观察58例EHF患者的中枢神经系统症状及实验室检查,其中大多数患者有中枢神经症状,50%患者的脑脊液的汉坦病毒IgM阳性,蛋白或淋巴细胞计数升高。其中2例患者的头颅MRI存在垂体出血,继而伴随头痛、失明,且都进展为垂体功能减低,1例患者需要长期激素替代治疗。人体在应激状态下,血中皮质醇升高,抑制促甲状腺激素释放激素的分泌及TSH对TRH刺激的反应性,可导致TSH水平下降,血T3、T4水平降低。但无证据排除病毒直接侵害腺垂体致其功能减退。
本例患者在6年前曾出现EHF伴休克、高热、AKI,考虑当时垂体缺血导致腺垂体功能减退,继而出现一系列功能减退的症状包括TSH分泌不足的症状:怕冷、淡漠、反应迟钝、毛发稀疏等及促性腺激素分泌不足的表现。
腺垂体功能减退症的治疗主要在于去除病因并行靶腺激素的长期替代治疗。治疗全垂体前叶功能减退的首要治疗是补充肾上腺皮质激素,要先于甲状腺激素和性激素的替代。首选氢化可的松或可的松或泼尼松,原则为最小有效替代剂量。严重感染、大手术等严重应激时,可静滴氢化可的松,避免发生危象。为防止腺垂体功能减退者发生急性肾上腺皮质功能不全,应在皮质激素替代1~2周后方可补充甲状腺素(L-T4)或干甲状腺片,小剂量开始逐步加量至最小有效替代量。剂量较大时可分次服用,尤其对冠心病、心肌缺血或老年患者。对于生育期妇女及男性分别使用雌、雄激素维持第二性征和性功能。儿童在骨骺愈合前可使用GH等。
本例患者在诊断明确后予激素替代治疗,泼尼松7.5 mg/d服用2周后加用优甲乐25 μg/d,患者乏力、神情淡漠较前缓解。出院1月后复查SCr 133.5 μmol/L;2014-10-24日随访患者的乏力、精神萎靡、怕冷、反应迟钝、记忆力减退、口齿不清等症状明显改善,SCr降至115.8 μmol/L,血脂降至正常,未出现不良反应,继续优甲乐替代治疗。由于本例患者在补充甲状腺激素后SCr明显下降,提示腺垂体功能减退继发甲减影响肾脏功能,不支持为EHF诱发的AKI未完全恢复转为慢性肾功能不全。
结论:本例患者由EHF诱发的腺垂体功能障碍最终导致甲减,继而引起肾功能损害,经激素替代治疗后,临床表现及肾功能改善明显。对于肾脏损害尤其以肾功能不全伴尿检较轻的患者需注意询问病史,伴甲减症状的患者需完善甲状腺功能检测,并进一步追溯潜在病因,避免漏诊、误诊。
1 Levey AS,Stevens LA,Schmid CH,et al.A new equation to estimate glomerular filtration rate.Ann Inter Med,2009,150(9):604-612.
2 庄永泽,王金泉.流行性出血热肾损害//黎磊石,刘志红.中国肾脏病学.北京:人民军医出版社,2008:738-751.
3 Mariani LH,Berns JS.The renal manifestations of thyroid disease.J Am Soc Nephrol,2012,23(1):22-26.
4 Iglesias P,Díez JJ.Thyroid dysfunction and kidney disease.Eur J Endocrinol,2009,160(4):503-515.
5 Suher M,Koc E,Ata N,et al.Relation of thyroid disfunction,thyroid autoantibodies,and renal function.Ren Fail,2005,27(6):739-742.
6 Chakera A,Paul HJ,O’Callaghan CA.Reversible renal impairment caused by thyroid disease.Scand J Urol Nephrol,2010,44(3):190-192.
7 Zhang Y,Chang Y,Ryu S,et al.Thyroid hormone levels and incident chronic kidney disease in euthyroid individuals:the Kangbuk Samsung Health Study.Int J Epidemiol,2014,43(5):1624-1632.
8 Neves PD,Bridi RA,Balbi AL,et al.Hypothyroidism and acute kidney injury:an unusual association.BMJ Case Rep,2013.
9 Vikrant S,Chander S,Kumar S,et al.Hypothyroidism presenting as reversible renal impairment:an interesting case report.Ren Fail,2013,35(9):1292-1294.
10 Makino Y,Fujii T,Kuroda S,et al.Exacerbation of renal failure due to hypothyroidism in a patient with ischemic nephropathy.Nephron,2000,84(3):267-269.
11 Shin DH,Lee MJ,Lee HS,et al.Thyroid hormone replacement therapy attenuates the decline of renal function in chronic kidney disease patients with subclinical hypothyroidism.Thyroid,2013,23(6):654-661.
12 Kim EO,Lee IS,Choi YA,et al.Unresolved subclinical hypothyroidism is independently associated with progression of chronic kidney disease.Int J Med Sci,2014,11(1):52-59.
13 Hataya Y,Igarashi S,Yamashita T,et al.Thyroid hormone replacement therapy for primary hypothyroidism leads to significant improvement of renal function in chronic kidney disease patients.Clin Exp Nephrol,2013,17(4):525-531.
14 Ardalan MR,Ghabili K,Mirnour R,et al.Hypothyroidism-induced rhabdomyolysis and renal failure.Ren Fail,2011,33(5):553-554.
15 姚立君,邓国安,黄蓓,等.肾综合征出血热病毒对肾小管上皮细胞损伤的研究.中华肾脏病杂志,2003,16 (3) :173.
16 翁亚丽,孙志坚.腺垂体功能减退症∥白雪枫,徐志凯.肾综合征出血热.北京:人民卫生出版社,2013:526-529.
17 Stojanovic M,Pekic S,Cvijovic G,et al.High risk of hypopituitarism in patients who recovered from hemorrhagic fever with renal syndrome.J Clin Endocrinol Metab,2008,93(7):2722-2728.
18 Hautala T,Mähönen SM,Sironen T,et al.Central nervous system-related symptoms and findings are common in acute puumala hantavirus infection.Ann Med,2010,42(5):344-351.
(本文编辑 律 舟 莫 非)
Epidemic hemorrhagic fever, hypopituitarism, and renal insufficiency
ZHOUYan,CHENGZhen,LIUZhihong
NationalClinicalResearchCenterofKidneyDiseases,JinlingHospital,NanjingUniversitySchoolofMedicine,Nanjing210002,China
A 51-year-old man was hospitalized with persistent renal dysfunction after onset of epidemic hemorrhagic fever 6 years ago.His renal biopsy revealed mild mesangio-proliferative change without immune complex deposition.In view of the mismatch of renal dysfunction and renal pathologic features, we took additional effort to find the etiology and ascribed his renal insufficiency to hypothyroidism secondary to hypopituitarism which was caused by epidemic hemorrhagic fever.After hormone compensation therapy with glucocorticosteroid and levothyroxine, his renal function was ameliorated.
adenohypophysis hypothyroidism hormone renal dysfunction
南京军区南京总医院肾脏科 国家肾脏疾病临床医学研究中心 全军肾脏病研究所(南京,210016)
2015-02-26

