用RP-HPLC法测定天目地黄中梓醇和毛蕊花糖苷的含量
蒙雄裕,徐 良,李华强,王 亮,郑承剑*,秦路平*
(1.宁夏医科大学药学院生药学教研室,银川 750004;2.第二军医大学药学院生药学教研室,上海 200433;3.浙江天目山国家级自然保护区管理局科研宣教科,杭州 311300;4.上海师范大学生命与环境科学学院植物学教研室,上海 200234)
用RP-HPLC法测定天目地黄中梓醇和毛蕊花糖苷的含量
蒙雄裕1,2,徐 良3,李华强2,4,王 亮2,郑承剑2*,秦路平2*
(1.宁夏医科大学药学院生药学教研室,银川 750004;2.第二军医大学药学院生药学教研室,上海 200433;3.浙江天目山国家级自然保护区管理局科研宣教科,杭州 311300;4.上海师范大学生命与环境科学学院植物学教研室,上海 200234)
目的:建立RP-HPLC法测定天目地黄中梓醇与毛蕊花糖苷的含量,分析两种成分在天目地黄中的动态积累规律,为其资源开发和质量标准建立提供参考依据。方法:采用甲醇回流提取法进行提取,用RP-HPLC法测定不同发育阶段新鲜药材块根与全草中梓醇和毛蕊花糖苷的含量。结果:梓醇和毛蕊花糖苷在天目地黄块根和全草中含量有显著差异,其中梓醇主要分布于块根,在5月份成长期含量最高(3.42%);而毛蕊花糖苷主要分布在全草,于6月份开花结实期含量较高(0.47%)。结论:本研究初步探索了天目地黄中有效成分的动态积累规律,为该药材资源的合理利用提供了科学依据。
天目地黄;梓醇;毛蕊花糖苷;含量测定;色谱法,高效液相
[Pharm Care Res,2015,15(4):273-276]
天目地黄Rehmannia chingiiLi.为玄参科地黄属多年生草本植物,收载于《中国植物志》。据民间用药记载,其块根状茎和全草均可入药。地黄属Rehmannia共有6种,其中天目地黄与地黄化学成分相似[1,2],主要为环烯醚萜类、紫罗兰酮类、地黄脑苷类、糖类等成分,其中梓醇(catalpol)和毛蕊花糖苷(verbascoside)作为地黄的主要有效成分,已经被《中华人民共和国药典》2010年版列为地黄的指标性成分,并对其含量做出明确规定[3,4]。研究表明,梓醇与毛蕊花糖苷具有神经保护、抗肿瘤、降血糖、免疫调节作用等多种药理学作用[5,6]。
天目地黄是浙江省天目山所特有的药用植物资源,在当地民间广泛使用。目前关于天目地黄的研究鲜有报道。为了保证用药的安全与有效,本课题组与浙江天目山国家级自然保护区管理局合作,通过采集不同生长阶段,即幼苗期、成长期、开花结果期、枯萎期的天目地黄植株,采用RP-HPLC法对天目地黄块根和全草中的梓醇和毛蕊花糖苷进行含量测定;同时选择两个道地产区(河南焦阳和安徽亳州)的地黄药材与浙江天目地黄药材进行比较,为天目地黄药材资源的开发利用及质量标准的制定提供一定的科学依据。
1 仪器和试药
1.1 仪器 Agilent 1200系列高效液相色谱仪,包括二极管阵列检测器(DAD)、Chemstation10.2工作站、Eclipse-XDB C18柱(250mm×4.6mm,5μm)(美国Agilent公司);BP211D十万分之一电子天平(德国Sartorius公司);电热恒温水浴锅(上海一恒科学仪器有限公司)。
1.2 药品和试剂 梓醇对照品(含量>99%,批号140508-200908)、毛蕊花糖苷对照品(含量>99%,批号YM0505YA14)购自上海源叶生物有限公司。甲醇(色谱纯,批号201405023)、乙腈(色谱纯,批号201404015)购自上海斯炯化工科技有限公司;磷酸(优级试剂,批号201403018)和冰醋酸(优级试剂,批号201301018)购自上海国药集团化学试剂有限公司;娃哈哈纯净水购自杭州娃哈哈集团有限公司。
1.3 药材 实验所用10批(批号见表1)新鲜天目地黄药材均由浙江天目山国家级自然保护区管理局徐良采自浙江省天目山,两批野生地黄购买于河南焦阳(批号140507011)和安徽亳州(批号140510012),经第二军医大学药学院生药学教研室秦路平教授鉴定为玄参科地黄属Rehmannia植物Rehmannia chingiiLi.和Rehmannia glutinosaLibosch.。
2 方法和结果
2.1 色谱条件 (1)梓醇:采用反相高效液相色谱Eclipse-XDB C18柱(250mm×4.6mm,5μm);流动相为乙腈-0.1%磷酸水溶液,梯度洗脱,0~2min,0.3%乙腈,流速0.6ml/min;2~8min,0.3%~0.8%乙腈,流速0.6ml/min;8~20min,1%乙腈,流速1ml/min。检测波长为210nm,柱温25℃,理论塔板数按梓醇峰计≥5000。对照品及样品的HPLC谱图见图1。(2)毛蕊花糖苷:采用反相高效液相色谱Eclipse-XDB C18柱,流动相为乙腈-0.1%乙酸水溶液(16:84)等度洗脱。检测波长为340nm,流速1.0ml/min,柱温2 5℃,理论塔板数按毛蕊花糖苷峰计≥5 0 0 0。对照品及样品的HPLC谱图见图1。
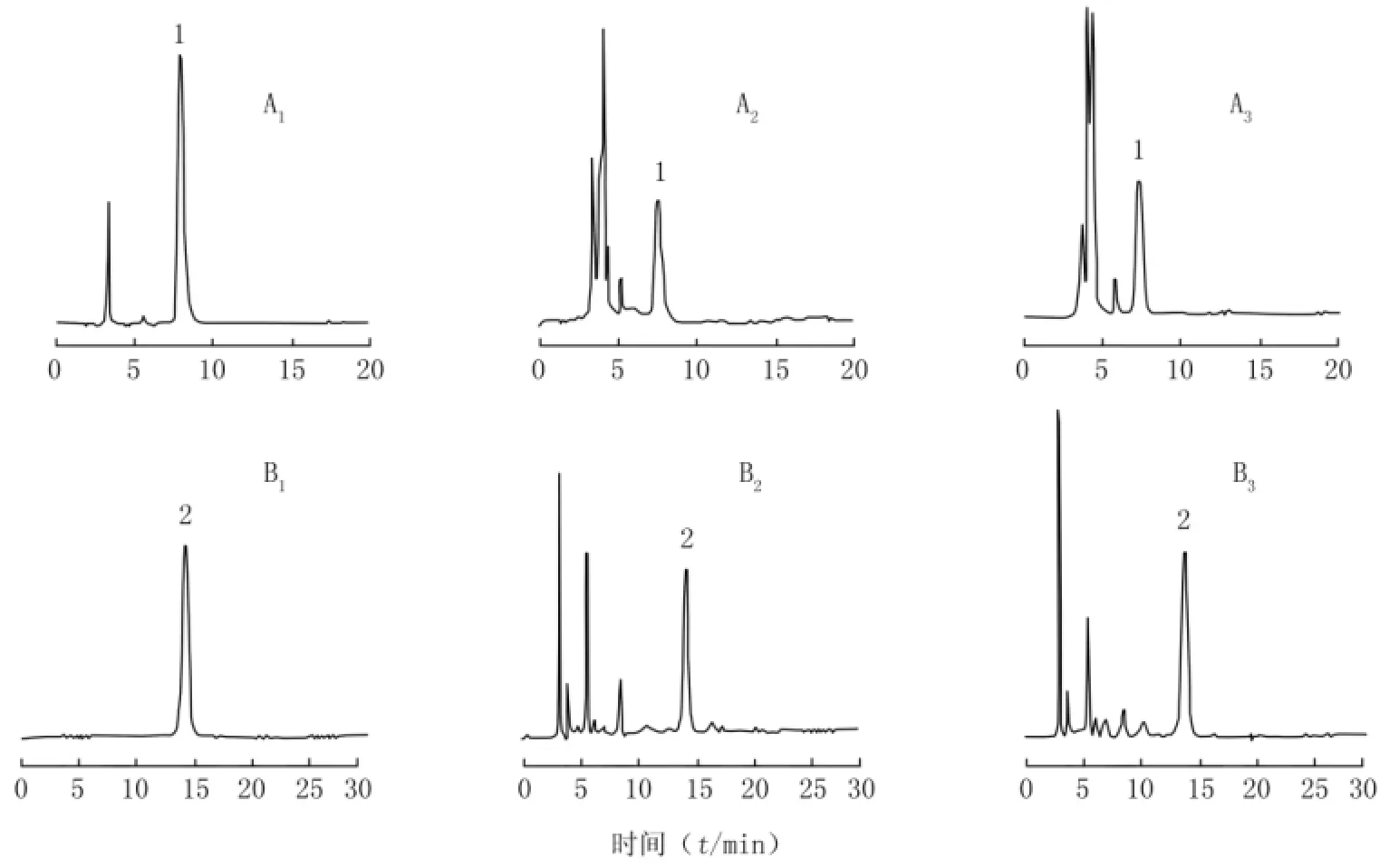
图1 梓醇和毛蕊花糖苷的RP-HPLC谱图Figure 1 RP-HPLC photograms of catalpol and verbascoside
2.2 对照品储备液的制备 分别精密称取梓醇及毛蕊花糖苷对照品14.40、5.48mg,置于10ml量瓶中,加甲醇溶解并定容,摇匀,即得对照品储备液,梓醇浓度为1.440mg/ml,毛蕊花糖苷浓度为0.548mg/ml,置4℃冰箱保存待用。
2.3 供试品溶液的制备 取天目地黄块根和全草洗净,经50℃减压干燥20h后,磨成粗粉。称取约0.4g,置具塞100ml锥形瓶中,精密加入甲醇25ml,称定重量,加热回流提取1.5h,放冷,静置15min后再次称定重量,用甲醇补足减失的重量,摇匀静置,用0.45μm微孔滤膜滤过,即得供试品溶液。
取地黄药材(批号140507011、140510012)洗净,擦干表面水分,去除须根后切成2~4mm细丝。制备方法同上。
2.4 标准曲线的制备 精密吸取2.2项下对照品储备液适量,用甲醇稀释成梓醇浓度为0.022 5、0.045 0、0.090 0、0.180、0.360、0.720、1.440mg/ml;毛蕊花糖苷0.008 56、0.017 1、0.034 3、0.068 5、0.137、0.274、0.548mg/ml的系列对照品溶液,用0.45μm微孔滤膜过滤;按2.1项下色谱条件,分别精密吸取上述对照品溶液10μl进样,以梓醇及毛蕊花糖苷的峰面积值为纵坐标(Y),质量浓度为横坐标(X)绘制标准曲线,得梓醇回归方程Y1=3 260.1X1+18.800,r=0.999 9(n=6);毛蕊花糖苷回归方程为Y2=440.60X2-434.77,r=0.999 5(n=6)。结果表明,梓醇、毛蕊花糖苷分别在22.5~1440μg/ml、8.56~548μg/ml范围内与峰面积线性关系良好。
2.5 精密度实验 精密吸取梓醇和毛蕊花糖苷对照品溶液各10μl,连续进样6次,记录峰面积值,求得梓醇和毛蕊花糖苷峰面积RSD分别为2.09%和1.31%(n=6),结果表明仪器具有良好的精密度。
2.6 稳定性实验 取批号为14050105的天目地黄供试品溶液,分别在配制后0、2、4、8、12、24、48h进样,结果天目地黄块根和全草中梓醇峰面积的RSD分别为1.07%、0.510%(n=7),毛蕊花糖苷峰面积的RSD分别为1.55%、1.87%(n=7),结果表明样品溶液在48h内稳定。
2.7 重复性实验 取批号为14050105的天目地黄药材,按2.3项下方法平行制备6份供试品溶液,按照2.1项下色谱条件分别进样测定。结果天目地黄块根和全草的梓醇峰面积RSD分别为1.47%、0.426%(n=6),毛蕊花糖苷峰面积RSD分别为1.07%、0.816%(n=6),表明方法重复性良好。
2.8 加样回收率实验 (1)梓醇:分别精密称取批号为14050105的天目地黄块根和全草药材细粉0.4g,6份,分别精密加入梓醇对照品4.675、3.200mg,按2.3项下方法制备,进样10μl,按照2.1项下色谱条件分别进样测定,计算回收率。结果加样回收率分别为(98.96±1.53)%、(98.32± 1.72)%(n=6),RSD分别为1.95%、1.26%(n=6),结果表明本法具有良好的回收率。(2)毛蕊花糖苷:分别精密称取批号为14050105的天目地黄块根和全草药材细粉0.4g,6份,分别精密加入毛蕊花糖苷对照品1.200、1.320mg,按2.3项下方法制备后进行测定。结果加样回收率分别为(101.4± 2.01)%、(100.1±1.89)%(n=6),RSD分别为1.77%、0.21%(n=6),结果表明本法回收率良好。
2.9 样品含量测定 取同一产地不同采收季节的10批天目地黄和另两个产地各一批(批号140507011、140510012)地黄药材,按2.3项下方法制备供试品溶液,平行3份,分别精密吸取供试品溶液10μl,按照2.1项下色谱条件进样,测定梓醇及毛蕊花糖苷的质量分数,结果见表1和表2。
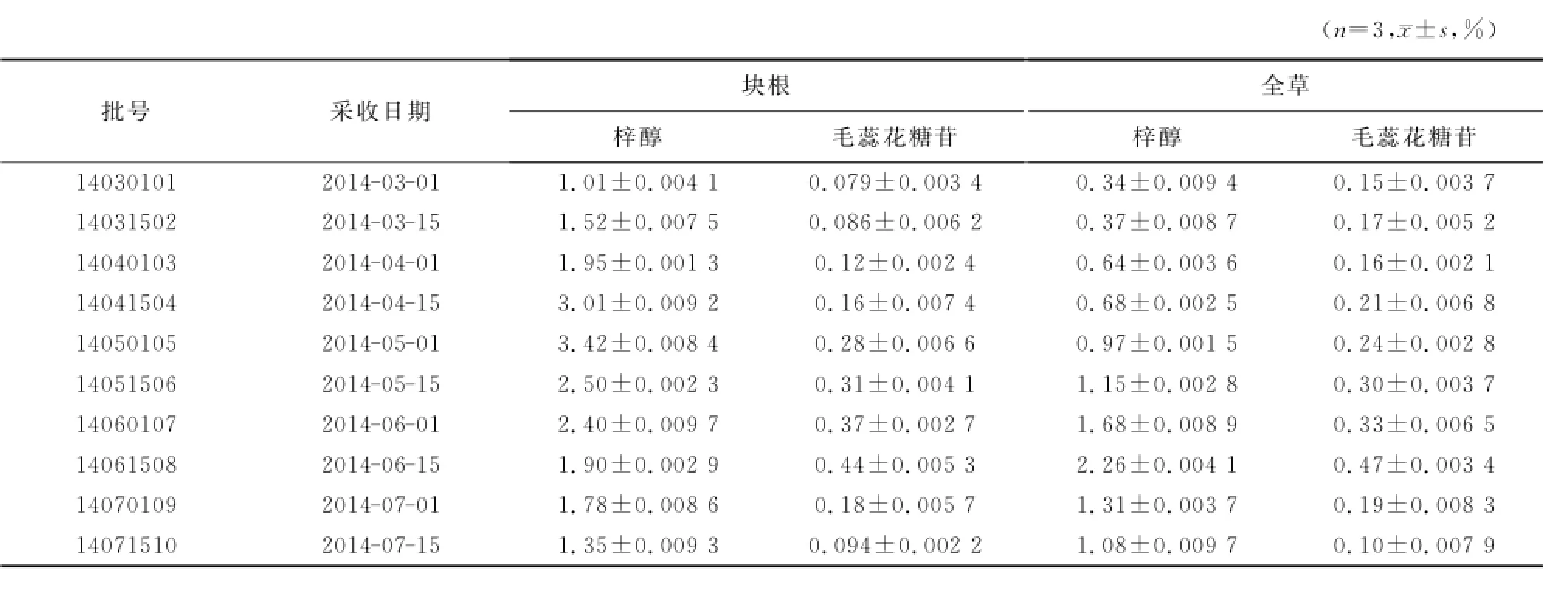
表1 天目地黄块根和全草在不同生长阶段梓醇和毛蕊花糖苷的质量分数Table 1 Contents of catalpol and verbascoside in roots and whole plants of Rehmannia chingii Li.at different growth stages
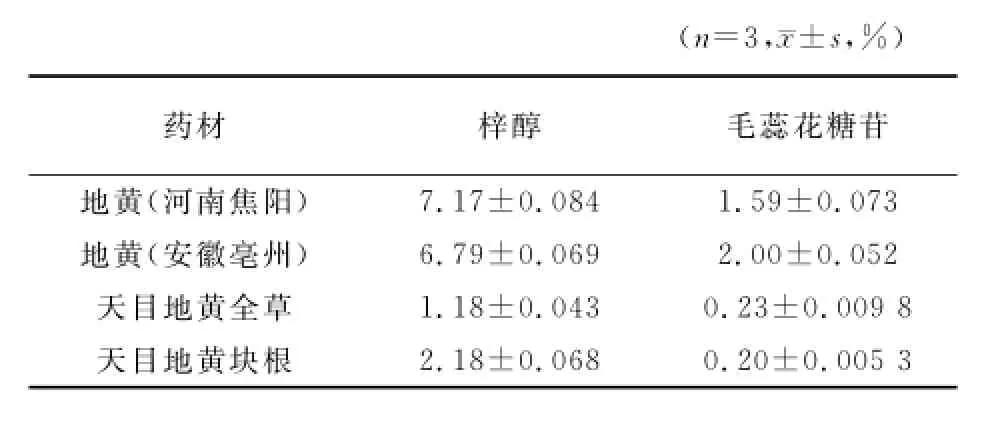
表2 天目地黄与地黄中梓醇、毛蕊花糖苷含量的比较Table 2 Comparison of the contents of catalpol and verbascoside between Rehmannia chingii Li.and Rehmannia glutinosa Libosch.
3 讨 论
天目地黄在浙江省天目山地区资源较为丰富,但由于其化学成分和药理作用均未得到较系统的阐明,限制了该植物资源的进一步开发利用。本研究以地黄属植物中的主要活性成分梓醇和毛蕊花糖苷作为指标性成分,采用RP-HPLC法测定两者在天目地黄块根和全草中的含量。通过采集不同生长阶段新鲜植株块根与全草进行RP-HPLC分析,明确块根和全草中梓醇和毛蕊花糖苷的动态积累规律。其中,天目地黄全草中梓醇的含量在整个生长周期中呈现先上升后下降的趋势,至开花结实期含量达到最高值。而块根中梓醇随着植株生长到成年期(5月份)含量达到最高。毛蕊花糖苷在全草与块根中分布规律没有明显差别,植物开花结实期6月份达到最大,随后含量逐渐降低。但总体而言,毛蕊花糖苷在全草中含量略高于块根。
本研究曾参照《中华人民共和国药典》2010年版地黄中梓醇和毛蕊花糖苷的含量测定方法[4],但此方法在天目地黄中梓醇的含量测定方面效果并不太理想。作者在预实验中分别以甲醇-水、乙腈-水、乙腈-水(0.1%磷酸)等不同溶液体系作为RP-HPLC流动相,在不同流速及不同分析时间中反复实验优选,结果发现流动相为乙腈-0.1%磷酸,梯度洗脱(见2.1项梓醇色谱条件),对梓醇和天目地黄中其他成分的分离效果较好,色谱峰分离度高,不拖尾。
[1]Zhang RuXue,Li MaoXing,Jia ZhengPing.Rehmannia glutinosa:review of botany,chemistry and pharmacology[J].J Ethnopharmacol,2008,117(2):199-214.
[2]Zheng ChengJian,Wu Yu,Zhu JianYong,et al. Chemical constituents of the aerial parts ofRehmannia chingii[J]. Chem Nat Comp,2014,50(3):560-561.
[3]黄莉婷,孙少平,郑 颖.生地黄中梓醇和毛蕊花糖苷的HPLC测定及提取工艺优化[J].中药材,2012,35(8):1318-1322.
Huang LiTing,Sun ShaoPing,Zheng Ying.Simultaneous determination and optimization of extraction process of catalpol and acteoside from Rehmanniae Radix[J].J Chin Med Mat,2012,35(8):1318-1322.In Chinese with English abstract.
[4]国家药典委员会.中华人民共和国药典.2010年版一部[S].北京:中国医药科技出版社,2010:115-116.
State Pharmacopoeia Committee.Pharmacopoeia of the People’s Republic of China.2010ed.Volume 1[S].Beijing:Chinese Medical and Science Press,2010:115-116.In Chinese.
[5]董 炤,陈长勋.梓醇药理作用的研究进展[J].中成药,2013,35(5):1047-1051.
Dong Zhao,Chen ChangXun.Research progress in pharmacological effects of catalpol[J].Chin Tradit Pat Med,2013,35(5):1047-1051.In Chinese.
[6]刘卫欣,卢兖伟,杜海涛,等.地黄及其活性成分药理作用研究进展[J].国际药学研究杂志,2009,36(4):277-280.
Liu WeiXin,Lu YanWei,Du HaiTao,et al. Phamacological actions of Radix Rehmanniae and its active components:research advances[J]. J Int Pharm Res,2009,36(4):277-280. In Chinese with English abstract.
Determination of the contents of catalpol and verbascoside in Rehmannia chingii Li.by RP-HPLC method
MENG XiongYu1,2,XU Liang3,LI HuaQiang2,4,WANG Liang2,ZHENG ChengJian2*,QIN LuPing2*
(1.Department of Pharmacognosy,School of Pharmacy,Ningxia Medical University,Yinchuan 750004,China;2.Department of Pharmacognosy,School of Pharmacy,Second Military Medical University,Shanghai 200433,China;3.Department of Research and Education,Tianmu Mountain National Nature Reserve Administration of Zhejiang Province,Hangzhou 311300,China;4.Department of Botany,College of Life and Environmental Sciences,Shanghai Normal University,Shanghai 200234,China)
Objective:To establish a RP-HPLC method for the quantification and dynamic accumulation analysis of catalpol and verbascoside inRehmannia chingiiLi. ,so as to provide scientific basis for the resource utilization and quality standard establishment.Methods:The whole plants and roots ofR.chingiiat different growth stages were extracted with methanol under reflux. Contents of catalpol and verbascoside were determined by RP-HPLC method.Results:The contents of catalpol and verbascoside varied considerably in whole plants and roots ofR.chingii. Catalpol was mainly distributed in the root and reached the peak in May with a content of 3. 42%,whereas verbascoside was mainly distributed in the whole plant and reached the peak at flowering and fruit bearing stage in June with a content of 0. 47%.Conclusion:This study has made a preliminary exploration into the regular pattern of dynamic accumulation of active components inR.chingii,and could provide experimental data for rational utilization of the medicinal resource ofR.chingii.
Rehmannia chingiiLi.;catalpol;verbascoside;content determination;chromatography,high performance liquid
R927.2 [
] A [
] 1671-2838(2015)04-0273-04
10.5428/pcar20150411
2015-04-07
] 2015-07-20
全军医学科技青年培育项目(13QNP098),上海市卫生系统优秀青年人才项目(XYQ2013100)
蒙雄裕(男),硕士生.E-mail:mengxiongyu2011@126.com;徐 良(男),工程师.E-mail:363356921@qq.com;两人为共同第一作者
秦路平,E-mail:qinsmmu@126.com;郑承剑,E-mail:zhengchengjian@smmu.edu.cn
[
[本文编辑]阳凌燕
——浅谈天目窑传承与创新,黑与青

