洗涤红细胞不同制备方法的比较
肖乐宇 马振芳 王新梅 李建伟
【摘 要】 目的 观察ACP 215血细胞处理机制备的洗涤红细胞和传统手工法制备的洗涤红细胞的质量差异。方法 将40袋悬浮红细胞随机分为2组:机洗组和手工组,每组各20袋,2U/袋,分别对两种方法制备的洗涤红细胞的红细胞回收率、白细胞清除率及血浆蛋白清除率进行比较。结果 使用ACP 215血细胞处理机制备的洗涤红细胞,其红细胞回收率及血浆蛋白清除率明顯优于传统手工法制备的洗涤红细胞,差异具有统计学意义(P<0.05),而白细胞清除率差别不明显,无统计学意义(P>0.05)。结论 ACP 215血细胞处理机洗涤制备的红细胞质量好,临床使用安全可靠,值得推广和应用。
【关键词】 洗涤红细胞;ACP215血细胞处理机;手工法;制备
【中图分类号】 R446.11+3 【文献标识码】 A
洗涤红细胞是将保存期内的浓缩红细胞、悬浮红细胞、少白细胞红细胞或全血在无菌条件下用生理盐水反复洗涤后制备而成的,其特点是去除了80%以上的白细胞、98%以上的血浆蛋白,保留了70%以上的红细胞。使用该制品可以减少或避免血浆蛋白所致的过敏反应,降低FNHTR的发生,也适用于IgA缺乏及肝肾功能不全的患者输用。目前国内制备洗涤红细胞的方法有全自动血细胞处理机洗涤制备和传统手工法洗涤制备,为进一步观察两种方法制备的洗涤红细胞质量的差异,我们于2014年3月将使用全自动血细胞处理机制备的洗涤红细胞和手工法制备的洗涤红细胞进行比较,现报告如下。
1 材料与方法
1.1 仪器与试剂 ACP215血细胞处理机及一次性使用附件(美国血液技术公司),TSCD-Ⅱ无菌接管机(日本泰尔茂公司),CR-7型大容量冷冻离心机(日本工机株式会),全自动血细胞计数仪(日本希森美康公司),Nageotte细胞计数板(HORSHAM公司);0.9%生理盐水四联袋(上海输血技术公司),双缩脲剂(自配)。
1.2 材料制备 抽取本站于2014年3月采集制备的保存期均在35天内的悬浮红细胞40袋,2U/袋(每200ml全血制备的红细胞为1个U),随机分为2组:机洗组和手工组,每组各20袋。机洗组使用ACP215血细胞处理机制备,首先用无菌接管机将悬浮红细胞与血细胞处理机一次性使用附件相连接,安装好管路,按照设定的程序进行洗涤,具体操作过程参照ACP215血细胞处理机CELL WASH操作手册;手工组采用手工方法制备,首先将悬浮红细胞与0.9%生理盐水四联袋用无菌接管机进行连接,将四联袋中首袋生理盐水加入悬浮红细胞中,边加边混匀,加完后称重配平,在温度4℃、离心速度3400r/min、时间8min的条件下离心,离心后用分浆夹将上清液及白膜层挤入空袋中弃去。再将第二袋生理盐水加入红细胞中,同以上步骤,如此依次洗涤红细胞3次,最后将剩下的一袋生理盐水酌量加入红细胞中,使最终洗涤红细胞的体积在250ml±10%.具体操作过程参照《血站技术操作规程》[1]。红细胞洗涤前后分别留样备检。
1.3 检测方法 红细胞的数量采用全自动血细胞计数仪检测;残余白细胞的数量采用Nageotte计数板检测;血浆蛋白含量采用双缩脲法检测。试剂配制及检测过程均严格按照《全国临床检验操作规程》的要求操作[2]。红细胞回收率(%)=(洗涤后红细胞计数/洗涤前红细胞计数)×100%,白细胞清除率(%)=(1-洗涤后白细胞计数/洗涤前白细胞计数)×100%,血浆蛋白清除率(%)=(1-洗涤后上清蛋白含量/洗涤前上清蛋白含量)×100%。
1.4 统计方法 采用SPSS17.0统计软件,应用配对样本的t检验进行统计,以P<0.05有统计学意义。
2 结果
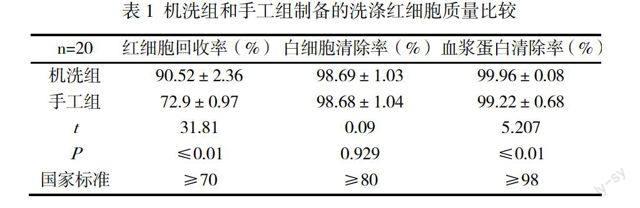
机洗组和手工组制备的洗涤红细胞经过检测,其结果见表1。
3 讨论
临床输血并不是绝对安全的,它有可能引发多种输血不良反应以及输血传播病毒的危险,不同的血液成分引发的输血不良反应发生率是不一样的[3],其中白细胞和血浆带来的危险度最高,红细胞和血小板则相对比较安全,而洗涤红细胞由于去除了血液中绝大部分血浆和白细胞以及一些电解质、枸橼酸盐和微聚物等物质,从而明显降低了输血不良反应的发生及传播输血相关疾病的风险,临床使用更安全可靠。目前国内制备洗涤红细胞的方法有全自动血细胞处理机洗涤法和传统手工洗涤法,传统手工洗涤法制备的时间较长,操作繁琐,易受工作人员技术水平及离心机转速、温度等影响,造成制品质量的不稳定性,但由于比较经济,因而国内多数血站仍采用手工法。而全自动血细胞处理机的应用使得洗涤红细胞的制备过程程序化、标准化和规范化,操作方便,节约人力,节省时间,保证了制品的质量,但成本较高,国内应用较少。
血浆蛋白清除率是洗涤红细胞质量监控的一项重要指标。在原料血中蛋白的含量越高,则血浆蛋白清除率就越高[4]。在手工法洗涤制备中,我们发现随着血浆蛋白清除率的增加,红细胞回收率却会出现下降的情况,二者具有无法调和的矛盾,而全自动血细胞处理机解决了这一难题,它不仅提高了血浆蛋白清除率,同时也增加了红细胞的回收率。从本次试验中可以看出,两种方法制备的洗涤红细胞均可以达到国家规定的质量标准,全自动血细胞处理机制备的洗涤红细胞的红细胞回收率及血浆蛋白清除率明显优于手工法制备的,差异具有统计学意义(P<0.05),这与国内相关的文献报道基本相符[5,6]。另有学者认为,最好不要使用保存期末的悬浮红细胞做原料血[7],如果制备洗涤红细胞采用去白细胞悬浮红细胞做原料血则效果会更好,红细胞回收率可以提高5%-6%,而白细胞残留量可以降低1000倍[8]。
总之,使用全自动血细胞处理机洗涤制备红细胞更科学合理,制备的产品更安全可靠,完全可以替代手工法为临床提供高质量的血液制品,值得在血站大力推广应用。
参考文献
[1] 中华人民共和国卫生部.血站技术操作规程[S].2012版.
[2] 中华人民共和国卫生部. 全国临床检验操作规程[M].3版.南京:东南大学出版社,2006:337-338.
[3] 危燕芬,米仕清.输血不良反应的分析[J].实验与检验医学,2012,30(2):178-179.
[4] 徐利强,李建华,周忠英.洗涤红细胞制备工艺的研究[J].药物生物技术,2012,19(3):245-246.
[5] 凌吟.使用ACP215血液处理仪洗涤红细胞和手工洗涤红细胞的效果比较[J].临床血液学杂志,2012,25(8):520-521.
[6] 周俊,吴涛,姜瑞民,等.悬浮红细胞制备洗涤红细胞不同方式的比较分析[J].中国输血杂志,2013,26(9):887-888.
[7] 冯博,段澜,王景文,等.悬浮红细胞储存时间对制备的洗涤红细胞钾离子和游离血红蛋白含量的影响[J].中国输血杂志,2012,9(9):834-836.
[8] 刘颖,康炜,周世航.两种原料血制备洗涤红细胞的效果分析[J].临床输血与检验,2011,7(3):267-268.

