后腹腔镜包膜下肾切除技术治疗无功能肾附36例报导*
李萍 施丽华 周锦波 叶海榛 赵华 胡海兵 罗超
感染性无功能肾的临床治疗较棘手,由于感染导致肾周组织发生广泛而致密的粘连,肾周组织与肾包膜无明显界限,强行分离易误入肾实质而导致大量出血。手术野出血多引起手术难度增加。有时腹膜间位脏器如十二指肠、结肠和靠近腹膜后的脏器如胰腺、脾脏等与肾周组织粘连,在解剖层次不清时损伤风险较大。在包膜下行肾切除术可避开粘连,在肾包膜和肾实质之间将无功能肾游离后切除,手术效果较满意[1]。本文分析了后腹腔镜包膜下肾切除技术和开放手术治疗无功能肾的效果,现将研究结果分析报道如下。
1 资料与方法
1.1 一般资料 选取本院泌尿外科2010年2月-2014年1月采用后腹腔镜包膜下肾切除术治疗的36例无功能肾患者作为试验组,其中男24例,女12例;年龄33~65岁,平均(51.26±11.52)岁;体重50~78 kg,平均(61.35±10.54)kg;左肾病变16例,右肾病变20例。将同期采用开放手术治疗的36例患者作为对照组,其中25例,女11例;年龄30~68岁,平均(51.63±11.45)岁;体重49~80 kg,平均(61.22±10.32)kg;左肾病变16例,右肾病变20例。所有患者静脉肾盂造影结果提示患侧肾不显影,对侧肾形态、功能良好。研究对象排除合并严重心、肝、肺功能障碍,控制不良的高血压、糖尿病,妊娠期女性,未成年人,既往有腹部手术史,有后腹腔镜手术禁忌证,不能耐受全身麻醉等的患者。所有患者术前均对手术治疗方案知情同意,并签署知情同意书。本研究经医院伦理委员会批准后实施,符合伦理学原则。两组性别、年龄、体重、病变位置等一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 治疗方法
1.2.1 对照组 对照组患者接受常规开放手术治疗,行气管插管全身麻醉,取健侧卧位,于第11肋间或12肋下作一长18~22 cm的切口。直视状态下打开肾周筋膜,寻找肾脏。分离肾周脂肪,肾门处分离肾动静脉,分别切断、缝扎肾动静脉。如粘连严重或渗血较多者结扎肾动静脉,再于肾下极分离输尿管,尽量在远端切断并缝扎,防止尿液外漏引起感染播散,完整切除患侧肾脏后取出。切口放置引流管[2]。术后常规给予抗感染治疗,如无异常情况可拔除引流管。
1.2.2 试验组 试验组患者接受后腹腔镜包膜下肾切除术治疗。行气管插管全身麻醉,取健侧卧位,于十二肋缘下腋后线交叉点作一长约2 cm的纵行小切口(A点),采用血管钳钝性撑开肌层和腰背筋膜,手指钝性分离肌层、腰背筋膜、腹膜后间隙后,置入自制水囊注水300~500 mL,扩张腹膜后间隙,并建立腹膜后间隙手术操作空间。于腋中线至腋前线间髂嵴水平偏上1 cm处(B点)和腋前线肋缘下(C点)分别作10 mm、5 mm的小切口。在手指引导下插入Trocar,观察镜置于B点。以腰大肌作为解剖参照标准,仔细辨认腰大肌、腹膜外脂肪和腹膜,首先清理腹膜外脂肪,将其翻转置于髂窝内。如腹膜外脂肪较多,可将其游离后取出体外。靠在肾脏背侧采用超声刀纵行切开肾周筋膜,沿着肾实质表面寻找肾周脂肪囊和包膜之间的相对无血管平面。于肾门处游离肾动脉主干,肾动脉近心端采用2枚Ham-o-lok夹闭,远心端采用1枚Ham-o-lok夹闭后切断。同法处理肾静脉,肾静脉近心端采用2枚Ham-o-lok夹闭,远心端采用1枚Ham-o-lok夹闭后切断。伴有严重肾积水者可选择较薄的肾皮质处刺破以释放肾积水,吸干积液,以增加手术空间。打开肾包膜,在肾包膜和肾实质之间将无功能肾游离并切除,低位游离输尿管,近远端分别采用Ham-o-lok夹闭输尿管后离断。将切除的肾脏装入标本袋,经A点切口取出[3]。术后常规给予抗感染治疗,观察比较两组手术时间、住院时间、术中出血量等手术情况及术后并发症的发生情况。
1.3 统计学处理 相关数据均录入SPSS 17.0软件进行统计学处理,计量资料以(±s)表示,比较采用t检验。计数资料以率(%)表示,比较采用 字2检验。以P<0.05表示差异有统计学意义。
2 结果
2.1 两组手术情况比较 所有患者均成功完成肾切除手术,术后均达到一期愈合。试验组手术时间长于对照组,住院时间及术中出血量均较对照组少,两组比较差异均有统计学意义(P<0.05),见表1。
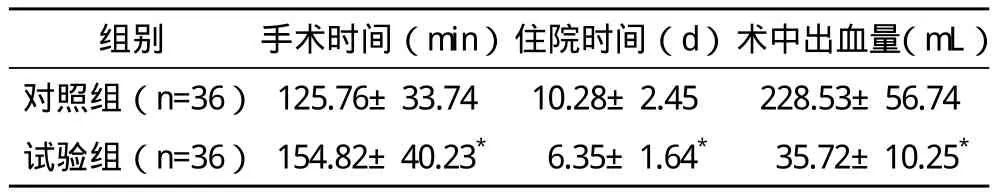
表1 两组手术情况比较(x-±s)
2.2 两组术后并发症发生情况比较 试验组术后并发症发生率明显低于对照组,比较差异有统计学意义(P<0.05),见表2。
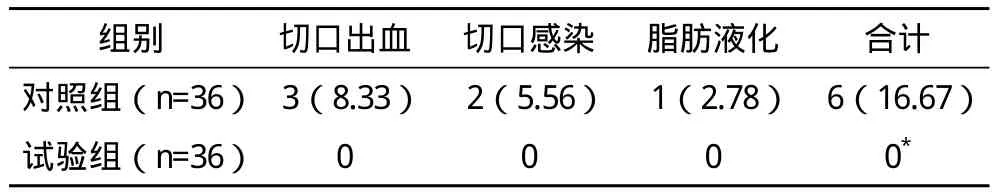
表2 两组术后并发症发生情况比较 例(%)
3 讨论
感染性无功能肾的临床治疗难度较大,因感染导致肾周组织发生广泛而致密的粘连,甚至累及肾周筋膜和肾周脂肪,使病灶周围正常的解剖层次消失,肾周组织和肾包膜无明显界限,在术中如强行分离易误入肾实质,导致大量出血而致手术视野不清,手术难度增加。如十二指肠、结肠等腹膜间位脏器和胰腺、脾脏等靠近腹膜后的脏器与肾周组织发生粘连,则损伤风险更大。在包膜下进行肾切除可避开粘连,减少手术风险[4]。
肾切除术是泌尿外科的常见术式之一,是将整个肾脏连同包覆其外的筋膜、输尿管上段、肾上腺、淋巴腺进行广泛性切除,是未转移的肾脏恶性肿瘤、无功能肾的首选手术治疗方案。传统的开放性手术经腹或经腰部切口入路,可以较好地切除肾脏,但手术切口长达二十多厘米,术中出血量大,术中可能需要输血治疗,术后疼痛剧烈,影响患者早期下床活动,延迟肠蠕动功能的恢复,存在着手术切口大、出血多、并发症多、术后恢复慢等缺陷,对患者造成了巨大的身心痛苦。近年来随着微创手术技术的发展,腹腔镜技术在泌尿系疾病的治疗中应用越来越广泛,技术也日趋成熟。经腹腔入路的腹腔镜肾脏切除术虽然气腹空间大、操作方便,但术中需要采用器械牵拉推开肾脏周围脏器,增加穿刺通道,且对腹腔干扰大,术后胃肠道功能恢复慢。后腹腔镜手术很好地解决了上述问题[5]。目前后腹腔镜手术在肾囊肿切除术、肾上腺肿瘤切除术方面可完全代替开放性手术。肾、肾上腺和输尿管等器官位于腹膜后,泌尿外科经腹膜后途径手术应用较多,可避免肠损伤、肠麻痹和腹膜炎等并发症风险[6]。后腹腔镜手术的优点是入路直接,不干扰腹腔内其他脏器,不会污染腹腔,减少了胃肠道反应、腹腔感染和粘连等风险[7]。感染性无功能肾经腹膜后途径进行肾切除效果较好,建立有效的后腹膜空间是后腹腔镜手术获得成功的关键[9]。
在开展后腹腔镜下肾切除技术时,术中首先扩张后腹膜间隙,操作时注意避免腹膜破裂。一旦发生腹膜破裂需要及时转开放手术治疗。后腹腔镜下肾切除手术要求手术操作者充分了解、正确辨认腹膜后各脏器的解剖位置关系,准确、迅速寻找腹腔镜下解剖标志与分离层面。一般以腰大肌作为基本标志寻找肾脏和输尿管[9]。在腹膜后水囊扩张完成后,应首先尝试分离肾周筋膜和脂肪囊,如粘连不严重且可分离出肾脏即行常规后腹腔镜肾切除,对肾脏的游离可在肾筋膜内进行[10]。如果伴有严重肾积水,可先刺破肾脏,释放出积水后,使手术空间明显增大,有利于后腹腔镜下对肾脏的游离。如粘连严重时考虑包膜下肾切除[11]。术中对于肾蒂的处理是确保后腹腔镜包膜下肾切除手术成功的关键,分离出肾脏动静脉后应先结扎、后离断。在接近肾门处切开肾包膜,离断肾动静脉和输尿管。分离肾门周围粘连时应选择超声刀进行安全分离,以防造成脏器和血管的意外损伤[12]。由于肾门周围有较厚的脂肪结缔组织,选择在接近肾门处切开肾包膜,暴露并分离肾蒂周围脂肪结缔组织,较厚的肾蒂逐渐变薄可游离并清晰暴露肾蒂血管,可用hemo-lock结扎夹分别离断肾动、静脉和输尿管。由于腹膜后气腹压力的关系,游离肾脏过程中不明显的出血点可能在气腹解除后出血,导致棘手的术后腹膜后腔渗液、积液,故游离肾脏时应边游离边仔细止血[13]。虽然包膜下肾切除游离肾实质时已将与肾包膜粘连毗邻的脏器旷置,但超声刀在分离肾门周围粘连时较电刀安全、术野亦更清晰[14]。由于超声刀的凝固或切割范围仅限于刀头的金属工作件和非工作件之间,没有能量弥散,不会造成脏器和血管的意外损伤;在肾周组织感染严重时,肾周解剖层次不清、瘢痕牵拉使肾蒂或与肾脏毗邻的脏器如肠管、胰腺、脾脏等的相对位置关系紊乱,超声刀的安全分离作用显得尤为重要,且超声刀无碳化、无烟雾,不影响手术视野,不造成额外损伤,比较适合腹膜后操作的需要[15]。
本研究中所有患者均成功完成肾切除,这一结果提示后腹腔镜包膜下肾切除术与常规开放手术具有同样良好的手术切除效果。所有患者切口均达到一期愈合,这一结果提示后腹腔镜包膜下肾切除术与常规开放手术具有同样满意的切口愈合效果。其中后腹腔镜下包膜下肾切除手术时间长于开放手术,比较差异有统计学意义(P<0.05),这一结果提示后腹腔镜手术需要建立腹膜后间隙,操作更加复杂,对手术操作者的技术要求也较高。后腹腔镜下包膜下肾切除患者住院时间明显短于开放手术患者,比较差异有统计学意义(P<0.05),这一结果提示后腹腔镜下包膜下肾切除患者术后康复更快,这与后腹腔镜下包膜下肾切除的手术切口微创有关。患者住院时间缩短后也会在一定程度上降低医疗费用,减轻患者及其家庭的经济负担。后腹腔镜下包膜下肾切除患者术中出血量明显少于开放手术患者,比较差异有统计学意义(P<0.05),这一结果提示后腹腔镜下包膜下肾切除患者切口更小,出血量少,术中对患者造成的损伤程度更小,对患者术后的康复进程更加有利。试验组术后并发症发生率明显低于对照组,比较差异有统计学意义(P<0.05),这一结果提示后腹腔镜下包膜下肾切除术无明显并发症,给患者造成的痛苦轻微,有利于术后的康复进程。
本次研究结果提示采取后腹腔镜下包膜下肾切除技术处理感染性无功能肾可以明显降低手术风险并达到治疗效果,相对于开放手术而言具有切口小、出血少、恢复快、并发症少等优点,是一种安全可靠的肾切除方法,对于无功能肾的后腹腔镜切除具有良好的应用前景。后腹腔镜下包膜下肾切除技术可缩短患者住院时间,降低治疗费用,且操作简便,各基层单位均可开展该技术,可解决感染性无功能肾的外科治疗这一技术难题,便于在基层单位的推广,可创造良好的社会效益和经济效益。
[1]毕海,侯小飞,马潞林,等.后腹腔镜手术切除结核性无功能肾与开放手术的临床比较[J].临床泌尿外科杂志,2010,25(12):902-905.
[2]谢永鹏,马鑫,高宇,等.后腹腔镜肾切除术治疗重度积水无功能肾(附36例报告)[J].微创泌尿外科杂志,2014,7(3):142-145.
[3]韦兴华,欧汝彪,杨文俊,等.后腹腔镜与开放肾切除术治疗重度积水无功能肾的疗效观察[J].国际医药卫生导报,2014,20(19):2930-2932.
[4]潘进洪,熊恩庆,沈文浩,等.后腹腔镜肾切除治疗结核性无功能肾临床分析[J].局解手术学杂志,2011,20(6):636-637.
[5]刘学进,张涛,熊建荣,等.后腹腔镜单纯性肾切除术治疗无功能肾26例报告[J].临床医学,2014,41(5):58-59.
[6]郑浩,李怀富,郑小青,等.后腹腔镜切除积水无功能肾17例[J].中华腔镜泌尿外科杂志(电子版),2011,5(5):379-381.
[7] Justinger C,Sperling J,Katoh M,et al.Retroperitoneal abscess with consecutive acute renal failure caused by a lost gallstone 2 years after laparoscopic cholecystectomy[J].Langenbeck’s Archives of Surgery,2010,395(3):285-287.
[8] Stein R J, Quinn PK,Berger M,et al.Laparoscopic ureterolysis with omental wrap for idiopathic retroperitoneal fibrosis[J].BJU International,2010,106(5):703-707.
[9] Tepeler A,Akman T,Tok A,et al.Retroperitoneoscopic nephrectomy for non-functioning kidneys related to renal stone disease[J].Urological Research,2012,40(5):559-565.
[10]白忠原,刘红艳,黄东龙,等.经腹膜后腹腔镜肾切除术35例临床分析[J].中国医学创新,2012,9(21):135-136.
[11]李金芳,文建军.后腹腔镜下肾切除15例报告[J].中国医学创新,2011,8(15):162-163.
[12]王德昕,单存密,柳荣强,等.后腹腔镜肾切除术86例临床体会[J].中国医学创新,2012,9(31):110-111.
[13]付承忠.肾脏炎性假瘤诊治分析[J].中外医学研究,2012,10(25):118-119.
[14]吴兆春,韩巧军.非特异性肾周围炎及肾周围脓肿诊治分析[J].中外医学研究,2014,12(31):51-53.
[15]杨丹丹,栾桂娟,蒋维,等.后腹腔镜肾癌根治术64例报告[J].中国医学创新,2010,7(34):174-175.

