β分子筛负载钒催化剂丙烷氧化脱氢制丙烯
范爱鑫,聂素双,傅吉全,张聚华
(北京服装学院 材料科学与工程学院,北京 100029)
丙烯是生产聚丙烯、丙烯醛、丙烯酸等的理想原料,在石油化工领域的需求量逐渐增加[1-2]。丙烷直接脱氢制丙烯在20世纪90年代实现了工业化,并成为丙烯生产的主要来源,但丙烷无氧脱氢是强吸热反应,反应温度达600 ℃以上才能获得相对较高的丙烷转化率。丙烷氧化脱氢反应副产物为H2O,是强放热反应,使得该反应在较低温度下即可进行,符合绿色化工的发展趋势。但该反应在氧的参与下,产物丙烯易发生深度氧化形成CO2,因此相比反应物,丙烷转化率、丙烯收率和催化剂的丙烯选择性是人们更加关注的指标。
目前,丙烷氧化脱氢反应主要以负载型V基催化剂为主,载体包括Al2O3,MgO,SiO2,TiO,ZrO2等[3-9]。一般认为该反应遵循Mars-Van Krevelen反应机理[10],参与丙烷中C—H键活化的是晶格氧物种,而高度分散、无定形的V-O物种更有利于丙烷氧化脱氢。汪玉等[11]将V负载在m-Al2O3上,其丙烷转化率和丙烯选择性均高于V/SiO2催化剂,这是由于m-Al2O3的大比表面积有利于V的高度分散形成孤立态V物种,同时载体一定的酸性位有利于吸附丙烷,起到了协同作用。β分子筛具有独特的三维十二元孔道结构[12],有很好的稳定性,在烷烃异构化、醚化 、酯化、芳烃烷基化等方面表现出很好的催化性能[13-16]。而关于β分子筛为载体用于丙烷氧化脱氢制丙烯的催化剂鲜有报道,其独特的孔道结构、不易积碳等特性是烷烃催化氧化中很好的载体。
本工作以V为活性组分,采用浸渍法制备以β分子筛为载体、V为活性组分的系列V/β催化剂,利用XRD,UV-Vis,BET,H2-TPR,NH3-TPD等手段对制得的催化剂进行表征,考察了V/β催化剂丙烷氧化脱氢制丙烯的催化性能。
1 实验部分
1.1 试剂
NH4VO3:分析纯,天津市光复科技发展有限公司;β分子筛:自制,粒径0.425~0.850 mm。
1.2 催化剂的制备
采用浸渍法制备不同V负载量的V/β系列催化剂。首先称取适量的NH4VO3于锥形瓶中,向其中加入50 mL蒸馏水,然后将锥形瓶置于70 ℃水浴锅中,溶解NH4VO3。溶解后将5 g β分子筛载体浸渍到溶液中,静置过夜,抽滤,于110 ℃下烘干10 h,烘干后的产物置于马弗炉中,在空气气氛下程序升温至600 ℃,最后在600 ℃下煅烧4 h得到不同V负载量的系列催化剂。V的负载量(w)为3%,5%,8%,11%的催化剂分别标记为3V/β,5V/β,8V/β,11V/β。
1.3 催化剂性能的评价
采用丙烷氧化脱氢制丙烯反应评价催化剂的性能,评价反应在固定床微型反应器中进行,反应器为内径8 mm的石英管,长度500 mm,催化剂填充量0.5 g,床层高度20 mm,置于反应器恒温段。原料气组成V(C3H8)∶V(O2)∶V(N2)=2∶1∶4,气体总流量70 mL/min。采用上海天美仪器公司的GC-7890Ⅱ型气相色谱仪在线分析反应尾气组成,HayeSep D型填充柱(3 mm×6 m),检测器TCD。气相色谱条件:载气为氢气,流量30 mL/min,柱温110 ℃,气化室温度120 ℃,检测室温度120℃,柱前压0.24 MPa,进样量0.5 mL。
1.4 试样的表征
采用北京彼奥德电子技术有限公司的MFA-140多功能吸附仪测定试样的BET,测试前试样在250 ℃下抽真空处理3 h;采用BET方法计算试样的比表面积;采用HK模型方法计算试样的孔体积和孔分布;采用理学公司的D/max-b型X射线衍射仪进行试样的物相分析,Cu Kα射线,管电压40 kV,管电流40 mA,2θ=10°~90°,扫描速率6(°)/min;采用PE公司Lambda 750紫外-可见光谱分析仪测定试样的UV-Vis DRS谱图,测量范围200~800 nm,高纯BaSO4为参比;采用天津先权公司的TP-5000型程序升温脱附仪测定试样的H2-TPR谱图,TCD进行检测,将0.1 g 试样颗粒放入石英管中,在高纯氮气氛围下于350 ℃下吹扫0.5 h,降至室温后通入5%(φ)H2-95%(φ)N2的还原气,流量30 mL/min,以10 ℃/min的速率从60 ℃升至900 ℃;采用天津先权仪器有限公司的TP-5000型程序升温脱附仪测定NH3-TPD曲线,TCD检测,试样在500 ℃氮气中预处理0.5 h,降温至60 ℃进行NH3吸附,吸附饱和后以10 ℃/min的速率升至100 ℃,停留0.5 h,然后升至600 ℃。
2 结果与讨论
2.1 试样的表征结果
2.1.1 BET表征结果
试样的孔结构数据见表1。由表1可知,β分子筛和所制备的V/β催化剂均为微孔结构,负载V后孔径均有所减小,说明负载的V进入分子筛孔道造成孔径变小。负载V后,8V/β催化剂的比表面积明显减小,其他V/β催化剂的比表面积则变化较小,这是由于8V/β催化剂中的V均匀负载到β分子筛的表面和孔道内。
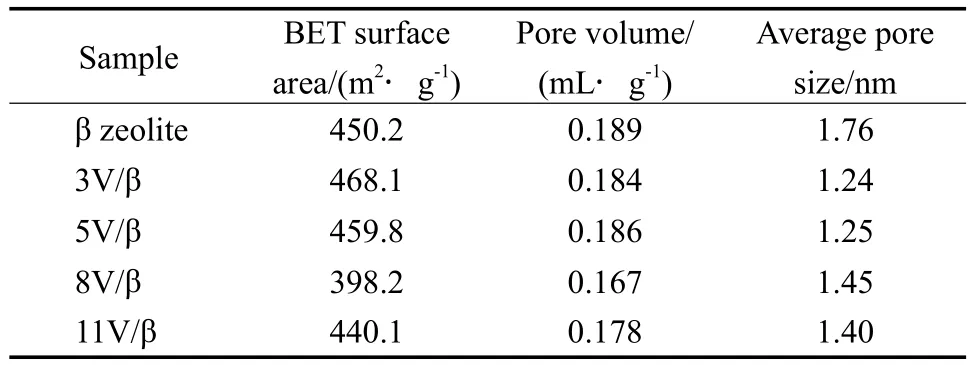
表1 试样的孔结构数据Table 1 Pore structures of samples
试样的N2吸附-脱附等温线见图1。由图1可知,5种试样均具有典型的H4滞后环[17],说明V/β催化剂的孔道均匀, 且孔分布较窄,有利于丙烷进入V/β催化剂孔道与活性组分发生作用,且产物丙烯容易脱附。
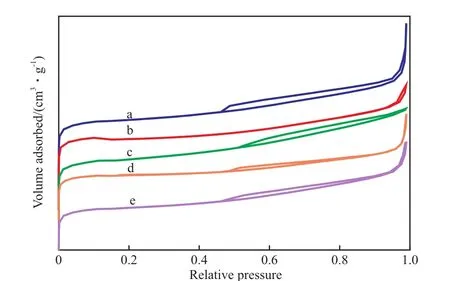
图1 试样的N2吸附-脱附等温线Fig.1 N2 adsorption-desorption isotherms of the samples.
2.1.2 XRD表征结果
试样的XRD谱图见图2。由图2可知,随V负载量的增加,β分子筛的一些特征峰强度减弱直至被覆盖,2θ=14°,15°,22.7°,29°,30°,44°处的峰形逐渐减弱直至完全被覆盖,汪玉等[11]研究xV/m-Al2O3催化剂时也发现类似变化,这可能与V氧化物对X光的吸收强于β分子筛、高负载量降低了催化剂有序性等有关。而4种V/β催化剂均未发现晶态V氧化物的特征峰,表明浸渍的V均以无定形或高度分散的氧化物状态存在,没有形成完整晶相的V2O5。
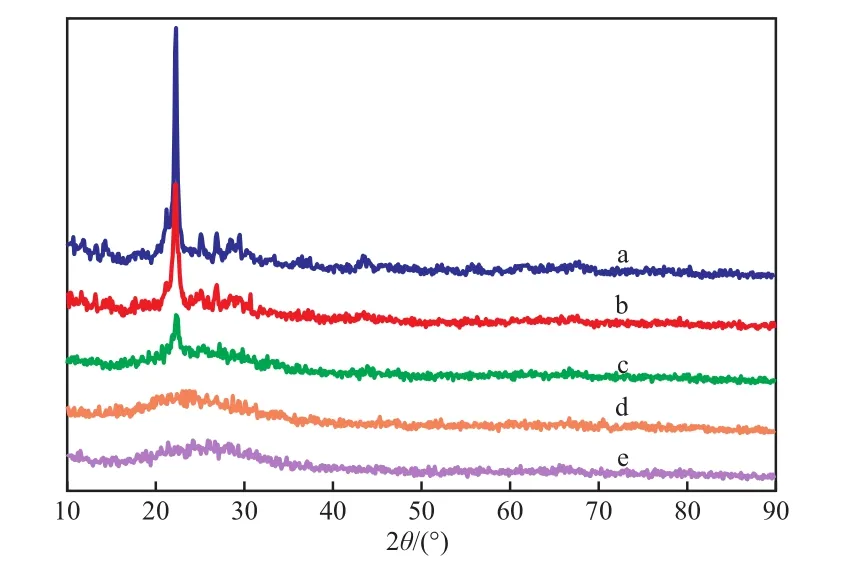
图2 试样的XRD谱图Fig.2 XRD patterns of the samples.
2.1.3 UV-Vis DRS表征结果
试样的UV-Vis DRS谱图见图3。从图3可看出,245 nm和280 nm处的吸收峰归属于高度分散的孤立四配位V5+物种(VO4)[18],320 nm处的吸收峰归属于低聚的四配位V5+物种,420 nm处的吸收峰归属于六配位的聚集态V物种,420 nm处吸收峰强度随V负载量的增加而增强,说明V聚集态增加,而始终未出现晶态V物种的吸收峰,表明V物种均以高度分散的孤立四配位V5+物种和低聚的四配位V5+物种存在,此结论与XRD测试未检出完整晶相的V2O5相吻合。
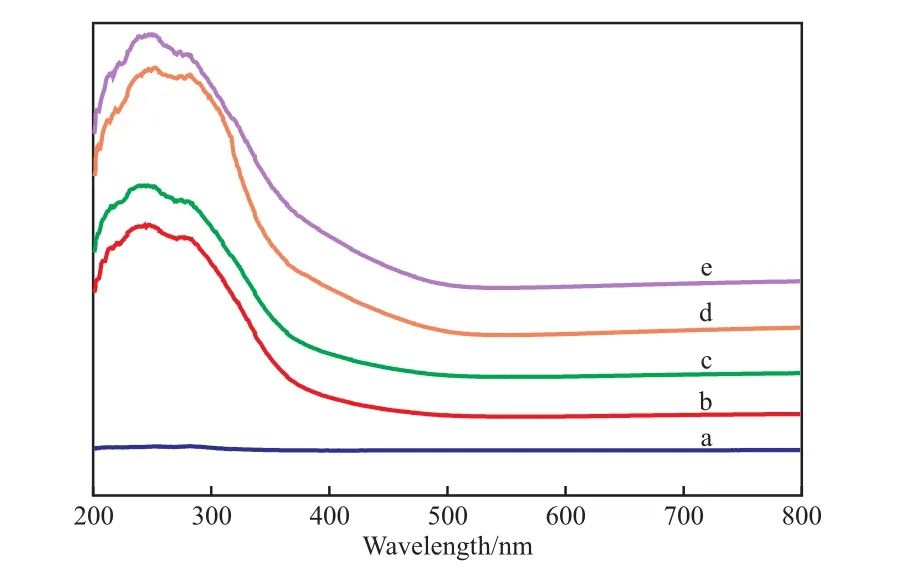
图3 试样的UV-Vis谱图Fig.3 UV-Vis patterns of the samples.
2.1.4 H2-TPR表征结果
试样的H2-TPR谱图见图4。由图4可知,β分子筛本身未出现还原峰,当V负载量从3%(w)增至8%(w)时,V/β催化剂最高还原峰温度从554 ℃降至545 ℃,当V负载量为11%(w)时还原峰温度升至565 ℃。较低负载量时V主要以高度分散的孤立四配位V5+形态存在,随V含量的增加,易还原的二维链状聚集态V 物种增加, 由于聚集态V物种的V—O键强度相对较弱,还原峰温度低移,V负载量为11%(w)的V/β催化剂还原峰温度升至565 ℃,与V物种聚集形成类V2O5微晶体有关,此结果与UV-Vis DRS变化规律一致。
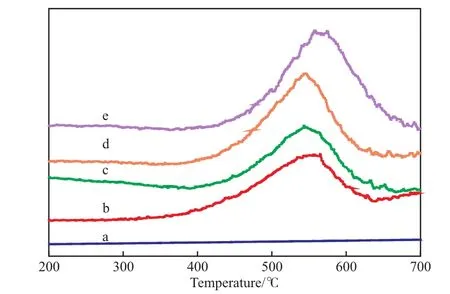
图4 试样的H2-TPR谱图Fig.4 H2-TPR curves of the samples.
2.1.5 NH3-TPD表征结果
试样的NH3-TPD谱图见图5。由图5可知,β分子筛具有两个NH3的脱附峰,200 ℃处出现了归属于弱酸性位NH3脱附峰,是吸附的NH3从弱酸中心Si—O—Si上脱附时产生的脱附峰,350 ℃出现了归属于强酸性位NH3脱附峰,是吸附的NH3从强酸中心(主要与骨架Al有关)上脱附时产生的脱附。随V负载量的增加,弱酸性位脱附峰增强,强酸性位脱附峰减弱,当V负载量达到11%(w)时,V/β催化剂强酸性位脱附峰几乎消失,表明负载的V覆盖了部分β分子筛自身的酸性位,并在β分子筛表面产生弱酸性位。
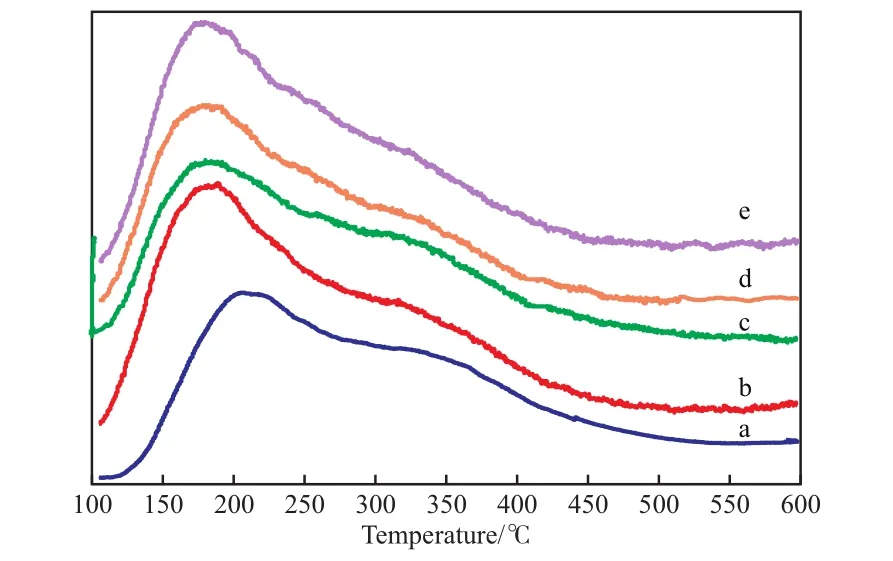
图5 试样的NH3-TPD谱图Fig.5 NH3-TPD curves of the samples.
2.2 催化剂性能的评价结果
不同V负载量的V/β催化剂催化丙烷氧化脱氢制丙烯的反应结果见表2。由表2可知,丙烷转化率和丙烯选择性随温度的升高均提高,表明高温有利于烷烃的活化,使反应变易。β分子筛单独作为催化剂时也有一定的活性,450 ℃时选择性达49.4%,高于同类分子筛,这与β分子筛独特的孔结构和本身的酸性位有关,500 ℃时丙烯选择性为39.5%,较450 ℃时有所下降,这是由于β分子筛酸性较强,较高温度时产物丙烯未及时脱附而发生深度氧化生成了CO2。负载一定量V的V/β催化剂上丙烷转化率和丙烯选择性均提高,根据Mars-Van Krevelen氧化还原机理,丙烷氧化脱氢反应中C—H键的活化需要晶格氧的参与,V氧化物种具有活泼的V—O键,能迅速发生氧化还原反应,因而具有很高的催化活性。与β分子筛相比,500 ℃时8V/β催化剂的丙烷转化率(13.4%)、丙烯选择性(63.2%)均最佳,表明负载的V掩盖了一定的V/β催化剂和β分子筛酸性位,使产物丙烯的脱附变得容易。
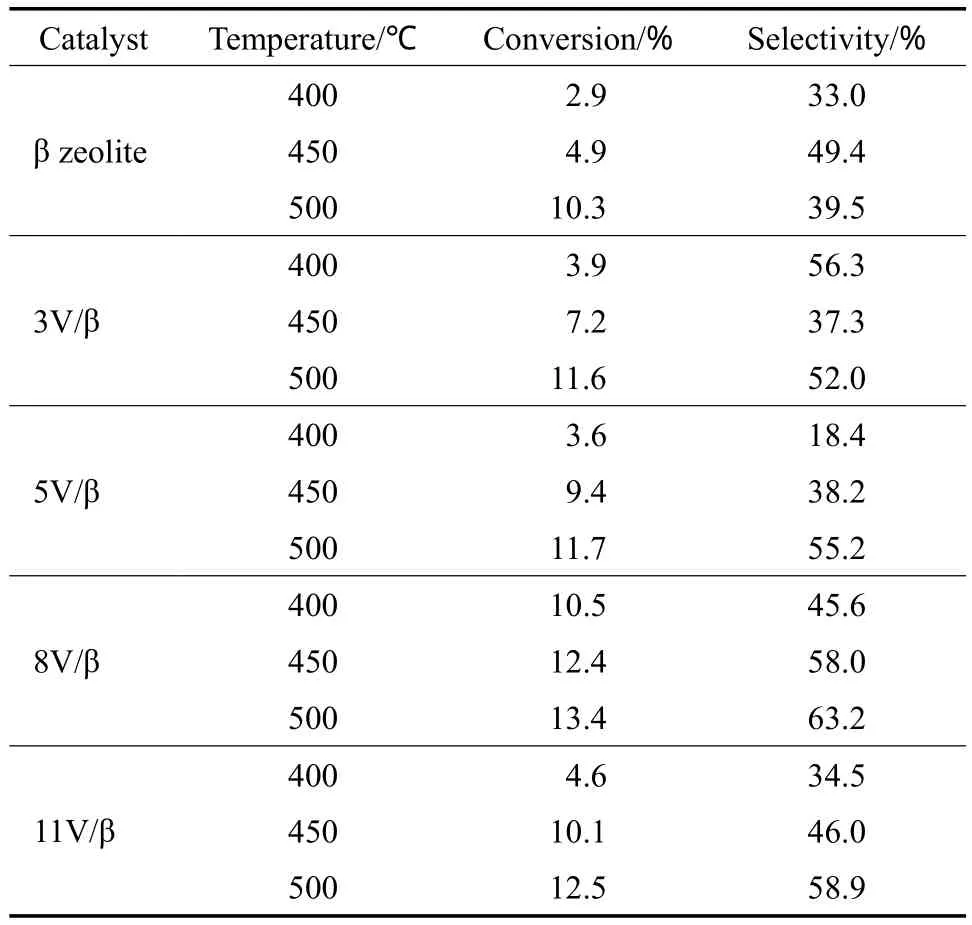
表2 不同V负载量的V/β催化剂上丙烷氧化脱氢制丙烯的反应结果Table 2 Oxydehydrogenation of propane to propene over the catalyst samples
3 结论
1)V/β催化剂的孔道均匀, 孔分布窄,有利于丙烷进入催化剂孔道与活性组分发生作用。
2)β分子筛负载较低V时催化剂中V物种主要以高度分散的孤立四配位V5+形态存在;随负载V含量的增加,二维链状聚集态V物种增加;负载V过多时易形成晶相V2O5。
3)负载的V覆盖了部分β分子筛自身的酸性位,并在β分子筛表面产生弱酸性位,使丙烯的脱附变易,提高了丙烷转化率和丙烯选择性。
4)8V/β催化剂在V(C3H8)∶V(O2)∶V(N2)=2∶1∶4、气态空速8 400 h-1、500 ℃时,丙烯选择性达到63.2%。
[1]Hugo Zea,Luis Carballo.Oxidative Dehydrogenation of Propane on Pd-Mo/γ-Al2O3Catalyst:A Kinetic Study[J].Aust J Basic Appl Sci,2015,9(5):78-83.
[2]陈硕,王定博,吉媛媛,等.丙烯为目的产物的技术进展[J].石油化工,2011,40(2):217-224.
[3]Meilana D P,Saeed M,Al-Zahrani,et al.Oxidative Dehydrogenation of Propane to Propylene over Al2O3-Supported Sr-V-Mo Catalysts[J].Catal Commun,2011,14(1):107-109.
[4]Argyle M D,Chen Kaidong,Bell A T,et al.Effect of Catalyst Structure on Oxidative Dehydrogenation of Ethane and Propane on Alumina-Supported Vanadia[J].J Catal,2002,208(1):139-141.
[5]Puglisi M,Arena F,Frusteri F,et al.Effect of Vanadia Loading in Propane Oxidative Dehydrogenation on V2O5/SiO2Catalysts[J].Catal Lett,1996,41(1/2):41-43.
[6]Comite A,Sorrentino A,Capannelli G,et al.Oxidative Dehydrogenation of Propane Using V2O5/TiO2/SiO2Catalysts Prepared by Grafting Titanium and Vanadium Alkoxides on Silica[J].Catal Lett,2003,198(1/2):151-153.
[7]Machli M,Lemonidou A A.Optimization of V2O5-MgO/TiO2Catalyst for the Oxidative Dehydrogenation of Propane Effect of Magnesia Loading and Preparation Procedure[J].Catal Lett,2005,99(3/4):221-225.
[8]De M,Kunzru D.Oxidative Dehydrogenation of Propane on V2O5/ZrO2Catalyst[J].Catal Lett,2004,96(1/2):33-35.
[9]张伟德,沙开清,李基涛,等.V2O5/MPO4在丙烷氧化脱氢中的催化作用[J].石油化工,1999,28(3):141-144.
[10]Creaser D,Andersson B.Oxidative Dehydrogenation of Propane over V-Mg-O:Kinetic Investigation by Nonlinear Regression Analysis[J].Appl Catal,A,1996,141(1/2):131-152.
[11]汪玉,谢颂海,岳斌,等.介孔氧化铝负载钒催化剂上丙烷氧化脱氢制丙烯[J].催化学报,2010,31(8):1054-1060.
[12]Martens J A,Jacobs P A.The Potential and Limitatoins of the n-Decane Hydroconversion a Test Reaction for Characterization of the Void Space of Molecular Sieve Zeolites[J].Zeolites,1986,6(5):334-348.
[13]Sambhu Radhakrishnan,Martin Purino,Konstantinos Alexopoulos,et al.Selective Etheri fi cation of β-Citronellene Catalyzed by Zeolite Beta[J].Green Chem,2015,17(5):2840-2845.
[14]Srivastava R,Iwasa N,Fujita S,et al.Dealumination of Zeolite Beta Catalyst Under Controlled Conditions for Enhancing its Activity in Acylation and Esterification[J].Catal Lett,2009,130(3/4):655.
[15]Silva-Machado M D,Cardoso D,Pérez-Pariente J,et al.Esterification of Lauric Acid with Glycerol Using Modified Zeolite Beta as Catalyst[J].Stud Surf Sci Catal,2000,130(12):3417-3422.
[16]Primo Ana,Garcia Hermenegildo.Zeolites as Catalysts in Oil Re fi ning[J].Chem Soc Rev,2014,43(22):7548-7561.
[17]徐如人,庞文琴.分子筛与多孔材料化学[M].北京:科学出版社,2004:145-146.
[18]Fornes V,Lopez C,Lopez H H,et al.Catalytic Performance of Mesoporous VOx/SBA-15 Catalysts for the Partial Oxidation of Methane to Formaldehyde[J].Appl Catal,A,2003,249(2):345-354.

