体内探针药物法研究巴戟天低聚糖对大鼠CYP3A4的影响
邓少东,卢洪梅,林 励,林靖然,张 鹏
(1.广东医学院 第二临床医学院,广东 东莞 523808;2.广州中医药大学 中药学院,广东 广州 510006)
体内探针药物法研究巴戟天低聚糖对大鼠CYP3A4的影响
邓少东1,卢洪梅1,林 励2,林靖然2,张 鹏2
(1.广东医学院 第二临床医学院,广东 东莞 523808;2.广州中医药大学 中药学院,广东 广州 510006)
目的:研究巴戟天低聚糖(BD)及其活性成分巴戟甲素(BJ)对肝药酶CYP3A4的影响。方法:采用固相萃取法处理血样,UPLC测定探针药物氨苯砜在大鼠体内的血药浓度,采用DAS2.0软件计算药动学参数并进行比较分析。结果:BD对CYP3A4有显著的诱导作用,而BJ对CYP3A4有抑制作用。结论:巴戟天中含有大量对CYP3A4有诱导作用的低聚糖类成分,与其他通过CYP3A4酶代谢的药物合用时需注意配伍禁忌。
巴戟天;低聚糖;巴戟甲素;肝药酶CYP3A4
肝脏是重要的药物代谢器官,是药物生物转化的主要场所,其中细胞色素P450酶(CYP450)是肝脏中重要的代谢外源性和内源性化合物的混合功能氧化酶系,同时在激活各种毒性物质及前致癌物中发挥着重要作用[1]。CYP450酶系活性的改变可影响外源物的代谢,进而对其药理或毒理活性产生影响。在机体中,大部分处方药均需要在CYP450酶系统参与下通过Ⅰ相和Ⅱ相代谢反应进行生物转化。CYP450同工酶易受到药物或其他化合物的诱导或抑制,这是药物间发生相互作用的主要原因。其中CYP450中的亚型酶CYP3A4是人类肝脏中重要的代谢酶,约有55%药物经CYP3A4代谢[2]。CYP450酶的活性可通过一些特异性敏感底物来测定,称为探针药物法,是测定其相关亚型酶活性的常用方法[3-4],其中氨苯砜为CYP3A4常用的探针药物[5-6]。
巴戟天为茜草科植物巴戟天MorindaofficinalisHow.的肉质根,归肾、肝经,自古被誉为“补肾阳之要药”,是我国著名的“四大南药”之一。巴戟天无论是组方配伍的汤剂,还是提取物制成的制剂、保健品等,均已被广泛应用。然而至今还未发现关于巴戟天中有效成分对CYP450主要亚型酶活性影响的系统研究。因此,本实验以氨苯砜为探针底物,考察巴戟天低聚糖提取物(BD)及其主要活性成分巴戟甲素(BJ)对CYP3A4活性的影响,以预测其联合应用CYP3A4亚型酶代谢型药物时发生相互作用的可能性,从而为该药的开发及临床合理应用提供科学依据。
1 材料与试剂
1.1 试药
巴戟天低聚糖提取物(自制,纯度>98%);巴戟甲素(按专利201010224513.2方法自制,纯度>98%);氨苯砜对照品 (美国Sigma公司,纯度98%,批号:SZBC072XV);内标为苯巴比妥(中国食品药品检定研究院,纯度99%,批号:171222-200605);乙腈、甲醇(色谱纯,德国Merkel公司),其他试剂均为国产分析纯;实验用水为自制超纯水。
1.2 仪器
美国Waters ACQUITY UPLC系统(QSM四元溶剂管理系统、FTN样品管理系统自动进样器、CH-A型柱温箱、UPLC专用二极管阵列检测器、真空脱气机、Empower3 色谱工作站);BP211D型十万分之一电子天平(德国Sartorius公司);KQ-500型超声波清洗器(昆山市超声仪器有限公司);Genpure超纯水系统(德国TKA公司);Cleanerrt固相萃取柱(天津博纳艾杰尔科技有限公司,C18,50~100mg);12位负压SPE固相萃取装置(天津博纳艾杰尔科技有限公司);MTN-2800D型氮吹仪(天津奥特赛恩斯仪器有限公司);佳美SK-1快速混匀器(江苏金坛市佳美仪器厂);TGL-16aR型台式离心机(上海安亭科学仪器厂)。
1.3 动物
雄性SD大鼠,18只,体重200~250g,由广州中医药大学实验动物中心提供[许可证号:SCXK(粤)2008-0020],实验前动物禁食12h,自由饮水。
2 方法与结果
2.1 分组、给药及样品采集
将18只SD大鼠随机分为空白对照组、巴戟天低聚糖提取物组(BD组)、巴戟甲素组(BJ组),每组6只。BD组大鼠每天清晨按240mg·kg-1的剂量灌胃给药,BJ组大鼠按80mg·kg-1的剂量灌胃给药,空白对照组大鼠按10mg·kg-1的剂量灌胃给药,连续给药14天。于第15天清晨尾静脉注射探针药物氨苯砜,按照4mg·kg-1的剂量给药,于探针给药后0、2、5、10、30、60、90、120、240、360、480、600min从大鼠眼底静脉丛采血,每次采血约0.5mL,静置30min,再以3 000rpm·min-1转速离心5min,取出上清液,于-80℃冰箱中保存。
2.2 固相萃取柱活化
取C18固相萃取小柱,加入4mL甲醇活化,再加入超纯水4mL平衡萃取柱,最后加入5%甲醇4mL冲洗萃取柱,备用。
2.3 血样前处理
精密吸取含药血清200μL,加入800μL超纯水和40μL内标溶液(含苯巴比妥105μg·mL-1),涡旋混匀30s后,加入已活化的C18固相萃取小柱中,静置5min后,加入1mL超纯水,以2mL·min-1流速洗脱杂质,再加入2mL甲醇以0.5mL·min-1流速洗脱目标物,收集洗脱液,氮气吹干,残留物中精密加入200μL甲醇涡旋溶解,待测。
2.4 色谱条件
ACQUITY UPLC BEH C18色谱柱(3.0mm×100mm,1.7μm);流动相:乙腈-0.1%乙酸水溶液(36∶64),等度洗脱;流速:0.3mL·min-1;柱温:30℃;检测波长:258nm;进样量:2μL。
2.5 方法学考察
2.5.1 专属性实验 分别取空白血清、空白血清+氨苯砜+内标、注射氨苯砜后采集的血清,按照“2.3”项下方法处理,进样分析。结果显示,氨苯砜和内标苯巴比妥的保留时间分别为2.452、3.072min,两个色谱峰互不干扰且血清中内源性杂质不影响分析物的测定,具有良好的特异性和分离度(见图1)。
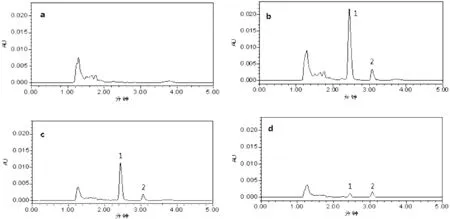
图1 专属性实验色谱
注:a.空白血清;b.空白血清+氨苯砜+内标;c.给药后10min;d.给药后10h;1.氨苯砜;2.苯巴比妥
2.5.2 标准曲线制备 精密称取氨苯砜对照品适量,加入超纯水溶解配制得4μg·mL-1的对照品储备液。分别取上述对照品储备液0.625、1.25、2.5、5、10、20mL置于2mL容量瓶中,以超纯水定容至刻度,摇匀,配制得浓度分别为0.125、0.25、0.5、1、2、4μg·mL-1的氨苯砜对照品工作液。精密吸取以上6种浓度的工作液各200μL,分别加入200μL空白血清、600μL超纯水和40μL内标溶液(含苯巴比妥105μg·mL-1),按照“2.3”项下方法处理, 进样分析,记录色谱图。以氨苯砜浓度X(μg·mL-1)为横坐标,氨苯砜和内标峰面积的比值Y为纵坐标绘制标准曲线,得回归方程:Y= 2.039 3X -0.079 1(r=0.998 7)。结果表明,氨苯砜血药浓度在0.125~4μg·mL-1范围内与峰面积比值线性关系良好。
2.5.3 精密度与回收率 精密吸取“2.5.2”项下配制的0.125、1.000、4.000μg·mL-1对照品工作液各200μL,分别加入200μL空白血清、600μL超纯水和40μL内标溶液(含苯巴比妥105μg·mL-1),按照“2.3”项下方法处理,平行制备5份,于同一天内测定5次和连续5天分别测定1次,计算日内和日间精密度,以RSD表示。以测得浓度与配制的理论浓度进行比较,计算该方法的回收率。结果显示(见表1),探针药物的日内、日间精密度RSD均<10%,表明该实验精密性良好。探针药物在低、中、高3个质量浓度的样品中回收率均介于81. 87%~104. 31%之间,符合药动学样品测定的要求。

表1 精密度与回收率试验结果 (n=5)
2.5.4 样品稳定性 取给予探针药物10、240、600min后采集的血清适量,按照“2.3”项下方法处理,于室温中放置。分别取以上3个不同时间点制备的样品于1、2、4、8、12h后分别进样分析,计算各时间点氨苯砜的浓度,以放置12h内各样品浓度的RSD表示其稳定性。结果显示(见表2),3个不同时间点所采集的样品在12h内进样,氨苯砜浓度的RSD均在5%之内,表明在该实验条件下,血清样品在12h内稳定性良好。

表2 稳定性试验结果
2.6 统计学方法
2.7 探针药物药-时曲线
空白对照组、BD组、BJ组SD大鼠尾静脉注射氨苯砜后,按照“2.1”及“2.3”项下方法操作,测得其血药浓度。结果见表3、图2。
表3 各组大鼠不同时点测得探针药物血中浓度

组别时间t(min)2510306090120240360480600空白组0.60±0.121.87±0.183.09±0.442.12±0.131.82±0.161.45±0.201.34±0.130.99±0.150.82±0.120.49±0.070.35±0.05BD组0.48±0.051.04±0.132.51±0.711.89±0.481.52±0.291.20±0.2880.91±0.160.60±0.120.39±0.090.27±0.060.14±0.03BJ组0.39±0.031.38±0.111.95±0.211.28±0.091.18±0.081.15±0.071.00±0.160.84±0.120.59±0.030.47±0.050.31±0.04
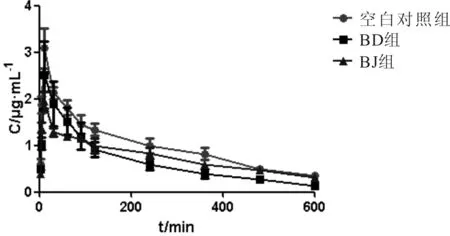
图2 探针药物的平均药-时曲线
2.8 探针药物动学参数
采用DAS2.0软件处理氨苯砜药动学数据,经拟合后,氨苯砜的药-时曲线符合一房室模型,空白组、BD组、BJ组的权重分别为1/CC、1/CC、1。同时采用非房室模型统计矩原理计算得各项参数,结果见表4。
采用SPSS19.0进行单因素方差分析,结果显示:与空白组比较,BD组大鼠t1/2、MRT0-∞均显著降低(P<0.05);而BJ组大鼠t1/2、MRT0-∞均显著增加(P<0.01)。经过综合分析,巴戟天低聚糖部位对CYP3A4有显著的诱导作用,而巴戟甲素对CYP3A4有显著的抑制作用。
表4 大鼠血液中探针药物动力学参数 ±s,n=6)
注:△P<0.05,△△P<0.01 vs 空白组。
3 讨论
本实验建立的固相萃取-超高效液相色谱法适用于血液中氨苯砜浓度的测定,其专属性强、精密度好、回收率高。本研究采用体内探针药物法评价了巴戟天低聚糖部位和巴戟甲素对CYP450酶系的影响。在非房室模型分析中,MRT是一个非常重要的参数,由于药物代谢遵从“对数-正态分布”,静脉注射给药时MRT表示的是药物被机体消除给药剂量的63.2%所需要的时间。通过对半衰期t1/2与平均滞留时间MRT0-∞进行综合分析,表明巴戟天低聚糖部位对CYP3A4有显著的诱导作用,而巴戟甲素对CYP3A4有显著的抑制作用,提示巴戟天低聚糖部位中可能还含有大量对CYP3A4有较强诱导作用的低聚糖类成分。
作为原料药,巴戟天提取物在中药组方配伍、制药、保健品开发中被广泛应用。在临床用药中,巴戟天可能与其他药物联合用药,值得注意的是,在与其他通过CYP3A4酶代谢的药物合用时,需密切监测血药浓度,根据药动学参数调整给药方案。
[1] OMURA T. Heme-thiolate proteins[J]. Biochem Biophys Res Commun, 2005, 338(1):404.
[2] 刘高峰,甄立棉,黄丽军. RP-HPLC法同时测定家兔体内氨苯砜、咖啡因和美托洛尔的含量[J].药物分析杂志,2010(12):2263.
[3] 和凡,赵立子,毕惠嫦,等. 6种细胞色素P450酶亚型特异性底物的酶动力学研究[J].中国药房,2009,20(17):1310.
[4] 张鉴,彭向前,李军.咖啡因探针法测定正常人肝脏药物代谢酶 CYP1A2活性[J].中国药房,2005,16(16):1216.
[5] 谢建芬,陈荣,夏宗玲,等.HPLC法测定人血清中CYP3A4探针药物氨苯砜的浓度[J].中国药房,2011,18(10):889.
[6] 扈金萍,闫淑莲,徐艳霞,等.反相高效液相色谱法同时检测3种探针药物[J].色谱,2002,20(6):540.
(责任编辑:尹晨茹)
Effect of Oligosaccharides from Morinda Officinalis on CYP3A4 Using the Probe Drug Method in Vivo
Deng Shaodong1, Lu Hongmei1, Lin Li2, Lin Jingran2, Zhang Peng2
(1.The Second School of Clinical Medicine,Guangdong Medical College,Dongguan 523808,China;2.College of Chinese Materia Medica,Guangzhou University of Traditional Chinese Medicine,Guangzhou 510006,China)
Objective:To investigate the effects of BD and BJ on CYP3A4 for the safety assessment.Methods:Plasma was treated by SPE. The plasma concentration of probe drug dapsone was determinated by UPLC. The pharmacokinetic parameters were calculated by DAS2.0.Results:BD induced CYP3A4 in vivo while BJ inhibited CYP3A4.Conclusion:Oligosaccharides of Morinda officinalis contain a lot of Oligosaccharides that can induced CYP3A4 in vivo.When Oligosaccharides of Morinda officinalis are used combined with other drugs which are metablized by CYP3A4 enzyme, the different effects should be considered to avoid the potential adverse reactions.
MorindaofficinalisHow.;Oligosaccharide; Bajijiasu;CYP3A4
2015-04-01
国家自然科学基金项目(81403085);东莞市医疗卫生科技计划一般项目(2014105101295);广东医学院科研基金博士学位人员科研启动项目(B2013007)
邓少东(1986-),男,广东医学院博士,研究方向为中药资源开发利用与新药研发。
R285.5
A
1673-2197(2015)17-0005-04
10.11954/ytctyy.201517003

