新鲜全血在不同血液分析仪比对试验中的应用
陈立松,周芹
(阜宁县沟墩医院检验科,江苏 阜宁 224433)
血液分析仪广泛运用在各级医院的临床检验中,伴随着工作量的增加,同一实验室同时使用不同品牌或同一品牌不同型号的血液分析仪的现象已很普遍。由于不同型号的血液分析仪因检测方法和检测原理不尽相同,对同一标本的测定结果必然存在着系统误差[1],所以关注检验结果的溯源性和可比性,提高血细胞分析系统的可比性非常重要[2]。我们自2008年以来试用新鲜抗凝全血在两台血液分析仪之间进行结果比对,经过几年的改进和完善,现已形成了一套较为规范的科内血液分析仪比对操作程序,取得了较为满意的临床效果。
1 材料与方法
1.1 材料
1.1 .1仪器与试剂 血液分析仪2台,分别为Sysmex XS-800i(日本希森美康公司)和BC-5300(深圳迈瑞公司)。所用试剂均为仪器配套试剂。
1.1 .2校准品和质控物 仪器均使用各自配套的校准品和质控物。
1.1 .3比对物 EDTA-K2抗凝的新鲜全血。为了避免抗凝剂、温度等各方面的影响[3,4],每次所有标本的检测均在2h内完成。
1.2 方法
1.2 .1比对前的仪器准备 为保证结果的准确性和重复性,要求室温20~250C,湿度小于80%。试验前每台血液分析仪进行日保养,以去除管道中残留的血液、吸附的蛋白纤维等,确保管路通畅和清洁,然后做空白计数和携带污染率测定,本底和携带污染率必须符合要求。
1.2 .2精密度测定 取新鲜抗凝全血2份,分别在两台仪器上重复检测11次,计算第2~11次结果的白细胞、红细胞、血红蛋白、平均红细胞体积和血小板的均值(x)、标准差(s)及变异系数(CV%)。
1.2 .3参比仪器的确定与校准 我们以多年参加室间质评且成绩优秀的Sysmex XS-800i血液分析仪作为参比仪器,并用配套的校准品进行校准。
1.2 .4比对方法 取5份新鲜抗凝全血标本(低值1份,正常参考范围内2份,较高1份,高值1份),按照仪器的操作规程在试验仪器和参比仪器上平行测定,每份标本测定两次(顺序1,2,3,4,5,5,4,3,2,1),结果取两次的均值,第二天以同样的方式再测5份标本,计算10份标本在试验仪器和参比仪器上各参数测定结果的平均相对偏差。相对偏差=(试验仪器测定值-参比仪器测定值)/参比仪器测定值。
1.2 .5统计学处理 依据实验结果求出回归方程,分析试验仪器和参比仪器的相关性。
1.2 .6评价标准 仪器精密度评价参照美国临床实验室标准化协会(CLSI)实验室改进修正案(CLIA’88)规定的室间质量评价标准允许误差的1/4作为判定规则,即CV值满足:WBC≤3.75%、RBC≤1.5%、Hb≤1.75%、MCV≤1.5%、PLT≤6.25%;仪器比对的相关系数参照ICSH和NCCLS制定的标准作为判定规则:r>0.95;不同血液分析仪之间各指标的评价依据CLIA,88规定的允许误差的1/2作为判定规则:采用 WBC≤±7.5%、RBC≤±3.0%、Hb≤±3.5%、MCV≤±3.0%、PLT≤±12.5%。
1.2 .7试验仪器的调整 如果试验仪器和参比仪器参数的相关系数或平均相对偏差超过质量控制范围,需要对试验仪器进行校准。(1)采集同一健康人新鲜抗凝血2份,分别在参比仪器和试验仪器上连续测定11次,计算2~11次各参数测定结果的均值,并以参比仪器的结果作为试验仪器各参数的靶值。(2)调整系数=靶值/测定值×原系数。如果靶值/测定值大于1.1或小于0.9,需工程师进行仪器维护或维修。(3)系数调整后应重新做比对试验,保证质量控制指标在允许范围之内。
2 结果
2.1 两台仪器的精密度测定结果 见表1。

表1 仪器精密度测试的变异系数(CV%)
2.2 两台仪器相关性及平均相对偏差 见表2。
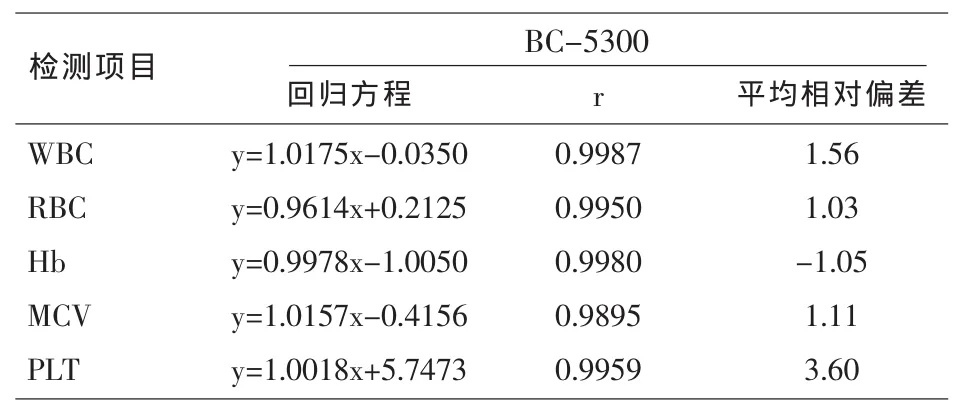
表2 实验仪器与参比仪器相关性比较及平均相对偏差(%)
3 讨论
血液分析仪比对结果的评价应包括仪器的日保养、空白计数、携带污染率、准确度和精密度、可测定范围以及比对期间室内质量控制的监测等,在保证仪器运行正常的情况下,综合评价各仪器质量控制指标,对质量指标超过控制范围,应查找原因,必要时对仪器进行检修或校准,特别是参比仪器应溯源至国际标准或使用溯源至国际标准的二级标准检测系统[5]。从表1可以看出,在仪器的本底及携带污染率均符合要求的前提下,两台仪器测定的WBC、RBC、Hb、HCT和PLT的精密度均在CLIA’88规定的1/4允许误差的可接受范围内,最大CV值为BC-5300的PLT 3.48%,各仪器测定结果的重复性好,具备仪器比对的前提条件。从仪器角度分析XS-800i的精密度稍好于BC-5300。
实验方面,我们采用不同水平的全血标本、连续两天的均值作为靶值进行比对,增加试验的客观性。表2的结果显示,本次比对(2013.09.21-22)试验仪器的各项参数与参比仪器具有良好的相关性,r值均>0.98,各参数与参比仪器的平均相对偏差均在CLIA’88规定允许误差的1/2范围内,最高为PLT 3.60%。试验仪器与参比仪器检测结果的相对偏差在允许范围内,各参数的系数无需调整。综合以上结果还可以发现,血小板计数结果在两台仪器上的差异较大,这是由于血小板在自动化分析过程中可能受多种因素的影响所致。日本临床实验室标准化委员会 (JCCLS)规定不同血液分析仪血小板测定的最大误差为10%,这也从另一侧面说明不同血液分析仪在保证血小板测定结果的一致性具有一定难度。随着新技术原理的血液分析仪相继问世,此问题会有良好的解决办法。
血液分析仪检测结果的准确性直接影响患者疾病的诊断和疗效监测,不同检测系统对同一份标本的同一项目的检测结果应具有溯源性和可比性[6],而不同的血液分析仪不可避免的均存在系统误差,因此,同一实验室同时使用多台血液分析仪,除了有完整的质量控制体系,还应定期用可溯源的血液检测系统对其他仪器进行比对,保证不同检测系统间结果的准确性和一致性[7]。新鲜抗凝全血为仪器间的比对提供了简便可行的途径,特别是小型实验室更可以用周边大型实验室“定值”的新鲜抗凝全血校准或比对仪器,既方便又经济,也有利于实现溯源标准的传递以及不同级别实验室之间结果互认。
[1]彭文红,兰晓梅,王海,等.不同血细胞分析仪多水平比对试验方案的建立和应用[J].军医进修学院学报,2010,31(12):1224-1226.
[2]胡绿荫,杨冀,吴文娟.两种血细胞分析系统检测结果的可比性研究[J].现代检验医学杂志,2011,26(5):115-118.
[3]肖木洲,郑惠红,梁淑慧,等.静脉血标本静置时间对血细胞分析仪测定结果的影响[J].实用医学杂志,2006,22(15):1822-1823.
[4]陈黔,唐斌,沈毅,等.对BC-3000plus全自动血液分析仪测定结果的影响因素分析和对策[J].医疗卫生装备,2010,31(11):111-112.
[5]彭明婷,申子瑜.血细胞分析溯源体系的建立及有关问题的探讨[J].中华检验医学杂志,2004,27(3):132-133.
[6]黄永富,曹兴建.三个不同血细胞分析检测系统间检验结果的偏差评估与比对性研究[J].现代检验医学杂志,2012,27(6):86-94.
[7]武锦彪,陈晓玲,任春云,等.多台血液分析仪检测结果一致性比较[J].实验与检验医学,2013,31(1):27-30.

