比较两种核酸检测系统检测能力的结果分析
庄养林,熊丽红
(江西省血液中心检验科,南昌330000)
由于窗口期感染、隐匿性感染等原因,ELISA法检测献血者血液中的抗体或抗原存在一定的局限性,输血残余感染风险也时有发生[1-8]。因此从2010年开始,我国在15所采供血机构开展核酸检测(NAT)试点工作,我单位2010年成为首批试点单位后,并于当年引进罗氏Cobas s 201核酸检测系统,目前已平稳运行4年有余,为更好地推动核酸检测工作,我单位于2013年4月引进诺华TIGRIS全自动核酸检测分析系统,该系统也平稳运行1年。由于这两个检测系统的检测模式不同,实际检测效果也有所不同,在引进诺华核酸检测系统的初期,为全面评估两种核酸检测系统的检测能力,对此我们也做了相关的比较工作。
1 对象与方法
1.1 标本来源 选自2013年7月24日-2013年10月16日南昌市无偿献血者标本262例,所有标本均用带分离胶的5ml进口无菌乙二胺四乙酸抗凝管留取血样 (美国BD公司),4℃低温离心机离心(3000r/min,15 min)使血浆分层,2~8℃保存,24h内进行核酸检测;2014年卫生部核酸室间质评(NCCL)标本10例。
1.2 仪器 罗氏公司Cobas s 201核酸检测系统,诺华公司TIGRIS全自动核酸检测分析系统,瑞士Hamlton全自动STAR加样仪,瑞士Hamilton FAME全自动酶免分析仪,西门子DIMENSION XPAND全自动生化分析仪,XANTUS全自动加样与血型分析仪及长沙湘麓DL-6M大容量低温离心机。
1.3主要试剂 (1)常规血清学筛查酶免试剂盒:HBsAg酶免试剂 (厦门英科新创科技有限公司,批号:2012125133),抗-HCV酶免试剂(北京万泰生物药 业 股 份 有 限 公 司 , 批 号 :C20130102、C20130406),抗-HIV酶免试剂(厦门英科新创科技有限公司,批号:2013026605),抗-TP酶免试剂(北京华大吉比爱生物技术有限公司,批号:20130206、20130516;北京金豪制药股份有限公司,批号:2012111033、2013041008);(2)核酸检测试剂盒:COBASTaqScreen MPX test核酸检测试剂盒(瑞士 Roche 公司,批号:R01528、R07643),该试剂可同时定性检测人类血浆中的HIV-1,2 RNA、HCV RNA 和 HBV DNA;Procleix ULTRIO Assay核酸检测试剂盒 (Novartis公司,批号:36247751509149)该试剂可同时定性检测人类血浆中的HIV-1 RNA、HCV RNA 和HBV DNA。
1.4 实验方法 先进行常规一遍HBsAg、抗-HCV、抗-HIV,两遍抗-TP和ALT检测,筛选出ELISA及ALT合格献血者标本及不合格标本,然后将262例标本进行罗氏6人份混样检测及诺华单人份检测,NCCL核酸室间质评标本与献血者标本同批进行检测。(1)进行罗氏6人份混样核酸检测时,初混无反应性标本判为NAT检测阴性,初混有反应性时,进行下一步拆分检测工作:其一,拆分有反应性标本判为NAT阳性标本;其二,拆分无反应性标本判为NAT检测阴性。(2)运用诺华单人份检测时,无反应性标本判为NAT阴性,有反应性标本判为NAT阳性。(3)ELISA检测阴性而罗氏拆分检测NAT阳性标本或诺华检测NAT阳性的标本进行下一步HBV、HCV及HIV鉴别实验。
2 结果
2.1 262例血液标本ELISA检测结果 262例无偿献血者血液标本中经ELISA检测阴性为245例,阳性为17例。
2.2 245例血液标本两种核酸检测系统检测结果245例ELISA阴性献血者标本两种核酸检测系统检测结果情况,详见下表1。
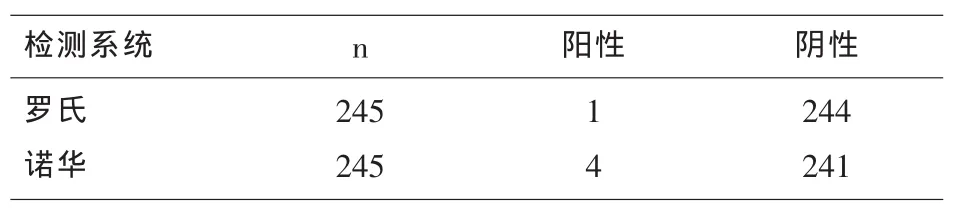
表1 245例ELISA合格献血者标本两种检测系统NAT检测结果
2.3 17例ELISA不合格标本及10例NCCL核酸室间质评标本两种检测系统NAT检测情况,详见表2。
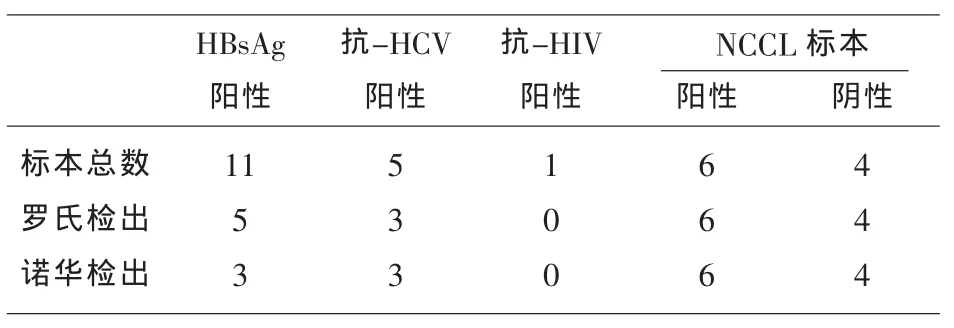
表2 17例ELISA不合格标本及10例NCCL核酸室间质评标本两种检测系统NAT检测情况
2.4 ELISA阴性标本而罗氏拆分检测NAT阳性标本或诺华检测NAT阳性鉴别情况 245例ELISA检测阴性的标本中,罗氏和诺华各检出1例和4例NAT阳性标本。通过鉴别实验,罗氏的1例NAT阳性标本未能鉴别,诺华的4例NAT阳性标本中1例为HBV,其余3例则未能鉴别。
3 讨论
在本文中,245例ELISA检测阴性献血者的标本中,罗氏系统检出1例NAT阳性标本(此例标本诺华NAT检测也为阳性),而诺华系统则检出4例NAT阳性的标本,后通过鉴别实验显示,罗氏的1例NAT阳性标本未能鉴别,诺华的4例NAT阳性标本中1例为HBV,其余3例则未能鉴别。此项结果也从一方面体现了混样检测与单人份检测的差别:混样检测由于吸取检测的量较单人份检测少,当病毒载量比较低时,混样检测就有可能检测不出,这与国内外的研究[9-11]结果也比较一致,有单人份检出率 (1:9862)及8人份混样检测率(1:5l011);还有单人份检测率 (26:7613)及16人份混样检测率(27:16064)。因此,诺华系统采用单人份检测方式在病毒载量比较低时实施血液核酸筛查可能有一定的优势,诺华1人份标本吸取的量为500μl,罗氏为167μl,相对而言诺华检测到病毒的概率大一些。从另一方面讲,由于没能做追踪实验,无法确证诺华其余3例NAT检测阳性的这部分标本中是否存在病毒。因此,诺华未能鉴别的3例NAT阳性的标本也有可能是假阳性,从节约血液资源上讲,这部分血液经NAT检测有可能因实验的假阳性而造成血液资源的浪费,从而影响无偿献血者的献血积极性。此外,在本实验出现了罗氏与诺华NAT检测同为阳性的1例标本中,鉴别实验却未能鉴别,因条件所限,我们没能进一步追踪检测,因此是实验假阳性还是病毒载量过低导致未能鉴别就不得而知。
在11例HBsAg阳性标本的NAT检测结果显示,罗氏和诺华系统分别有5例和3例检出NAT阳性,其中同为阳性的有3例,5份抗-HCV阳性的标本中两者都有3例NAT检出。此项实验结果显示在ELISA阳性的标本运用NAT检测中,罗氏系统较诺华系统有较高的检出率。因为11例HBsAg阳性标本我们未进行确证及鉴别实验,因此不能排除有ELISA实验假阳性的部分,但是可能也与HBV在血液中的存在形式有关,有可能是以小球形颗粒或管状颗粒的形式存在,致NAT检测不出。因此此项实验结果也表明,在日常的血筛工作中,不能有依赖NAT检测结果的思想,因为NAT技术和血清学检测的病毒标志物不同,NAT可以作为血清学的补充,但不能完全替代。在10份NCCL核酸室间质评标本中,两种核酸检测系统也全部正确检出,这表明这两种核酸检测系统均能较好地胜任日常核酸检测工作。
从日常检测工作流程上看,诺华的应用不如罗氏简便,具体体现在:对设备维护的要求较高、维护时间长、加载试剂及耗材费时;实验运行中工作人员即使发现可当时解决的问题也无法人为纠正。但是从检测及出具检验报告时间上看,罗氏系统可能会长于诺华系统,因为罗氏为6人份混样检测,检测前需进行标本6人份混样,而且为减少拆分检测,罗氏系统检测一般需要等ELISA检测结束后挑取ELISA阴性的标本才能进行,而诺华系统则与ELISA检测同步进行,单人份直接加样检测,减少了出具报告时间。再者,ELISA阴性的标本进行罗氏系统检测时如果初混有反应性,则需要进行拆分检测,又增加了工作量,出具报告的时间则又会相应延长,不利于应急标本的检测,而诺华是单人份检测则不存在这种情况。总之,两种核酸检测系统在日常血筛检测工作中各有优势和劣势,但均能较好地胜任日常的核酸检测工作。
[1]Allain J-P.Occult hepatitis B virus infection:implications in transfusion[J].Vox Sanguinis,2009,86(2):83-91.
[2]Soldan K,Barbara JA,Ramsay ME,et al.Estimation of the risk of hepatitis B virus,hepatitis C virus and human immunodeficiency virus infectious donations entering the blood supply in England,1993-2001[J].Vox Sanguinis,2003,84(4):274-286.
[3]欧阳玲,黄建国,谢秀华,等.无偿献血人群HCV感染的检测和输血残余风险分析[J].实验与检验医学,2010,28(4):344-348.
[4]欧山海,林永财,倪宏英,等.闽南地区无偿献血者隐匿性乙型肝炎病毒感染研究[J].中国输血杂志,2010,23(12):1033-1037.
[5]王良华,叶贤林,尚桂芳,等.免疫筛查阴性献血者血样病毒核酸检测的研究[J].中国输血杂志,2005,18(4):286-289.
[6]纪勇平,赵龙友,周斌,等.丽水地区无偿献血者中隐匿性乙型肝炎病毒感染调查与分析[J].中华实验和临床病毒学杂志,2011,25(6):457-459.
[7]戴钰,张振华,张玲,等.献血员隐匿性乙型肝炎病毒感染的分子流行病学[J].中华传染病杂志,2012,30(4):235-239.
[8]方昌志,傅颖媛,钱榕,等.HBsAg阴性献血者输血HBV感染残余风险分析[J].南昌大学学报:医学版,2012,52(12):35-37.
[9]宋美兰,任芙蓉,龚晓燕,等.单检及16份混样检测模式对献血者核酸检测效果的比较研究[J].中华检验医学杂志,2012,35(1):53-58.
[10]Gonzalez R,Torres P,Castro E,et al.Efficacy of hepatitis B virus(HBV)DNA screening and characterization of acute and occult HBV infections among blood donom from Madrid,Spain[J].Transfusion,2010,50(1):221-230.
[11]Assal A,Barlet V,Deschaseaux M,et a1.Sensitivity of two hepatitis B virus,hepatitis C virus(HCV),and human immanodeficiency virus(HIV)nucleic acid test systems relative to hepatitis B surface antigen,anti-HCV,anti-HIV,and P24/anti-HIV combination assays in seroeonversion panels[J].Transfusion,2009,49(2):301-310.

