试验序贯性分析在随机对照试验Meta分析中的运用*
王 欢 综述,胡厚祥审校
(川北医学院附属医院心内科,四川南充 637000)
Meta分析是将两个或者多个相似的研究结果进行定量综合分析的一种方法学。随机对照试验(random control trial,RCT)的Meta分析能够增加干预效果评估的力度和精确度[1-4]。当任何可利用的研究被一一纳入后,Meta分析被认为目前最佳的方法学。但是“最佳方法学”被广泛运用不代表它就是“证据确凿”或者“证据有力”[5-6]。传统 Meta分析方法,比如在Review Manager V.5.1并没有考虑到纳入研究的数量是否足够[7],而干预组显著性差异的广泛运用,忽略了研究样本的数目对结果的影响。如果得到的结果不具备统计学意义,就简单考虑是“样本量不足”的问题[8-10]。建立在有限的样本量基础上进行干预疗效的评估是不可靠的,大约有25%传统的系统评价纳入了小样本的研究而得出了错误的阳性结果[11]。样本量过小会影响Meta分析的结果,于是新的研究发表后,Meta分析就需要及时更新,在Cochrane网上的Meta分析需每隔2年要更新1次[12]。但是Meta分析反复更新,却可能使Ⅰ型错误(type Ⅰ error)——假阳性增加[5,11,13-14];其次,Meta分析也没有太多关注“检验效能”(发现两个总体参数间差异的能力),记为(1-β),因此,通过现有样本量计算得到的最后结果也可能不是真实的。故采用序贯Meta分析(sequential analysis)方法,通过引进成组序贯设原理来克服Meta分析的样本量。
1 试验序贯性分析概念
目前序贯 Meta分析包括试验序贯分析(trail sequential analysis,TSA)[15]和whitehea三角检验序贯 Meta分析(sequential Meta-analysis,SMA)。SMA 方法学在评估随机对照实验的Meta分析中也是有用的一个工具,和TSA比较具备不需要提前估算总体样本量等优点[16],但是由于方法学尚不成熟,实践运用受限,故目前运用最为广泛的是TSA。试验序贯性分析指每纳入一个研究后,都进行一次期中分析(interim analysis),校正α值,目的是控制Ⅰ类错误稳定在0.05的水平[12,17]。TSA能够在传统Meta分析的基础上关注“校正后的信息量”(heterogeneity-adjusted information size,HIS),采用随机对照实验中累积数据重复性显著性检验的方法学,校正显著性检验和无效检验的阈值,运用软件绘制出序贯Meta分析的界值图(trail sequential monitoring boundary,TSMB)。运用校正后的信息量来计算显著性检验α值和传统的Meta分析比较能有效地减少Ⅰ类错误的发生,得到的结果也更有信服力[6]。
2 试验序贯性分析的重点步骤
TSA重点在于根据HIS的数据,计算并绘制TSMB曲线。
第一步:明确未有校正的信息量(informaztion size,IS)、HIS和I2的关系[3],见公式(1)。

I2为通过传统Meta分析得到的异质性检验值[13]。当纳入的各研究之间的异质性增加,I2增加,HIS也会增加。
第二步:计算IS。
(1)当效应量是连续性变量,见公式(2)。

α是Ⅰ型错误的最大风险,β是Ⅱ型错误的最大风险,α/2是双侧检验,1-β是检验效能,σ2是方差,δ2是允许误差[3]。
(2)当效应量是二分类变量资料,见公式(3)。
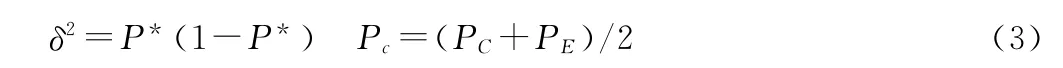
PE是干预组的率,PC是对照组的率。Meta分析包括固定效应模型和随机效应模型。当异质性小的时候,Meta分析采用固定型效应模型(fixed effect model,FIX);异质性大的时候,则采用随机效应模型(random effect model,Ran)[18]。IS也是分为固定效应模型 和随机效应模型IS。
(3)如果是二分类变量,则δ值见公式(4)。

RRR 是相对危险度的减少率(relative risk reduce,RRR)。(1)当原始文献质量不高,可以采用经验制定δ,则:RRR=15%、25%、35%等,计算出的HIS是先验的异质性调整后信息量(aprior heterogeneity-adjusted information size,APHIS);(2)如果纳入的原始文献为低风险,则见公式(5)。

RR是高质量文献的相对危险度[3],得到的HIS是低风险异质性调整后信息量(low risk heterogeneity-adjusted information size,LRHIS)。选择何种方法,当RRR增加时,计算后得到的HIS减少,反之亦然。
第三步、计算信息比(information fraction,IF),见公式(6)。

ISi是纳入的第i个研究时候的信息量,i=1,2,3...,IF指纳入的第i个研究的信息量占总的信息量的比值,HIS是校正后的信息量[3]。如果纳入的第i研究的IS比较大,则该研究对应的信息比也大。
第四步、计算α(IF),又称名义显著水平,也是校正后的显著性水平α,和IF的关系表示[3]见公式(7)。

Φ是正态分布的分布函数。当IF越大,则α(IF)越大,越接近传统α值。
第五步、计算显著性阈值Ci,见公式(8)。

Ci表示每个研究的显著性阈值(i=1,2…),Z代表每次Meta分析信息比对应的统计量。Ci和α(IF)成反比,当α(IF)越大,则C值越小,越接近传统的Z=1.96。
第六步、绘制TSMB曲线图。将纳入的研究按照时间顺序(或者累计的样本量)排列作为X坐标,Z值作为Y坐标。根据每一个IF计算得出一个Ci,连接每一个Ci,绘制的曲线图就是TSMB。当Y=1.96时,平行于X坐标的直线就是传统界线(Z=1.96,α=0.05)。将每个研究所对应的Z值连接起来就是Z曲线。
第七步、解读TSMB和Z曲线的关系。对于随机对照试验,当已经纳入研究的Z曲线大于TSMB,则考虑干预组和对照组疗效差异有统计学意义,表示[3]为公式(9)。

Pr表示为概率。如果Z值曲线小于所对应的TSMB,而IS小于HIS,应该扩大样本量。如果Z值曲线小于所对应的TSMB,且IS大于HIS,则实验组的干预疗效不优于对照组(可能比对照组更差),并且不需要再加大样本量继续实验,以免浪费资源[13]。
3 试验序贯性分析的运用要点
3.1 期中分析在TSA的运用 HIS的计算要依据合适的Ⅰ型错误和Ⅱ型错误,对照组的事件发生率和干预措施的疗效综合考虑。Meta分析中足量的HIS不少于一个独立的,大规模的随机对照试验的样本量[19]。在TSA中校正显著性检验水平有两个目的:一是可以利用最大信息量进行分析,一是当重复显著性检验时候必须有效地控制统计学误差(Ⅰ型错误和Ⅱ型错误)增加。当Meta分析的信息量还没有达到HIS的水准,那么重复的检验就要求“显著性指标”(实验组的干预措施优于对照组)的阈值进行调整,以便可以将Ⅰ型错误控制在5%内。同样,控制Ⅱ型错误也需要调整“不优越指标”(实验组和干预措施和对照组比较无差异)的阈值。在单个随机对照实验中,Armitage和Pocock建立了“成组序贯方法”,在他们的理论,随机对照临床试验的期中分析能够更早得到的结果,但同时也增加了Ⅰ型错误的发生。Lan和DeMets把单个样本使用的序贯分析中的“期中分析”理论运用在TSA,并且制定了显著性指标的阈值以及绘制TSMB来控制统计学误差的增加。控制Ⅱ型错误的理论延续了DeMets方法学,只是将计算“显著性指标”的阈值替换为“不优越指标”的阈值,从而就算得到了futility界线。因此,完整的TSA方法可以就绘制出两条曲线(monitoring界线和futility界线)。上述理论建立在现代概率的基础上,运用 的是重对数 定律(the law of the iterated logarithm)[3]。
3.2 α耗损作用和TMSB曲线 α耗损作用指信息比IF的连续性函数被耗损,每次Meta分析耗损了总α的一部分,但是不断增加的信息比不会增加总的Ⅰ型错误的产生,表示[3]为公式(10)。

α(IFi)是名义显著水平,i是纳入的第1,2…i个研究。
3.3 β耗损作用和Futility曲线 前面提到,当Z曲线超过TSMB被认为实验组干预效果和对照组比较有显著性差异;当Z曲线超过了HIS却没有超过TSMB,可以认为两组没有显著性差异;当Z曲线未有达到HIS,但是又“极其低下”,如何判断呢?仅仅需要进一步增加样本量吗?在此,可以参照Z曲线和Futility界线的关系。当Z曲线低于Futility界线,可以考虑是实验组疗效未有优于对照组(但是不提示差于对照组),表示[3]为公式(11)。

Pr表示为概率,C是“不优越指标”的阈值,β指假阴性的概率。在反复检验中,控制Ⅰ类错误的同时也期望减少Ⅱ类错误的增加。类似于α耗损,β耗损作用指信息比IF的连续性函数被耗损,Meta分析每次重复性检验耗损了总β的一部分,但是不断增加的信息比并不会增加总的Ⅱ型错误的产生,表示[3]为公式(12)。

3.4 固定效应模型的IS、随机效应模型IS和校正后的I2的关系 在Meta分析中纳入的研究,包括了广泛的实验人群,使用的干预方法也有一定差异,使用的干预衡量标准也不完全相同,因此导致了很多差异,也就是所谓的异质性(heterogeneity)或者是“研究组间的差异”。目前,广泛应用于 Meta分析的异质性检验指标I2值用于解释纳入研究的样本之间的误差[20]。由于增加的误差可以减少结果的准确度,在计算HIS时要考虑到所有的变量因素。在计算固定效应模型的HIS,使用方法可以沿用单样本随机对照试验的公式;但是在计算随

ISRandom表示随机效应模型的IS,ISFIX表示固定效应模型的IS,VR表示在随机效应模型的 Meta分析中的总方差,VF表示在固定效应模型的Meta分析中的方差。I2是异质性检验值。在TSA运用中要得到HIS,必须要估计对照组事件发生率和干预疗效。对于二分类变量,对照组事件发生率是通过临床经验和相关研究的证据而来。当文献的质量受限,在APHIS方法中要获得RRR,就要采用既往研究可靠的经验数据。例如,在Bianca Hemmingsen的Meta分析中,对照组是传统的糖尿病控制组的非致死型心肌梗死,其RRR是根据既往的研究数据而估计为10%[21]。不同的研究领域,所估计的RRR不同。
4 试验序贯性分析的争议
HIS的计算有一定的限制性。在单个随机对照试验中,很容易就控制一些可能影响实验结果的混杂因素。但是,系统评价不同于此,他是建立在有差异的既往研究的基础上,尤其是无法预测新的研究对既往Meta分析的结果有何决定性的影响。文献质量在Mete分析中的重要性是众所周知的,由于原始文献的质量问题(高风险偏倚),不少Meta分析干预疗效的评价是不准确的。当文献质量受限,即使由既往文献估计RRR得到APHIS也不能完全准确,而被认为有随机误差的增加。
使用不可预测的新研究的I2值来计算HIS是比较困难的,可以通过预测一些可靠的异质性水平来解决。但是,这方法也有局限性,当可利用研究的数量很少时候,很难去预测异质性,即使采用了敏感性方法[18,22]也不能得出真实的结果。
Miladinovic等考虑“TSA可以显著性治疗的导致不成熟结论,需要更多的累积的证据来证明干预疗效;TSA虽然可以执行二分类变量和连续性变量,却不能兼顾时间-事件数据,使TSA运用受限”。Imberger等[6]否定了上述的观点,认为之所以Miladinovic等人怀疑TSA的作用,主要是因为他们估计RRR指标的方法选择不恰当,并且忽视了原始文献质量对结果判定的影响,Imberger认为TSA在Meta分析中是有用的工具,可以通过调整阈值来有效的控制误差的增加,并且支持这个方法学的推广和改进[6]。
5 展 望
系统评价广泛应于原始文献的二次分析。但是由于其纳入文献低定时更新而导致Ⅰ类和Ⅱ类错误的增加。引入试验序贯分析理论,通过调整显著性阈值,在不断增加样本量的同时又能有效控制误差的增加。但是,TSA受到原始文献质量的限制,文献的质量可以影响RRR数据的选择,为了提高Meta分析的质量,除了优化统计学的应用,最根本还是纳入高质量的文章,并且在评价原始文献质量方面也要进一步加强客观性和系统性[25]。
[1]Wang JY,Xiao L,Chen J,et al.Potential effectiveness of traditional Chinese medicine for cardiac syndrome X(CSX):a systematic review and meta-analysis[J].BMC Complement Altern Med,2013,13(1):62.机对照实验Meta分析的HIS,则要校正I2值,将固定效应模型和随机效应模型的总变量一起考虑;两则关系表示[3]为公式(13)。
[2]Wang HF,Yu JT,Tang SW,et al.Efficacy and safety of cholinesterase inhibitors and memantine in cognitive impairment in Parkinson′s disease,Parkinson′s disease dementia,and dementia with Lewy bodies:systematic review with meta-analysis and trial sequential analysis[J].J Neurol Neurosurg Psychiatry,2015,86(2):135-143.
[3]Thorlund K,Engstr OMJ,Wetterslev J,et al.User manual for trial sequential analysis(TSA)[EB/OL].[2015-3-26].http://wwwctudk/tsa/files/tsa_manual.pdf.
[4]Higgins,Julian PT,ed.Cochrane handbook for systematic reviews of interventions[M].Chichester:Wiley-Blackwell,2008:1-24.
[5]Brok J,Thorlund K,Wetterslev J,et al.Apparently conclusive meta-analyses May be inconclusive--Trial sequential analysis adjustment of random error risk due to repetitive testing of accumulating data in apparently conclusive neonatal meta-analyses[J].Int J Epidemiol,2009,38(1):287-298.
[6]Imberger G,Wetterslev J,Gluud C.Trial sequential analysis has the potential to improve the reliability of conclusions in meta-analysis[J].Contemp Clin Trials,2013,36(1):254-255.
[7]Higgins JP,Whitehead A,Simmonds M.Sequential methods for random-effects meta-analysis[J].Stat Med,2011,30(9):903-921.
[8]Ma B,Guo J,Qi G,et al.Epidemiology,quality and reporting characteristics of systematic reviews of traditional Chinese medicine interventions published in Chinese journals[J].PLoS One,2011,6(5):e20185.
[9]Kimer N,Krag A,Moller S,et al.Systematic review with meta-analysis:the effects of rifaximin in hepatic encephalopathy[J].Aliment Pharmacol Ther,2014,40(2):123-132.
[10]Thorlund K,Imberger G,Walsh M,et al.The number of patients and events required to limit the risk of overestimation of intervention effects in meta-analysis--a simulation study[J].PLoS One,2011,6(10):e25491.
[11]Thorlund K,Devereaux PJ,Wetterslev J,et al.Can trial sequential monitoring boundaries reduce spurious inferences from meta-analyses?[J].Int J Epidemiol,2009,38(1):276-286.
[12]Li S,Zeng XT,Ruan XL,et al.Holmium laser enucleation versus transurethral resection in patients with benign prostate hyperplasia:an updated systematic review with meta-analysis and trial sequential analysis[J].PLoS One,2014,9(7):e101615.
[13]Haase N,Perner A,Hennings LI,et al.Hydroxyethyl starch 130/0.38-0.45versus crystalloid or albumin in patients with sepsis:systematic review with meta-analysis and trial sequential analysis[J].BMJ,2013,346:839.
[14]Chiarotti F,Acconcia MC,Sergi D,et al.Trial sequential analysis:the role of the number needed-to-treat in evaluating the clinical relevance of relative risk reduction values in the intra-aortic balloon pump support[J].Int J Cardi-ol,2013,168(5):5097-5099.
[15]Koning GG,Wetterslev J,Van Laarhoven CJ,et al.The totally extraperitoneal method versus Lichtenstein′s technique for inguinal hernia repair:a systematic review with meta-analyses and trial sequential analyses of randomized clinical trials[J].PLoS One,2013,8(1):e52599.
[16]Van Der Tweel I,Bollen C.Sequential meta-analysis:an efficient decision-making tool[J].Clin Trials,2010,7(2):136-146.
[17]Thorlund K,Anema A,Mills E.Interpreting meta-analysis according to the adequacy of sample size.An example using isoniazid chemoprophylaxis for tuberculosis in purified protein derivative negative HIV-infected individuals[J].Clin Epidemiol,2010,2:57-66.
[18]He Q L,Zhong F,Ye F,et al.Does intraoperative ulinastatin improve postoperative clinical outcomes in patients undergoing cardiac surgery:a meta-analysis of randomized controlled trials[J].Biomed Res Int,2014,2014:630835.
[19]Piccolo R,Galasso G,Capuano E,et al.Transradial versus transfemoral approach in patients undergoing percutaneous coronary intervention for acute coronary syndrome.A meta-analysis and trial sequential analysis of randomized controlled trials[J].PLoS One,2014,9(5):e96127.
[20]Thorlund K,Imberger G,Johnston BC,et al.Evolution of heterogeneity(I2)estimates and their 95%confidence intervals in large meta-analyses[J].PLoS One,2012,7(7):e39471.
[21]Hemmingsen B,Lund S S,Gluud C,et al.Intensive glycaemic control for patients with type 2diabetes:systematic review with meta-analysis and trial sequential analysis of randomised clinical trials[J].BMJ,2011,343:d6898.
[22]Caldeira D,Costa J,Fernandes RM,et al.Performance of the HAS-BLED high bleeding-risk category,compared to ATRIA and HEMORR2HAGES in patients with atrial fibrillation:a systematic review and meta-analysis[J].J Interv Card Electrophysiol,2014,40(3):277-284.
[23]Miladinovic B,Kumar A,Hozo I,et al.Trial sequential analysis May be insufficient to draw firm conclusions regarding statistically significant treatment differences using observed intervention effects:a case study of metaanalyses of multiple myeloma trials[J].Contemp Clin Trials,2013,34(2):257-261.
[24]Miladinovic B,Mhaskar R,Hozo I,et al.Optimal information size in trial sequential analysis of time-to-event outcomes reveals potentially inconclusive results because of the risk of random error[J].J Clin Epidemiol,2013,66(6):654-659.
[25]Tong A,Flemming K,McInnes E,et al.Enhancing transparency in reporting the synthesis of qualitative research:ENTREQ[J].BMC Med Res Methodol,2012,12:181.

