压片法制备氯离子传感器的工作性能
李振垒,李伟华,2
(1.青岛理工大学,青岛266000;2.中国科学院海洋研究所,青岛266000)
目前可用于环境监测或者生物医学的微型电化学传感器是一个非常热门的研究方向。微型传感器简单、快速、便携以及低成本的优点越来越受到各界的欢迎[1-2]。为了实现上述传感器优点,要求无论是传感器工作电极还是参比电极其体积必须是微型化的,尤其是参比电极。因为参比电极是各个电化学传感器的一个非常重要的组成部分[3]。
Ag/AgCl电极因其电位稳定、重现性好,制备简单被广泛应用于各个领域,既可以作为参比电极也可以作为工作电极。C.P.Atkins[4]等采用Ag/AgCl电极测试实验室中配置混凝土模拟液和采用压汞法压出混凝土孔隙液中的氯离子浓度,试验结果表明,所测得氯离子浓度与根据活度系数理论计算出的值相吻合良好;研究者同时也测试了各种环境中传感器误差,包括温度误差、离子误差等。M.A.Climent-Llorca[5-6]等将Ag/AgCl电极埋入采用不同氯化钠掺量的砂浆试块中测试其性能,试验证明该电极在一定浓度氯离子条件下表现出良好的线性响应。M.F.Montemor[7]等将所制备银电极埋入混凝土试块的不同深度,监测在氯离子溶液中氯离子向混凝土试件中扩散的过程,表明该银电极在整个试验过程中具有良好的稳定性。由此可见Ag/AgCl电极型传感器在混凝土中监测氯离子浓度有巨大潜力。如果采用甘汞电极作为参比电极应用在混凝土外部,监测结果较差还会带来液接误差。
本工作以Ag/AgCl为工作电极,以高效实用的二氧化锰做为参比电极,采用特殊工艺、组装方法制备可埋入混凝土中的氯离子浓度监测传感器,并对传感器各方面工作性能进行了大量试验。
1 试验
1.1 试剂、材料及设备
高纯纳米银粉(纯度99.99%);高纯超细AgCl粉;无水乙醇;NaCl;去离子水。PARSTAT 2273电化学工作站;万用表;饱和甘汞电极;钢模具;压片机;三型聚丙烯(PPR)管;有机玻璃管;干扰线。
1.2 传感器制备
氯离子传感器由两个电极组成:Ag/AgCl电极作为工作电极,MnO2电极作为参比电极,两个电极均采用压片法制备。压制过程:将混合均匀的电极粉末(工作电极为银粉和氯化银粉,参比电极为二氧化锰、炭黑、聚四氟乙烯)放入钢模具中在压片机上压制成型即可,见图1。电极直径为Φ13mm,Ag/AgCl电极厚度为3mm,MnO2电极厚度为5mm。将压制好的MnO2电极浸入碱性功能层中一起放入底部用半透膜封闭的PPR管中,上部采用有机玻璃盖拧紧,然后将Ag/AgCl电极固定在旁边即组装成全固态、可埋入式混凝土氯离子传感。图2为制得的参比电极和传感器示意图。

图1 模具和压片机Fig.1 Model and tablet machine

图2 参比电极和氯离子传感器Fig.2 The reference electrode and chloride ion sensor
2 结果与讨论
2.1 氯离子传感器稳定性测试
将氯离子传感器放入室温环境中0.01mol/L的NaCl溶液中,长期监测每天的电位值变化情况,电极电位校验试验和稳定性试验具体方法参考国标BG/T 7387-1987。测定传感器在0.01mol/L NaCl孔隙液中7d、14d、28d、56d的电位值变化情况,判断其电位稳定性。试验所用模拟液采用保鲜膜进行密封,尽量保证模拟液浓度不变,每隔几天更换一次NaCl模拟液。

图3 传感器稳定性测试Fig.3 The sensor′s stability test
图3为氯离子传感器在模拟液中电位值随时间变化图。表1为氯离子传感器参照GB/T 7381-1987测试所得结果,分别得出传感器在7d、14d、28d、56d的电位平均值和最大偏差。

表1 参照GB/T 7387-1987的测试结果Tab.1 The test results of GB/T 73897-1987
氯离子传感器在浸泡第56天时,已经达到国标GB/T 7387-1987所述要求。从图中数据分析可以看出随着浸泡时间的增长,氯离子传感器之间的电位值偏差越来越小,平行性越好。在浸泡第56天时,所测试6个氯离子传感器电位值电位值偏差小于1mV,这是因为Ag/AgCl电极需要一个活化的过程,Ag/AgCl电极的电极电势与溶液中Cl-活度有关,因此Ag/AgCl电极需要有建立离子平衡和稳定的过程。电极稳定后电位值波动较小,因为AgCl微溶于溶液,电极稳定后AgCl含量基本保持在平衡阶段不会产生变化。试验证明氯离子传感器具有良好的电化学性能。
2.2 氯离子传感器能斯特方程
图4为传感器在氯离子浓度为10-4mol/L,10-3mol/L,10-2mol/L,10-1mol/L,1mol/L溶液中的氯离子传感器能斯特方程测试。在0.01mol/L氯化钠溶液中,采用的参比电极对饱和甘汞电极电位值为-96.61mV,工作电极对应饱和甘汞电极的电位值为-91.2mV。
由上图可得:Y=A+BX,式中:A=69.187 8,B=21.904,相关系数R2=0.995 48。由此可见该氯离子传感器线性相关性良好。
2.3 温度变化对氯离子传感器工作电位的影响
图5为10~60℃温度范围内,温度由低到高变化时对氯离子传感器性能影响的曲线图,采用的氯离子浓度为0.1mol/L。

传感器在10~40℃范围内电位值从大约100mV变化到103mV左右,电位变化值小于5mV,几乎可以忽略不计。温度在50℃时相比较室温下电位值上升了约4.8mV左右。温度在60℃时相比较室温下电位值上升约9.59mV。由Nernst方程得:温度增高会增加表面离子活度,电极电位值增加,而氯离子传感器还有一个参比电极,同样在温度升高时其表面活性也会增大,电位值也会相应的升高。由此可见,当传感器在温度为10~40℃温度范围内工作时,温度对传感器电位值几乎没有影响。当温度超过40℃以上时可以做一个温度修正。因此氯离子传感器在一般情况下可以不考虑温度影响。
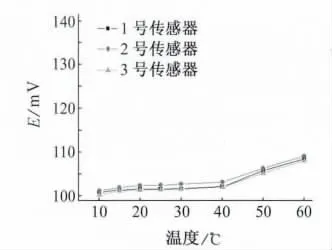
图5 温度对传感器电位值影响Fig.5 Effect of temperature on the sensor′s potential value
2.4 其他离子对传感器电位值干扰试验
氯离子传感器在固定浓度0.1mol/L氯化钠溶液中,以氢氧化钙、混凝土模拟液(0.2mol/L NaOH,0.6mol/L KOH,饱和氢氧化钙)、混凝土模拟液+SO2-4和混凝土模拟液+Mg2++SO2-4溶剂4种溶剂、2种不同浓度氯盐溶液为试验环境,测试了传感器的工作性能,以研究混凝土中存在其他离子对传感器电位值的干扰,结果见图6。具体试验环境见表2。
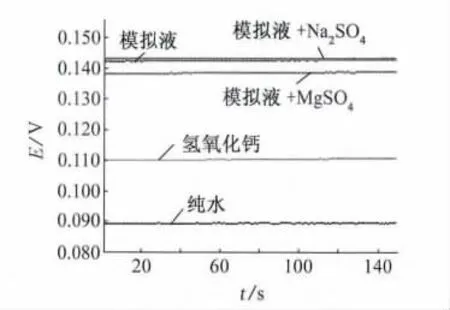
图6 离子干扰试验结果Fig.6 Test of ion interference
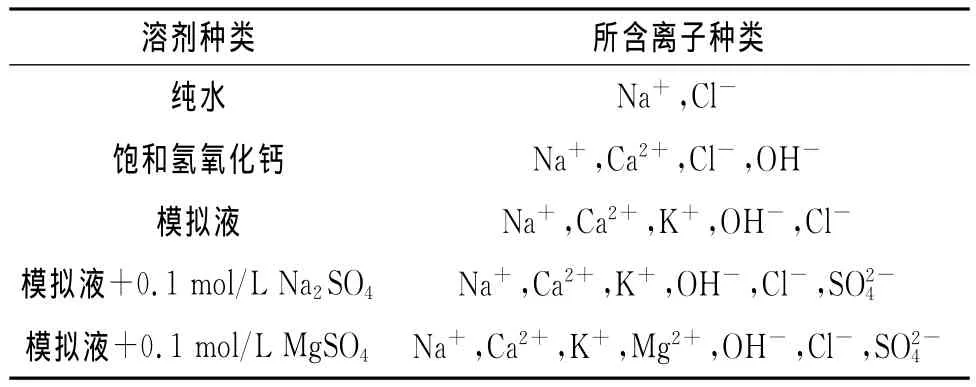
表2 不同离子的盐溶液Tab.2 Salt solution of different ions
图6中曲线由下至上依次为纯水,饱和氢氧化钙,模拟液+MgSO4,模拟液和模拟液+Na2SO4。其中,模拟液和模拟液+Na2SO4的曲线几乎重合。在纯0.1mol/L NaCl溶液中,传感器电位值最小为89.558mV,其次为饱和氢氧化钙,电位值为108.881mV,传感器在混凝土模拟液中最高,电位值为140.778mV。由此可以看出传感器的电位响应值会随着模拟液pH的上升而升高。在混凝土模拟液中加入SO时,如图6中曲线所示,所得混凝土模拟液曲线与在其中加入SO时所得曲线几乎相同,因此混凝土中SO含量对该传感器电位值影响不大。随后在混凝土模拟液中加入Mg2+,SO时所测得的传感器电位值曲线比混凝土模拟液低,为136.791mV左右,相比较模拟液与模拟液+SO曲线,加入Mg2+,SO时所得电位值,比模拟液与模拟液+SO电位值低4mV左右。由此可见,该氯离子传感器会受混凝土中pH变化的影响,随着pH的降低传感器的电位值也会随着减少,因此pH是该传感器的一个重要影响因素。在实际环境中,混凝土为高碱性环境,碳化因素对钢筋周围pH的影响较小,因此埋入钢筋周围的氯离子传感器可保持长期的监测效果。其他离子对传感器的干扰较小。
2.5 氯离子传感器恒电流极化性能测试
图7为传感器浸泡在3.5%NaCl模拟溶液中的恒电流极化测试图。恒电流极化所用的三电极体系:银电极为工作电极、二氧化锰为参比电极、铂片做辅助电极,采用的极化电流为10μA,极化时间为2h。
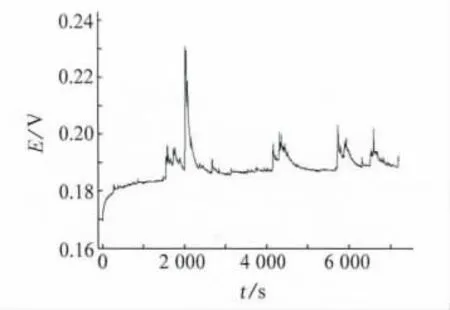
图7 恒电流极化试验Fig.7 Constant current polarizationg test
从图2中可以看出在前1 200s内传感器电位值几乎没有漂移,在1 200s时突然由0.152V上升到0.2V,之后电位值一直处于波动状态,波动范围为0.03V。由整体来看传感器整体电位值初始为0.15V,稳定时电位值为0.21V,电位值最大值为0.373 94V。因此传感器在10μA极化电流作用下,电位值漂移为0.058V。在1 200s电位值突然发生变化,这是因为工作电极或参比电极受极化电流影响破坏了原有的工作面导致。但是传感器所采用的屏蔽线可以起到一定的防电磁等干扰的能力。总体来说该氯离子监测传感器不能很好的抵抗极化电流影响。
3 结论
(1)该方法制作的氯离子传感器稳定性良好,并且所测得的能斯特方程相关性较强,理论上可适用于氯离子浓度监测。
(2)温度变化对氯离子传感器工作电位影响不大,但是pH会对氯离子传感器电位值产生一定的影响。
(3)恒电流极化试验表明传感器抗极化电流影响的能力较差。
[1] ISAOS,HIROYUKIK,MASAYUKII.Improvement in the long-term stability of screen-printed planar type solid-state Ag/AgCl reference electrode by introducing poly(dimethylsiloxane)liquid juction[J].Electrochimica Acta,2011,58:528-531.
[2] SUZUKIH,SUGAMA A,KOJIMAN.Micromachined clark oxy-gen electrode[J].Sens Actuators,1993(B10):91-98.
[3] MURALIDHARAN S,HA T,BAE J,et al.Electrochemical studies on the solid embeddable reference sensors for corrosion monitoring in concrete structure[J].Materials Letters,2006,60(5):651-655.
[4] THANGAVEL K,RENGASAMY N S.Relationship between chloride/hydride and corrosion rate of steel in concrete[J].Cement and Concrete Composites,1998,20(4):283-292.
[5] DE VERA G,CLIMENT M A,ANTONC,et al.Determination of the selectivity coefficient of a chloride ion selective electrode in alkaline media simulating the cement paste pore solution[J].Journal of Electroanalytical Chemistry,2010(639):43-49.
[6] ATKINS C P,SCANTLEBURY J D,NEDWELL P J,et al.Monitoring chloride concentrations in hardened cement pastes using ion selective electrodes[J].Cement and Concrete Research,1996,26(2):319-324.
[7] MONTENOR M F,SIMOES A M P,FERREIRA M G S.Chloride-induced corrosion on reinforcing steel:From the fundamentals to the monitoring techniques[J].Cement and Concrete Composites,2003,24(5):491-502.

