恩替卡韦治疗不同HBV基因型慢性乙型肝炎疗效的观察
刘必铿 林清标 林太顺
恩替卡韦治疗不同HBV基因型慢性乙型肝炎疗效的观察
刘必铿 林清标 林太顺
目的探讨不同乙型肝炎病毒(HBV)基因型与恩替卡韦抗病毒治疗慢性乙型肝炎患者疗效的关系。方法167例应用恩替卡韦治疗的慢性乙型肝炎患者于治疗前进行HBV基因分型, 并检测治疗前和治疗24、96周时乙肝两对半定量、HBV-DNA定量、肝功能, 比较不同基因型患者的抗病毒疗效。结果167例患者HBV基因分型中B基因型有98例, 占58.7%, C基因型69例, 占41.3%,未检出其他基因型。恩替卡韦抗病毒治疗24周时和治疗96周时, B基因型与C基因型慢性乙型肝炎患者丙氨酸氨基转移酶(ALT)复常率、DNA低于检测下限率(103copies/ml)、乙肝e抗原(HBeAg)转阴率、HBeAg血清学转换率差异均无统计学意义(P>0.05);按HBeAg分组后, 两种基因型在治疗96周时的疗效差异无统计学意义(P>0.05)。结论HBV基因型B或C对恩替卡韦抗病毒疗效无明显影响。
乙型肝炎病毒;基因型;恩替卡韦;疗效
乙型肝炎病毒(hepatitis B virus, HBV)感染呈世界性流行,我国是HBV感染患者最多的国家之一。恩替卡韦作为慢性乙型肝炎患者抗病毒治疗的一线用药, 运用广泛, 其疗效较为明确, 和HBV感染途径、病程长短、肝脏病变程度、遗传背景等密切相关。尤其HBV基因型是否对抗病毒治疗疗效影响引起了众多学者的关注。本研究对167例应用恩替卡韦抗病毒治疗的慢性乙型肝炎患者的基因型、HBV-DNA水平、肝功能、乙肝两对半定量进行分析, 探讨HBV基因型与恩替卡韦抗病毒治疗疗效的关系, 为临床抗病毒治疗提供依据。
1 资料与方法
1.1 一般资料2010年6月~2012年6月就诊福建医科大学附属第一医院和福州市传染病医院诊断为慢性乙型肝炎的患者。慢性乙型肝炎诊断标准及抗病毒治疗指征符合《慢性乙型肝炎防治指南(2010年版)》[1]的标准和指征。排除合并甲、戊、丙、丁型病毒性肝炎、艾滋病病毒感染、酒精性肝病、非酒精性脂肪性肝病、药物性肝损害、自身免疫性肝病、遗传代谢性肝病。167例患者均为初治患者(治疗前未使用抗病毒治疗)且应用恩替卡韦单药抗病毒治疗。其中男106例,女61例, 年龄19~43岁, 平均年龄(28.1±11.7)岁。
1.2 治疗方法 恩替卡韦(博路定, 中美上海施贵宝制药有限公司)0.5 mg口服,1次/d, 疗程≥96周。
1.3 检测指标与方法 治疗前检测HBV基因型, 治疗前和治疗后第24、96周检测乙肝两对半定量、HBV-DNA定量、肝功能。HBV基因型:采用PCR微量板核酸杂交酶联免疫法,试剂盒由广州蓝星生物科技开发公司生产。乙肝两对半定量:美国雅培i2000SR免疫分析仪, 采用化学发光法完成。HBVDNA:采用深圳匹基乙肝DNA试剂盒、罗氏Lightcycler检测, 灵敏度下限为103copies/ml。肝功能:全自动生化分析仪OLYMPUS (AU270)及配套试剂完成。
1.4 统计学方法 所有数据均采用SPSS19.0统计学软件进行统计分析。计量资料以均数±标准差(±s)表示, 采用t检验;计数资料以率(%)表示, 采用χ2检验。P<0.05为差异具有统计学意义。
2 结果
2.1 治疗前基线情况167例患者HBV基因分型中B基因型有98例, C基因型69例, 未检出其他基因型。其中B基因型慢性乙型肝炎患者中HBeAg阳性者51例, C基因型慢性乙型肝炎患者中HBeAg阳性者37例。两种基因型患者治疗前的年龄、性别构成比、HBeAg阳性率、ALT水平、HBV-DNA水平(log10 copies/ml)基本一致, 差异均无统计学意义(P>0.05)。见表1。
2.2 HBV基因型与抗病毒治疗24周疗效的关系 B基因型患者治疗24周时ALT复常68例(69.4%), C基因型患者ALT复常41例(59.4%), B基因型患者的ALT复常率高于C基因型, 但差异无统计学意义(χ2=1.775, P=0.183)。见表2。B基因型患者HBV-DNA低于检测下限(103copies/ml)的有78例(79.6%), C基因型患者有50例(72.5%), 差异无统计学意义(χ2=1.149, P=0.284)。B基因型患者发生HBeAg转阴的有2例(2.0%), C基因型患者有1例(1.4%), 差异无统计学意义(χ2=0.080, P=0.777)。B基因型和C基因型患者均无发生HBeAg血清学转换。
2.3 HBV基因型与抗病毒治疗96周疗效的关系 恩替卡韦抗病毒治疗96周时, B基因型与C基因型慢性乙型肝炎患者ALT复常率、HBV-DNA低于检测下限率、HBeAg转阴率、HBeAg血清学转换率差异均无统计学意义(P>0.05), 见表3。但是B基因型和C基因型患者的ALT复常率及HBV-DNA低于检测下限率均较治疗24周时有增高, 发生HBeAg转阴及HBeAg血清学转换的例数也较治疗24周时增多。
2.4 HBeAg阳性/阴性患者HBV基因型与抗病毒治疗96周疗效的关系 依据HBeAg是否阳性分为HBeAg阳性组88例, HBeAg阴性组79例, HBeAg阳性慢性乙型肝炎患者, B基因型与C基因型患者抗病毒治疗96周时的ALT复常率、HBV-DNA低于检测下限率、HBeAg转阴率、HBeAg血清学转换率差异无统计学意义(P>0.05)。HBeAg阴性慢性乙型肝炎患者中, 两种基因型患者治疗96周时的ALT复常率、HBV-DNA低于检测下限率差异均无统计学意义(P>0.05)。见表4。
表1167 例患者抗病毒治疗前的基线情况[n(%),±s]

表1167 例患者抗病毒治疗前的基线情况[n(%),±s]
注:两组比较, P>0.05
基因型 例数 年龄(岁) 男/女 HBeAg阳性例数 HBV-DNA(log10 copies/ml) ALT(U/L) B基因型 98(58.7) 27.2±12.5 60/38 51(52.0) 7.5±0.8 213±112 C基因型 69(41.3) 28.3±10.7 46/23 37(53.6) 7.3±1.1 198±140

表2167 例不同HBV基因型患者抗病毒治疗24周时的疗效比较[n(%)]

表3 不同HBV基因型患者抗病毒治疗96周时的疗效比较[n(%)]
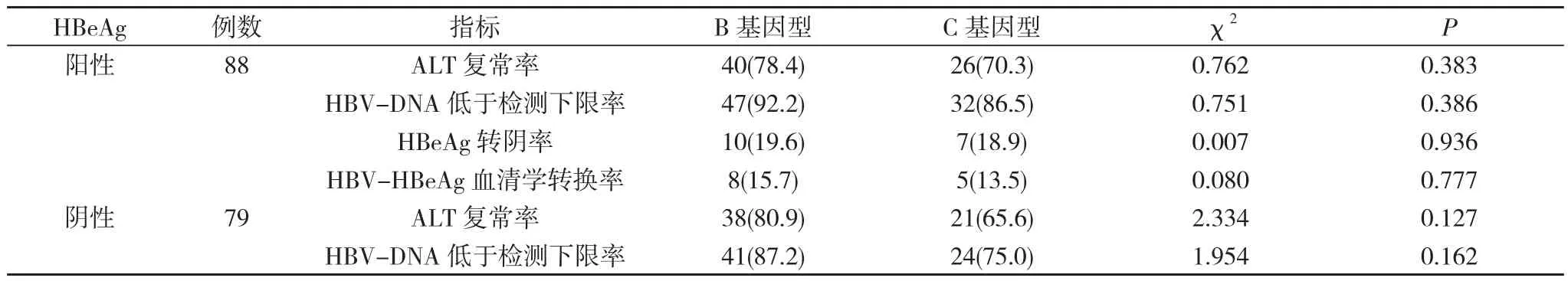
表4 HBeAg阳性/阴性患者不同基因型与治疗96周时疗效的比较[n(%)]
3 讨论
乙型肝炎病毒依据全基因系列异质性≥8%或S基因系列异质性≥4%分为不同基因型, 目前已经发现10种, 分别是A~J。HBV基因型的分布呈一定的地域性, 基因型A分布于全球, 基因型B和C主要分布于亚洲, 基因型D分布于南欧, 基因型E分布于非洲, 基因型F分布于美国, 基因型G分布于美国和法国, 基因型H分布于中美洲[2];在我国主要是B型和C型为主, 其中在南方B型多于C型, 而北方以C型多见[3]。本研究患者来源于福建, 研究结果提示HBV基因型分布基因型B多于基因型C, 分别为58.7%和41.3%, 未检出其他基因型, 与国内报道一致。
合理使用抗病毒药物可以抑制HBV复制, 减轻肝脏肝炎, 延缓肝脏疾病进展。目前常用的抗病毒药物包括干扰素(普通干扰素和聚乙二醇干扰素)和核苷(酸)类似物(拉米夫定、阿德福韦酯、恩替卡韦、替比夫定、替诺福韦)。恩替卡韦为鸟嘌呤核苷类似物, 对乙型肝炎病毒多聚酶具有抑制作用, 为抗乙型肝炎病毒一线药物[4]。恩替卡韦具有抗病毒作用强、起效快、耐药率低及安全性好等优势[5-7]。本研究中恩替卡韦治疗24周时即起到快速抑制病毒作用, 其中B基因型患者HBV-DNA低于检测下限率79.6%, C基因型患者72.5%;ALT复常率也较高, 基因型B和C分别69.4%和59.4%。随着治疗时间延长, ALT复常率、HBV-DNA低于检测下限率、HBeAg转阴率及HBeAg血清学转换率均升高, 治疗至96周时, 基因型B和C患者的ALT复常率分别达79.6%和68.1%, HBV-DNA低于检测下限率分别为89.8%和81.2%, HBeAg转阴率分别为10.2%和10.1%, HBeAg血清学转换率分别为8.2%和7.2%。
不同HBV基因型与抗病毒疗效是否存在相关性, 是近几年来乙型肝炎抗病毒治疗研究的热点。目前较多学者认为HBV基因型影响干扰素治疗的疗效, Hou等[6]研究发现HBV基因型A患者对干扰素的治疗效果优于基因型D, 而基因型B患者对干扰素的应答率高于基因型C, 与其他研究结论[7-9]一致。然而HBV基因型是否影响核苷(酸)类似物抗病毒疗效尚存在争议。杨丽敏等[8]研究发现应用拉米夫定、恩替卡韦和替比夫定抗病毒治疗, 基因型B患者ALT复常率、HBV-DNA阴转率和HBeAg血清学转换率均高于基因型C及B/C基因型。徐严等[9]研究发现HBV基因型对恩替卡韦抗病毒疗效无显著影响, 李颖等[10]研究也表明基因型B与基因型C慢性乙型肝炎患者应用恩替卡韦抗病毒治疗48周的疗效无明显差异。本研究病例数较多, 共纳入研究对象167例, 其中基因型B慢性乙型肝炎患者98例, 基因型C患者69例;HBV基因型与恩替卡韦抗病毒治疗24周时和96周时的ALT复常率、DNA低于检测下限率、HBeAg转阴率、HBeAg血清学转换率均无明显联系。
总之, 不同HBV基因型对恩替卡韦抗病毒疗效的影响尚无统一意见, 其具体机制及其相关性尚需进一步研究, 以便指导临床抗病毒药物治疗及疗效判断。
[1]中华医学会肝病学分会, 中结医学会感染病学分会. 慢性乙型肝炎防治指南(2010年版). 临床肝胆病杂志,2011(1):256-258.
[2]Sugauchi F, Orito E, Ichida T, et al. Hepatitis B virus of genotype B with or without recombination with genotype C over the precore region plus the core gene. J Virol ,2002,76(12):5985-5992.
[3]殷继明, 金荣华, 严研, 等.慢性乙型肝炎患者HBV基因型及亚型分布调查.实用肝脏病杂志,2010,13(1):19-21.
[4]Tong MJ, Pan CQ, Hann HW, et al. The management of chronic hepatitis B in Asian Americans. Dig Dis Sci,2011,56(11):3143-3162.
[5]Chang TT, Gish RG, de Man R, et al. A comparison of entecavir and lamivudine for HBeAg-positive chronic hepatitis B. N Engl J Med,2006,354(10):1001-1010.
[6]Hou J, Schilling R, Janssen H, et al. Molecular characteristics of hepatitis B virus genotypes A confer a higher response rate to interferon treatment. J Hepatol,2001,34(Suppl1):15-21.
[7]Erhardt A, Blondin D, Hauck K, et al. Response to interferon alfa is hepatitis B virus genotype dependent: genotype A is more sensitive to interferon than genotype D. Gut,2005,54(7):1009-1013.
[8]杨丽敏, 彭勋, 赵艳茹, 等.不同HBV基因型感染慢性乙型肝炎患者对核苷(酸)类药物治疗的应答反应比较. 实用肝脏病杂志,2012,15(2):120-122.
[9]徐严, 张永贵, 季尚玮, 等.乙型肝炎病毒基因型检测的临床意义.中国实验诊断学,2010,14(1):61-63.
[10]李颖, 刘均娟, 曹丽霞, 等. 乙型肝炎病毒基因型与恩替卡韦抗病毒疗效关系. 临床荟萃,2009,24(13):1133-1135.
Observation of curative effect by entecavir in the treatment of chronic hepatitis B with different HBV genotypes
LIU Bi-keng, LIN Qing-biao, LIN Tai-shun. The First Affiliated Hospital of Fujian Medical University, Fuzhou350003, China
ObjectiveTo investigate the relationship between different hepatitis B virus (HBV) genotypes and curative effect of entecavir in antiviral treatment of chronic hepatitis B.MethodsHBV genotypes of167 chronic hepatitis B treated by entecavir were detected, and their two pairs of semi hepatitis B, HBV-DNA quantify, and liver function were detected before treatment and in24,96 weeks in treatment. Comparison was made on antiviral effects for different genotypes.ResultsAmong the167 cases, there were98 cases with B genotype, accounting for58.7%, and69 cases with C genotype, accounting for41.3%. No other genotype was found. In24 weeks and96 weeks of entecavir treatment, the differences of alanine aminotransferase (ALT) recovery rate, DNA under lower detection limit rate (103 copies/ml), hepatitis Be antigen (HBeAg) negative rate, and HBeAg serologic conversion rate had no statistical significance between B genotype and C genotype (P>0.05). There was also no statistically significant difference between the two genotypes in96 weeks after divided by HBeAg (P>0.05).ConclusionB or C HBV genotype has no obvious influence on antiviral effect of entecavir.
Hepatitis B virus; Genotype; Entecavir; Curative effect
10.14164/j.cnki.cn11-5581/r.2015.09.003
2014-12-26]
350003 福建医科大学附属第一医院(刘必铿);福州市传染病医院(林清标 林太顺)

