异甘草酸镁治疗抗结核药物所致肝损伤临床疗效分析
异甘草酸镁治疗抗结核药物所致肝损伤临床疗效分析
于新喜1, 王智亮2
(1. 山东省潍坊市寒亭区人民医院 药事办, 山东 潍坊, 261100;
2. 山东省潍坊市人民医院 药学部, 山东 潍坊, 261041)
关键词:药物性肝损伤; 异甘草酸镁注射液; 抗结核药物; 肺结核; 肝功能
结核病是由结核分枝杆菌感染引起的传染病[1], 常用的一线抗结核药对肝脏几乎均具有潜在毒性,以异烟肼、利福平等药物性肝损伤最常见,甚至影响治疗进程[2-3]。异甘草酸镁作为一种肝细胞保护剂,其保肝抗炎、改善肝功能作用显著[4]。药效学研究表明其具有减轻肝细胞变性、坏死及炎细胞浸润等作用,临床研究证实异甘草酸镁能显著改善病毒性、药物性、酒精性等急慢性肝炎的临床症状和肝功能指标,且安全性高[5-6], 但该药用于治疗抗结核药物所致的中度以上急性肝损伤的疗效尚不确切。本研究观察了异甘草酸镁注射液结合传统保肝药物硫普罗宁在治疗抗结核药物性肝损伤中的有效性和安全性,现报告如下。
1资料与方法
选择2011年3月—2013年6月在山东省潍坊市寒亭区人民医院感染科门诊或住院治疗的结核患者1132例,均经标准化疗方案治疗,其中在治疗过程中发生中度以上药物性肝损伤者93例,肝损伤程度参照Maria评分标准[7]和中华医学会《急性药物性肝损伤诊治建议》[8],男36例,女57例;年龄18~78岁,平均(43.7±12.4)岁。根据治疗意愿将患者分为观察组57例和对照组36例。入选标准: ① 4项主要肝功能指标血清丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、碱性磷酸酶(ALP)及总胆红素(TBIL)中,至少1项检测值≥2倍正常上限(ULN); ② 肝功能异常持续时间2周~3个月; ③ 无既往肝病史患者或排除其他原因导致急性肝损伤; ④ 无严重心肺脑肾胃肠道及全身系统疾病。2组患者年龄、性别、病情程度等一般资料比较无显著差异(P>0.05)。
患者入组后均暂停抗结核药物,给予对症支持治疗,包括卧床休息,营养支持,食欲缺乏者静脉补充葡萄糖,同时维持水和电解质平衡及加速药物排泄。对照组应用200 mg硫普罗宁注射液加10%葡萄糖溶液250 mL静脉滴注;观察组为硫普罗宁200 mg加用异甘草酸镁注射液200 mg, 10%葡萄糖溶液250 mL静脉滴注, 1次/d, 疗程2周。治疗前后均行空腹采血,检测患者血尿常规和肝肾功能。
近期疗效评价标准[9]为:显效:治疗前4项肝功能指标(ALT、AST、ALP及TBIL)全部复常;有效:至少2个肝功能指标较治疗前下降≥50%;无效:未达显效或有效标准,总有效率=(显效+有效)例数/总例数×100%。
2结果
2.1 2组近期疗效比较
治疗前观察组ALT异常55例,AST异常52例, ALP异常34例,TBIL异常27例;对照组ALT异常36例,AST异常33例, ALP异常21例, TBIL异常19例,2组比较差异无统计学意义(P>0.05)。治疗后观察组显效31例,好转20例,无效6例,总有效率为89.5%(51/57), 对照组显效4例,好转16例,无效16例,总有效率为55.6%(20/36)。2组比较,差异有统计学意义(P<0.01)。
2.2 2组肝功能指标变化情况
治疗前2组ALT、AST、ALP和TBIL水平差异无统计学意义(P>0.05)。治疗后2组各项指标与治疗前相比均显著下降(P<0.01); 与对照组比较,治疗后观察组ALT、AST、TBIL下降显著,差异有统计学意义(P<0.01), 见表1。
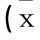
表1 2组肝功能指标治疗前后的变化情况±s)
与治疗前比较,**P<0.01; 与对照组比较,##P<0.01。
2.3 不良反应
观察组药物不良反应3例(5.2%), 包括1例眼睑水肿和2例皮疹,均为轻度,经对症治疗后恢复正常,未减量或停药;对照组不良反应2例(5.6%),包括1例乏力、纳差和1例腹胀。2组不良反应发生率差异无统计学意义(P>0.05),治疗后均未出现因药物引起的血、尿常规和肾功能异常。
3讨论
抗结核药物所致肝损伤是指在抗结核药物使用过程中,由于药物或其代谢产物引起的肝细胞毒性或肝脏对药物及代谢产物的变态反应所致的病理过程[10-12]。一旦发生,一般采取停用该药、抗感染、降酶、退黄等措施,造成抗结核治疗费用增加、周期延长、治疗成功率下降等不良影响[13]。抗结核药所致肝损伤的确切机制目前尚不明确,临床表现各异且无特异性,可为无症状性肝酶增高,也可为有肝炎样表现甚至肝衰竭,多发生于用药后1周~3月内,分别于1~2周和2个月左右出现高峰期[14]。
寻找快速、安全、有效治疗抗结核药物所致急性肝损伤的药物意义重大。异甘草酸镁作为第四代甘草酸制剂,具有较强的抗感染、保护肝细胞及改善肝功能的作用。药理研究表明,其对四氯化碳、D-氨基半乳糖及硫代乙酰胺引起的血清ALT、AST的升高有明显降低作用,具有较强的抗炎、保护肝细胞膜、解毒、抗生物氧化及改善肝功能作用[15-16]。并能显著减轻D-氨基半乳糖对肝脏的形态损伤和改善免疫因子对肝脏形态的慢性损伤。此外,药物性肝损伤中,异甘草酸镁能够抑制CYP450的表达,阻断CYP2E1、CYP1A1活化前体毒性药物,减少药物毒性,安全性较高[17]。
参考文献
[1]Bruixola G, Diaz-Beveridge R, Jimenez E, et al. Pleuropulmonary angiosarcoma involving the liver, the jejunum and the spine, developed from chronic tuberculosis pyothorax: Multidisciplinary approach and review of literature[J]. Lung Cancer, 2014, 86(1): 105.
[2]Debnath P K, Chattopadhyay J, Mitra A, et al. Adjunct therapy of Ayurvedic medicine with anti tubercular drugs on the therapeutic management of pulmonary tuberculosis[J]. J Ayurveda Integr Med, 2012, 3(3): 141.
[3]高丽, 李世明, 史哲, 等. GSTA1/GSTM3基因多态性与抗结核药物性肝损伤的相关性分析[J]. 中华疾病控制杂志, 2014, 18(7): 585.
[4]Huang X, Qin J, Lu S. Magnesium isoglycyrrhizinate protects hepatic L02 cells from ischemia/reperfusion induced injury[J]. Int J Clin Exp Pathol, 2014, 7(8): 4755.
[5]金雯彦; 于锋. 异甘草酸镁防治药物性肝损伤的药理及临床研究进展[J]. 药学进展, 2013, 37(4): 161.
[6]林睿, 周璐, 张洁, 等. 异甘草酸镁对自身免疫性肝炎单核细胞免疫功能影响的实验研究[J]. 上海交通大学学报: 医学版, 2014, 34(8): 1132.
[7]许彪, 何卫平, 张爱民, 等. 230例药物性肝损害与Maria诊断评分标准的关联性评价[J]. 中华消化杂志, 2008, 28(8): 566.
[8]中华医学会消化病学分会肝胆疾病协作组. 急性药物性肝损伤诊治建议(草案)[J]. 中华消化杂志, 2007, 27(11): 765.
[9]曾玲玲, 周桂琴. 药物性肝损害诊断标准及其临床应用[J]. 药物不良反应杂志, 2011, 13(1): 17.
[10]Chang K C, Leung C C, Yew W W, et al. Hepatotoxicity of pyrazinamide: cohort and case-control analyses[J]. Am J Respir Crit Care Med, 2008, 17(12): 1391.
[11]Xiang Y, Ma L, Wu W, et al. The incidence of liver injury in Uyghur patients treated for TB in Xinjiang Uyghur autonomous region, China, and its association with hepatic enzyme polymorphisms nat2, cyp2e1, gstm1 and gstt1[J]. PLoS One. 2014, 9(1): e85905.
[12]Lee K K, Boelsterli U A. Bypassing the compromised mitochondrial electron transport with methylene blue alleviates efavirenz/isoniazid-induced oxidant stress and mitochondria-mediated cell death in mouse hepatocytes[J]. Redox Biol, 2014, 2: 599.
[13]Devarbhavi H, Dierkhising R, Kremers W K, et al. Single-center experience with drug-induced liver injury from India: causes, out come, prognosis, and predictors of mortality[J]. Am J Gastroenterol, 2010, 105(11): 2396.
[14]Feng F M, Guo M, Chen Y, et al. Genetic polymorphisms in metabolic enzymes and susceptibility to anti-tuberculosis drug-induced hepatic injury[J]. Genet Mol Res, 2014, 13(4): 9463.
[15]徐中南, 吴锡铭, 王佩, 等. 18α甘草酸对D-氨基半乳糖引起的大鼠急性肝损伤治疗作用[J]. 临床肝胆病杂志, 2012, 28(1): 63.
[16]宋佳伟, 邢蓉. 异甘草酸镁的药理与临床[J]. 中国新药与临床杂志, 2012, 31(10): 578.
[17]陈东风, 孙文静, 熊吉. 药物性肝损伤的诊断与治疗[J]. 中华肝脏病杂志, 2012, 20(3): 170.
基金项目:中国高校医学期刊临床专项资金(11520131)
收稿日期:2014-11-15
中图分类号:R 575
文献标志码:A
文章编号:1672-2353(2015)05-106-02DOI: 10.7619/jcmp.201505035

