贝伐珠单抗对小鼠肾脏损害作用及机制研究
何艺 徐群红 陈雪琴 王鸣 费晓 赵宁 王本勇 谢祥成 邱冬豪
贝伐珠单抗对小鼠肾脏损害作用及机制研究
何艺 徐群红 陈雪琴 王鸣 费晓 赵宁 王本勇 谢祥成 邱冬豪
目的 了解贝伐珠单抗及不同剂量鼠源贝伐珠单抗对小鼠肾脏的损害作用并探讨其机制。方法 将42只C57BL/6小鼠随机分为对照组(12只)及贝伐珠单抗组、低剂量鼠源贝伐珠单抗组、高剂量鼠源贝伐珠单抗组(各10只)。4周后处死小鼠,收集尿液、血清,检测尿微量白蛋白(MA)、血清半胱氨酸蛋白酶抑制剂C(Cys-C)、血尿素氮(BUN)及血肌酐(Cr);取肾脏组织,HE染色后光镜观察肾脏组织结构,免疫荧光染色观察免疫复合物IgM、IgG、IgA沉积,免疫组化染色观察IgM、IgG、IgA、血管内皮生长因子(VEGF)及Nephrin表达,电镜观察肾脏组织超微结构。结果 贝伐珠单抗组、低剂量鼠源贝伐珠单抗组及高剂量鼠源贝伐珠单抗组尿MA、血清Cys-c水平均明显高于对照组,差异均有统计学意义(均P<0.05)。贝伐珠单抗组和高剂量鼠源贝伐珠单抗组血清BUN、Cr水平均高于对照组,差异均有统计学意义(均P<0.05)。高剂量鼠源贝伐珠单抗组血清BUN及Cr水平与贝伐珠单抗组、低剂量鼠源贝伐珠单抗组比较,差异均有统计学意义(均P<0.05)。贝伐珠单抗组免疫荧光IgG+~++;高剂量鼠源贝伐珠单抗组免疫荧光IgM++,免疫组化VEGF表达下调,电镜见肾小球足细胞足突融合。 结论 贝伐珠单抗引起肾脏损害的机制可能是下调VEGF的表达,引起免疫复合物沉积,导致肾小球内皮细胞足突融合,损害肾小球滤过膜,最终导致蛋白尿的形成及肾功能的损害。
贝伐珠单抗 肾脏损害 蛋白尿 肾脏病理
新型靶向药物贝伐珠单抗是Genentech公司开发的一种重组人源化单克隆抗体,自从美国FDA于2004年2月26日批准用于临床以来,国内外众多临床研究已显示,贝伐珠单抗临床使用安全性良好,主要不良反应为肾脏损害、高血压和出血,其中肾脏损害主要表现为蛋白尿,轻度蛋白尿发生率21%~63%,尽管发病率很高,大多数患者症状不严重,蛋白尿>3.5g/d约占6.5%,且蛋白尿可能与贝伐珠单抗呈剂量依赖性[1]。但它所引起蛋白尿等肾脏损害的机制、不同剂量引起肾脏损害的严重程度、早期检测方法及有效、安全的干预手段等,均还缺乏进一步的系统研究。本研究以C57BL/6小鼠为对象,观察贝伐珠单抗及不同剂量鼠源贝伐珠单抗对肾功能的损害作用,分析其引起肾脏损害的初步机制,为临床安全使用贝伐珠单抗提供理论依据。
1 材料和方法
1.1 材料 C57BL/6小鼠42只(上海斯莱克实验动物有限公司),月龄6~8个月,体重l8~22g。贝伐珠单抗购自罗氏公司;鼠源贝伐珠单抗(Recombinant Mouse VEGF)购自美国ebioscience公司;兔抗鼠VEGF抗体购自美国ebioscience公司;兔抗鼠Nephrin抗体购自美国ebioscience公司;DAB显色剂购自福州迈新生物技术开发公司;FITC标记兔抗小鼠抗体购自美国Sigma公司;760型全自动生化分析仪购自日本日立公司;OLYMPUSBX51lF320H1型光学显微镜、JEM-1230型透射电子显微镜购自日本电子株式会社;LKB-NOVA型超薄切片机购自瑞典LKB公司;低温高速离心机购自德国Heraeus公司。
1.2 方法 将小鼠随机分为4组,对照组12只,其余每组10只。对照组:给予0.9%氯化钠注射液10mg/kg尾静脉给药,5次/周;贝伐珠单抗组:给予5mg/kg尾静脉给药,5次/周;低剂量鼠源贝伐珠单抗组:给予2.5mg/ kg尾静脉给药,5次/周;高剂量鼠源贝伐珠单抗组:给予5mg/kg尾静脉给药,5次/周。4周后使用颈椎脱臼法处死小鼠,抽取血液280μl,膀胱穿刺法收集尿液500μl,并取肾脏组织,用于制作冷冻切片、石蜡切片和电镜标本。采用双缩脲法检测小鼠尿微白蛋白(MA),HcY循环酶法检测半胱氨酸蛋白酶抑制剂C(Cys-C),全自动生化分析检测血尿素氮(BUN)和血肌酐(Cr)。
1.3 光镜观察肾脏组织病理学改变 冷冻切片的标本在4%多聚甲醛中固定1h,接着用PBS液洗6次×30min,然后用25%蔗糖水脱水过夜,次日用冷冻切片包埋剂OCT包埋剂包埋、切片,并在-20℃中保存。用于石蜡切片的标本在甲醛中固定48h以上,再洗涤、脱水、透明、浸蜡、包埋、切片,最后在二甲苯里脱蜡,并于室温保存。光镜观察肾脏组织病理学改变。
1.4 免疫荧光染色观察免疫复合物沉积 将冷冻切片的标本从-20℃取出,平放在湿盒中晾干,1×PBS液洗3次×5min,封闭液(1×PBS+5%羊血清+0.3%Triton-100)封闭1h,加一抗(IgM抗体、IgG抗体及IgA抗体,1∶500,用封闭液稀释)4℃孵育过夜,1×PBS液洗3次×5min,加二抗(cy2、cy3荧光染料,1∶1 000,用封闭液稀释)室温孵育1h,DAPI(1∶5 000,用1×PBS液稀释)室温染细胞核5min,1×PBS液洗3次×5min,加抗淬灭剂封片。采用荧光显微镜观察并记录结果,根据显现的荧光强度来判断免疫复合物的多少:阴性;高倍镜下似乎可见为±;低倍镜下似乎可见,高倍镜下明显可见为+;低倍镜下明显可见,高倍镜下清晰可见为++;低倍镜下清晰可见,高倍镜下耀眼为+++;低倍镜下耀眼,高倍镜下刺眼为++++。
1.5 免疫组化染色观察免疫复合物、VEGF及Nephrin的表达 将石蜡切片的标本用微波法修复抗原(抗原修复液为柠檬酸盐缓冲液),每次中火5min,重复3遍。待冷却至室温后采用3%双氧水处理10min阻断内源性过氧化物酶,1×PBS液洗3次×5min,封闭采用正常山羊血清工作液室温孵育20min,加一抗(IgM抗体、IgG抗体、IgA抗体、VEGF抗体及Nephrin抗体)4℃过夜,1×PBS液洗3次×5min,加通用型生物素化二抗工作液室温孵育30min,1×PBS液洗3次×5min,HPR标记链亲和素工作液室温孵育30min,1×PBS液洗3次×5min,DAB显色3~5min,并用自来水终止显色。苏木精复染,盐酸乙醇分化,脱水,透明,封片,镜检。
1.6 透射电镜观察肾脏组织超微结构 用于电镜观察的肾脏组织标本在2.5%戊二醛中固定3d,用1×PBS液洗2次×15min,再用1%锇酸固定2h,用1×PBS液清洗2遍,然后用丙酮梯度脱水,最后用OCT包埋剂进行浸透和包埋,切片。在透射电子显微镜下观察各组大鼠肾脏组织超微结构并记录。
1.7 统计学处理 采用SPSS 18.0统计软件,计量资料以表示,多组间比较采用单因素方差分析,进一步两两比较采用SNK-q检验。
2 结果
2.1 各组小鼠尿MA和血清Cys-C、BUN、Cr水平的比较 见表1。
由表1可见,贝伐珠单抗组、低剂量鼠源贝伐珠单抗组及高剂量鼠源贝伐珠单抗组尿MA水平均明显高于对照组,差异均有统计学意义(均P<0.05),且尿MA水平随鼠源贝伐珠单抗的剂量增加呈上升趋势。贝伐珠单抗组、低剂量鼠源贝伐珠单抗组及高剂量鼠源贝伐珠单抗组血清Cys-c水平均明显高于对照组,差异均有统计学意义(均P<0.05),且血清Cys-c水平随鼠源贝伐珠单抗的剂量增加呈上升趋势。贝伐珠单抗组及高剂量鼠源贝伐珠单抗组血清BUN、Cr水平均明显高于对照组,差异均有统计学意义(均P<0.05)。高剂量鼠源贝伐珠单抗组血清BUN、Cr水平与贝伐珠单抗组比较,差异均有统计学意义(均P<0.05)。高剂量鼠源贝伐珠单抗组血清BUN、Cr水平与低剂量鼠源贝伐珠单抗组比较,差异均有统计学意义(均P<0.05)。
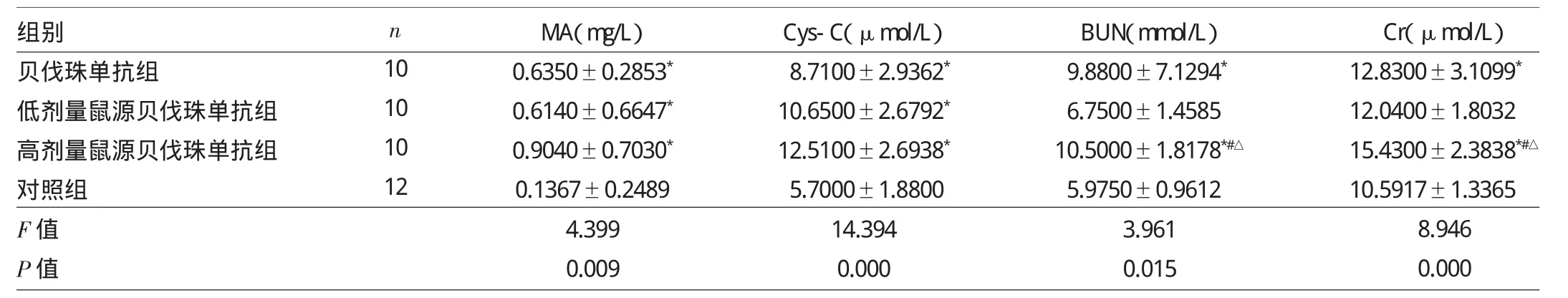
表1 各组小鼠尿MA和血清Cys-C、BUN、Cr水平的比较
2.2 病理检查结果
2.2.1 光镜所见 各组小鼠肾小球结构清晰,系膜区无明显增宽,系膜细胞及上皮细胞无明显增生,外周袢开放良好,详见图1(见插页)。
2.2.2 荧光显微镜所见 IgM抗体免疫荧光显示高剂量鼠源贝伐珠单抗组++,肾小球系膜区IgM成颗粒样分布,其他组未见免疫复合物沉积(图2,见插页);IgG抗体免疫荧光显示贝伐珠单抗组+~++,其他组未见免疫复合物沉积(图3,见插页);IgA抗体免疫荧光未见明显显像,提示无明显免疫复合物沉积(图4,见插页)。
2.2.3 免疫组化检测IgM、IgG及IgA 各组免疫组化无明显显像,IgM、IgG、IgA在系膜区、血管袢内外侧均未见明显沉积,详见图5-7(见插页)。
2.2.4 免疫组化检测VEGF表达 VEGF阳性细胞胞质染色为棕黄色,对照组、贝伐珠单抗组及低剂量鼠源贝伐珠单抗组均有棕黄色染色,而高剂量鼠源贝伐珠单抗组未见明显染色,表明VEGF的表达被抑制,提示高剂量鼠源贝伐珠单抗下调了VEGF的表达,详见图8(见插页)。
2.2.5 免疫组化检测Nephrin表达 Nephrin阳性细胞胞质染色为棕色,4组均呈现棕色(图9,见插页)。对Nephrin的免疫组化结果进行定量分析和统计,各组间的Nephrin表达比较差异无统计学意义(P>0.05),各剂量鼠源贝伐珠单抗均未影响Nephrin的表达,详见图10(见插页)。
2.2.6 电镜检查 高剂量鼠源贝伐珠单抗组可见足突广泛融合,各组中均无明显肾小球基底膜增厚,未见系膜基质增宽,无明显电子致密斑沉积的显像(图11,见插页),提示高剂量鼠源贝伐珠单抗通过对足细胞的损害可导致肾脏滤过膜的破坏。
3 讨论
贝伐珠单抗是一个针对VEGF靶点、作用机制相对明确的单克隆IgG抗体药物,由93%的人IgG1框架区和7%的鼠源性抗原结合互补决定区组成,可以与循环中VEGF的所有异构体发生竞争性高亲和力结合,阻止其与内皮细胞表面相应的VEGF受体结合,使受体无法活化,抑制内皮细胞有丝分裂,减少新生血管生成,从而阻止肿瘤细胞生长所需的血液、氧气和其它营养供应,抑制肿瘤的生长[2]。临床试验已证明,贝伐珠单抗联合化疗对转移性结直肠癌[3]、非小细胞肺癌[4]、转移性肾癌[5]及胶质母细胞瘤[6]等多种实体瘤有确切的疗效,并延长患者的无进展生存期和总生存期。国内外众多研究显示,其主要不良反应为肾脏损害、高血压和出血,其中肾脏损害主要表现为蛋白尿。
在肾脏中,肾小球足细胞和肾小管上皮细胞VEGF的表达最为突出[7],由肾小球脏层上皮细胞及远端集合管上皮细胞合成与分泌,尤其是近髓及髓放线处的肾小球足突细胞及小管上皮细胞。而VEGF受体主要分布在入球小动脉、肾小球和肾小管周围血管内皮细胞。肾单位逐渐减少的过程中,适量的VEGF可以促使肾小球和肾小管增生、肥大,进而维持肾小球结构和功能完整,具有保护肾功能的作用[8]。长期使用贝伐珠单抗可与VEGF结合,导致血管内皮损伤而出现肾脏损害,表现为内皮细胞孔径扩大,血浆蛋白渗入皮下,导致残余肾脏的肾小球硬化和肾小管间质纤维化的发展。
贝伐珠单抗在临床使用过程中引起肾脏损害、蛋白尿的主要机制为各种原因引起的足细胞或内皮细胞的损伤、内皮细胞表面多糖蛋白复合物的减少、VEGF的调节失衡等,可能的原因有:(1)贝伐珠单抗可能抑制足细胞VEGF的表达,下调足细胞裂孔隔膜膜蛋白Nephrin表达,引起肾小球内皮细胞肥大、脱落,从而引起多种肾小球、肾小管病变,导致肾小球滤过膜通透性增高,肾小球滤液中的蛋白质增多,超过了肾小管的重吸收能力时,最终导致蛋白尿的形成,严重者可引起肾病综合征[9]。(2)贝伐珠单抗可导致继发性高血压[10],引起肾小球内压增加,从而造成肾损伤。Teramachi等[10]对2010年2月至2011年2月期间接受贝伐珠单抗联合化疗的47例患者进行分析,表明收缩压(≥130mmHg)是贝伐珠单抗联合化疗导致蛋白尿的危险因素。(3)贝伐珠单抗可引起亚急性肾小球血栓性微血管病[11]。近期Izzedine等[12]随访了29例接受以VEGF为靶点的抗肿瘤治疗后,逐渐出现蛋白尿、高血压和(或)肾功能不全的患者,其中21例患者肾活检结果异常,血栓性微血管病占61.9%,相关肾小球中几乎检测不到VEGF水平。
尿MA是常规肾功能检查,可用于评价肾小球及近端肾小管功能。血清Cys-C水平已成为评估肾小球滤过率优于血肌酐的敏感指标[13]。本研究显示各实验组均可引起小鼠尿MA、血清Cys-C水平增高,提示尿MA、血清Cys-C可较敏感的反映肾脏功能的损害,且高剂量鼠源贝伐珠单抗组所引起小鼠尿MA、血清Cys-C水平较低剂量鼠源贝伐珠单抗组更明显,提示鼠源贝伐珠单抗对肾脏的损害呈现剂量依赖性。贝伐珠单抗组及高剂量鼠源贝伐珠单抗组可进一步引起血清BUN、Cr水平升高,也提示血清BUN、Cr水平的敏感性稍差。此外,本实验研究对象为C57BL/6小鼠,贝伐珠单抗为重组人源化单克隆抗体,由93%的人IgG1框架区和7%的鼠源性抗原结合互补决定区组成,鼠源性贝伐珠单抗较其更具有种族优势,对小鼠肾脏的损害相对更明显。
本研究发现高剂量鼠源贝伐珠单抗组较其他组VEGF棕色染色较轻,提示高剂量鼠源贝伐珠单抗下调了VEGF的表达,考虑高剂量鼠源贝伐珠单抗与小鼠体内VEGF结合,导致了VEGF表达减少;而Nephrin在各组间未见明显的差异,可能与此次实验用药时间较短、剂量不足相关,故而在VEGF下游的Nephrin表达未受到影响。通过本研究可以证明贝伐珠单抗通过减少VEGF的表达造成肾脏滤过膜破坏,从而造成肾小球功能损伤。此外,免疫荧光染色显示高剂量鼠源贝伐珠单抗组免疫复合物IgM沉积较其他组明显,同时IgG抗体免疫荧光显示贝伐珠单抗组+~++,由此提示贝伐珠单抗导致的尿蛋白与免疫复合物沉积有关。
贝伐珠单抗及各剂量鼠源贝伐珠单抗组均未引起小鼠HE染色组织病理学的改变,仅电镜观察到高剂量鼠源贝伐珠单抗组肾小球内皮细胞足突融合,一方面考虑贝伐珠单抗的肾脏损伤作用可能为一过性,未造成永久性的病理改变;另一方面,可能与贝伐珠单抗用药时间不够长、用药剂量不够大有关。若进一步研究贝伐珠单抗所致肾脏损害的分子机制,需要建立更为理想的实验模型,国外研究提示转基因小鼠可能较为理想,但是受动物实验条件和实验费用限制,目前国内尚未建立此模型。
目前临床上应用抗VEGF靶向治疗的大多为晚期恶性肿瘤患者,需长程单一使用贝伐珠单抗,或联合顺铂等化疗药物同时使用。早期识别贝伐珠单抗等抗VEGF药物的并发症可以允许医师及时地调整药物剂量、积极干预,从而进行序贯治疗,使患者获得最大益处。基于本实验,笔者建议在临床上可以将尿MA、血清Cys-C作为早期监测指标,联合血清BUN、Cr的检测,并密切随访血压,及时发现贝伐珠单抗引起肾脏的早期损害,从而指导临床医师及时调整用药方案、尽早积极干预。对于有肾脏疾病史及尿蛋白阳性的患者,当尿蛋白+++或24h尿蛋白>3.5g时需要请肾脏专科医师会诊,必要时考虑永久停药。
综上所述,本研究显示贝伐珠单抗引起肾脏损害的机制可能是下调VEGF的表达、引起免疫复合物沉积、导致肾小球内皮细胞足突融合,进一步损害肾小球滤过膜,最终导致蛋白尿的形成及肾功能的损害,初步证实了贝伐珠单抗对小鼠肾脏功能的损害及其机制。
[1] Zhu X,Wu S,Dahut W L,et al.Risks of proteinuria and hypertension with bevacizumab,an antibody against vascular endothelial growth factor:systematic review and meta-analysis[J].Am J Kidney Dis,2007,49(2):186-193.
[2] Vaziri S A,Kim J,Ganapathi M K,et al.Vascular endothelial growth factor polymorphism s:role in response and toxicity of tyrosine kinase inhibitors[J].Curr Oncol Rep,2010,12(2):102-108.
[3] Deng T,Zhang L,Liu X J,et al.Bevacizumab plus irinotecan, 5-fluorouracil,and leucovorin(FOLFIRI)as the second-line therapy for patients with metastatic colorectal cancer,a multicenter study[J].Med Oncol,2013,30(4):752.
[4] RaezLE,Santos ES,Webb R T,et al.Amulticenterphase II study of docetaxel,oxaliplatin,and bevacizumab in first-line therapy forunresectable locally advanced or metastatic non-squamous cell histology non-small-cell lung cancer (NSCLC)[J].Cancer Chemother Pharmacol,2013,72(5):1103-1110.
[5] Melichar B,Bracarda S,Matveev V,et al.A multinational phase II trial of bevacizumab with low-dose interferon-alpha2a as first-line treatment of metastatic renal cell carcinoma:BEVLiN[J]. Ann Oncol,2013,24(9):2396-2402.
[6] Arakawa Y,MizowakiT,Murata D,et al.Retrospective analysis of bevacizumab in combination with ifosfamide,carboplatin,and etoposide in patients with second recurrence of glioblastoma[J]. Neurol Med Chir(Tokyo),2013,53(11):779-785.
[7] Tesarova P,Tesar V.Proteinuria and hypertension in patients treated with inhibitors of the VEGF signalling pathway--incidence,mechanism s and management[J].Folia Biol(Praha),2013, 59(1):15-25.
[8] 赵静,李航,张力,等.四例贝伐单抗所致肾损害临床和病理特征分析[J].中国医学科学院学报,2012,34(2):153-158.
[9] Izzedine H,Massard C,Spano J P,et al.VEGF signalling inhibition-induced proteinuria:Mechanisms,significance and management[J].Eur J Cancer,2010,46(2):439-448.
[10] Teramachi H,Shiga H,Komada N,et al.Risk factors contributing to urinary protein expression resulting from bevacizumab combination chemotherapy[J].Pharmazie,2013,68(3):217-220.
[11] Luthra S,Narayanan R,Marques L E,et al.Evaluation of in vitro effects of bevacizumab(Avastin)on retinal pigment epithelial, neurosensory retinal,and microvascular endothelial cells[J]. Retina,2006,26(5):512-518.
[12] Izzedine H,MangierM,Ory V,et al.Expression patterns of RelA and c-mip are associated with different glomerular diseases following anti-VEGF therapy[J].Kidney Int,2014,85(2):457-470.
[13] Weinert L S,Prates A B,Do A F,et al.Gender does not influence cystatin C concentrations in healthy volunteers[J].Clin Chemlab Med,2010,48(3):405-408.
Bevacizumab-induced renal impairment in mice and its mechanism
HE Yi,XU Qunhong,CHEN Xueqin,et al.Department of Nephrology,Hangzhou Geriatric Hospital,Hangzhou 310022,China
Bevacizumab Renal impairment Proteinuria Renalpathology
2015-07-19)
(本文编辑:严玮雯)
杭州市卫生科技计划(2011Z002);吴阶平医学基金会临床科研专项资助基金(320.6750.12364)
310022杭州市老年病医院内科(何艺);杭州市第一人民医院肾内科(徐群红、王鸣、费晓、赵宁、王本勇、谢祥成、邱冬豪),肿瘤内科(陈雪琴)
徐群红,E-mail:helloxqh@sina.com
【 Abstract】 Objective To investigate bevacizumab-induced renal impairment in mice and its mechanism. Methods Forty two C57BL/6mice were randomly divided into 4 groups:control group(n=12),bevacizumab group(n=10),low-dosemurine bevacizumab group(n=10),high-dosemurine bevacizumab group(n=10).The animals were sacrificed 4 weeks after treatment, and urine,serum and renal tissue samples were collected.The urinary micro-albumin (MA),serum cystatin C (Cys-C),blood urea nitrogen(BUN)and creatinine(Cr)were measured.Renal morphological changes and ultrastructural changes were observed by HE staining-light microscopy and electron microscope,respectively.Immune complexes IgG/IgA/IgM deposition in renal tissue was detected with immunofluorescence and immunohistochemisty,the expression of VEGF and nephrin in renal tissue was examined by immunohistochemisty. Results Compared with control group,the levels of urinary MA and serum cys-C were significantly increased in bevacizumab group,low-dose and high-dose murine bevacizumab groups(P<0.05).Compared with control group,the levels of serum BUN and Cr were significantly increased in bevacizumab group and high-dose murine bevacizumab group(P<0.05).The serumlevels of BUN and Cr in high-dose murine bevacizumab group were remarkably higher than that in bevacizumab group and low-dose murine bevacizumab group(P<0.05).Pathological results showed that the immune complexes IgG deposition in bevacizumab group showed+~ ++in immunofluorescence staining.High-dose murine bevacizumab group immunofluorescence IgM deposition ++ and the expression of VEGF was decreased in immunohistochemistry.Meanwhile electron microscopy showed that foot processes of glomerular podocytes were significantly fused in high-dose murine bevacizumab group. Conclusion Bevacizamab-induced renal impairment is associated with down-regulation of VEGF expression and immune complexes deposition,which may lead to the podocytes foot processes fusion and renal function impairment.

