硝酸钾生产工艺概述及复分解法存在的问题与对策*
段正康,谢 帆,张 涛,李 晟,闫建华
(湘潭大学化工学院,湖南湘潭411105)
硝酸钾生产工艺概述及复分解法存在的问题与对策*
段正康,谢 帆,张 涛,李 晟,闫建华
(湘潭大学化工学院,湖南湘潭411105)
概述了国内外生产硝酸钾的4种主要工艺方法:硝酸钠与氯化钾转化法、硝酸铵与氯化钾离子交换法、硝酸与氯化钾溶剂萃取法和硝酸铵与氯化钾复分解循环法,并比较了这4种不同生产工艺方法的特点。其中硝酸铵与氯化钾复分解循环法是中国生产硝酸钾主要采用的工艺方法,重点介绍了该工艺存在的一些主要问题,如硝酸钾分离效果差,硝酸钾冷却结晶率低,结晶器换热面结垢严重,除杂效果不理想等,并提出了相应的建议与改进措施。
硝酸钾;生产工艺;复分解循环法;改进措施
硝酸钾又名硝石、盐硝、火硝,化学式为KNO3,是一种无氯高品质肥料和无机化工产品,在农业和工业上均有广泛的应用。农业上,硝酸钾作为一种优质的无氯钾肥,特别适用于烟草、咖啡、茶叶、花卉等忌氯喜钾的旱地经济作物,而且硝酸钾作为肥料是由有效物质组成,施用后不会改变土壤质量或引起作物病变;工业上,硝酸钾主要用于制造火药、金属焊接助剂、合成氨催化剂、玻璃制品、陶瓷等;食品方面可用作肉制品的发色剂、防腐剂等;医药方面还可用作利尿剂、清凉剂以及生产青霉素钾盐、利福平等药物[1-2]。此外,工业级硝酸钾在玻璃制造方面的应用上近年来也展现了良好的发展前景[3],早前美国就已经开始将硝酸钾用于光学玻璃的制造,现在很多玻璃厂家也相继开始采用硝酸钾生产手机屏幕和平板电脑等高端化学强化玻璃,随着中国经济持续、稳定的发展,硝酸钾的发展空间将会越来越大,市场需求也会不断地增加。
目前,国内外生产硝酸钾的主要工艺有转化法、离子交换法、溶剂萃取法和复分解法,其中复分解法是中国生产硝酸钾的主要工艺方法[4-5]。笔者简要介绍了这4种工艺,对复分解循环法生产硝酸钾存在的主要问题做了分析,并提出了相应的改进措施。
1 硝酸钾主要生产工艺
1.1 硝酸钠与氯化钾转化法
20世纪50年代以前,硝酸钾的生产工艺主要采用以智利硝石和氯化钾为原料的转化法,利用可溶性盐在不同温度下溶解度的差异来达到生产硝酸钾的目的。此法的副产物为氯化钠,反应式如下:
KCl+NaNO3→KNO3+NaCl
在循环母液中溶解氯化钾和智利硝石,先通过蒸发、增浓、离心分离得到氯化钠副产物,再将分离的母液加水调节浓度、经真空冷却结晶、增浓、离心分离得到粗硝酸钾,最后通过精制釜重结晶可得到工业级的硝酸钾产品。工艺流程如图1所示。
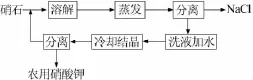
图1 复分解循环法工艺流程图
1986年,新疆乌宗布拉克地区发现了罕见的钾硝石矿,吐鲁番地区化工厂首创了直接从钾石矿中提取硝酸钾的工艺[6]。经分析,该矿还含有较多硝酸钠,张永录[7]提出可以通过加入氯化钾将矿石中的硝酸钠转化为硝酸钾产品。但该法在蒸发结晶提取氯化钠的操作过程中容易产生爆沸现象,不利于真空高效蒸发器及多效蒸发设施的采用,而且经此法析出的氯化钠晶体晶粒细、质量差、过滤困难,析出的硝酸钾晶体质量也不高。为克服这些不足,张罡[8]研发了先提硝酸钾,后提氯化钠的方法。该法在硝酸钾冷却结晶析出的过程中,氯化钠没有达到饱和,不会有晶体析出,因此所得的硝酸钾晶粒大,晶体质量好,同时其副产物氯化钠晶体晶粒大,夹带的硝酸钾含量少,容易过滤分离。
转化法流程简单,主要缺点是容易受到资源的限制,副产物氯化钠市场价值不大,集中堆放会对环境造成污染。
1.2 硝酸铵与氯化钾离子交换法
离子交换树脂是一种功能型高分子材料,可解离出阳离子或阴离子基团,其功能主要是实现树脂内部的相对离子与水中存在同电荷的离子的交换反应[9]。当溶液中的钾离子通过铵型离子交换树脂时,与树脂中的铵离子发生交换反应,为吸附反应,离子交换树脂由铵型转变为钾型,反应式为:
RNH4+KCl=RK+NH4Cl
当溶液中的铵离子通过钾型离子交换树脂时,与树脂中的钾离子发生交换反应,为洗脱反应,同时离子交换树脂由钾型变为铵型,反应式为:
RK+NH4NO3=RNH4+KNO3[10-11]
先将氯化钾溶液打入离子交换柱内进行吸附反应,反应生成的氯化铵溶液经三效蒸发、冷却结晶、增浓、离心分离得氯化铵产品;再将硝酸铵溶液打入离子交换柱内进行洗脱反应,反应生成的硝酸钾溶液经三效蒸发后,再经冷却结晶、增浓、离心分离、干燥、造粒即可得到颗粒硝酸钾产品。工艺流程如图2所示。
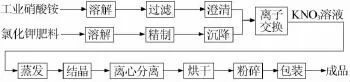
图2 离子交换法工艺流程图
为了解决固定床离子交换技术存在的“浓度脉冲”现象,美国先进分离技术公司(简称AST)研究开发了ISEP技术,即连续式离子交换技术。该法流出的硝酸钾溶液纯度高,工艺流程短,可连续操作[12];主要缺点是交换所得溶液浓度低,蒸发成本高,设备要求较高。
1.3 硝酸和氯化钾溶剂萃取法
溶剂萃取法大体可分为3类:萃取HCl法[13]、萃取HNO3法[14]、HCl和HNO3分别萃取法[15-17]。以色列利用有机溶剂萃取HCl的IMI法是目前主要应用在工业上的溶剂萃取法,该工艺在低温和有机溶剂的存在下不容易发生副反应,副产物盐酸可用于分解磷矿生产磷酸。反应式为:
KCl+HNO3→KNO3+HCl
氯化钾与冷却的硝酸以化学计算量加入到5~10℃下的串联反应器中,循环液与溶剂也一并加入槽中,反应完全后再通过分离、干燥得到硝酸钾产品。系统中未反应的硝酸和盐酸被移除到溶剂相中,对溶剂相进行处理,回收纯的盐酸,剩余溶剂和硝酸的混合物循环返回反应系统。工艺流程如图3所示。
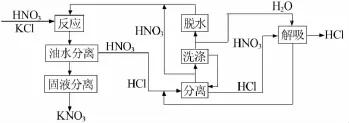
图3 溶剂萃取法工艺流程图
硝酸和氯化钾溶剂萃取法工艺是在常温、低压的条件下操作,需配置冷冻装置,由此增加了能耗;萃取剂使用异戊醇,在工厂应用中有爆炸的危险;副产物盐酸的质量分数只有22%左右,不能作为商品出售。王振山等[18]采用磷酸三丁酯为萃取剂,脱芳烃煤油为稀释剂对溶剂相中的硝酸进行萃取,经3次萃取后,母液中的硝酸基本上能被全部除去,剩余母液主要含有盐酸和钾盐,通过萃取或蒸馏可得到高纯度的盐酸。常福松[19]采用辛烯醛为萃取剂,萃取后用水对其洗涤,剩余的萃余相再通过选择性较好的萃取剂乙醇将水相中的硝酸萃取出来,此方法能使硝酸的质量分数降至10%~30%,得到的副产物为纯净的盐酸,可作为商品直接出售。
1.4 硝酸铵与氯化钾复分解法
复分解法制取硝酸钾分为非循环法和循环法2种。陈文威[20]采用复分解非循环法制备硝酸钾,在剩余母液中加入磷肥蒸发后还可得到含氮、磷、钾等含多种元素的复合肥料。复分解循环法则是由法国Auby公司最早开发,在工艺上又分为3步循环法和4步循环法,二者主要区别在于3步循环法析出硝酸钾晶体的温度为0℃,而4步循环法为20℃,析出硝酸钾晶体后3步循环法升温至60℃直接析出氯化铵晶体,而4步循环法需先加入硝酸铵升温浓缩后,再降温冷却至60℃析出氯化铵晶体[21]。3步循环法虽然操作流程相对简单,但其在析出硝酸钾时需人工制冷,而且结晶范围小,产品收率比较低,因此中国大部分企业采用4步循环法工艺生产硝酸钾。此外,如果使用硝酸铵溶液为原料,4步循环法则需先将硝酸铵溶液中的水蒸发除去,由此导致能耗增加;而3步循环法则可将溶液中的水作为系统所需水的一部分直接参与生产,因此3步循环法特别适用于以半成品硝酸铵溶液为原料的生产工艺[22-23],其反应式为:
NH4NO3+KCl→KNO3+NH4Cl
将氯化钾经计量在溶解槽中溶解,过滤除去杂质后与来自氯化铵离心机的二次母液及精制母液在二次母液槽中混合,制成合格的原液。原液经换热器换热降温流入真空结晶器,通过真空冷却结晶后,析出粗硝酸钾,经粗钾稠厚器增稠后进行离心分离,干燥后得到农用硝酸钾产品,通过精制釜重结晶即可制得工业级别的硝酸钾产品。同时将离心分离的一次母液送入一次母液槽,加入一定量的硝酸铵溶液,通过换热器升温后进入二效蒸发室蒸发、浓缩,再通过氯化铵冷却结晶釜冷却降温,析出氯化铵粗品,经氯化铵稠厚器增稠后进行离心分离,可得到氯化铵副产品,二次母液槽可循环使用[24]。工艺流程如图4所示。

图4 复分解循环法工艺流程图
复分解工艺原料来源较广,成本低,工艺设备简单,投资少,见效快,蒸发能耗低,副产品氯化铵容易回收,可用作混合肥料,基本无环境污染。赵家春[25]提出将析出的硝酸钾晶体在复分解装置中进行重新加水、加热、溶解、过滤再降温析出的复分解反应,可以有效地提高硝酸钾的产品含量和生产收率。
由上述生产工艺可以看出,硝酸钾一般情况下是以廉价易得的氯化钾与硝酸盐为原料制备得到的。目前,以色列和智利是世界上最大的硝酸钾生产国,中国产量位居第三。以色列主要采用溶剂萃取法制取硝酸钾,智利因具有得天独厚的硝酸钠矿石资源,主要采用转化法制取硝酸钾[26]。中国硝酸钾生产历史比较长,20世纪80年代初期,中国开始采用离子交换法生产硝酸钾,20世纪80年代中期,又研究开发了复分解法生产硝酸钾,该法现已实现连续化生产,成为中国生产硝酸钾的主要工艺方法[27]。
2 复分解法现有问题的分析
中国复分解法生产硝酸钾工艺经过多年的发展,存在它特有的优势,但该技术仍存在一些不足需要改进[28]。
2.1 硝酸钾分离效果差
作为复分解法生产硝酸钾工艺中主要副产物氯化铵,如何将其与硝酸钾完全分离是生产高纯度硝酸钾的关键。传统的方法是通过若干个结晶器分别单独完成硝酸钾半成品的结晶及氯化铵的分离过程,得到硝酸钾固液混合物,再经过滤、漂洗等后续处理制成硝酸钾成品,这种结晶分离方法耗时长,分离出的氯化铵含钾量高,硝酸钾损失大,清水使用量大,收率低,很难获得高质量的硝酸钾。针对这一问题,赵家春[29]对硝酸钾中分离氯化铵的方法做了改进,采用若干结晶器串联浮选分离,半成品过滤器及排放液漂洗分离相结合的方法,其中排放液漂洗方法有别于传统的分离方法,即将各种不同浓度的过滤溶液排放于同一储存罐中用作硝酸钾初成品漂洗水,它采用的是将不同生产工序中排放出的过滤液分别单独对硝酸钾初产品进行漂洗分离,最后再用清水洗涤的方法,此法经2次过滤,多次漂洗,使硝酸钾的生产结晶时间缩短,损耗降低,清水使用量减少,分离效果好,产品质量得到提高。朱建江[30]将传统方法中2次结晶所得的固液混合物先用生产过程中产生的结晶水、洗涤水或者清水重新进行固液调配,体积比为(20~40)∶100,再通过重力选矿设备进行固液分离,有效地提高了氯化铵的结晶质量,减少了氯化铵中携带硝酸钾的含量,降低了硝酸钾的损失。
2.2 硝酸钾冷却结晶率低
硝酸钾结晶率是指溶液冷却结晶析出的硝酸钾晶体中钾离子占原溶液中钾离子的百分数。理论上,只要工艺条件和工艺参数选择恰当,操作无误,硝酸钾的结晶率可以达到65%以上,但大部分企业在生产过程中硝酸钾的结晶率一般只有40%~45%。这可能是因为K+与NH4+的离子半径十分接近(K+为0.133 nm,NH4+为0.143 nm),在结晶过程中存在晶格互相取代,或者以某种形式相互深入到晶体中去。因此,在硝酸钾和氯化铵的结晶过程中,不仅仅有单一的硝酸钾和氯化铵的结晶,还有一部分复盐K2NH4(NO3)3、(K·NH4)Cl2和固溶体NH4·K(NO3)2生成,从而导致硝酸钾的结晶率低[31]。针对此现象,沈晃宏等[32-33]提出在溶液中加入助剂硝酸钠,改变溶液形成固溶体和复盐的特性,从而达到改善产品结晶质量,提高产品产率的目的。
2.3 结晶器换热面结垢严重
中国硝酸钾冷却结晶工艺主要有自然冷却工艺、蛇管冷却工艺、夹套冷却工艺、真空冷却工艺、喷雾冷却工艺、自冷冷却工艺和长槽搅拌冷却工艺,其中蛇管和夹套冷却结晶工艺为中国大多数企业所采用[34]。虽然各种冷却工艺采用的结晶器有所不同,但均存在不同程度的换热面结垢现象,严重时会导致热阻增加,传热系数减少,能耗增加,生产效率降低。据分析[35-36],换热面结垢原因主要有2个:1)因为水的极性分子作用,换热器表面金属发生水化,表面金属离子借由水化面进入溶液中的金属表面层中,致使结晶器钢材表面带有负电荷,吸附溶液中的阳离子,当换热面冷却时其表面吸附的硝酸钾分子诱使硝酸钾晶核在吸附层生长,成为晶体;2)因为分子间的相互作用力,紧靠金属表面溶液中的硝酸钾晶体与金属表面形成的硝酸钾晶体会连接在一起,形成结垢。为提高硝酸钾的结晶效率,防止结垢,可以适当提高溶液中n(NH4+)/n(K+)值,使金属表面层吸附的NH4+增多,K+相对减少。但n(NH4+)/n(K+)值不宜太高,否则会降低硝酸钾的产率。或者对金属表面层进行化学抛光或者电化学抛光处理,使换热面产生一层光滑的覆盖层,降低金属表面静电层的电荷密度,减弱吸附作用,减少结垢。但不能对金属表面进行机械抛光处理,否则会破坏金属表面的氧化膜,加强水化作用,加大静电荷密度,使结垢现象更加严重。
2.4 除杂效果不理想
复分解法制备硝酸钾体系中杂质的主要来源: 1)原料氯化钾带入的杂质,主要有氯化钠、氯化镁、硫酸钾和碳酸钾;2)反应中的副产物氯化铵。硝酸钾产品中上述杂质含量如果超标,会加强黑火药、导火索的吸湿性,影响质量,严重的会造成重大伤亡事故。同时杂质中氯化钠含量过高则会腐蚀金属,硫酸钾含量过高则会降低光学玻璃的透明度,氯化镁含量过高则会使母液蒸发困难,换热面结垢严重。因此,为了得到高纯度的硝酸钾,生产过程中必须加强对杂质的处理[37-38]。
3 结语
综上所述,转化法容易受到资源的限制,离子交换法设备成本比较高,溶剂萃取法工厂存在爆炸的风险;而复分解法原料来源广、成本低、工艺设备简单、蒸发能耗低,已经成为中国生产硝酸钾的主要方法。尽管如此,该方法在生产上仍然存在硝酸钾分离效果差、冷却结晶率低、换热面结垢严重和除杂效果不理想等问题,有待继续改进和完善,向高品质、高效益的硝酸钾生产模式发展。
[1] 刘风方,亓昭英,谢军旺.发展具有我国特色的硝酸钾生产[J].矿业快报,2004,20(11):4-7.
[2] 汪家铭.我国硝酸钾发展概况与市场前景[J].化工科技市场,2009,32(1):23-28.
[3] René Gy.Ion exchange for glass strengthening[J].Materials Science and Engineering:B,2008,149(2):159-165.
[4] 李雅芙,刘素芹.硝酸钾生产工艺综述[J].海湖盐与化工,2004,34(3):27-30.
[5] 李刚,张廷福.我国硝酸钾技术进展[J].无机盐工业,1999,31(2): 21-23.
[6] 李佳鹏,余福元,白灵卫,等.利用钾长石制取硝酸钾的方法:中国,103539166A[P].2014-01-29.
[7] 张永录.钾硝石矿提取硝酸钾新工艺[J].无机盐工业,1993,25(4):3-5.
[8] 张罡.硝酸钠转化法制取硝酸钾新工艺[J].化工设计,2009,19(5):11-13,33.
[9] 钱庭宝,许风楼.离子交换树脂的应用技术(Ⅰ)[J].化工进展,1986:48-51,44.
[10] Alvaro Abidaud.Continuous production of potassium nitrate via ion exchange:US,5110578[P].1992-05-05.
[11] 车荣睿.离子交换法制备硝酸钾[J].辽宁化工.1987(6):29.
[12] 张沂圭,王增平.连续式离子交换法生产硝酸钾[J].硫磷设计与粉体工程,2000(1):30-32.
[13] 谢伟胜.溶剂萃取法制取硝酸钾研究进展[J].现代化工,2008,28(6):32-36.
[14] Portela L S.Process for obtaining potassium nitrate from potassium chloride and nitric acid:US,4668495[P].1987-05-26.
[15] Manor S,Bar-Guri M,Alexandron A,et al.Process for the manufacture of potassium nitrate with co-production of hydrochloric acid:US,4364914[P].1982-12-21.
[16] Manor S,Bar-Guri M,Alexandron A,et al.Process for the manufacture of potassium nitrate:US,4378342[P].1983-03-29.
[17] 王桂云,陈之川,马林松,等.溶剂萃取法制备农用硝酸钾[J].无机盐工业,1998,30(3):13-15.
[18] 王振山,刘鸿雁,郝杰,等.萃取法制取硝酸钾的工艺研究[J].吉林化工学院学报,2004,21(2):1-3.
[19] 常福松.一种溶剂萃取法制取硝酸钾的方法:中国,101734690A[P].2010-06-16.
[20] 陈文威,郎小川.硝酸铵和氯化钾生产硝酸钾的研究[J].适用技术市场,2000(2):25-26.
[21] 赵启文.温度对复分解法制硝酸钾生产过程的影响[J].盐湖研究,2001,9(3):43-45.
[22] 张建策.复分解法生产硝酸钾工艺研究[J].海湖盐与化工,2002,31(4):12-14.
[23] 张罡,沈晃宏,张一甫.复分解三步循环法生产硝酸钾[J].现代化工,2002,22(1):41-42,44.
[24] 姚涛.年产2万吨工业硝酸钾装置工程设计总结[J].安徽化工,2006,32(5):34-36.
[25] 赵家春.复分解法生产硝酸钾的方法:中国,101659431A[P]. 2009-03-03.
[26] 张宝全.中国硝酸盐资源开发利用现状及其前景展望[J].化工矿物与加工,2007,36(11):1-5,24.
[27] 张罡,夏重阳,何斌鸿,等.我国硝酸钾市场竞争力分析[J].化学工业,2007,25(9):16-17.
[28] 张罡,易健民,沈晃宏.复分解法生产硝酸钾技术存在的问题与建议[J].化肥设计,2006,44(3):39-41.
[29] 赵家春,赵晨.硝酸钾生产中分离氯化铵的方法及分离装置:中国,102092747A[P].2011-06-15.
[30] 朱建江.硝酸钾生产方法的改进:中国,103253687A[P].2013-08-21.
[31] 史建斌,于湖.浅谈硝酸钾的结晶[J].无机盐工业,2000,32(3): 26-27.
[32] 沈晃宏,谭淑珍,张罡.万吨级硝酸钾生产装置[J].化工设计通讯,2001,27(3):43-46.
[33] 沈晃宏,张罡,张一甫.复分解三步循环法生产硝酸钾:中国,1388065A[P].2003-01-01.
[34] 张罡,何斌鸿,沈晃宏.硝酸钾冷却结晶技术进展及应用[J].化肥设计,2008,46(2):59-61,64.
[35] 张罡,李岳华.硝酸钾生产中的防结垢方法[J].化肥工业,2001,28(3):52-53.
[36] 张罡.浅谈硝酸钾结垢与防治方法[J].化肥设计,2001,39(6): 42-34.
[37] 阎天太.复分解法生产硝酸钾的除杂质[J].无机盐工业,1985,17(1):30.
[38] 牟邦志,牟红光.一种高纯度、大批量硝酸钾的制备方法:中国,103204522A[P].2013-07-17.
Summary of production process of potassium nitrate and existing problems and solutions in complex decomposition cycle method
Duan Zhengkang,Xie Fan,Zhang Tao,Li Sheng,Yan Jianhua
(College of Chemical Engineering,Xiangtan University,Xiangtan 411105,China)
The four main production technologies,including conversion method of sodium nitrate and potassium chloride,ion exchange method of ammonium nitrate and potassium chloride,solvent extraction method of nitric acid and potassium chloride,and complex decomposition cycle method of ammonium nitrate and potassium chloride,of potassium nitrate both in China and abroad were summarized.The characteristics of these four different production technologies were compared.In the four kinds of production technologies,complex decomposition cycle method of ammonium nitrate and potassium chloride is the main production technology for potassium nitrate in China.Some major existing problems,such as poor separation effect of potassium nitrate,bad cooling crystallization effect of potassium nitrate,serious scaling of heat exchange surface of crystallizer,and bad purification,in this production technology were introduced emphatically.Furthermore,advices and measures for improving these problems were put forward.
potassium nitrate;production process;complex decomposition cycle method;improving measures
TQ131.13
A
1006-4990(2015)05-0004-05
2014-11-29
段正康(1964— ),男,教授,硕士生导师。主要从事化学品的定性与定量分析方法建立研究;医药及其中间体、染料及其中间体等的合成方法研究;加氢与脱氢催化剂的合成与表征方法研究;高端玻璃制造用材料的制备与表征研究等。已发表核心期刊论文20多篇,授权发明专利3件。
湖南省科技厅工业支撑计划重点项目(2014GK4013)。
联系方式:dzk0607@163.com

