Co-Cu/ZrO2-La2O3催化剂用于合成气制低碳醇的研究
潘东明,刘贵龙,刘 源
(天津大学化工学院,天津 300072)
在世界的能源构成中,煤炭资源占了几乎80%,以煤为原料,制备合成气(CO+H2),而后通过合成气催化制备低碳醇具有重要的战略意义和应用前景[1-2]。低碳醇作为良好的汽油添加剂或汽油替代品燃烧充分、效率高且 CO、NOx及烃类排放量少,具有重要的环保和经济价值[3]。Cu-Co基催化剂因其在较温和的条件下,具有较高的活性和较好的低碳醇选择性,被视为前景较好的合成低碳醇催化剂体系之一[4-5]。目前所报道的关于铜钴催化剂催化合成气反应的原理研究通常认为铜和钴会形成双金属活性中心,它们的协同作用促使了醇的合成[4-6]。铜钴合金的形成,会在很大程度上影响反应的活性和选择性,所以如何改善铜钴双金属的分布状态,使它们产生更好的协同作用促进反应的进行,一直是铜钴催化剂研究的重点。
Nguyen等研究了 LaCo1-xCuxO3(x=0~0.6)催化剂用于合成低碳醇反应,结果表明,LaCo1-xCuxO3钙钛矿中铜和钴经还原之后形成了氧化镧负载铜钴合金颗粒,有效地减少催化剂表面金属粒子的团聚,提高了催化剂性能[7-8]。Fang通过对 Co3O4/LaFe0.7Cu0.3O3前驱体进行还原处理,得到 LaFeO3钙钛矿负载的Cu@Co和Cu-Co alloy,对合成低碳醇反应有较好的活性、选择性和稳定性[9]。事实上,以钙钛矿性复合氧化物为前驱体形成的铜钴催化剂,可以使铜钴成比例的在载体上呈原子水平均匀分散,经还原后铜钴较容易产生相互作用或形成合金,促进合成低碳醇反应的进行。但由于这种制备方法制备出的催化剂载体含量被限制,使得它的比表面积较小,铜钴活性组分在较高温度下易烧结,抑制了反应的进行。
本研究采用多次浸渍法制备了x%LaCo0.7Cu0.3O3/ZrO2(x=12,16,18)催化剂。 一方面可以有效地提高催化剂的比表面积,改善铜钴纳米粒子在载体表面的分散状态,利于形成合金、抑制它们的烧结和团聚;另一方面催化剂前驱体经还原之后形成氧化镧可作为助剂有利于催化反应的进行;此外利用氧化锆载体本身对合成低碳醇反应的催化效果,可提高反应的活性与C2+醇的选择性。
1 实验部分
1.1 催化剂的制备
采用沉淀法制备氧化锆载体[10]。将一定浓度的氧氯化锆水溶液滴加到氨水中,控制pH值在9~10之间。沉淀物在母液中室温陈化12 h后,洗涤过滤至无Cl-存在。用无水乙醇洗涤后于110℃下干燥10 h,700℃下煅烧5 h后得到氧化锆载体。
柠檬酸络合-多次浸渍法制备 x%LaCo0.7Cu0.3O3/ZrO2(x=12, 16, 18)[11],即将特定比例的硝酸镧、硝酸钴、硝酸铜溶于一定量去离子水中,向混合溶液中加入一定量柠檬酸和乙二醇[n(La+Co+Cu)∶n(柠檬酸)∶n(乙二醇) =1.00∶1.20∶0.24],85℃下搅拌至全部溶解后以等体积浸渍法将一定量前驱体浸渍到氧化锆载体上。浸渍完后的样品室温静置24 h,120℃下干燥24 h,300℃下焙烧2 h,升温速率为2℃/min。再次重复上述等体积浸渍过程后,将干燥后样品于300℃煅烧2 h,650℃下煅烧5 h,得到上述催化剂。采用同样的方法制备16%LaCoO3/ZrO2作为对比。
1.2 催化剂的性能评价
催化剂在加压微型固定床催化反应器上进行性能评价,在内径为8 mm的不锈钢反应管,装填800 mg催化剂,颗粒度为80~100目。反应前首先将催化剂在反应器中于650℃通入纯氢原位还原,然后降至室温切换成合成气升压至3 MPa,从室温加热至310℃进行连续反应,合成气H2/CO/N2的体积比为 8∶4∶1。 生成的气相产物 CH4、CO2与未反应的H2和CO一起由六通阀取样进入SP3400气相色谱仪,通过TDX-01分子筛进行在线分析,检测器为热导检测器(TCD);气相烃类和经过冷凝后的液相产物通过Porapak Q柱进行离线分析,检测器为氢火焰检测器(FID)。色谱载气为高纯 He,柱前压为69 kPa。
1.3 催化剂的表征
由Bruker D8-Focus X射线衍射仪测定催化剂的物相组成,Cu-Kα射线(λ=0.15406 nm),管电压和管电流分别为40 kV和40 mA,扫描角度为20°~52.5°,扫描速率为 5(°) /min。 采用 Quantachrome QuadraSorb SI型自动物理吸附仪测定各催化剂的比表面积,测试前样品在300℃下真空脱气4 h。程序升温还原的测定采用Thermo-Finnigan吸附-脱附-还原-反应多功能实验装置。以体积分数为5%H2-Ar混合气为还原气,还原气流速:20 mL/min,试样用量为50 mg,颗粒度为80~100目。将样品放置好后,以10℃/min的速率从室温升至850℃,TCD检测。样品的微观形貌采用JEOL JEM-2100F电子显微镜测试,样品经研磨和超声分散后置于镍网之上,经真空蒸发碳膜处理后,在200 kV下观测。
2 结果与讨论
2.1 催化剂的XRD
图1为x%LaCo0.7Cu0.3O3/ZrO2样品和载体ZrO2的XRD图,ZrO2以单斜相为主,混有少量的四方相,x%LaCo0.7Cu0.3O3/ZrO2样品在 2θ≈33°找到了钙钛矿的衍射峰,说明钙钛矿负载到氧化锆载体上。与LaCoO3/ZrO2样品的钙钛矿主衍射峰相比,x%LaCo0.7Cu0.3O3/ZrO2的钙钛矿衍射峰向高角度偏移,这主要是由于Cu2+的离子半径(0.0730 nm)小于Co3+的离子半径(0.0745 nm),Cu2+取代 Co3+之后,减小了LaCoO3的晶面间距,使得2θ角向高角度有不同程度的偏移[9]。反过来讲,衍射峰的偏移也说明 Cu2+进入了 LaCoO3钙钛矿的晶格,即LaCo0.7Cu0.3O3物相的形成。

图 1 x%LaCo0.7Cu0.3O3/Z rO2(x=12,16,18)和ZrO2的XRD谱图Fig.1 XRD patterns of x%LaCo0.7Cu0.3O3/Z rO2(x=12,16,18) and ZrO2
图2为x%LaCo0.7Cu0.3O3/ZrO2在H2气氛下经还原之后的 XRD图(还原条件:T=650℃,流量30 mL/min)。还原后,钙钛矿的衍射峰消失,氧化锆的衍射峰没有发生改变,表明氧化锆载体在还原气氛下稳定。将40°~46°范围内的XRD谱图放大,在含量为x=16和18还原后的样品中于2θ≈43.7°出现了Co0.52Cu0.48合金的衍射峰。但 x=12时并未找到合金的衍射峰,说明生成的CoCu合金高度分散。LaCo0.7Cu0.3O3中 La/(Co+Cu)的原子比例为1,在还原气氛下随着CoCu合金的形成,会有La2O3的形成,但未找到 La2O3的衍射峰,文献[12]中有报道La2O3在ZrO2上负载量质量分数高于14%时才可以找到La2O3的衍射峰。综上,经还原后形成了氧化镧修饰的氧化锆负载钴铜合金催化剂(Co-Cu/ZrO2-La2O3)。
反应后的XRD如图3所示,还原过程中形成的CoCu合金的衍射峰消失,在 x=16和18的样品中检测到了微弱的Co2C的衍射峰。表明还原形成的CoCu合金中的Co转化成了 Co2C,由于 Cu的高分散并未找到其衍射峰。Volkova[13]报道在合成气气氛下,CoCu合金促进了 Co2C的形成,Co2C通过活化非解离的CO并将其插入到Cn(n≥1)物种中,进而生成了醇。所以,在反应过程中形成了氧化镧修饰的氧化锆载体负载的Cu和Co2C颗粒(Co2C-Cu/ZrO2-La2O3),其中Co2C和Cu是合成醇的活性组分。

图2 x%LaCo0.7Cu0.3O3/ZrO2经还原后的XRD谱图Fig.2 XRD patterns of x%LaCo0.7Cu0.3O3/ZrO2after reduction

图3 x%LaCo0.7Cu0.3O3/ZrO2经反应后的XRD谱图Fig.3 XRD patterns of x%LaCo0.7Cu0.3O3/ZrO2after reaction
2.2 催化剂的BET和TEM表征
样品比表面积数据见表1。载体ZrO2的比表面积为92.2 m2/g,负载LaCo0.7Cu0.3O3后比表面积在56.9~63.2 m2/g之间,且随着 LaCo0.7Cu0.3O3负载量的增加,比表面积减少。这是由于负载钙钛矿量越大,越容易堵塞氧化锆载体的孔道。

表1 样品比表面积和LaCo0.7Cu0.3O3平均颗粒尺寸Tab le 1 BET surface areas and the mean particle size of LaCo0.7Cu0.3O3
图4为样品16%LaCo0.7Cu0.3O3/ZrO2在氢气气氛下于650℃还原3 h后的TEM图。

图4 16%LaCo0.7Cu0.3O3/ZrO2经还原之后的TEM图Fig.4 TEMmicrographs of 16%LaCo0.7Cu0.3O3/ZrO2after H2reduction
由图4可以看到有纳米颗粒分散在氧化锆表面上。对其进行傅里叶变换,将变换后的结果分别作为插图列于图 4a)和 4b)中。晶面间距 0.207和0.126 nm分别归属为 Co0.52Cu0.48的[111]和[220]晶面。结合XRD可判定样品经还原后形成了氧化镧修饰的氧化锆负载钴铜合金催化剂(Co-Cu/ZrO2-La2O3)。
2.3 H2-TPR表征
图5为x%LaCo0.7Cu0.3O3/ZrO2和LaCoO3/Zr O2的程序升温曲线。
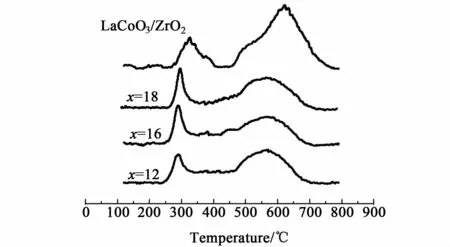
图5 x%LaCo0.7Cu0.3O3/ZrO2和LaCoO3/ZrO2的TPR图Fig.5 TPR p rofiles of x%LaCo0.7Cu0.3O3/ZrO2and LaCoO3/ZrO2
由图5可以看出所有的催化剂有2个还原峰。在300℃左右的低温还原峰对应Cu2+→Cu0、Co3+→Co2+的还原,在600℃的还原峰对应 Co2+→Co0以及部分Co3+→Co0的还原[14-15]。在负载量较低的x=12样品中,低温还原峰比负载量为 x=18的样品低10℃左右,高温还原峰的温度也较低。说明LaCo0.7Cu0.3O3的负载量越低,分散度越高,对应的还原温度也越低。与16%LaCoO3/ZrO2的还原峰相比,x%LaCo0.7Cu0.3O3/ZrO2的2个还原峰向低温方向有很大的偏移,这是由于在氢气的气氛下x%LaCo0.7Cu0.3O3/ZrO2中 Cu2+在较低温度下先还原为铜纳米粒子,生成的铜纳米粒子极大促进了相邻Co3+的还原,显著的降低了 Co的还原温度[9]。TPR结果表明,在T=650℃下 x%LaCo0.7Cu0.3O3/ZrO2可以被还原为 Co-Cu/ZrO2-La2O3,生成的La2O3作为助剂一方面可以提高抑制 ZrO2载体烧结,另一方面在合成气气氛下可以促进Co2C的生成进而催化醇产物的生成[16-17]。
2.4 催化性能评价
表2为 x%LaCo0.7Cu0.3O3/ZrO2催化剂上 CO加氢合成低碳醇反应。
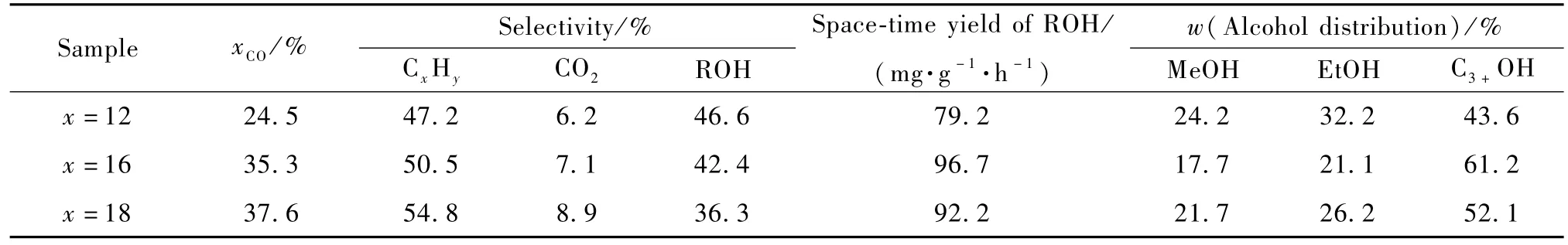
表2 CO加氢合成低碳醇的催化性能Table 2 Catalytic performance of CO hyd rogenation over the experimen tal catalysts
由表2可以看出在T=310℃时,催化剂都具有较好的醇选择性。随着负载量的增加CO的转化率由24.5%提高到37.6%,同时烃类与CO2的选择性随着负载量的升高而增大,导致醇的选择性由46.6%下降到36.3%;醇的选择性与CO转化率的共同作用使催化剂的时空产率随着负载量增加先增大后减小。由液相产物分布可以看出,催化剂具有良好的C2+醇的选择性,当x=16时液相产物中C2+醇含量占到82.3%。表3为文献中具有代表性催化剂CO加氢合成低碳醇的催化性能,与之相比可以看出x%LaCo0.7Cu0.3O3/ZrO2催化剂表现出了很好的醇选择性特别是C2+醇的选择性,有较大的应用潜力。
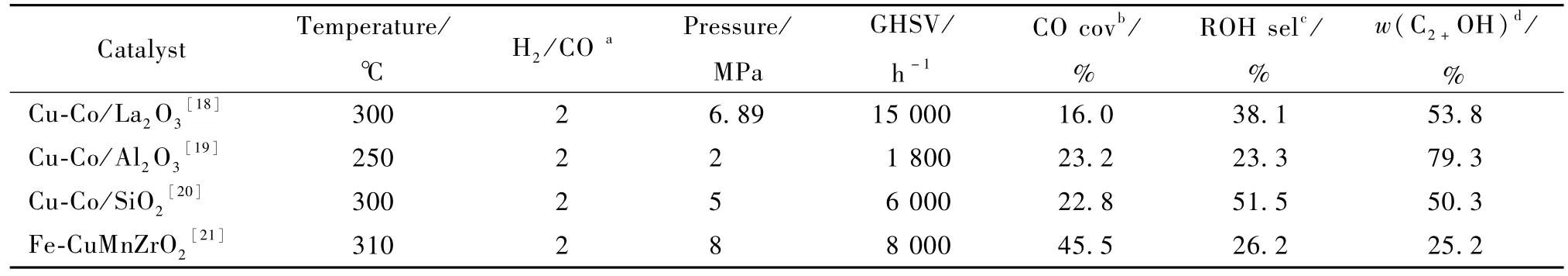
表3 文献中有代表性催化剂CO加氢合成低碳醇的催化性能Tab le 3 Catalytic performance of CO hyd rogenation over some rep resen tative catalysts repor ted in literatures
催化剂具有较好的醇选择性的原因是:一方面,还原后形成的 Cu-Co合金和 La2O3在合成气气氛会促进 Co2C的形成,催化剂前驱体变为 Co2CCu/ZrO2-La2O3,Co2C和Cu的共同作用促进了醇的生成;另一方面,文献报道[22],在合成低碳醇的反应中,四方相的ZrO2可以催化乙醇的生成,而单斜相的ZrO2可以催化异丁醇的生成。综上可以得出,氧化镧修饰的氧化锆载体和还原后分散在其表面的Cu-Co合金颗粒之间的共同作用使其具有很好的醇选择性特别是低碳醇的选择性。
3 结论
采用柠檬酸络合-多次浸渍法制备出了ZrO2负载LaCo0.7Cu0.3O3钙钛矿结构的催化剂,经还原形成了经氧化镧修饰的氧化锆负载钴铜合金催化剂(Co-Cu/ZrO2-La2O3)。 由同一个 LaCo0.7Cu0.3O3大分子还原而得的CoCu合金与La2O3的相互作用,在合成气气氛下促进了反应活性组分Co2C和Cu的形成;氧化镧修饰的氧化锆载体与其表面高度分散的CoCu合金颗粒之间的共同作用使催化剂显示了优良的醇选择性特别是C2+醇的选择性;x%LaCo0.7Cu0.3O3/ZrO2系列催化剂具有较大的应用潜力。
[1]Li D,Ma Y,Qi H,et al.Progress in synthesis ofmixed alcohols fromCO hydrogenation[J].Progress in Chemistry,2004,16(4): 584-592
[2]Mahdavi V,Peyrovi MH.Synthesis of C1-C6alcohols over copper/cobalt catalysts:Investigation of the influence of preparative procedures on the activity and selectivity of Cu-Co2O3/ZnO, Al2O3catalyst[J].Catalysis Communications,2006,7(8): 542-549
[3]Fang K,Li D,Lin M,et al.A short reviewof heterogene ous catalytic process for mixed alcohols synthesis via syngas[J].Catalysis Today, 2009, 147(2): 133-138
[4]Xiao K,Bao Z,Qi X,et al.Advances in bifunctional catalysis for higher alcohol synthesis fromsyngas[J].Chinese Journal of Catalysis, 2013, 34(1): 116-129
[5]Xu H,Chu W,Shi L,et al.Effect of glowdischarge plasma on copper-cobalt-aluminumcatalysts for higher alcohols synthesis[J].Journal of Fuel Chemistry and Technology, 2009, 37(2): 212-216
[6]Liu J,Ding M,Wang T,et al.Promoting effect of cobalt addition on higher alcohols synthesis over copperbased catalysts[J].Advanced Materials Research,2012,550:270-275
[7]Tien-Thao N,Alamdari H,Zahedi-Niaki MH,et al.LaCo1-xCuxO3-δperovskite catalysts for higher alcohol syn-thesis[J].Applied Catalysis A: General, 2006,311:204-212
[8]Nguyen T T,Zahedi-Niaki MH,A lamdari H,et al.Co-Cu metal alloys fromLaCo1-xCuxO3perovskites as catalysts for higher alcohol synthesis fromsyngas[J].International Journal of Chemical Reactor Engineering,2007, 5(1): 1 542-6 580
[9]Fang Y,Liu Y,Zhang L.LaFeO3-Supported nano Co-Cu catalysts for higher alcohol synthesis fromsyngas[J].Applied Catalysis A: General, 2011, 397(1):183-191
[10]Chuah G K, Jaenicke S, Pong B K.The preparation of high-surface-area zirconia:II.Influence of precipitating agent and digestion on the morphology and microstructure of hydrous zirconia[J].Journal of Catalysis, 1998,175(1): 80-92
[11]Colonna S, De Rossi S, Faticanti M, et al.Zirconia supported La, Co oxides and LaCoO3perovskite: Structural characterization and catalytic CO oxidation[J].Journal of Molecular Catalysis A: Chemical, 2002, 180(1): 161-168
[12]Sun H, Ding Y, Duan J, et al.Transesterification of sunflower oil to biodiesel on ZrO2supported La2O3catalyst[J].Bioresource Technology, 2010, 101 (3):953-958
[13]Volkova G G,Yurieva T M,Plyasova L M,et al.Role of the Cu-Co alloy and cobalt carbide in higher alcohol synthesis[J].Journal of Molecular Catalysis A: Chemical, 2000, 158(1): 389-393
[14]Toniolo F S, Magalhães R N SH, Perez C A C, et al.Structural investigation of LaCoO3and LaCoCuO3perovskite-type oxides and the effect of Cu on coke deposition in the partial oxidation ofmethane[J].Applied Catalysis B: Environmental, 2012, 117: 156-166
[15]Lisi L, Bagnasco G, Ciambelli P, et al.Perovskite-Type oxides:II.Redox properties of LaMn1-xCuxO3and La-Co1-xCuxO3and methane catalytic combustion[J].Journal of Solid State Chemistry, 1999, 146(1): 176-183
[16]Lebarbier V M, Mei D, KimD H, et al.Effects of La2O3on the mixed higher alcohols synthesis fromsyngas over Co catalysts:A combined theoretical and experimental study[J].The Journal of Physical Chemistry C,2011, 115(35): 17 440-17 451
[17]Trunschke A, Hoang D L, Radnik J, et al.Influence of lanthana on the nature of surface chromiumspecies in La2O3-modified CrOx/ZrO2catalysts[J].Journal of Catalysis, 2000, 191(2): 456-466
[18]Tien-Thao N, Zahedi-Niaki MH, Alamdari H, et al.Conversion of syngas to higher alcohols over nanosized LaCo0.7Cu0.3O3perovskite precursors[J].App lied Catalysis A: General, 2007, 326(2): 152-163
[19]Wang J, Chernavskii P A, Khodakov A Y, et al.Structure and catalytic performance of alumina-supported copper-cobalt catalysts for carbon monoxide hydrogenation[J].Journal of Catalysis, 2012, 286: 51-61
[20]Deng S, Chu W, Xu H, et al.Effects of impregnation sequence on the microstructure and performances of Cu-Co based catalysts for the synthesis of higher alcohols[J].Journal of Natural Gas Chemistry, 2008, 17(4):369-373
[21]Xu R,Yang C,WeiW,et al.Fe-Modified CuMnZrO2catalysts for higher alcohols synthesis fromsyngas[J].Journal of Molecular Catalysis A: Chemical, 2004, 221(1): 51-58
[22]He D,Ding Y,Luo H,et al.Effects of zirconia phase on the synthesis of higher alcohols over zirconia and modified zirconia[J].Journal of Molecular Catalysis A:Chemical, 2004, 208(1): 267-271

