金属有机框架材料在化学传感器中的应用
尚树川,孔令强,蔡婷婷,康 琪,申大忠
(山东师范大学化学化工与材料科学学院,山东济南250014)
金属有机框架材料在化学传感器中的应用
尚树川,孔令强,蔡婷婷,康 琪,申大忠*
(山东师范大学化学化工与材料科学学院,山东济南250014)
金属有机框架(metal-organic frameworks,MOFs)是一类由金属离子(簇)与有机桥联配体通过自组装连接而成的具有纳米孔穴的超分子晶体材料。它们具有极大的比表面积、可调控的孔径和拓扑结构、良好热稳定性和化学稳定性等优点,在化学传感方面有良好的应用前景。该文综述了近年来MOFs化学传感器方面的研究进展,侧重于光学、电化学、微天平、光电流等类型MOFs传感器的信号传导策略及其在检测挥发性有机物、金属离子、DNA、蛋白质及其它重要生物分子的分析应用。
金属有机框架;光学;电化学;微天平;综述
0 引言
金属有机框架 (metal-organic frameworks, MOFs)是由金属离子(簇)与含氧或氮的有机配体通过自组装连接而成的具有周期性网状结构的晶体材料,具有超大的比表面积和孔容积、可调的孔径和拓扑结构、良好的热稳定性和化学稳定性等优点[1]。在近年来,有关MOFs材料的研究领域发展迅猛,人们不仅设计合成了各种结构与性质的MOFs材料,而且开发了它们在气体储存、催化剂、吸附与分离等方面的应用[2-5]。此外,MOFs材料独特的光电特性及其它性质,使它们成为研制高性能化学传感器的重要敏感材料[6-8],该文选取部分有代表性的研究工作,简要介绍近几年来MOFs在化学传感器方面的研究和应用进展。
1 基于MOFs的光学传感器
MOFs具有丰富的多孔拓扑结构,当它们与待测物相互作用时,如果其结构或性质发生变化能引起荧光或颜色变化,为开发基于MOFs的光学传感器提供了有利条件。例如,以镧系金属离子为中心离子的很多MOFs,具有优良的固体荧光特性,待测物与之作用引起荧光光谱或强度的改变,而MOFs所具有的类似分子筛空间结构,使它们对目标分子的尺寸和分子结构具有一定的选择性,这种性质可用于金属离子以及小分子的传感监测[9]。因此,基于MOFs发光特性的传感分析是目前化学传感器领域中较为活跃的研究方向之一。
快速检测炸药及其类似物质关系到国家安全和环境保护。Pramanik等[10]报道了一种可用于选择性检测高能炸药及其它芳香烃的MOFs,它具有发达的三维多孔结构和很强的发光特性,含有吸电子基的化合物可使其荧光猝灭,而含有供电子基的化合物则使其荧光增强,并通过分子轨道理论对该现象进行了讨论分析。Campagnol等[11]在导电基底上以电化学方法合成了含Tb的发光MOFs膜,其荧光强度随2,4-二硝基甲苯(DNT)浓度的增加而下降,可用于炸药的测定,检测下限约为0.01 mmol/L。Gole等[12]合成了三种发光的Zn基MOFs,配体中的芳香环结构能够增强MOFs中的π-电子密度。基于荧光淬灭原理,这些富电子高发光性的MOFs可用于检测爆炸性硝基化合物。当这些MOFs分散在乙醇中时具有很强的荧光,存在硝基化合物时发生了荧光淬灭。与其它缺电子芳烃比较,所制备的三种MOFs对硝基化合物如DNT、TNT和TNB有较高的选择性,对TNT的检测限达到10-7%水平,且能重复使用。Nagarkar等[13]设计合成了一种多孔Zr-MOFs,其荧光也可被TNT猝灭,选择性很高,其它硝基苯类化合物的干扰较小,可用于水相中TNT的传感检测。
挥发性有机物 (volatile organic compounds, VOCs),是指沸点介于50~250℃的化合物,室温下饱和蒸气压超过0.001大气压,在常温下能够以蒸气形式存在于空气中的一类有机物,它们对人体健康有很大的危害,灵敏快速地检测VOCs是一项重要的环境分析任务。Lu等[14]利用光的干涉效应,不仅制备了随膜厚度变化的MOFs色阶条带,而且将其应用于丙烷浓度测定。Li等[15]设计合成了一种Ln-MOF,它与N,N-二甲基甲酰胺(DMF)蒸气接触,由DMF与配体相互作用产生强的荧光,且对DMF具有选择性的响应,当用水蒸气去除DMF后,其荧光猝灭。Shustova等[16]制备了两种在高温下仍旧具有很强的荧光的MOFs,Zn2(tcpe)与Mg(dhbdc),在常温下,Zn2(tcpe)对多种分析物包括NH3、三乙胺、乙二胺、N2、N,N-二乙基甲酰胺与H2O都有响应,当温度升高到100℃,这种MOF对NH3具有很高的选择性,而对其它分析物无响应。Zhang等[17]报道了一种2D层状具有宽通道的MOFs,这种特殊结构展示了很高的气体吸附性,吸附多种VOCs后具有荧光应答响应,在化学传感方面有良好的应用前景。Wan等[18]通过水热法合成了钇掺杂的MOF-5,并制备了基于催化发光的气体传感材料,当异丁醇接触这种材料的表面时,可观察到催化发光。在优化条件下,该传感器对异丁醇的检测下限为3.7 mg/L,与MOF-5相比,钇掺杂的MOF-5对异丁醇有更好的催化发光响应。Liu等[19]采用以四苯基乙烯为母体的配体与Zn2+反应,制备出多孔的[Zn2(TCPPE)],该MOFs具有很强的荧光,当它吸附VOCs后,或发射峰蓝移或荧光猝灭,可用于VOCs传感监测。
高效测定有机溶剂中水分含量的传感器在化学工业中有大的市场需求。Douvali等[20]合成了一种含Mg2+的MOFs,它在微量水(0.05%~5%, V/V)存在下产生荧光,可以用于多种有机溶剂中水分的测定,传感器响应快速可逆,具有良好的可重复使用性。Ohira等[21]利用MOFs(Cu-BTC)晶体在干燥条件下呈深蓝色而吸附水分后颜色变浅的原理,将Cu-BTC作为光导纤维传感器的敏感膜用于工业气体中含水量的测定,检测下限约为5×10-4%(V/V),该传感器响应快速、可逆,长期稳定性好。
手性分析是一项具有挑战性的分析测定工作。Wanderley等[22]用具有手性的桥联配体合成了一种高度多孔和强荧光的MOFs,其荧光能被氨基醇与配体间的氢键作用所猝灭,可用于手性氨基醇的传感检测,MOFs中的微通道对分析物具有富集作用有利于提高检测灵敏度,对映选择性源自MOFs中孔穴的手性识别特性,实验测定了四种氨基醇的Stern-Volmer常数为490~31200 L/mol,对映选择比为1.17~3.12。Qin等[23]合成了一种非贯穿的手性多孔多功能的MOFs,它的荧光发射峰可通过改变溶剂分子而调控,对质子溶剂与非质子溶剂表现出不同的荧光响应特性。例如,在乙酸中荧光发射峰位于556 nm,而在正己烷中发射峰蓝移151 nm至405 nm,实验发现发射峰位置与强度和溶剂的介电常数有一定的关联性,该MOFs有望用于传感和吸附小分子。
表面增强拉曼散射(SERS)的信号强度高度地依赖于分析物与纳米结构金属基底之间的相互作用与距离。Kreno等[24]利用层层自组装的方法在纳米Ag颗粒上生长可控厚度的Cu3(BTC)2(H2O)3(BTC=均苯三甲酸)膜,可大幅度提高局域表面等离子体共振的检测灵敏度,它对CO2的响应信号是单纯使用纳米Ag颗粒的14倍。Hu等[25]将嵌入MIL-101中的金纳米粒子(AuNPs)用于高灵敏SERS检测,所制备的AuNPs/MIL-101纳米复合材料综合了金纳米粒子的局域表面等离子共振性质和MOFs的高吸附性能,使分析物有效地富集在SERS活性金属表面的电磁场附近,大幅度地提高了SERS基底的响应灵敏度,在所用实验条件下,对罗丹明6G和对二氨基联苯的检测下限分别为42和0.54 fmol,该基底具有良好的响应稳定性和重现性以及分子筛效应。所建立的SERS方法用于对苯二胺和α胎甲球蛋白的测定,线性范围分别为1~100 ng/mL和1~130 ng/mL,检测下限为0.1 ng/mL。
离子组分的测定是一项重要的分析工作。Xiao等[26]合成了一种含稀土的可发光Eu-MOF,其微孔结构能够高效灵敏地实现对Cu2+识别。He等[27]在MOFs的配体中引入烷基硫醚单元,所得MOFs晶体对Pd(II)具有选择性的识别作用,低浓度的Pd(II)即可引起晶体颜色的显著变化,可用于Pd(II)的显色分析,其响应机制为多个官能团的共同作用,而且负载Pd的MOFs晶体是一种高效催化剂。Yang等[28]研究报道了基于离子交换原理的荧光法测定Fe3+,其原理如图1所示,MIL-53(Al)具有强荧光而MIL-53(Fe)荧光很弱,当MIL-53(Al)中的Al3+与溶液中的Fe3+进行离子交换,使MIL-53(Al)发生荧光淬灭,实现了对水溶液中Fe3+的选择性与灵敏检测,其线性范围在3~200 μmol/L,检测下限为0.9 μmol/L。

图1 基于离子交换原理荧光法检测Fe3+原理示意图[28]Fig.1 Schematic Illustration of the Cation Exchange Mechanism for the Use of MIL-53(Al)as a Fluorescent Probe for Sensing Fe3+[28]
Zhao等[29]将带正电的MOFs与带负电的ZnO量子点结合在一起设计成一种能够检测磷酸盐的荧光传感器,通过电子转移使ZnO量子点发生荧光淬灭,而加入磷酸根离子以后可以阻止这种淬灭并使ZnO量子点恢复荧光,荧光强度与磷酸根离子的浓度相关,磷酸根阻止ZnO量子点荧光淬灭的机理在于破坏MOFs的结构进而阻止MOFs与ZnO的结合。该传感器具有良好的响应灵敏度,线性范围在0.5~12 μmol/L之间,检测下限是53 nmol/L。
Lin等[30]将具有强荧光且带有胺基末端的碳量子点(BPEI-CQDs)组装到ZIF-8中去,合成一种新的荧光化MOFs。这种新的荧光化MOFs不仅具有卓越的荧光活性、对BPEI-CQDs灵敏的选择性,而且基于MOFs的吸附特性,能够对目标分析物进行大量并且选择性地富集(见图2)。这种BPEI-CQDs/ZIF-8复合物可用作制备检测Cu2+的超灵敏高选择性的传感器,其检测范围是2~1000 nmol/L,检测下限达80 pmol/L,并且已经成功应用于检测环境水样中的Cu2+浓度。

图2 基于碳量子点/ZIF-8荧光探针传感Cu2+原理图[30]Fig.2 Concept and process for sensing Cu2+based on fluorescence of carbon quantum dots in ZIF-8[30]
Hao等[31]合成了一种氧化石墨烯(GO)修饰的具有高荧光性能的Zn-MOFs,该材料具有良好的水分散性,当水溶液中有Cu2+时,Zn-MOFs中的配体与Cu2+作用会发生荧光猝灭,因此可用来检测溶液中的Cu2+含量,响应快速且选择性高,检测下限可达到1 μmol/L。Carboni等[32]合成了两种具有Zr-OXO二级结构单元的MOFs,配体分别是顺丁烯二酸(MOF-1)和正交琥珀酸(MOF-2),利用MOF-2在Mn2+的水溶液中的荧光猝灭,对Mn2+检测下限可达到8 nmol/L。Song等[33]在纳米SiO2表面合成一层 ZIF-8薄膜,合成多孔SiO2@ZIF-8材料。这种纳米材料对Cu2+展现出非常好的吸附性和富集性,其中咪唑基团中的N原子起到了非常大的作用。Cu2+浓度在 10~500 nmol/L范围内,荧光信号呈现良好的线性,检测下限可达到3.8 nmol/L,还可检测环境水样中的痕量的Cu2+。
近年来,MOFs材料在生物分析中的应用备受关注。Fang等[34]利用DNA嵌入染料与MOFs进行无标记的、灵敏的荧光方法识别特定序列DNA,以MIL-101作为淬灭平台,可以降低DNA探针复合物中荧光染料SYBR Green(SG)的背景荧光。其机理如图3所示:MIL-101通过π-π堆叠,以及静电相互作用,强烈吸附DNA探针复合物中的SG,使SG染料的荧光强度大大降低。当加入靶DNA后形成的双链DNA将远离MIL-101表面,而SG染料则以嵌入与小沟结合的方式与双链DNA结合,使SG染料的荧光强度大大增强,检测下限达73 pmol/L,大大低于碳纳米管与氧化石墨烯平台,MIL-101的引入,使信噪比提高了8倍。

图3 利用DNA嵌入染料在无MIL-101(A)及有MIL-101时降低背景信号(B)检测靶DNA示意图[34]Fig.3 Schematic illustration of using DNA-intercalating dye without(A)or with MIL-101 as a low background signal platform(B)for the detection of target[34]
Yang等[35]合成了Co-BTC,因其催化性能可提高鲁米诺的化学发光强度,其机理有可能是在Co-MOFs活性金属位点与氧自由基之间形成了过氧化氢类似物。Co-MOFs-鲁米诺体系能够用于检测L-半胱氨酸,在优化条件下,L-半胱氨酸的检测范围为 0.1~10 μmol/L,检测下限达18 nmol/L。Liu等[36]利用聚乙烯亚胺作为连接器将金纳米粒子 (AuNPs)通过静电吸引组装到Fe-MIL-88表面,所得杂化材料Au@Fe-MIL-88具有类过氧物酶活性。单链DNA很容易吸附在其表面,降低它的类过氧物酶活性,加入靶DNA能够使其活性复原 (见图4),且复原度与加入靶DNA的浓度成正比,该传感的线性范围是30~ 150 nmol/L,检测下限是11 nmol/L,可用于无标记比色方法检测DNA杂交。
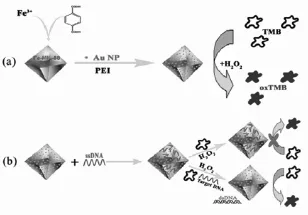
图4 Au@Fe-MIL-88的制备(a)与检测DNA原理(b)示意图[36]Fig.4 Schematic illustration of the proposed preparation method of Au@Fe-MIL-88 hybrids(a)and their application in the detection DNA(b)[36]
Zhu等[37]报道HKUST-1可高效催化鲁米诺与H2O2这一化学发光反应,它能促进自由基的生成和电子转移过程,使发光强度提高90倍,而多巴胺的存在导致发光强度下降,据此可用于测定多巴胺,检测下限为2.3 nmol/L。Xiong等[38]合成了一种混合价态的Ce-MOFs,该化合物具有类氧化酶活性,基于该物质良好的催化活性,构建了一种简易灵敏的比色测定方法用于高通量检测血清样品中生物巯基化合物。 Tian等[39]报道了一种基于Fe-MOFs的纳米棒的DNA荧光传感器,该传感器的检测下限为10 pmol/L,可识别单点突变,从“混合到检测”的时间为4 min,并讨论了纳米结构的组成对传感器响应特性的影响以及中心金属离子与配体的协同作用。
此外,纳米粒径的MOFs优良的荧光特性可进行成像分析[40]。硫化氢被认为是人体生理学和病理学过程中第三重要的气体信号传导分子,由于H2S的高反应活性和扩散性,实时检测活体生物样本中H2S的浓度变化具有重要意义,Ma等[41]以具3D纳米孔径Cu-MOFs作为检测H2S的荧光探针,它具有良好的生物兼容性,而且响应快速,灵敏度高,选择性好,在生理pH条件下可选择性识别H2S,可用于活体细胞共聚焦成像分析。
2 基于MOFs的电化学传感器
利用MOFs材料大的比表面积和催化活性,可以改善电化学传感器的响应性能。Hou等[42]用ZIF-8模板合成Co3O4纳米粒子,将Co3O4@ZIF-8修饰到玻碳电极上,通过循环伏安法,实现了对葡萄糖和双氧水的高灵敏检测,检测下限分别达0.1 μmol/L、0.8 μmol/L。Hosseini等[43]将负载Au-SH-SiO2纳米粒子的Cu-MOFs用于修饰玻碳电极检测L-半胱氨酸,结果表明Au-SH-SiO2@Cu-MOFs对L-半胱氨酸具有良好的催化活性,其氧化过电位明显下降而峰电流显著增加,测定L-半胱氨酸的线性范围为0.02~300 μmol/L,检测下限为8 nmol/L。 Ma等[44]以ZIF-70作为基质设计了一种检测体内葡萄糖的电化学生物传感器,其原理如图5所示,即利用ZIF-70催化氧化电极表面的亚甲基绿 (MG),产物与葡萄糖脱氢酶(GDH)和葡萄糖的酶催化反应产物NADH反应,以此检测葡萄糖,该传感器在葡萄糖浓度为0.1~ 2 mmol/L范围内有良好的线性。

图5 基于ZIF-70生物传感器原理示意图[44]Fig.5 Schematic illustration of the proposed ZIF-70-based biosensor[44]
Wang等[45]以MOF-5修饰的玻碳电极先自溶液中吸附富集 Pb2+后再用溶出伏安法测定Pb2+,在优化的实验条件下,校正曲线的线性范围为0.01~1 μmol/L (r2=0.9981),检测下限为5 nmol/L。Wang等[46]通过循环伏安法研究了多壁碳纳米管与金属有机纳米复合材料掺杂型材料MWCNTs@Cu3(BTC)2的电流信号对铅的响应,其检测下限可达7.9×10-10mol/L。Wang等[47]以胺基功能化的NH2-Cu3(BTC)2MOFs制备修饰电极检测溶液中痕量的铅,它利用NH2-Cu3(BTC)2的吸附特性将溶液中的铅离子富集在电极表面,然后进行电化学检测,在优化条件下,修饰电极的线性范围为0.01~0.5 μmol/L,检测下限为5 nmol/L。Zhang等[48]合成了一种Cu-MOFs,并将其混合在大孔径碳材料(MPC)的空穴内(Cu-MOFs-MPC),比较了Cu-MOFs、MPC和Cu-MOFs-MPC的稳定性,结果表明这些材料具有均匀的结构和稳定的化学性质,在水中能稳定存在,在pH为7.4的磷酸缓冲液中有稳定的电化学性质。利用Cu-MOFs-MPC作为探针检测抗坏血酸和血红蛋白的含量,检测下限分别达3.5 μmol/L、0.04 μmol/L。
Ling等[49]设计了一种基于卟啉MOFs与三螺旋分子开关信号传导的电化学DNA传感器(图6),streptavidin功能化的 Zr-卟啉 MOF(PCN-222@SA)具有很高的电催化还原O2的活性,因为存在较大的空间位阻,所设计的纳米探针与固定在玻碳电极表面的biotin标记的三螺旋之间的相互作用被阻塞,当存在目标DNA时,它与三螺旋中的辅助DNA杂交,导致三螺旋分子结构解体,因此远离电极的末端biotin被激活从而很容易接近信号纳米探针 (PCN-222@SA),传感器表面引入纳米探针能显著放大氧还原的电催化电流,结合DNA循环放大技术,该传感器的响应灵敏度进一步提高,检测下限可达0.3 fmol/L。
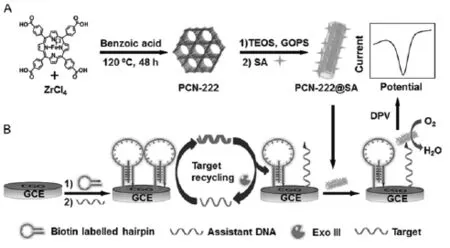
图6 (A)PCN-222@SA纳米探针的合成,(B)电化学策略结合滚环放大检测DNA[49]Fig.6 (A)Synthesis of PCN-222@SA composite,and(B)electrochemical strategy coupling with target recycling amplification for DNA sensing[49]
Guo等[50]在金电极表面电解含纳米金的对氨基硫酚溶液,并以三硝基甲苯(TNT)为模板分子,获得了分子印迹型微孔MOFs用于提高电化学TNT传感器的响应灵敏度与选择性,在优化的实验条件下,检测下限达到0.04 fmol/L,而且对DNT有很高的选择性。 基于同一思路,该课题组[51]还报道了分子印迹微孔MOFs测定抗肿瘤药物(吉西他滨),检测下限为3 fmol/L。Xu等[52]将预先合成的Pt纳米粒子 (Pt NPs)加入到一种Zr-MOF(UiO-66)中,制备复合材料Pt NPs@UiO-66,Pt NPs@UiO-66具有很好的晶体结构,Pt NPs很好地分散在了具有八面体结构的UiO-66框架中,为氧化还原反应提供了更多的电活性位点,该电极对过氧化氢具有优异的电催化活性,选择性良好,线性范围扩展为5 μmol/L~15 mmol/L,检测下限为2 μmol/L,为提高非酶电化学传感器的抗干扰能力提供了一种新途径。Yang等[53]以水热法合成了一种新的Co-MOFs并将其用于电化学修饰电极测定H2O2,线性范围为5 μmol/L~ 9 mmol/L,检测下限为3.8 μmol/L,此外还发现该Co-MOF具有很高的类过氧化氢氧化酶活性,可催化H2O2产生自由基,使底物对苯二酸氧化并产生颜色变化。Wang等[54]合成了一种Cu-MOFs,以它作为电化学生物传感媒介,选用酪氨酸酶为模型酶用于灵敏快速测定双酚A,Cu-MOFs的高比面积有利于酶及双酚A的吸附,进而提高传感器的响应灵敏度,所研制的传感器响应时间为11 s,线性范围0.05~3 μmol/L,检测下限为13 nmol/L。
除最常用的电流响应模式外,其它类型的电化学传感器与MOFs的结合也有不少文献报道。 Zhan等[55]在导电玻璃上以电化学方法制备ZnO纳米棒,以此为锌源与二甲基咪唑进行水热法合成反应制备ZIF-8层,获ZnO@ZIF-8膜,并构成光电流传感器,利用ZIF-8的孔径筛选作用,提高传感器的选择性,如H2O2可以透过ZIF-8的孔洞与ZnO接触,而抗坏血酸(AA)则不能进入ZIF-8的孔中,因此ZnO@ZIF-8膜的光电流随H2O2浓度增加而增加,而随抗坏血酸浓度增加而下降,其检测原理如图7所示。Xu等[56]将MOFs与电化学发光(ECL)相结合以含吡啶钌的配体和Zn2+合成了具有氧化还原活性的MOFs,它的结构不受电荷的影响具有电化学稳定性,在与共反应剂进行电子传递过程中产生强的ECL信号,显示了MOFs的选择性渗透、电荷选择性、催化选择性等优点,并应用于血液样品中可卡因的测定。

图7 ZnO@ZIF-8光电流传感器原理示意图[55]Fig.7 Schematic illustration of the proposed ZnO@ZIF-8 based photoelectrochemical sensor[55]
由于大多数MOFs材料本身的导电性较低,因此MOFs作为功能材料在电学传感器件中的应用报道较少。Campbell等[57]设计合成了Cu3(HITP)2,它是一种导电性较强的2D MOFs,其电导率达到0.2 S/cm,将Cu3(HITP)2分散液滴涂在两测量电极之间,即可构建成化学电阻型传感器,它与氨气接触时电导率明显增加,该阻抗响应可逆,对氨的检测灵敏度达到1×10-4%水平,通过与相同结构的Ni3(HITP)2比较,Cu3(HITP)2中Cu上的位点对氨的响应起关键作用。Gassensmith等[58]报道了一种基于MOFs电化学阻抗变化的CO2传感器,其原理是利用所合成MOFs中自由伯羟基与气相中的CO2反应生成烷基碳酸酯,在MOFs内的化学吸附过程将伴随形成C-O键的动力学过程,当在孔穴中充填醇作为反应介质时,所得MOFs具有很高的质子电导率,键合CO2使其离子电导率降低550倍,该现象可用于定量测定CO2浓度。Davydovskaya等[59]研究了基于Cu-BTC MOF为敏感材料的功函数型气体传感器用于乙醛测定,并讨论了气体分子与敏感层之间的可能反应机理。
Allendorf等[60]用微悬臂传感器监测了由吸附引起柔性MOFs结构变化所产生的应力变化,他们试验了HKUST-1吸附乙醇和CO2有较敏感的应力响应,而吸附N2和O2的应力变化很小,有望开发基于化学应力的气体传感器。Robinson等[61]以自动的层层组装方法将MOF(Cu-BTC)沉积在石英表面声波传感器表面,所研制的传感器对水气有高灵敏度响应,检测范围为0.00003%~ 1.5%(V/V),性能优于目前许多商用湿度传感器,Cu-BTC层直接共价键合在氧化硅表面,它可加热到100℃以上不分解,有利于解吸膜孔中的水,并讨论了膜厚度对响应灵敏度的影响。Chen等[62]以 ZIF-67膜替代传统的半导体氧化物(SnO2,ZnO,In2O3,NiO)膜制备阻抗型甲醛气敏传感器,可使工作温度从使用无机氧化物的200~ 400℃降至150℃,而ZIF-67的高比表面积有利于提高响应灵敏度,在所用条件下,该传感器对甲醛的响应灵敏度最高,检测下限为0.0005%,不过该传感器对甲醇和丙酮也有响应,而对氨和甲烷的响应灵敏度很低。
Venkatasubramanian等[63]分析了MOFs在微悬臂传感器中的响应机理,在SiO2、Al2O3和Si3N4的表面键合MOFs膜,研究了MOFs的杨氏模量、泊松比、密度等参数对传感器响应的影响,结果表明,提高杨氏模量与泊松比能够提高传感器的响应信号,而MOFs的密度对传感器的响应几乎无影响。Yim等[64]利用ZnO纳米棒作为金属离子源,在硅质微悬臂梁上合成纳米多孔ZIF-8膜层,该膜可用于检测甲醇、乙醇、1-丙醇蒸气,当醇类蒸气在ZIF-8层进行吸附-解析时,同时测定共振频率的变化与臂梁的偏向。能够引起该框架结构变化的醇蒸气浓度排序是1-丙醇>乙醇>甲醇。这种趋势是由于不同的醇需要不同浓度去诱导ZIF-8框架结构的“开-关”效应。依赖于醇蒸气分子量的吸附与解析动力学曲线可以用来从混合醇蒸气中分离目标醇。Deep等[65]以胺基功能化氧化铟为基底制备纳米结构的Cd-MOFs,并用于杀虫剂的免疫传感分析,所建立的对硫磷电化学阻抗传感器的响应范围为0.1~20 ng/mL,对其他有机磷化合物有良好的选择性。
3 石英晶体微天平表征MOFs的吸附特性
石英晶体微天平 (quartz crystal microbalance, QCM)作为一种高灵敏度的质量型传感器,在电化学、溶液化学、生物传感器等领域中有关界面传质过程的监测方面获得广泛的应用。QCM的技术优势之一是无需进行标记处理,信号连续直观。MOFs发达的孔穴结构使它们具有很强的吸附能力,吸附质量则可用QCM实时传感检测。气体在多孔材料中吸附特性的表征最常用的方法是使用吸附仪直接测定吸附前后的质量变化,但该方法设备投资和运行成本通常很高,另外需要较大的样品用量(通常>100 mg)。QCM在测定表面质量变化方面具有一定的技术优势,如灵敏度高,能检测纳克级的质量变化,响应速度快,能实现实时动态传感监测,而且测定的是质量变化,无需进行标记处理。以QCM研究材料的吸附特性,仅需数微克的样品即可,而且热传导和传质速率快,这样可以避免使用大取样吸附方法时传热与传质不均的问题。因此,近年来利用QCM研究MOFs吸附特性的文献报道逐渐增多。
Biemmi等[66]报道了利用自组装单层膜法在功能化的QCM表面上沉积上一层HKUST-1膜,研究不同厚度的MOFs膜对水蒸气的吸附行为。Ameloot等[67]利用电化学法在QCM表面上沉积Cu3(btc)2膜,并监测该膜吸附水蒸气的过程,结果表明,该膜对水蒸气的吸附为可逆吸附,吸附容量可达25%~30%膜质量。小分子与MOFs之间的扩散常数可以用MOFs修饰的QCM来测量。Zybaylo等[68]利用液相外延法在QCM金电极上沉积了高度有序的Cu-BTC薄膜,通过测量吡啶吸附的动力学曲线,测得在室温下吡啶的扩散系数为1.5×10-19m2/s,吡啶与Cu-BTC中Cu(II)位点的相应的结合能是18 kcal/mol,与通过量子化学计算得出的结论一致。
Huang等[69]研究了MIL-101 MOFs膜在大气压条件下对VOCs的吸附特性,测定了相关的吸附热力学参数,结果表明MIL-101比活性炭具有更高的吸附容量与吸附平衡常数。Khoshaman等[70]将MOFs用电喷雾涂覆在QCM上,在干燥的空气中检测丙酮、四氢呋喃、异丙醇,并与传统的滴涂法相比较,结果表明,电喷雾方法能够提高QCM谐振的稳定性,对丙酮、四氢呋喃、异丙醇三种挥发性有机气体的最小检测浓度分别是0.005%,0.001%和0.0002%。Venkatasubramanian等[71]以QCM测定了CO2,CH4和N2在两种小孔径MOFs(Cu-hfipbb和ZIF-90)上的吸附特性,其吸附强度顺序为CO2>CH4>N2,它们在两种MOFs上的吸附等温线存在差异,与其分子大小与孔径有关。Liu等[72]利用QCM监测了表面附着金属有机框架层的生长过程,在Au基底上先修饰一层胺基,然后利用液相外延的方法生长多层有序[Cu(ndc)-(dabco)0.5],由于胺基的作用,使薄膜分子层由非活性变为了能够键合异硫氰酸荧光素的活性分子层。Bétard等[73]采用分步沉积法在金电极表面沉积疏水的[Zn4O(dmcapz)3]n膜,以QCM监测该MOFs膜对烷基醇、苯、苯胺、二甲苯等小分子的吸附过程,并通过在配体连接臂中引入烷基侧链的方法调控其吸附选择性。
Brutschy等[74]用电喷雾把不同孔径的有机笼状化合物沉积到QCM上,研究了对芳香族溶剂的超亲作用。Liu等采用层层组装液相外延生长法制备了手性MOFs薄膜,研究了(2R,5R)-2,5-己二醇与 (2S,5S)-2,5-己二醇的对映选择性吸附[75],他们还在QCM表面定向生长[100]和[001]向外的 [Cu2(ndc)2(dabco)]MOF膜,比较了几种VOCs在不同晶面上的吸附差异,与MOFs晶体不同方向晶面中孔径大小差异相吻合[76]。Shekhah等[77]研究了在OH-功能化Au表面上的液相外延生长定向ZIF-8薄膜过程以及在饱和蒸气压条件下对五种烷基醇的吸附与解吸的动力学过程。Tsotsalas等[78]研究了分子在MOFs纳米孔穴中的脱附过程,揭示了吸附剂的化学性质对脱附动力学有明显的影响,提出分子与MOFs框架间的强相互作用将导致客体分子聚集形成一种临时性的亚稳态,从而引起脱附速率下降。Wannapaiboon等[79]在金基底上利用逐步液相外延沉积法合成出[Zn4O(L)3]n自组装单层膜,整个沉积和结晶过程利用QCM和X-射线衍射监测,监测过程发现不同的结晶机理。通过QCM监测其吸附不同结构的有机溶剂分子,研究了MOFs孔径对吸附的影响。Davydovskaya等[80]在室温下联合QCM与开尔文探针以Cu-BTC膜检测甲醇、乙醇、丙醇、异丙醇,两种方法都可以达到对1×10-4%水平醇类物质的检测,实验研究了醇链长度、几何结构以及它们的极性对吸附的影响,结果表明,在干燥环境下,醇类吸附在不饱和的Cu位点上,短链醇更易吸附在Cu-BTC上,然在潮湿环境中,醇类溶解在Cu-BTC膜表面的水层中,长链醇更易吸附。Hou等[81]以QCM监测了一种新的多孔Cu-MOF吸附小分子的动力学过程,该MOF对极性溶剂如甲醇、乙醇、丙酮等吸附量较大,对非极性分子如苯、甲苯、乙苯、氯苯的吸附则较小,结合分子构型讨论了小分子的吸附差异。
为克服腐蚀性组分对QCM电极腐蚀所造成的对传感器寿命以及吸附量测定可靠性的不利影响,Kang等[82]采用一种气隔电极式QCM监测了I2蒸气在ZIF-8上的吸附与转移动力学过程,在所设计的吸附实验装置中,QCM的激励电极置于吸附池之外不与I2分子接触,利用两个并联组合的QCM传感器同时监测了ZIF-8膜和石英表面吸附碘的过程,也试验了QCM与吸光度测定的联用以提供吸附无分子结构方面的信息。同时,还设计了两个串联组合的QCM传感器用于监测碘在两个ZIF-8膜之间的转移。
4 结论
MOFs由金属离子(簇)与有机配体桥联自组装而成,通过设计各种配体以及与多种金属离子组合,可以合成出成千上万种性质各异的新材料,MOFs家族在不断发展壮大之中。MOFs材料的高比表面积以及可以调控的多孔结构尺寸与化学环境,为改进化学传感器的响应性能提供了新的机遇,特别是功能化的MOFs与生物传感相结合,在手性分析、化学成像、生物分析方面的研究与探索已备受关注。MOFs材料的性质是影响传感器响应特性的关键性因素之一,虽然已报道的MOFs传感器很多,但很多研究仍然停留在材料合成、结构与性质表征,在实际应用中仍面临诸多挑战,如检测灵敏度、选择性等指标有待进一步提高等。因此,新材料的开发与有效利用、与生物识别与信号放大技术相结合将是MOFs传感器研究的主要方向。
[1]Zhou H C,Long J R,Yaghi OM.Introduction to metal-organic frameworks[J].Chem.Rev.,2012,112:673-674.
[2]Stock N,Biswas S.synthesis of metal-organic frameworks (MOFs):routes to various of topologies,morphologies, and composites[J].Chem.Rev.,2012,112:933-969.
[3]Jeong Y L,Omar K F,Roberts J,et al.Metal-organic framework materials as catalysts[J].Chem.Soc.Rev., 2009,38:1450-1459.
[4]Li J R,Sculley J,Zhou H C.Metal-organic frameworks for separations[J].Chem.Rev.,2012,112:869-932.
[5]De C J B,Peterson G W.Metal-organic frameworks for air purification of toxic chemicals[J].Chem.Rev., 2014,114:5695-5727.
[6]Gu Z Y,Yang C X,Chang N A,et al.Metal-organic frameworks for analytical chemistry:From sample collection to chromatographic separation[J].Accounts Chem. Res.,2012,45:734-745.
[7]Kreno L E,Leong K,Farha O K,et al.Metal-organic framework materials as chemical sensors[J].Chem. Rev.,2012,112:1105-1125.
[8]Lei J P,Qian R C,Pinghua Ling,et al.Design and sensing applications of metal-organic framework composites [J].Trends.Anal.Chem.,2014,58:71-78.
[9]Meyer L V,Schöfeld F,Müller-Buschbaum K.Lanthanide based tuning of luminescence in MOFs and dense frameworks-from mono-and multimetal systems to sensors and films[J].Chem.Commun.,2014,50: 8093-8108.
[10]Pramanik S,Zheng C,Zhang X,et al.New microporous metal-organic framework demonstrating unique selectivi-ty for detection of high explosives and aromatic compounds[J].J.Am.Chem.Soc.,2011,133:4153-4155.
[11]Campagnol N,Souza E R,De Vos D E,et al.Luminescent terbium-containing metal-organic framework films:new approaches for the electrochemical synthesis and application as detectors for explosives[J].Chem.Commun., 2014,83:12545-12547.
[12]Gole B,Arun K B,Mukherjee P S.Modification of extended open frameworks with fluorescent tags for sensing explosives:competition between size selectivity and electron deficiency [J].Chem.Eur.J,2014,20:2276-2291.
[13]Nagarkar S S,Desai A V,Ghosh S K.A fluorescent metal-organic framework for highly selective detection of nitro explosives in the aqueous phase[J].Chem.Commun.,2014,50:8915-8918.
[14]Lu G,Hupp J T.Metal-organic frameworks as sensors:A ZIF-8 based fabry-perot device as a selective sensor for chemical vapors and gases[J].J.Am.Chem.Soc.,2010, 132:7832-7833.
[15]Li Y,Zhang S,Song D.A luminescent metal-organic framework as a turn-on sensor for DMF vapor[J]. Angew.Chem.Int.Ed.,2013,52:710-713.
[16]Shustova N B,Cozzolino A F,Reineke S,et al.Selective turn-on ammonia sensing enabled by high-temperature fluorescence in metal-organic frameworks with open metal sites[J].J.Am.Chem.Soc.,2013,135:13326-13329.
[17]Zhang M,Feng G,Song Z,et al.Two-dimensional metalorganic framework with wide channels and responsive turn-on fluorescence for the chemical sensing of volatile organic compounds[J].J.Am.Chem.Soc.,2014,136: 7241-7244.
[18]Wan X Y,Song H J,Zhao D,et al.A Y-doped metal-organic framework-based cataluminescence gas sensor for isobutanol[J].Sens.Actuators B,2014,201:413-419.
[19]Liu X G,Wang H,Chen B,et al.A luminescent metal-organic framework constructed using a tetraphenylethenebased ligand for sensing volatile organic compounds[J]. Chem.Commun.,2015,51:1677-1680.
[20]Douvali A,Tsipis A C,Eliseeva S V,et al.Turn-on luminescence sensing and real-time detection of traces of water in organic solvents by a flexible metal-organic framework[J].Angew.Chem.Int.Ed.,2015,54:1651-1656.
[21]Ohira S I,Miki Y,Toru Matsuzaki T,et al.A fiber optic sensor with a metal organic framework as a sensing material for trace levels of water in industrial gases[J].Anal. Chim.Acta,2015,886:188-193.
[22]Wanderley M M,Wang C,Wu C D,et al.A chiral porous metal-organic framework for highly sensitive and enantioselective fluorescence sensing of amino alcohols[J]. J.Am.Chem.Soc.,2012,134:9050-9053.
[23]Qin L,Zheng M X,Guo Z J,et al.One non-interpenetrated chiral porous multifunctional metal-organic framework and its applications for sensing small solvent molecules and adsorption[J].Chem.Commun.,2015, 51:2447-2449.
[24]Kreno L E,Hupp J T.Metal-organic framework thin film for enhanced localized surface plasmon resonance gas sensing[J].Anal.Chem.,2010,82:8042-8046.
[25]Hu Y,Liao J,Wang D,et al.Fabrication of gold nanoparticle-embedded metal-organic framework for highly sensitive surface-enhanced Raman scattering detection[J]. Anal.Chem.,2014,86:3955-3963.
[26]Xiao Y Q,Cui Y J,Zheng Q,et al.A microporous luminescent metal-organic framework for highly selective and sensitive sensing of Cu2+in aqueous solution[J].Chem. Commun.,2010,46:5503-5505.
[27]He J,Zha M,Cui J,et al.Convenient detection of Pd(II) by a metal-organic framework with sulfur and olefin functions[J].J.Am.Chem.Soc.,2013,135:7807-7810. [28]Yang C X,Ren H B,Yan X P.Fluorescent metal-organic framework MIL-53(Al)for highly selective and sensitive detection of Fe3+in aqueous solution[J].Anal.Chem., 2013,85:7441-7446.
[29]Zhao D,Wan X Y,Song H J.Metal-organic frameworks (MOFs)combined with ZnO quantum dotsas a fluorescent sensing platform for phosphate[J].Sens.Actuators B, 2014,197:50-57.
[30]Lin X M,Gao G M,Zheng L Y,et al.Encapsulation of strongly fluorescent carbon quantum dots in metal-organic frameworks for enhancing chemical sensing[J].Anal. Chem.,2014,86:1223-1228.
[31]Hao L Y,Song H J,Su Y Y,et al.A cubic luminescent graphene oxide functionalized Zn-based metal-organic framework composite for fast and highly selective detection of Cu2+ions in aqueous solution[J].Analyst,2014, 139:764-770.
[32]Carboni M,Lin Z K,Abney C W,et al.A metal-organic framework containing unusual eight-connected zr-oxo secondary building units and orthogonal carboxylic acids for ultra-sensitive metal detection[J].Chem.Eur.J.,2014,20:14965-14970.
[33]Song Y H,Hu D Q,Liu F F,et al.Fabrication of fluorescent SiO2@zeolitic-imidazolate framework-8 nanosensor for Cu2+detection[J].Analyst,2015,140:623-629.
[34]Fang J M,Leng F,Zhao X J,et al.Metal-organic framework MIL-101 as a low background signal platform for label-free DNA detection[J].Analyst,2014,139:801-806.
[35]Yang N,Song H J,Wan X Y,et al.A metal(Co)-organic framework-based chemiluminescence system for selective detection of L-cysteine[J].Analyst,2015,140: 2656-2663.
[36]Liu Y L,Fu W L,Li C M,et al.Gold nanoparticles immobilized on metal-organic frameworks with enhanced catalytic performance for DNA detection[J].Anal. Chim.Acta,2015,861:55-61.
[37]Zhu Q,Chen Y,Wang W,et al.A sensitive biosensor for dopamine determination based on the unique catalytic chemiluminescence ofmetal-organic framework HKUST-1[J].Sens.Actuators B,2015,210:500-507.
[38]Xiong Y H,Chen S H,Ye F G,et al.Synthesis of a mixed valence state Ce-MOF as an oxidase mimetic for the colorimetric detection of biothiols A[J].Chem.Commun., 2015,51:4635-4638.
[39]Tian J,Liu Q,Shi J,et al.Rapid,sensitive,and selective fluorescent DNA detection using iron-based metal-organic framework nanorods:Synergies of the metal center and organic linker[J].Biosens.Bioelectron.,2015,71: 1-6.
[40]Liu D,Lu K,Poon C,et al.Metal-organic frameworks as sensory materials and imaging agents[J].Inorg.Chem., 2014,53:1916-1924.
[41]Ma Y,Su H,Kuang X,et al.Heterogeneous nano metalorganic framework fluorescence probe for highly selective and sensitive detection of hydrogen sulfide in living cells [J].Anal.Chem.,2014,86:11459-11463.
[42]Hou C T,Xu Q,Yin L,et al.Metal-organic framework templated synthesis of Co3O4nanoparticles for direct glucose and H2O2detection[J].Analyst,2012,137:5803-5808.
[43]Hosseini H,Ahmar H,Dehghani A,et al.A novel electrochemical sensor based on metal-organic framework for electro-catalytic oxidation of L-cysteine[J].Biosens. Bioelectron.,2013,42:426-429.
[44]Ma W J,Jiang Q,Yu P,et al.Zeolitic-imidazolate framework based electrochemical biosensor for in vivo electrochemical measurements[J].Anal.Chem.,2013,85: 7550-7557.
[45]Wang Y,Wu Y C,Xie J,et al.Metal-organic framework modified carbon paste electrode for lead sensor[J]. Sens.Actuators B,2013,177:1161-1166.
[46]Wang Y,Wu Y C,Xie J,et al.Multi-walled carbon nanotubes and metal-organic framework nanocomposites as novel hybrid electrode materials for the determination of nano-molar levels of lead in a lab-on-valve format[J]. Analyst,2013,138:5113-5120.
[47]Wang Y,Ge H L,Wu Y C,et al.Construction of an electrochemical sensor based on amino-functionalized metal-organic frameworks for differential pulse anodic stripping voltammetric determination of lead[J].Talanta, 2014,129:100-105.
[48]Zhang Y F,Nsabimana A,Zhu L D,et al.Metal-organic frameworks/macroporous carbon composites with enhanced stability properties and good electrocatalytic ability for ascorbic acid and hemoglobin [J].Talanta,2014, 129:55-62.
[49]Ling P,Lei J,Ju H.Porphyrinic metal-organic framework as electrochemical probe for DNA sensing via triple-helix molecular switch[J].Biosens.Bioelectron.,2015,71: 373-379.
[50]Guo Z Z,Florea A,Cristea C,et al.1,3,5-Trinitrotoluene detection by a molecularly imprinted polymer sensor based on electropolymerization of a microporous-metal-organic framework[J].Sens.Actuators B,2015, 207:960-966.
[51]Florea A,Guo Z Z,Cristea C,et al.Anticancer drug detection using a highly sensitive molecularly imprinted electrochemical sensor based on an electropolymerized microporous metal organic framework[J].Talanta,2015, 138:71-76.
[52]Xu Z D,Yang L Z,Xu C L.Pt@UiO-66 heterostructures for highlyselectivedetection ofhydrogen peroxide with an extended linear range[J].Anal.Chem.,2015, 87:3438-3444.
[53]Yang L Z,Xu C L,Ye W C,et al.An electrochemical sensor for H2O2based on a new Co-metal-organic framework modified electrode[J].Sens.Actuators B, 2015,215:489-496.
[54]Wang X,Lu X,Wu L,et al.3D metal-organic framework as highly efficient biosensing platform for ultrasensitive and rapid detection of bisphenol A[J].Biosens.Bioelectron.,2014,65:295-301.
[55]Zhan W W,Kuang Q,Zhou J Z,et al.Semiconductor@metal-organic framework core-shell heterostructures:acase of ZnO@ZIF-8 nanorods with selective photoelectrochemical response[J].J.Am.Chem.Soc., 2013,135:1926-1933.
[56]Xu Y,Yin X B,He X W,et al.Electrochemistry and electrochemiluminescence from a redox-active metal-organic framework[J].Biosens.Bioelectron.,2015,68:197-203.
[57]Campbell M G,Sheberla D,Liu S F,et al.Cu3(hexaiminotriphenylene)2:an electrically conductive 2D metal-organic framework for chemiresistive sensing[J]. Angew.Chem.Int.Ed.,2015,54:4349-4352.
[58]Gassensmith J J,Kim J Y,Holcroft J M,et al.A metal-organic framework-based material for electrochemical sensing of carbon dioxide[J].J.Am.Chem.Soc.,2014, 136:8277-8282.
[59]Davydovskaya P,Pohle R,Tawil A,et al.Work function based gas sensing with Cu-BTC metal-organic framework for selective aldehyde detection[J].Sens.Actuators B,2013,187:142-146.
[60]Allendorf M D,Houk R J T,Andruszkiewicz L,et al. Stress-induced chemical detection using flexible metalorganic frameworks[J].J.Am.Chem.Soc.,2008,130: 14404-14405.
[61]Robinson A L,Stavila V,Zeitler T R,et al.Ultrasensitive humidity detection using metal-organic frameworkcoated microsensors[J].Anal.Chem.,2012,21:7043-7051.
[62]Chen E X,Yang H,Zhang J.Zeolitic imidazolate framework as formaldehyde gas sensor[J].Inorg.Chem., 2014,53:5411-5413.
[63]Venkatasubramanian A,Lee J H,Stavila V,et al. MOF@MEMS:design optimization for high sensitivity chemical detection[J].Sens.Actuators B,2012,168: 256-262.
[64]Yim C Y,Lee M,Kim W,et al.Adsorption and desorption characteristics of alcohol vapors on a nanoporous ZIF-8 film investigated using silicon microcantilevers [J].Chem.Comm.,2015,51:6168-6171.
[65]Deep A,Bhardwaj S K,Paul A K,et al.Surface assembly of nano-metal organic framework on amine functionalized indiumtin oxide substrate for impedimetric sensing of parathion[J].Biosens.Bioelectron.,2015,65:226-231.
[66]Biemmi E,Darga A,Stock N,et al.Direct growth of Cu3(BTC)2(H2O)3-xH2O thin films on modified QCM-gold electrodes—Watersorption isotherms [J]. Microp. Mesop.Mater.,2008,114:380-386.
[67]Ameloot R,Stappers L,Fransaer J,et al.Patterned growth of metal-organic framework coatings by electrochemical synthesis[J].Chem.Mater.,2009,21:2580-2582.
[68]Zybaylo O,Shekhah O,Wang H,et al.A novel method to measure diffusion coefficients in porous metal-organic frameworks[J].Chem.Chem.Phys.,2010,12:8093-8098.
[69]Huang C Y,Song M,Gu Z Y,et al.Probing the adsorption characteristic of metal-organic framework MIL-101 for volatile organic compounds by quartz crystal microbalance[J].Environ.Sci.Technol.,2011,45:4490-4496.
[70]Khoshaman A H,Bahreyni B.Application of metal-organic framework crystals for sensing of volatile organic gases[J].Sensor.Actuators B,2012,162:114-119.
[71]Venkatasubramanian A,Navaei M,Bagnall K R,et al. Gas adsorption characteristics of metal-organic frameworks via quartz crystal microbalance techniques[J].J. Phys.Chem.C,2012,116:15313-15321.
[72]Liu B,Ma M Y,Zacher D,et al.Chemistry of SURMOFs: layer-selective installation of functional groups and post-synthetic covalent modification probed by fluorescence microscopy[J].J.Am.Chem.Soc.,2011,133: 1734-1737.
[73]Bétard A,Wannapaiboon S,Fischer R A.Assessing the adsorption selectivity of linker functionalized,moisturestable metal-organic framework thin films by means of an environment-controlled quartz crystal microbalance [J].Chem.Commun.,2012,48:10493-10495.
[74]Brutschy M,Schneider M W,Mastalerz M,et al.Porous organic cage compounds as highly potent affinity materials for sensing by quartz crystal microbalances[J].Adv. Mater.,2012,24:6049-6052.
[75]Liu B,Shekhah O,Arslan H K,et al.Enantiopure metalorganic framework thin films:oriented SURMOF growth and enantioselective adsorption[J].Angew.Chem.Int. Ed.,2012,51:807-810.
[76]Liu B,Tu M,Fischer R A.Metal-Organic framework thin films:crystallite orientation dependent adsorption[J]. Angew.Chem.Int.Ed.,2013,52:3486-3489.
[77]Shekhah O,Eddaoudi M.The liquid phase epitaxy method for the construction of oriented ZIF-8 thin films with controlled growth on functionalized surfaces[J]. Chem.Commun.,2013,49:10079-10081.
[78]Tsotsalas M,Hejcik P,Sumida K,et al.Impact of molec-ular clustering inside nanopores on desorption processes [J].J.Am.Chem.Soc.,2013,135:4608-4611.
[79]Wannapaiboon S,Tu M,Fischer R A.Liquid phase heteroepitaxial growth of moisture-tolerant MOF-5 isotype thin films and assessment of the sorption properties by quartz crystal microbalance[J].Adv.Funct.Mater., 2014,24:2696-2705.
[80]Davydovskaya P,Ranft A,Lotsch B V,et al.Analyte detection with cu-btc metal-organic framework thin films by means of mass-sensitive and work-function-based readout[J].Anal.Chem.,2014,86:6948-6958.
[81]Hou C,Bai Y L,Bao X,et al.A metal-organic framework constructed using a flexible tripodal ligand and tetranuclear copper cluster for sensing small molecules[J]. Dalton Trans.,2015,44:7770-7773.
[82]Kang Q,Zhu X L,Ma X L,et al.Response of an electrodeless quartz crystal microbalance in gaseous phase and monitoring adsorption of iodine vapor on zeolitic-imidazolate framework-8 film[J].Sens.Actuators B,2015,220:472-480.
Recent progress in applications of metal-organic frameworks in sensors
Shang Shu-chuan,Kong Ling-qiang,Cai Ting-ting,Kang Qi,Shen Da-zhong*
(College of Chemistry,Chemical Engineering and Materials Science,Shandong Normal University, Jinan 250014,China)
Metal-organic frameworks(MOFs)are a class of hybrid materials self-assembled from organic bridging ligands and metal ion/cluster connecting points.As nanoporous,supramolecular materials,MOFs have unique chemical and physical properties,such as ultrahigh surface area,tunable structure,and high thermal and chemical stability.These characteristics make MOFs very attractive for chemical sensing.That short-focused article reports on recent efforts and progress in MOFs-based sensors with an emphasis on the design of functional MOFs and signaltransduction strategy,including optical,electrochemical,microbalance,and photoelectrochemical schemes,for analytical applications in detection of volatile organic compounds,metal ions,DNA,proteins,and other important biomolecules.
MOFs;optical;electrochemical;microbalance;review
国家自然科学基金资助项目(21175084,21275091)
*通信联系人,E-mail:dzshen@sdnu.edu.cn

