脓毒血症诱发乙型肝炎相关慢加急性肝功能衰竭临床特征的研究
脓毒血症诱发乙型肝炎相关慢加急性肝功能衰竭临床特征的研究
陆蕴颖1*丁茹2*曾菠2陈柳莹2尹姗2张楠楠2李海2#
上海交通大学医学院附属仁济医院急诊科1(200127)
上海交通大学医学院附属仁济医院消化内科上海市消化疾病研究所2

*Email: jasminecong@hotmail.com
背景:目前脓毒血症作为诱因对乙型肝炎后肝硬化基础上发生的慢加急性肝功能衰竭(ACLF)的影响和预后尚无报道。目的:回顾性分析脓毒血症作为诱因对ACLF患者临床严重程度和短期死亡率的影响。方法:连续纳入2005年1月—2010年12月上海仁济医院HBV相关肝硬化合并急性失代偿的住院患者890例,以慢性肝功能衰竭联盟-器官功能衰竭评分(CLIF-C OFs)筛选出入院时为ACLF的患者。以脓毒血症作为诱因将ACLF患者分为脓毒血症诱因组和非脓毒血症诱因组,比较两组的基线资料、实验室检查、脏器衰竭发生率和短期病死率。结果:按照CLIF-C OFs标准入院时诊断为ACLF患者243例,其中脓毒血症为诱因的ACLF患者47例(19.3%),非脓毒血症为诱因者94例(38.7%),102例(42.0%)无明确诱因。脓毒血症诱因组和非脓毒血症诱因组的短期病死率均无明显差异(28 d: 46.8%对36.2%,P=0.224;90 d: 53.2%对42.6%,P=0.232)。与非脓毒血症诱因组相比,脓毒血症诱因组肝功能衰竭(72.3%对88.3%,P=0.030)和凝血障碍(53.2%对70.2%,P=0.046)的比例显著降低,而肾功能衰竭(48.9%对29.8%,P=0.026)和循环衰竭(14.9%对4.3%,P=0.042)的比例显著升高。结论:脓毒血症作为诱因的ACLF患者短期病死率与非脓毒血症诱因组相比无明显差异,但具有更高的肾脏、循环衰竭比例,而肝脏衰竭和凝血障碍发生率更低。
关键词脓毒症;慢加急性肝衰竭;多器官功能衰竭
在肝硬化基础上诱发的慢加急性肝功能衰竭(acute-on-chronic liver failure, ACLF)是近年来新发现的一类疾病[1],由于其病因、病理生理机制和临床表现的复杂性[2-7],国际上对ACLF的认识非常有限。欧美联合肝脏研究学会(EASL/AASLD)于2010年提出ACLF是一组肝硬化患者在有明确诱因或无诱因的情况下出现肝脏或肝脏以外的器官功能衰竭,且短期死亡率明显升高的疾病[6]。一项欧洲肝病协会-慢性肝衰竭联盟的8个国家29个肝病中心前瞻性研究CANONIC为这一定义提供了依据,ACLF具有快速恶化,多脏器功能衰竭,短期死亡率(28 d)>15%的临床特征[8]。
最新的研究发现细菌感染是较为常见的ACLF诱因,以自发性腹膜炎(SBP)和肺炎多见;其次为酒精摄入;其他诱因还可包括外伤、急性中毒、肝炎病毒重叠感染等[8]。目前有研究[9]将肝脏因素与肝外因素诱发的ACLF患者进行比较,发现两组患者的病因、自然病程和临床特征均不同,导致预后不同。目前尚缺乏关于脓毒血症对ACLF患者重症化和预后影响的报道。本研究将脓毒血症这个常见诱因诱发的ACLF与其他诱因相比较,旨在了解其对ACLF患者临床严重程度和死亡率的影响,进一步区分ACLF亚型。
对象与方法
一、研究对象
连续纳入2005年1月—2010年12月上海交通大学医学院附属仁济医院的HBV相关肝硬化合并急性失代偿的住院患者890例。纳入标准:HBV相关肝硬化合并入院前1个月内出现腹水、肝性脑病、上消化道出血或感染等急性失代偿表现的患者[10]。排除标准[10]:①年龄<18岁或>80岁;②妊娠;③合并HIV感染;④肝癌或其他肿瘤;⑤慢性肾功能不全;⑥其他严重疾病且伴器官衰竭;⑦曾行肝移植术(LT)。收集患者首次入院、入院后第3、7、14、21、28 d以及出院前24 h的各项临床资料和实验室检查资料。
二、实验室指标和肝功能评分。
1. 实验室指标:①血常规:白细胞(WBC)、红细胞压积、血小板(PLT);②生化指标:国际标准化比率(INR)、丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、γ-谷氨酰转移酶(γ-GT)、总胆红素(TB)、白蛋白(ALB)、血清钠(Na)、血肌酐(SCr)(应用罗氏D/P/P/ISE模块型自动化生化分析仪检测);③病毒学指标:HBV-DNA、HCV RNA载量(采用荧光定量聚合酶链反应法,试剂盒由中山大学达安基因股份有限公司提供)、乙型肝炎病毒血清学标记物、抗-HCV(采用ELISA法检测,试剂盒由上海科华生物工程股份有限公司提供)。
2. 慢性肝功能衰竭联盟-器官功能衰竭评分(Chronic Liver Failure-Consortium Organ Failure score, CLIF-C OFs)[11]:肝功能衰竭:血清TB≥12 mg/dL;肾功能衰竭:Cr≥2 mg/dL或需要肾替代治疗;神经系统衰竭:肝性脑病Ⅲ~Ⅳ级;凝血功能障碍:INR ≥2.5;呼吸衰竭:PaO2/FiO2≤200或SpO2/FiO2≤214;循环系统衰竭:血压需升压药支持[1]。
ACLF 1级符合以下任意一条:①单独肾功能衰竭;②单独非肾脏器官衰竭且Cr为1.5~1.9 mg/dL或肝性脑病Ⅰ~Ⅱ级;③肝性脑病Ⅲ~Ⅳ级且Cr为1.5~1.9 mg/dL。ACLF 2级有两个器官衰竭;ACLF 3级有3~6个器官衰竭。
三、ACLF诱因的分类
感染合并全身炎症反应综合征(SIRS)可明确诊断为脓毒血症[12-13]。感染符合以下任意一项:①SBP:腹水常规 WBC>250/μL;②血液培养阳性;③肺炎:新发肺部渗出、体温>38 ℃和呼吸道症状或听诊异常或WBC>10×109/L或<4×109/L;④尿路感染:尿常规 WBC>10/HP、尿培养阳性和尿路刺激症状;⑤其他:皮肤感染、腹腔内感染或不明原因感染。SIRS符合以下4项中2项:①体温>38 ℃或<36 ℃;②心率>90次/min;③呼吸频率>20次/min或PaCO2<32 mm Hg(1 mm Hg=0.133 kPa);④外周血WBC>12×109/L或<4×109/L或未成熟细胞的比例>10%。
四、随访
以入院为起始,发生肝病原因死亡或行LT为终点,随访至终点时间2013年12月31日,根据患者的个人信息或联系人信息,通过电话随访患者终点指标,记录患者行LT的时间、末次门诊随访时间,失访或研究结束时未死亡时间为截尾时间,此数据为截尾数据。
五、统计学分析

结果
一、入组患者的一般情况
研究期间依据纳入排除标准,最终纳入890例患者,按照CLIF-C OFs标准,入院时诊断为ACLF 243例,非ACLF患者647例。243例ACLF患者中,诱因为入院前4周内发生脓毒血症者47例,其他诱因的ACLF患者(非脓毒血症诱因组)94例,102例无明确诱因(不纳入分析)(表1)。

表1 243例入院时诊断为ACLF患者的诱因分类
*持续使用核苷类药物>6个月且治疗期间HBV-DNA<500 IU/mL,因耐药或自行停药后HBV-DNA再次>500 IU/mL,包括ALT正常或升高者;**合并HCV或HEV感染
二、脓毒血症诱因组与非脓毒血症诱因组的比较
脓毒血症诱因组的性别构成、年龄和平均动脉压与非脓毒血症诱因组相比差异无统计学意义(P>0.05);非脓毒血症诱因组合并腹水的发生率显著高于脓毒血症诱因组(88.3%对68.1%,P=0.005)。
脓毒血症诱因组与非脓毒血症诱因组的病因相比差异有统计学意义(P=0.014),两组患者入院时HBV-DNA水平无明显差异(P>0.05)。脓毒血症诱因组肝功能衰竭和凝血障碍比例分别为 72.3%和53.2%,均显著低于非脓毒血症诱因组(P=0.030,P=0.046);而脓毒血症诱因组肾功能衰竭和循环衰竭的比例为48.9%和14.9%,均显著高于非脓毒血症诱因组(P=0.026,P=0.042)。两组脑衰竭和呼吸衰竭比例无明显差异(P>0.05)。
表2入院时ACLF患者脓毒血症诱因组与非脓毒血症诱因组基线资料的比较
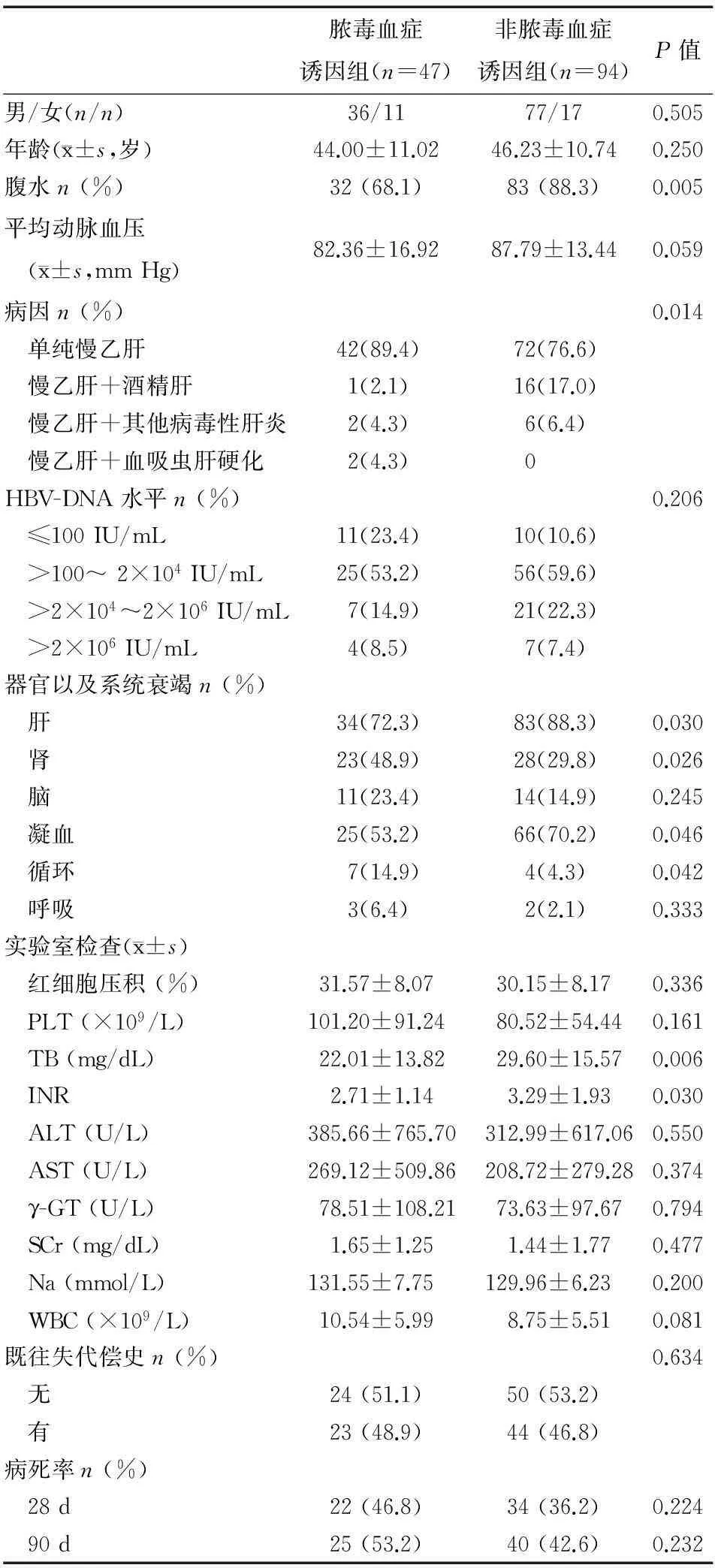
脓毒血症诱因组(n=47)非脓毒血症诱因组(n=94)P值男/女(n/n)36/1177/170.505年龄(x±s,岁)44.00±11.0246.23±10.740.250腹水n(%)32(68.1)83(88.3)0.005平均动脉血压 (x±s,mmHg)82.36±16.9287.79±13.440.059病因n(%)0.014 单纯慢乙肝42(89.4)72(76.6) 慢乙肝+酒精肝1(2.1)16(17.0) 慢乙肝+其他病毒性肝炎2(4.3)6(6.4) 慢乙肝+血吸虫肝硬化2(4.3)0HBV-DNA水平n(%)0.206 ≤100IU/mL11(23.4)10(10.6) >100~2×104IU/mL25(53.2)56(59.6) >2×104~2×106IU/mL7(14.9)21(22.3) >2×106IU/mL4(8.5)7(7.4)器官以及系统衰竭n(%) 肝34(72.3)83(88.3)0.030 肾23(48.9)28(29.8)0.026 脑11(23.4)14(14.9)0.245 凝血25(53.2)66(70.2)0.046 循环7(14.9)4(4.3)0.042 呼吸3(6.4)2(2.1)0.333实验室检查(x±s) 红细胞压积(%)31.57±8.0730.15±8.170.336 PLT(×109/L)101.20±91.2480.52±54.440.161 TB(mg/dL)22.01±13.8229.60±15.570.006 INR2.71±1.143.29±1.930.030 ALT(U/L)385.66±765.70312.99±617.060.550 AST(U/L)269.12±509.86208.72±279.280.374 γ-GT(U/L)78.51±108.2173.63±97.670.794 SCr(mg/dL)1.65±1.251.44±1.770.477 Na(mmol/L)131.55±7.75129.96±6.230.200 WBC(×109/L)10.54±5.998.75±5.510.081既往失代偿史n(%)0.634 无24(51.1)50(53.2) 有23(48.9)44(46.8)病死率n(%) 28d22(46.8)34(36.2)0.224 90d25(53.2)40(42.6)0.232
非脓毒血症诱因组血清TB和INR显著高于脓毒血症诱因组(P=0.006,P=0.030)。
脓毒血症诱因组的28 d和90 d LT-free死亡率分别为46.8%和53.2%,与非脓毒血症诱因组相比差异无统计学意义。Kaplan-Meier法显示,脓毒血症诱因组和非脓毒血症诱因组的半年累积生存率分别为37%和48%,1年的累积生存率分别为37%和43%(P=0.111)(图 1)。

图1入院时ACLF患者脓毒血症诱因组与非脓毒血症诱因组生存曲线(Kaplan-Meier法)
讨论
ACLF是近年来逐步被认识的一类疾病,在肝硬化急性失代偿患者中出现多个器官功能衰竭,短期死亡率可高达30%~40%。ACLF多发生于年轻患者,病因以酒精性肝硬化和乙型肝炎肝硬化多见[14]。欧洲CANONIC研究中1 343例患者的病因以酒精性肝硬化为主,还包括小部分丙型肝炎后肝硬化[8];本研究的研究对象均为乙型肝炎后肝硬化急性失代偿患者,可弥补CANONIC研究中缺少乙型肝炎后肝硬化失代偿患者的缺陷。
ACLF的发生机制中,较常见的诱因为细菌感染、酒精摄入和乙型肝炎病毒活化,40%的ACLF无明确诱因[14]。本研究中,入院时诊断为ACLF的患者中诱因为脓毒血症(19.3%)、乙型肝炎病毒复发(21.4%)的比例较高,酒精摄入和静脉曲张出血分别占8.2%和9.5%,无明确诱因占42.0%,这与欧洲的研究[1]较为一致。有研究将ACLF的诱因分为肝脏因素和肝外因素,肝脏因素中以酒精摄入为主,肝外因素中细菌感染所占的比例最高[9]。而我国肝硬化失代偿患者组成中乙型肝炎后肝硬化比例高,因此本研究中ACLF患者的诱因以乙型肝炎病毒复发比例最高。
ACLF的发生机制复杂,目前认为其机制包括过度炎症反应以及对病原体产生的全身氧化应激和机体组织因炎症导致自我稳态失调(由病原体直接导致组织器官功能失调)[13]。ACLF是一个动态的综合征,短期内50%的患者可改善或20%发生恶化,预后依赖于早期的临床进程。因此,明确脓毒血症诱因的ACLF患者的临床特征有助于了解ACLF的发病机制和预后。
脓毒血症导致发生ACLF的机制可能有两种[14]:第一,脓毒血症引起的ACLF是一类特殊形式的ACLF,是由严重感染导致循环损伤后器官低灌注或由炎症介质作用于细胞产生多个器官功能衰竭甚至死亡;第二,感染可能直接损伤宿主组织,改变了大量细胞功能,组织损伤可能与组织稳态(保护组织免于细菌和免疫病理所致的直接损伤)改变有关,从而导致器官功能衰竭。非脓毒血症诱因导致的ACLF通常与感染无关,可能通过细菌PAMPs释放或凋亡细胞释放内源性分子PRR活化产生过度的免疫应答,导致了组织损伤和器官衰竭。
本研究中,脓毒血症诱因组与非脓毒血症诱因组的28 d和90 d LT-free死亡率无明显差异,半年和一年的累积生存率亦无明显差异,说明两组患者虽然ACLF的发生机制可能不同,但脓毒血症并不增加ACLF的死亡率,即ACLF预后与诱因无关。有研究[11]发现,CLIF-C ACLFs(Liver-chronic liver failure-Consortium acute-on chronic liver failure score)可作为ACLF的预测模型,提示ACLF预后与年龄、WBC和器官衰竭数量有关。有研究指出器官衰竭由剧烈的炎症反应引起,WBC可作为独立的死亡预测指标;但ACLF患者中不管是否发生感染,WBC和C反应蛋白均可升高[8],故脓毒血症并不是惟一引起WBC升高的原因,因此本研究中两组患者的死亡率无明显区别。但CANONIC研究发现,ACLF患者的住院死亡率与感染作为诱因相关[14]。这可能是由于在已有确切肝损伤的患者中,脓毒血症通常并非作为最初的诱因导致ACLF,而是作为二次打击加重了器官功能的衰竭[9]。本研究脓毒血症诱因组中,40.4%的患者合并其他诱因,这部分诱因与非脓毒血症组诱因组重叠,可能导致了两组死亡率无明显差异。
Shi等[9]的研究发现,肝脏诱因组中肝脏衰竭和凝血障碍的比例高于肝外诱因组;而肝外诱因组中出现肾脏、循环、呼吸衰竭的比例较高。本研究中非脓毒血症诱因组肝脏诱因所占比例高,如乙型肝炎病毒复发、酒精摄入等;而脓毒血症是肝外诱因中最为常见的一类,脓毒血症诱因组的肾功能衰竭和循环衰竭的发生率高于非脓毒血症组,肝功能衰竭和凝血障碍的发生率低于非脓毒血症组。说明ACLF发生过程中可能存在不同的途径和自然病程。
ACLF的两种产生机制可能提示了ACLF有两种不同的亚型,一种与脓毒血症相关,感染可导致SIRS,在有系统炎症反应的患者中肾衰竭更为严重[8],在有感染的ACLF患者中(特别是SBP)过度的系统性促炎反应发展为急性肾损伤导致不良预后[8],这可能与肠内细菌易位后释放内源性分子激活TRL受体后直接损伤肾脏有关[14]。同时脓毒血症引起感染性休克可导致全身脏器低灌注,循环衰竭后导致一系列器官功能衰竭,这很好解释了为何脓毒血症诱因组中肾脏、循环衰竭的发生率高。另一种亚型与脓毒血症无关,由过度的免疫应答直接导致组织损伤和器官衰竭,通常直接导致肝脏损伤和凝血障碍。
综上所述,脓毒血症作为诱因并未增加ACLF的短期死亡率。但脓毒血症这个诱因可作为分类标准将ACLF分为两类不同临床特征的亚型,一类是由脓毒血症诱发的ACLF,肾脏、循环衰竭发生率更高;另一类则与脓毒血症无关,以肝脏衰竭和凝血功能障碍高发生率为主。通过以上简单的方法,将复杂的ACLF患者区分成不同病因、自然病程以及预后的不同亚型,将有利于今后对ACLF进行合理优化的治疗并改善预后。
参考文献
1 Moreau R, Jalan R, Gines P, et al; CANONIC Study Investigators of the EASL-CLIF Consortium. Acute-on-chronic liver failure is a distinct syndrome that develops in patients with acute decompensation of cirrhosis[J]. Gastroenterology, 2013, 144 (7): 1426-1437.
2 Sen S, Williams R, Jalan R. The pathophysiological basis of acute-on-chronic liver failure[J]. Liver, 2002, 22 Suppl 2: 5-13.
3 Jalan R, Williams R. Acute-on-chronic liver failure: pathophysiological basis of therapeutic options[J]. Blood Purif, 2002, 20 (3): 252-261.
4 Sarin SK, Kumar A, Almeida JA, et al. Acute-on-chronic liver failure: consensus recommendations of the Asian Pacific Association for the study of the liver (APASL) [J]. Hepatol Int, 2009, 3 (1): 269-282.
5 Graziadei IW. The clinical challenges of acute on chronic liver failure[J]. Liver Int, 2011, 31 Suppl 3: 24-26.
6 Jalan R, Gines P, Olson JC, et al. Acute-on chronic liver failure[J]. J Hepatol, 2012, 57 (6): 1336-1348.
7 Olson JC, Wendon JA, Kramer DJ, et al. Intensive care of the patient with cirrhosis[J]. Hepatology, 2011, 54 (5): 1864-1872.
8 Moreau R, Jalan R, Arroyo V. Acute-on-chronic liver failure: Recent concepts[J]. J Clin Exp Hepatol, 2015, 5 (1): 81-85.
9 Shi Y, Yang Y, Hu Y, et al. Acute-on-chronic liver failure precipitated by hepatic injury is distinct from that precipitated by extrahepatic insults[J]. Hepatology, 2015, 62 (1): 232-242.
10Li H, Pavesi M, Zeng B, et al. “Eastern” type of acute-on-chronic liver failure (ACLF) is similar in pathoophysiologic, diagnostic and prognostic criteria to the “Western” type: A comparison of Chinese hospitalized patients with hepatitis B with CANONIC data[J]. Hepatology, 2014, 60: 480A-481A.
11Jalan R, Saliba F, Pavesi M, et al; CANONIC study investigators of the EASL-CLIF Consortium. Development and validation of a prognostic score to predict mortality in patients with acute-on-chronic liver failure[J]. J Hepatol, 2014, 61 (5): 1038-1047.
12Fernández J, Gustot T. Management of bacterial infections in cirrhosis[J]. J Hepatol, 2012, 56 Suppl 1: S1-S12.
13Romero-Gómez M, Montagnese S, Jalan R. Hepatic encephalopathy in patients with acute decompensation of cirrhosis and acute-on-chronic liver failure[J]. J Hepatol, 2015, 62 (2): 437-447.
14Arroyo V, Moreau R, Jalan R, et al; EASL-CLIF Consortium CANONIC Study. Acute-on-chronic liver failure: A new syndrome that will re-classify cirrhosis[J]. J Hepatol, 2015, 62 (1 Suppl): S131-S143.
(2015-06-02收稿;2015-08-10修回)
·论著·
Clinical Characteristics of Acute-on-chronic Liver Failure in Patients with Hepatitis B-related Cirrhosis Precipitated by SepsisLUYunying1,DINGRu2,ZENGBo2,CHENLiuying2,YINShan2,ZHANGNannan2,LIHai2.1DepartmentofEmergency,RenJiHospital,SchoolofMedicine,ShanghaiJiaoTongUniversity,Shanghai(200127);2DivisionofGastroenterologyandHepatology,RenJiHospital,SchoolofMedicine,ShanghaiJiaoTongUniversity;ShanghaiInstituteofDigestiveDisease,Shanghai
Correspondence to: LI Hai, Email: haili_17@126.com
Background: The effect of sepsis on acute-on-chronic liver failure (ACLF) in patients with hepatitis B-related cirrhosis and its prognosis have not been reported. Aims: To retrospectively analyze the effect of sepsis as a precipitating cause on clinical severity and short-term mortality of ACLF. Methods: A total of 890 hospitalized HBV-related cirrhosis patients with acute decompensation from Jan. 2005 to Dec. 2010 were enrolled. Patients with ACLF were diagnosed by Chronic Liver Failure-Consortium Organ Failure score (CLIF-C OFs) at admission, and then were divided into sepsis (precipitated) group and non-sepsis (precipitated) group. Baseline data, laboratory examination, incidence of organ failure and short-term mortality were compared between the two groups. Results: According to CLIF-C OFs, 243 patients were diagnosed as ACLF. Of them, 47 (19.3%)patients were sepsis precipitated, 94 (38.7%) patients were non-sepsis precipitated, and 102 (42.0%) patients had no clear precipitating events. No significant difference in short-term mortality was found between sepsis group and non-sepsis group (28-day mortality: 46.8%vs. 36.2%,P=0.224; 90-day mortality: 53.2%vs. 42.6%,P=0.232). Compared with non-sepsis group, proportions of liver failure (72.3%vs. 88.3%,P=0.030) and coagulation disorder (53.2%vs. 70.2%,P=0.046) were significantly decreased while proportions of renal failure (48.9%vs. 29.8%,P=0.026) and circulation failure (14.9%vs. 4.3%,P=0.042) were significantly increased in sepsis group. Conclusions: There is no significant difference in short-term mortality between sepsis group and non-sepsis group. However, ACLF patients precipitated by sepsis have a higher proportion of renal/circulation failure, and a lower proportion of liver failure and coagulation disorders.
Key wordsSepsis; Acute-On-Chronic Liver Failure;Multiple Organ Failure
通信作者#本文,Email: haili17@126.com
DOI:10.3969/j.issn.1008-7125.2015.12.002

