餐厨废油壳聚糖脱酸初探
陈学锐+任连海+王永京+王攀

摘要:指出了游离脂肪酸含量过高会对餐厨废油后续碱性酯化处理产生不利影响,通过碱液对壳聚糖进行(活化)改性,并对不同活化条件下的壳聚糖吸附餐厨废油中游离脂肪酸的效果进行了评价。研究发现:壳聚糖在40℃,0.9mol/L NaOH-乙醇溶液中活化6h后,吸附效率得到极大提升,再与餐厨废油发生吸附,当吸附时间为6h,吸附温度为65℃时,吸附量最大,为131.1mgKOH/g。
关键词:餐厨废油;壳聚糖;脂肪酸;活化;吸附
中图分类号:TS224.6
文献标识码:A文章编号:1674-9944(2014)12-0151-04
1引言
餐厨废弃物产生量日益增加,其资源化利用重要性也日益明显。餐厨废油是餐厨废弃物重要组成部分,回收利用价值也较大。但在氧化酸败和水解的作用下,游离脂肪酸含量非常高,餐厨废油品质较差,影响后续工艺的运行。因此,有必要对餐厨废油进行脱酸处理。目前,常用的油脂脱酸工艺包括酯化、碱炼、蒸馏、萃取、酶催化、膜分离,吸附脱酸等[1,2]。其中,考虑工艺、设备、成本等因素,工业中最常使用酯化法和碱炼法脱酸,但酯化法工艺相对复杂,酸催化剂腐蚀设备,排放大量废液。碱炼法脱酸,工艺简单,成本低廉,但皂化严重,产物分离困难,腐蚀设备[3]。
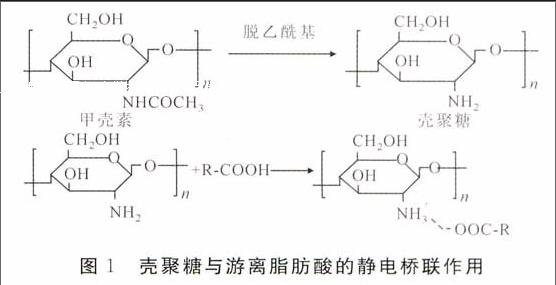
壳聚糖(Chitosan)又名脱乙酰甲壳素,甲壳素脱乙酰化的产物, 甲壳素的N-乙酰基脱去50%以上的就称为壳聚糖,是迄今为止发现的唯一天然碱性多糖,且储量丰富。壳聚糖分子中含有大量的氨基。氨基在一定条件下会和游离脂肪酸的羧基相结合,使脂肪酸分子与壳聚糖大分子之间形成化学键。程霜等[4]探讨了壳聚糖吸附游离脂肪酸的机理,即壳聚糖中的氨基与游离脂肪酸中的羧基发生静电桥联作用,是主要的吸附作用力。林宝凤[5,6]等人研究表明壳聚糖与长碳链脂肪酸之间的相互作用,不但有简单的物理吸附,还有通过盐键的相互作用。但由于天然壳聚糖分子量很高,其分子上的氨基和羟基间大多以氢键结合,性质稳定。用碱液处理壳聚糖可以破坏氢键,使壳聚糖分子活化,性质更加活泼[7]。
以前的研究成果只介绍了壳聚糖吸附脂肪酸的机理,并将其用在污水重金属处理中,而对壳聚糖改性和吸附脂肪酸效果评价的研究较少。同时,餐厨废油的脱酸工艺仍是制约餐厨废油利用的重点和难点,在本研究中,我们将壳聚糖用于餐厨废油脱酸,取得了良好的效果,为餐厨废油脱酸指出新的方向。
图1壳聚糖与游离脂肪酸的静电桥联作用
2材料与方法
2.1实验材料与仪器
餐厨废油,由北京环卫集团提供(已除杂);壳聚糖(脱乙酰度>80%)购于江苏南通兴城生物制品厂;无水乙醇,分析纯,购于国药集团化学试剂有限公司;KOH,分析纯,购于国药集团化学试剂有限公司;酚酞,分析纯,购于北京化工厂;氯化钠,分析纯,购于北京化工厂;冰醋酸,分析纯,购于北京化工厂。
HH-SY11-N电热恒温水浴锅,电热恒温水浴锅,R-201旋转蒸发器,上海申顺生物科技有限公司;DF-101S集热式恒温加热磁力搅拌器,郑州恒岩仪器有限公司;ZD-85A气浴恒温振荡器,金坛市科析仪器有限公司;DHG-9145A电热恒温鼓风干燥箱,上海一恒科技有限公司。
2.2壳聚糖活化实验
活化条件优化实验先进行单因素实验,在此基础上,通过正交实验进行验证分析。具体步骤:取2g原壳聚糖,粉碎后过50目筛,加入25mL一定浓度的NaOH-乙醇溶液,加热到一定温度,开始计时,浸泡到一定时间后取出,过滤分离,多次冲洗滤饼至冲洗液呈中性。将滤饼置于40℃烘箱内低温烘干。取3g地沟油溶解于25mL乙醇中,加入1g不同条件下处理的壳聚糖,密封后在气浴摇床中50℃条件下反应4h后测定酸值,同时测定经同样处理但未加壳聚糖空白样酸值。样品与空白样的酸值的差值为壳聚糖吸附的脂肪酸量。同时,通过乌氏粘度法,对活化前后壳聚糖分子量进行测定。
参照国标 GB/264-83 测定酸值。油脂酸值,即中和 1g油脂中游离脂肪酸所需 KOH 的毫克数。计算方法:
酸值 = V×C×56.1M
式中:V为滴定KOH 标准溶液的毫升数;C为KOH标准溶液的摩尔浓度;M为称取油样的克数。56.1为氢氧化钾的摩尔质量,g/mol。
参照项尚林[8]等方法测定分子量,先计算G值,再求分子量。计算方法:
[G]=In(T/T0)c
[G]=K·MvA
式中:[G] 为特征粘度;T为样品平均流出时间;T0为空白样平均流出时间;c为溶液中壳聚糖浓度(g/mL),K=1.8×10-3,A=0.93。
2.3脂肪酸吸附实验
取上一步骤中得出的壳聚糖改性最佳条件,处理一定量的壳聚糖,烘干后备用。取1g地沟油溶于25mL乙醇中,加入1g处理后壳聚糖,密封后置于一定温度的集热式恒温加热磁力搅拌器加热一段时间,过滤后滴定酸值,同时测量空白酸值,确定壳聚糖吸附量。以考察吸附温度和时间对改性后壳聚糖吸附量的影响。
3结果与分析
3.1壳聚糖活化条件单因素分析
3.1.1活化温度对壳聚糖吸附的影响
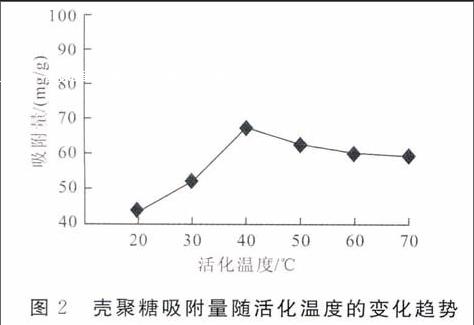
在活化时间为4h,NaOH-乙醇浓度为0.5mol/L条件下,设置20℃、30℃、40℃、50℃、60℃及70℃这6个温度梯度,考察活化温度对壳聚糖吸附量的影响,所得结果如图2所示。
图2壳聚糖吸附量随活化温度的变化趋势
由图2可知,壳聚糖的吸附量随活化温度先增加后降低,在40℃时吸附量达到最大值,为67.5mg/g。这是因为温度升高,整个体系热运动加快,传质速率加快,在碱性环境下,壳聚糖中的氨基和羟基之间的氢键被破坏,壳聚糖吸附量得到明显提升。但是温度过高,壳聚糖分子上活泼的氨基易发生副反应,尤其是羰氨反应,产物带有颜色[9],使得在后续吸附过程中起作用的氨基减少,因此,不利于壳聚糖的吸附。endprint
3.1.2活化时间对壳聚糖吸附的影响
在活化温度为40℃,NaOH-乙醇浓度为0.5mol/L条件下,设置2h,4h,6h,8h,10h及12h这6个时间梯度,考察活化时间对壳聚糖吸附量的影响,所得结果如图3所示。
图3壳聚糖吸附量随活化时间的变化趋势
由图3可知,壳聚糖的吸附量随着活化时间的延长先增加后降低。这是因为壳聚糖分子较大,氨基和羟基易结合氢键也较为稳定,碱液破坏羟基的过程较为缓慢,活化时间过短,氢键不易完全打开。同时壳聚糖属于不完全脱N-乙酰基产物(甲壳素的N-乙酰基脱去50%以上的就称为壳聚糖),其中尚有N-乙酰基存在 ,碱性环境下使甲壳素进一步脱去N-乙酰基,随着活化时间延长,反应体系提供更多的氨基[10],促进壳聚糖对游离脂肪酸的吸收。而活化时间过长,会使得壳聚糖主链断裂,氨基与羧基的静电桥联作用减退,降低了壳聚糖对游离脂肪酸的吸附能力[11]。
3.1.3NaOH浓度对壳聚糖吸附的影响
在活化温度为40℃,活化时间6h条件下,设置0.1mol/L,0.3 mol/L,0.5 mol/L,0.7 mol/L,0.9 mol/L及1.1mol/L这6个浓度梯度,考察NaOH浓度对壳聚糖吸附量的影响,所得结果如图4所示。
图4壳聚糖吸附量随NaOH浓度的变化趋势
由图4可知,随着NaOH浓度的增加,壳聚糖的吸附量也随之增加,这是因为浓度的增加,就意味着Na+数量的增加,对壳聚糖大分子间的氧键破坏作用更加强烈,释放出更多的自由氨基。同时,浓度增加到0.9mol/L时,整个溶液体系的氧键破坏水平达到临界值,此时自由氨基量最大,也不再随浓度变化而变化,所得结果与李友良研究一致[12]。
3.2壳聚糖活化正交验证
通过单因素实验,得出大致较优的活化条件,通过设置三因素三水平正交实验,排除交互作用的影响,进一步验证最佳活化条件,正交设计和结果如表1所示。
由表1中极值R值知,各因素对脱色率影响大小顺序为:活化时间>活化温度>NaOH浓度。均值分析可知,相对较优条件为活化时间6h,活化温度40℃,NaOH浓度为0.9mol/L。正交实验结果和单因素实验结果相吻合,在此条件下,壳聚糖此时的吸附量为87.6mg/L。
3.3壳聚糖活化前后分子量的变化
通过粘度法测定处理后壳聚糖的分子量约为2.6×105,小于原壳聚糖的7.5×105。这说明了壳聚糖分子发生了降解。分子量较高的壳聚糖,其分子上的氨基和羟基易结合氢键,使氨基活性降低,不利于吸附。随着分子量的降低,氢键数量减少,使壳聚糖中活性氨基数量增多。在碱性条件下,壳聚糖分子内部已经结成的氢键会被打开,同时,壳聚糖会发生脱羧反应,释放出更多氨基。这些变化都是利于壳聚糖吸附游离脂肪酸。
3.4脂肪酸吸附最佳条件
3.4.1吸附时间对脂肪酸吸附的影响
为考察吸附时间对壳聚糖吸附量的影响,吸附时间设定为2h、4h、6h、8h、10h及12h 6个时间梯度,吸附温度取45℃。吸附完毕后记录数据如下(表2、图5)。
由图5可知,当反应时间为6h时,壳聚糖的吸附量最大。当时间大于6h时,壳聚糖吸附量并未趋于平稳,反而呈现下降趋势,可能是由于时间的继续延长,使得已结合的盐键趋向于分解,使得吸附量降低[13]。故壳聚糖吸附游离脂肪酸的最佳吸附时间为6h。
3.4.2 反应时间对脂肪酸吸附的影响
为考察吸附温度对壳聚糖吸附量的影响,吸附温度设定为25℃、35℃、45℃、55℃、65℃及75℃6个温度梯度,反应时间取6h。吸附完毕后记录数据如下(表3、图6)。
由图6可知,在65℃时,壳聚糖的吸附量最大。温度较低时,吸附速率较低,随着温度的增加,吸附量也会增加,但壳聚糖吸附过程是动态的,当温度过大时,吸附相脂肪酸有足够的能量,可能摆脱盐键的吸附力[14],重新进入液相。故壳聚糖吸附游离脂肪酸的最佳吸附温度为65℃,此时吸附量为131.1mgKOH/g,而餐厨废油的酸值为159.3mgKOH/g,脱酸效率能到达82.3%
4结论
本研究通过活化后壳聚糖吸附游离脂肪酸的研究,考察了壳聚糖活化的最佳条件以及温度和时间对脂肪酸吸附的影响,得到如下结论。
(1)壳聚糖在40℃,0.9mol/L NaOH-乙醇溶液中活化6h后,壳聚糖吸附效率得到极大提升,各因素对脱色率影响大小顺序为:活化时间>活化温度>NaOH浓度。
(2)活化后的壳聚糖吸附时间为6h,吸附温度为65℃时,对脂肪酸的吸附量最大,为131.1mgKOH/g。
壳聚糖改性后应用于餐厨废油脱酸不仅可行,而且具有较高的脱除率。该方法为餐厨废油脱酸提供了新的思路。
参考文献:
[1]沈鹏.地沟油的综合利用技术综述[J].环境与可持续发展,2010,11(6):12.
[2]Proctor A,Sevugan P.Adsorption of Soybean Free Fatty Acid by Rice Hull Ash[J].Am.Oil.Chem.Soc,1990,67:15~17.
[3]Bhosle B M,Subramanian R.New approaches in deacidification of edible oils-a review[J].Journal of Food Engineering,2005,69:481~494.
[4]程霜.壳聚糖对油脂中游离脂肪酸的吸附研究[J].食品工业科技,2002,23(10):13~15.
[5]林宝凤,周妤莲, 黎演明.壳聚糖脂肪酸盐对酚醛树脂聚集态的影响[J].广西大学学报:自然科学版,2010,35(5):724~728.
[6]许益雨.壳聚糖硬脂酸盐的制备及降脂活性研究[D].无锡:江南大学,2013.
[7]高群.壳聚糖在稀溶液中的分子构象及其影响因素[J].化学通报,2009,72:1~5.
[8]项尚林,余人同.粘度法测定高聚物分子量实验的改进[J].实验科学与技术,2009,7(5):37~41.
[9]许秀丽,任荷玲.气相色谱—质谱法测定脂肪酸组成鉴别地沟油的方法研究[J].检验检疫学刊,2012,22(4):32~35.
[10]蒋英.壳聚糖降解及其分子量分布的研究[D].杭州:浙江工程学院,2003.
[11]周安娜,张国栋,张文艺.“一步法”壳聚糖制备新工艺[J].食品工业科技,2003,24(1):73~74.
[12]王英.改性壳聚糖制备胶粘剂及其胶合机理研究[D].杨凌:西北农林科技大学,2009.
[13]李友良.基于碱性溶剂体系制备壳聚糖新材料的研究[D].杭州:浙江大学,2012.
[14]梁辉.降低贻贝蒸煮液中重金属镉、铬含量的工艺优化研究[D].杭州:浙江工商大学,2007.endprint

