In2S3-Ag/TiO2三元纳米体系光催化降解2,4-D的实验研究*
余 健,赵令晖,唐 浩,刘承斌,李 玥
(1. 湖南大学 土木工程学院,湖南 长沙 410082;2. 湖南大学 化学化工学院,湖南 长沙 410082)
In2S3-Ag/TiO2三元纳米体系光催化降解2,4-D的实验研究*
余 健1†,赵令晖1,唐 浩1,刘承斌2,李 玥2
(1. 湖南大学 土木工程学院,湖南 长沙 410082;2. 湖南大学 化学化工学院,湖南 长沙 410082)
采用两步沉积法首次合成出新三元纳米材料-In2S3-Ag/TiO2纳米管阵列,并用电子扫描显微镜(SEM)、光致发光光谱仪(PL)等仪器对该三元催化剂进行形貌、元素、晶体结构的表征与光电性能的测试,并将该三元催化体系应用于2,4-二氯苯氧乙酸(2,4-D)的光降解实验.结果表明,In2S3-Ag/TiO2三元纳米材料所特有的两步光激发体系使它的催化降解能力显著提高,在溶液pH为4.23时,140 min内可实现对2,4-D 100%的去除;强酸和强碱的环境都不利于三元催化剂In2S3-Ag/TiO2对 2,4-D的催化降解.最后对三元催化剂的光催化降解机理进行了探讨.
光催化;In2S3-Ag/TiO2;两步沉积法;两步光激发
2,4-二氯苯氧乙酸(2,4-D)是一种植物生长调节剂和除草剂,在常温条件下性质稳定,微溶于水,使用后残留的大部分2,4-D进入土壤与水环境中. 虽然2,4-D遇紫外线照射会引起部分分解,但自然分解速率缓慢,在黑土中的降解半衰期为27.3 d,红土中为301.4 d.2,4-D属于低毒类有机物,能经口、皮肤吸附进入人体造成损害,对眼睛、皮肤均有刺激作用,其急性毒性主要表现为神经毒性[1].目前对存在于环境中的2,4-D的去除方法主要有生物降解、臭氧氧化以及光降解等.其中,光催化降解是一种新兴的绿色水处理技术,它具有高效、无二次污染、适用范围广等优点,在环境污染治理领域已初步显示出其明显的优越性[2].
光催化作用是光催化剂(多数指半导体材料)在光照条件下,通过在空间内不同类型纳米分子之间的联动作用,有效地将太阳能转化为其它能量形式的反应[3-6].二氧化钛纳米管阵列(TiO2nanotube arrays,简称TiO2NTs)以其无毒、价廉、化学稳定性强、催化活性高等优良特性在水处理领域展现出广阔的应用前景[7-8].TiO2是一种宽禁带的半导体材料(Eg=3.2 eV),为了增强其对可见光的吸收能力,提高其光生电子空穴对的分离效率,需要对TiO2纳米管阵列进行修饰[9-10].而三元复合纳米催化剂由于其特有的两步光激发过程和电子转移中介作用而使光生电子空穴对的分离效率得到提高,受到了研究人员的广泛关注[11-13].
硫化铟(In2S3)具有绿色环保、带隙窄(2.0 eV)、能级结构理想等优点[14];而银(Ag)成本低,且可加强局部表面等离子体共振效应[15],提高半导体之间的电子转移效率,因此可作为二者之间的电子转移桥梁.
迄今为止,用于光催化降解的In2S3-Ag/TiO2NTs三元纳米材料还未见报道,因此,本文采用物理化学方法制备出In2S3-Ag/TiO2NTs三元复合纳米材料,对其进行表征,并将其应用于2,4-D的光催化降解,探讨三元纳米材料In2S3-Ag/TiO2NTs作为光催化剂应用于芳香烃类有机物光催化降解的效果.
1 实 验
1.1 材料与试剂
钛片(纯度为99.8%,厚度为0.127 mm)购买于Aldrich(Milwaukee,WI)公司.2,4-D购买于Johnson Matthey Alfa AESAR.硫酸氢钠(NaHSO4)、氟化钠(NaF)、氯化铟(InCl3)、硫代硫酸钠(Na2S2O3)以及其他化学试剂均为分析纯.整个实验过程中使用的水均为去离子水.
1.2 二氧化钛纳米管阵列(TiO2NTs)的制备
阳极氧化反应前,将钛片剪成4 cm×1 cm的长方形,然后用稀氢氟酸(1∶3)和去离子水清洗掉表面的有机物,干燥后备用.将此钛片作为两电极体系中的阳极,用铂电极作为阴极.将电极浸入到含有0.5 mol/L NaHSO4和0.1 mol/L NaF的电解液中,在室温下用15 V的电压氧化阳极2 h.为了获得具有较高光催化活性的锐钛矿晶型TiO2,需要将其进行高温热处理:在500 ℃下煅烧3 h,然后降至室温,升温和降温速率均为2 ℃·min-1.
1.3 Ag和In2S3纳米粒子对TiO2NTs的修饰
首先用Ag纳米粒子修饰TiO2NTs.采用循环伏安法将Ag+还原为Ag,并使其生长在TiO2纳米管阵列的表面.该实验使用CHI660D型电化学工作站,在其三电极体系中,参比电极为甘汞电极,对电极为铂电极,工作电极为二氧化钛纳米管阵列.分散液为预配的0.5 mM Na3[Ag(S2O3)2]溶液.参数设置为:起始电位-1.5 V,结束电位-1.5 V,最高电位1.0 V,扫速0.05 V/s.扫描电位从-1.5 V开始,经最高电位1.0 V,最终回到结束电位-1.5 V,这个过程称为一个循环.循环次数(cycle number,简称c)分别设为5 c,7 c和10 c.循环次数增加,沉积Ag纳米粒子的量随之增多.
其次用连续离子层吸附法(Successive Ionic Layer Adsorption And Reaction,简称SILAR)使In2S3纳米粒子生长在Ag/TiO2NTs表面.将上一步制备好的Ag/TiO2NTs先浸泡在0.025 mol/L InCl3溶液中1 min,后浸泡在去离子水中30 s,再浸泡在0.375 mol/L Na2S溶液中1 min,最后浸泡在去离子水中30 s.同样,将上述4步程序称为一个循环(c).在本实验中,循环次数仍然设为5 c,7 c和10 c.循环次数增加,沉积In2S3纳米粒子的量随之增多.最后将制备好的In2S3-Ag/TiO2NTs在氩气保护下,于400 ℃下煅烧1 h,然后冷却至室温.
Ag和In2S3纳米粒子在TiO2NTs表面的沉积过程见图1.
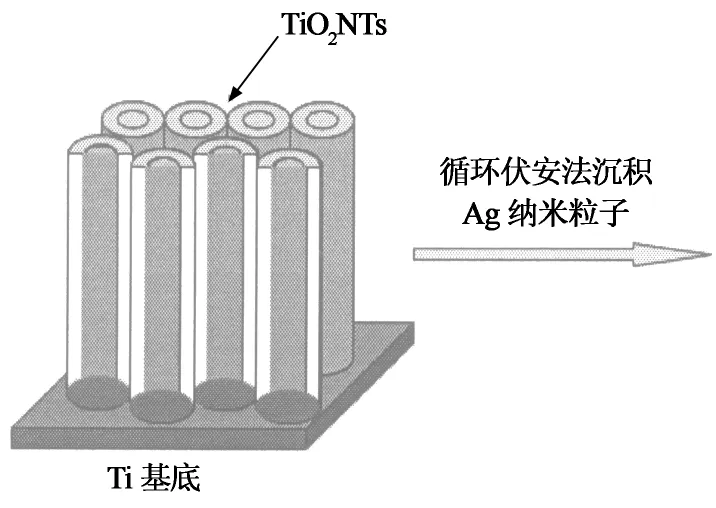


图1 In2S3-Ag/TiO2NTs制备过程示意图
1.4 In2S3-Ag/TiO2NTs的物理化学表征与光电性 能测试
使用扫描电子显微镜(FE-SEM) (Hitachi, model S-4800, 日本)检测样品的表面形貌.X-射线能量色谱仪(EDX)用来分析样品中的元素.带有Cu-Kα射线的X射线衍射仪(XRD,M21X,MAC Science Ltd.,日本)用来检测样品的晶体结构.光致发光光谱仪(FL,F-2500, Hitachi,Japan)、紫外-可见漫反射光谱仪(DRS,Cary 300,USA)用来测试材料的光电性能.
1.5 In2S3-Ag/TiO2NTs的光催化降解实验
光降解实验前,将3片具有相同掺杂物质及掺杂量的纳米管(3 cm×3 cm)垂直置于装有50 mL,15 mg/L 2,4-D溶液的石英杯中,避光条件下浸泡30 min,以达到吸附平衡.然后在模拟太阳光照射下进行光降解实验.光源为一个氙灯,功率500 W(PLS-SXE300, Beijing Changtuo Co. Ltd., China);石英杯与光源的距离是25 cm.
在磁力搅拌和光照下进行光降解实验.实验过程中,每隔20 min取一次样.在紫外-可见分光光度计上测量样品的吸光度,再根据吸光度与浓度的关系式换算出2,4-D的浓度.
2 结果与分析
2.1 催化剂的物理化学表征
2.1.1 催化剂的扫描电镜图(SEM)分析
图2(a)为未修饰的纯TiO2纳米管.从图中可以直接观察到用阳极氧化法制得的纯二氧化钛纳米管具有高度有序、排列整齐的管结构,管壁较薄,厚度大约为3~5 nm,且纳米管孔径大小均匀,直径大约为70~100 nm.从图2(b)可见,采用循环伏安法使Ag纳米粒子长在TiO2NTs表面上时,制得的Ag/TiO2NTs上均匀地分散着粒径为15~20 nm的球状Ag纳米粒子.从其嵌入图可知,采用循环伏安法沉积在纳米管表面的粒子具有高度分散性,且未损坏原来的纳米管管状结构.从图2(c)可知,在In2S3/TiO2NTs二元催化体系中,采用连续离子层吸附的方法在纳米管表面生长出来的In2S3纳米粒子尺寸非常小,有利于形成量子尺寸效应.从其嵌入图可知,经过7个SILAR循环后,In2S3纳米粒子同样可以有效地负载在TiO2NTs表面.图2(d)显示了7 cIn2S3-5 cAg/TiO2NTs的形貌特征.从图中可以看出,Ag和In2S3纳米粒子分布均匀,粒径大约为15~30 nm,它们的共同修饰使三元纳米材料的表面相对于二元催化剂Ag/TiO2NTs和In2S3/TiO2NTs来说更加粗糙.
2.1.2 催化剂的能谱(EDX)分析
图3很好地证明了Ag,In,S,Ti,O 5种元素存在于该三元结构体系中.根据EDX能谱图,Ag,In,S,Ti和O等原子分数分别为0.64%,0.30%,0.56%,64.63%和33.87%.

(a) 纯TiO2NTs

(b) Ag/TiO2NTs

(c) In2S3/TiO2NTs

(d) 7cIn2S3-5cAg/TiO2NTs
2.1.3 催化剂的X射线衍射(XRD)分析
由于每一种晶体结构都存在相对应的X射线衍射图(XRD),故采用X射线衍射仪对In2S3-Ag/TiO2NTs的组成成分和晶体结构进行分析.图4是复合型催化剂和纯二氧化钛的X射线衍射图(XRD).图中展示了与锐钛矿型二氧化钛符合良好的特征峰,以及相对较弱的Ag的特征峰(38.0°, 44.4°, 64.6°和77.5°)和In2S3的特征峰(28.487°和47.99°).出现这种现象的原因可能是Ag和In2S3在整个三元复合材料中相对于TiO2的含量较少.而锐钛矿的特征峰是25.4°,38.0°和48.1°,这说明了500 ℃的条件下煅烧可以转化为锐钛矿型TiO2.
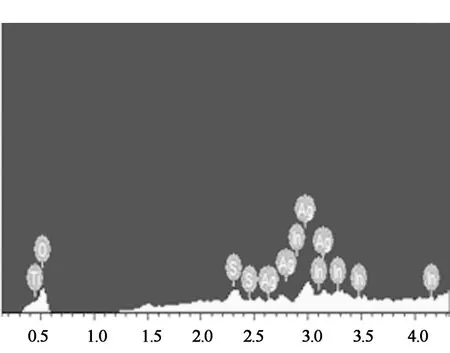
V/keV
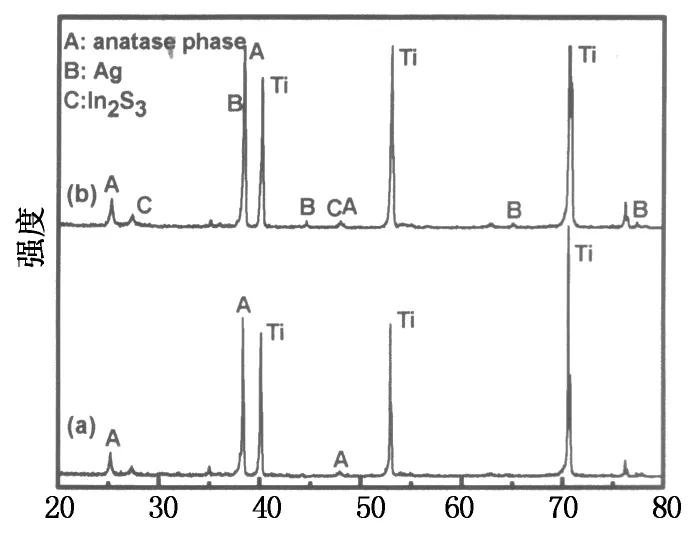
2θ/(°)
2.2 催化剂的光电性能测试
2.2.1 光致发光光谱分析
光致发光强度越大,材料的光生电子和空穴的复合几率就越大,光生电荷的寿命就越短,材料的光催化能力就越弱[16].为了研究Ag和In2S3纳米粒子的引入对光生电子和空穴分离效率的影响,将材料的激发波长设在275 nm处,对TiO2NTs,Ag/TiO2NTs,In2S3/TiO2NTs和In2S3-Ag/TiO2NTs等4种催化剂进行了光致发光光谱的分析.由图5可知,In2S3-Ag/TiO2NTs表现出的光致发光强度最低,而未加修饰的TiO2NTs的光致发光强度最高.这说明Ag和In2S3纳米粒子的共修饰作用使二氧化钛的光生电子和空穴的复合几率显著降低,有利于延长光生电荷的寿命.
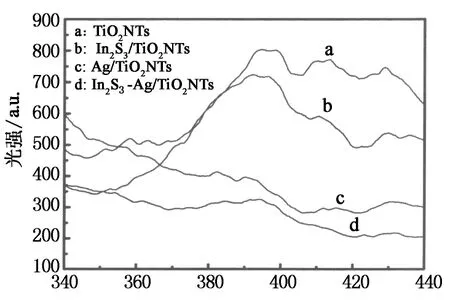
波长/nm
2.2.2 催化剂的漫反射光谱(DRS)分析
紫外-可见漫反射光谱一般用于测定催化剂在可见光和紫外光照射下的光吸收性能.图6为纯TiO2NTs,Ag/TiO2NTs,In2S3/TiO2NTs和In2S3-Ag/TiO2NTs的紫外可见漫反射光谱曲线.
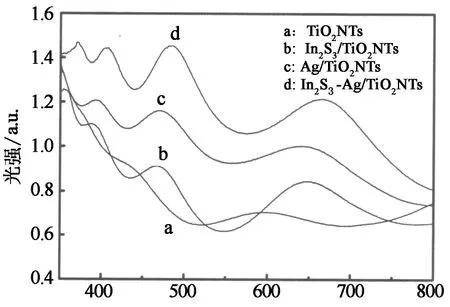
波长/nm
据文献可知,小于400 nm的峰是锐钛矿二氧化钛固有的吸收峰[17],在经过Ag或In2S3纳米粒子修饰后,4种材料在400~700 nm的范围内均能产生较强的可见光吸收,并且向可见光区域产生明显的红移.出现这种现象的原因可能是15~20 nm的银纳米粒子产生了局部表面等离子体共振效应(LSPR),和窄带隙半导体硫化铟的引入使TiO2NTs对可见光区域的响应范围得以拓宽,对可见光的吸收能力得以加强[18].而Ag和In2S3纳米粒子的共修饰作用使TiO2纳米管表面更加粗糙,与光的接触面积增加,以及二者之间的协同作用,使In2S3-Ag/TiO2NTs对可见光的吸收强度远大于一元材料和二元材料.
2.3 催化剂的光降解实验
2.3.1 Ag/TiO2NTs和In2S3/TiO2NTs二元催化 剂中纳米粒子最佳负载量的确定
Ag和In2S3纳米粒子在TiO2纳米管表面的最佳负载量是通过对有机污染物2,4-D的光降解效率确定的.图7是不同成分的二元催化剂-Ag/TiO2NTs和In2S3/TiO2NTs对2,4-D的光降解效率.从图中可以看出,二元复合纳米材料相对于一元材料TiO2NTs而言,可以显著地提高纳米管的光催化降解效果,其中,以7 c Ag/TiO2NTs和7 c In2S3/TiO2NTs的降解效果为最佳.在光照时间为140 min时,它们对2,4-D的降解效率分别为79.5%和71.5%.

光照时间/min
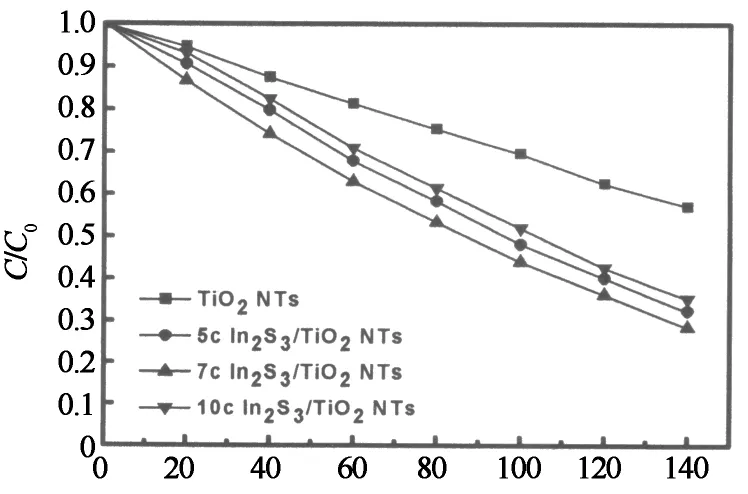
光照时间/min
2.3.2 In2S3-Ag/TiO2NTs三元催化剂中纳米粒 子最佳负载量的确定
在保持TiO2量不变的基础上,改变Ag和In2S3的负载量,以找出三元体系中具有最高光催化活性的两种纳米粒子组合条件.从图8(a)可以看出,在In2S3-Ag/TiO2NTs三元复合纳米材料中,7 c In2S3-5 c Ag/TiO2NTs的降解速率最快:光照时间为140 min时,2,4-D的去除率即达100%.从2,4-D的紫外可见分光光谱图(图8(b))看出,在只有7 c In2S3-5 c Ag/TiO2NTs而无其它任何助催化剂的情况下,溶液2,4-D的吸收特征峰值随着时间的延长逐步降低,经过140 min光照后,其吸收特征峰(228 nm)基本消失.
出现该结果的原因可能是:当Ag纳米粒子的负载量一定时,适当地增加In2S3纳米粒子的沉积量,可以为纳米材料表面提供更多的反应活性位点.然而当Ag纳米粒子或者In2S3纳米粒子在TiO2NTs上的负载量过大时,会导致催化剂表面形成一些尺寸较大的纳米粒子聚合体,这些聚合体将减弱光的穿透能力,造成光的散射.且定量的TiO2晶格对这两种纳米粒子的容纳空间有限,当三元催化剂为7 cIn2S3-5 cAg/TiO2NTs时,负载量已达到上限,此时的材料具有稳定的结构,其光催化降解性能为最佳.从7 cIn2S3-5 cAg/TiO2NTs的SEM图可知,此时TiO2纳米管表面均匀地分散着直径小于30 nm的纳米粒子,无粒子团聚现象出现,且其光电性能最佳,这说明在这种组合条件下,TiO2表面产生的活性位点能够得到充分的利用,光生电子(e-)和空穴(h+)可以得到有效分离,有利于提高光催化剂的降解效率.
图8(c)表明,在无催化剂、只有光照的条件下,2,4-D可以发生微弱的降解.而在有催化剂的情况下,一元纳米材料(纯TiO2NTs)的光催化活性最低;当引入Ag或者In2S3纳米颗粒后,光催化降解速率明显提高;在Ag和In2S3纳米粒子的共同修饰下,光催化活性最高,两种纳米粒子处于最佳组合状态时,140 min内可实现对2,4-D 100%的去除.这一结果与Zhu等研制的三元催化剂CdS-Au/TiO2的光催化降解效果相比更好:CdS-Au/TiO2在120 min内对亚甲基蓝仅有72%的催化氧化去除率[12].
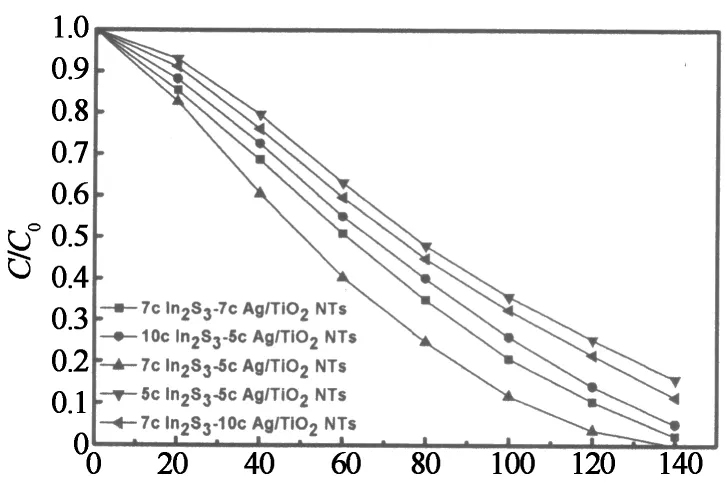
光照时间/min
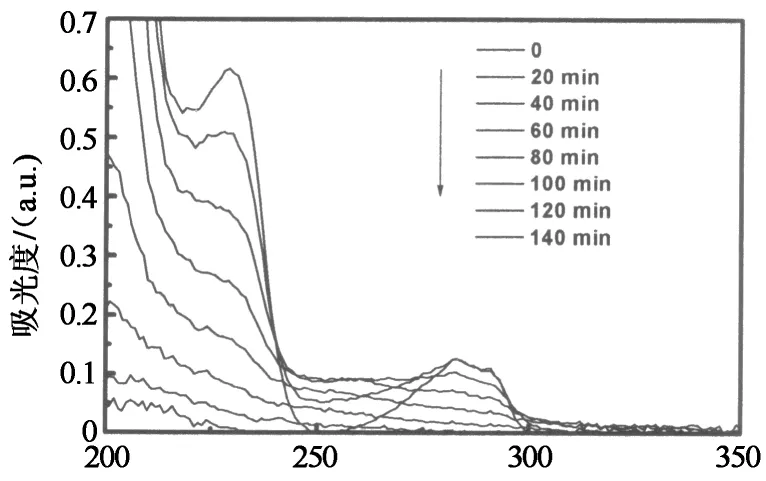
光照时间/min
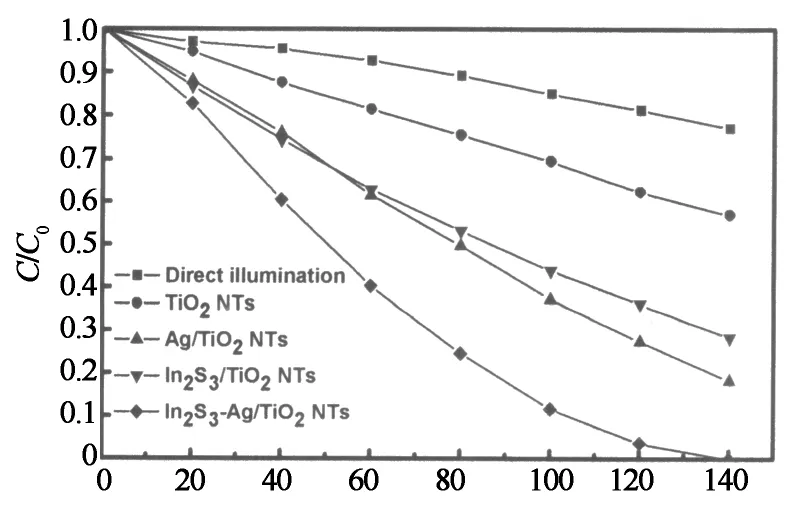
光照时间/min
2.4 pH值对光降解效果的影响
在以7 cIn2S3-5 cAg/TiO2NTs为光催化剂的2,4-D光降解实验中,用H2SO4和NaOH调节待降解溶液的pH值,使其分别为2.05,4.23,6.00,7.98,9.87,保持2,4-D的浓度在15 mg/L,光降解效率曲线见图9.当pH从2.05增加到4.23时,光降解速率随着pH的增加而增加;当pH从4.23增加到9.87时,光降解速率随着pH的增加而减小.该结果说明7 cIn2S3-5 cAg/TiO2NTs光降解2,4-D的最佳pH是在4.23,即弱酸性环境.其主要原因可能有以下几点:
1) 空穴与水的反应是形成羟基自由基主要途径之一,所以当溶液呈强酸性时,会造成H+浓度增加,从而不利于反应TiO2(h+) + H2O → TiO2+ ·OH+H+的进行,羟基自由基的数量也会随之减少,导致光催化降解速率下降;
2)偏酸性的环境下,H+数量增加非常有限,不会对·OH的形成造成很大影响(TiO2(h+) + H2O → TiO2+·OH+H+);且有助于形成HO2· (O2·_+ H2O →HO2·+OH-),这种自由基可以补充由于H+的增加而减少的·OH活性基团的量,并且可以促进HO2·+ H2O → ·OH + H2O2的反应,从而产生更多的羟基自由基;
3) 碱性溶液中,OH-浓度过高,使反应O2·_+ H2O →HO2·+OH-的进行受到阻碍,HO2·的减少会使下一步反应HO2·+ H2O →·OH + H2O2生成·OH的数量减少,导致光催化降解效果变差.
4) pH不同,TiO2对羟基和质子的吸附就不均等.由于TiO2纳米管的等电点为6.0~6.5,当溶液pH值大于等电点时,TiO2纳米管将吸附OH-,其表面将带负电(·TiOH+OH-→TiO-+H2O);当pH值小于等电点时,TiO2纳米管将吸附H+,其表面将带正电(·TiOH+H+→TiOH2+).2,4-D的酸离解常数pKa为2.64~3.31[19],当溶液呈强碱性时,2,4-D主要呈电负性,带负电的2,4-D分子与表面呈负电的TiO2和In2S3之间存在静电斥力;当溶液呈强酸性时,2,4-D呈正电性,带正电的2,4-D会与带正电的TiO2和In2S3也存在静电斥力,因此强酸和强碱的环境都会影响2,4-D与催化剂表面的接触,从而降低光降解速率.

光照时间/min
2.5 In2S3-Ag/TiO2NTs三元结构体系光催化降 解机理的初步探讨
图10说明了In2S3-Ag/TiO2NTs三元结构体系中半导体的能级结构及电子转移的路径.对于In2S3-Ag/TiO2NTs,其光生电子转移路径包含了两步[13]:TiO2→Ag;Ag→In2S3.在该两步光激发体系中,TiO2和In2S3都会产生光生电子和空穴的分离,而Ag是光生电子从TiO2向In2S3转移的桥梁.
光生电子转移过程见方程式(1)~(9).当受到光照时,TiO2和In2S3都会产生光生电子和空穴的分离,它们的电子分别从各自的价带(valance band,简称VB)跃迁到导带(conduction band,简称CB)上,见式(1),(2);TiO2被激发的电子通过肖特基势垒效应[15]从TiO2的导带上转移至Ag上(光生电子的一次转移:TiO2→Ag),而空穴就留在TiO2的价带上,见式(3);同时,Ag纳米粒子表面积累的电子与In2S3价带上的空穴结合(光生电子的二次转移:Ag→In2S3),进一步促进了In2S3光生电子和空穴的分离,见式(4);最后留在TiO2价带上的空穴与水分子进行氧化反应,留在In2S3导带上的电子与溶解氧进行还原反应.
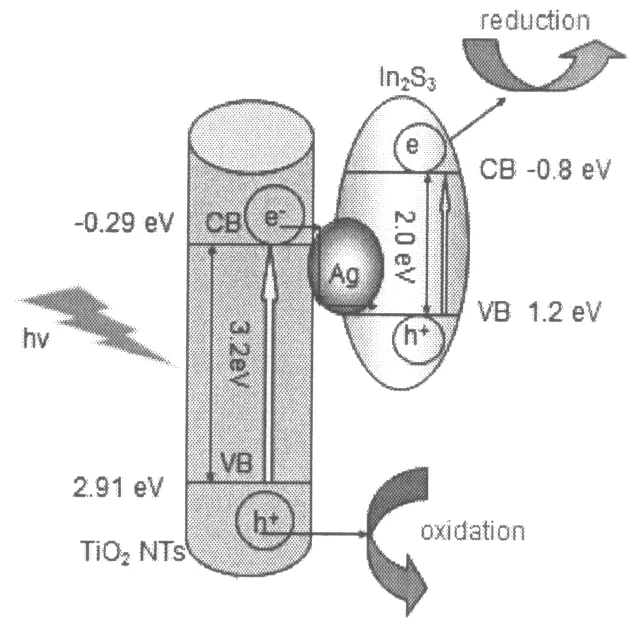
图10 In2S3-Ag/TiO2NTs的电子转移路径图
光生电子通过与溶解氧分子的反应及质子化作用生成·OH和H2O2,见式((5)~式(7));留在TiO2上的一部分光生空穴将被H2O捕获而生成羟基自由基,见式(8).由以上反应生成的活性物种(·OH)以及空穴作为一种强氧化剂参与到2,4-D的降解反应中,见式(9).
一种催化剂能否具有良好的光催化性能取决于该催化剂的光吸收性能及其对光生电子空穴对的分离能力.对于一元催化剂TiO2NTs而言,其带隙较宽,对可见光的吸收能力弱,光生电子和空穴的复合率高,故光催化活性很低.对于二元催化剂Ag/TiO2NTs和In2S3/TiO2NTs而言,由于Ag具有良好的导电性,而In2S3的带隙窄,对可见光响应能力强,因此Ag或In2S3的修饰可加快TiO2光生电子的转移速率,使其光催化活性有所提高.对于新型三元纳米复合材料In2S3-Ag/TiO2NTs而言,由于Ag和In2S3两种纳米粒子的共修饰作用,使TiO2NTs对光的吸收能力增强(见图6),且由于Ag具有优良的导电性能,能够将TiO2的光生电子及时转移至In2S3的导带,促进TiO2和In2S3的光生电子与空穴快速分离(见图5),从而使In2S3-Ag/TiO2NTs具有良好的光催化降解性能.
TiO2+ hν→ e-+ h+,
(1)
In2S3+ hν→ e-+ h+,
(2)
TiO2(h++e-) + Ag→ TiO2(h+) +
Ag (e-),
(3)
Ag (e-) + In2S3(h++e-) → Ag +
In2S3(e-) ,
(4)
In2S3(e-) +O2→ In2S3+ O2·-,
(5)
O2·_+ H2O →HO2·+OH-,
(6)
HO2·+ H2O → ·OH + H2O2,
(7)
TiO2(h+) + H2O → TiO2+·OH+H+,
(8)
·OH or h++2, 4-D→ Degradation.
(9)
3 结 论
1)通过两步沉积法首次成功合成一种光降解芳香族化合物的新型催化剂——三元纳米复合材料In2S3-Ag/TiO2NTs.
2)在合成三元光催化剂In2S3-Ag/TiO2NTs 时,Ag的循环以5次为佳,In2S3循环以7次较好.
3)在溶液pH为4.23的条件下,以7 cIn2S3-5 cAg/TiO2NTs为催化剂,浓度为15 mg/L 的2,4-D在140 min内的光催化去除率可达到100%.
[1] 薄存香, 张振岭, 戈扬, 等. 2, 4-二氯苯氧乙酸毒性效应研究进展[J]. 中国职业医学, 2011, 38(1): 75-76.
BO Cun-xiang, ZHANG Zheng-ling, GE Yang,etal. Research progress on the toxicity of 2,4-dichlorophenoxyacetic acid[J]. China Occupational Medicine, 2011, 38(1): 75-76. (In Chinese)[2] 石宗利, 徐松梅, 高朋召. Fe, Gd 共掺杂改性 TiO2的可见光光催化活性[J]. 湖南大学学报: 自然科学版, 2009, 36(3): 51-54.
SHI Zong-li, XU Song-mei, GAO Peng-zhao. Visible photocatalytic activity of nano-TiO2Co-doped with Fe and Gd[J]. Journal of Hunan University: Natural Sciences, 2009, 36(3): 51-54. (In Chinese)[3] YUN H J, LEE H, KIM N D,etal. A combination of two visible-light responsive photocatalysts for achieving the Z-scheme in the solid state[J]. ACS Nano, 2011, 5(5): 4084-4090.
[4] TADA H, MITSUI T, KIYONAGA T,etal. All-solid-state Z-scheme in CdS-Au-TiO2three-component nanojunction system[J]. Nature Materials, 2006, 5(10): 782-786.
[5] CHEN W T, HSU Y J. l-Cysteine-assisted growth of core-satellite ZnS-Au nanoassemblies with high photocatalytic efficiency[J]. Langmuir, 2009, 26(8): 5918-5925.
[6] FUJISHIMA A, HONDA K. Electrochemical photolysis of water at a semiconductor electrode[J]. Nature, 1972 (238): 37-45.
[7] 刘振儒, 暴勇超, 刘辉. 负载型TiO2膜太阳光光催化降解活性深蓝 KR 的研究[J]. 环境工程学报, 2007, 1(3): 46-49.
LIU Zhen-ru, BAO Yong-chao, LIU Hui. Solar photocatalytic degradation of reactive deep blue K-R by immobilized TiO2-film catalyst[J]. Chinese Journal of Environmental Engineering, 2007, 1(3): 46-49. (In Chinese)
[8] 周艺, 黄可龙, 杨波, 等. 稀土共掺杂纳米TiO2/MWCNT复合光催化剂的研究[J]. 湖南大学学报: 自然科学版, 2008, 35(6): 57-61.
ZHOU Yi, HUANG Ke-long, YANG Bo,etal. Study on rare earth codoping nanometer TiO2/MWCNT multiplex photocatalyst[J]. Journal of Hunan University: Natural Sciences, 2008, 35(6): 57-61. (In Chinese)
[9] ZHU J, REN J, HUO Y,etal. Nanocrystalline Fe/TiO2visible photocatalyst with a mesoporous structure prepared via a nonhydrolytic sol-gel route[J]. The Journal of Physical Chemistry C, 2007, 111(51): 18965-18969.
[10]RATANATAWANATE C, BUI A, VU K,etal. Low-temperature synthesis of copper (II) sulfide quantum dot decorated TiO2nanotubes and their photocatalytic properties[J]. The Journal of Physical Chemistry C, 2011, 115(14): 6175-6180.
[11]KATO H, HORI M, KONTA R,etal. Construction of Z-scheme type heterogeneous photocatalysis systems for water splitting into H2and O2under visible light irradiation[J]. Chemistry Letters, 2004, 33(10): 1348-1349.
[12]ZHU H, YANG B, XU J,etal. Construction of Z-scheme type CdS-Au-TiO2hollow nanorod arrays with enhanced photocatalytic activity[J].Applied Catalysis B: Environmental, 2009, 90(3): 463-469.
[13]XIE K, WU Q, WANG Y,etal. Electrochemical construction of Z-scheme type CdS-Ag-TiO2nanotube arrays with enhanced photocatalytic activity[J]. Electrochemistry Communications, 2011, 13(12): 1469-1472.
[14]KHANCHANDANI S, KUNDU S, PATRA A,etal. Band gap tuning of ZnO/In2S3core/shell nanorod arrays for enhanced visible-light-driven photocatalysis[J]. The Journal of Physical Chemistry C, 2013, 117(11): 5558-5567.
[15]EOM H, JUNG J Y, SHIN Y,etal. Strong localized surface plasmon resonance effects of Ag/TiO2core-shell nanowire arrays in UV and visible light for photocatalytic activity[J]. Nanoscale, 2014, 6(1): 226-234.
[16]LI Y, LUO S, WEI Z,etal. Electrodeposition technique-dependent photoelectrochemical and photocatalytic properties of an In2S3/TiO2nanotube array[J]. Physical Chemistry Chemical Physics, 2014, 16(9): 4361-4368.
[17]FANG J, XU L, ZHANG Z,etal. Au@TiO2-CdS ternary nanostructures for efficient visible-light-driven hydrogen generation[J]. ACS Applied Materials & Interfaces, 2013, 5(16): 8088-8092.
[18]WANG Q, YANG X, LIU D,etal. Ag and CdS nanoparticles co-sensitized TiO2nanotubes for enhancing visible photoelectrochemical performance[J]. Electrochimica Acta, 2012, 83: 140-145.
[19]PEI C C, CHU W. The photocatalyic degradation and modeling of 2, 4-Dichlorophenoxyacetic acid by bismuth tungstate/peroxide[J]. Chemical Engineering Journal, 2013, 223: 665-669.
The Investigation of Photodegradation of 2,4-D by the Three-component System In2S3-Ag/TiO2Nanotube Arrays
YU Jian1†, ZHAO Ling-hui1, TANG Hao1, LIU Cheng-bin2, LI Yue2
(1. College of Civil Engineering, Hunan Univ, Changsha,Hunan 410082, China;2. College of Chemistry and Chemical Engineering, Hunan Univ, Changsha,Hunan 410082,China)
A new kind of three-component nanomaterials-In2S3-Ag/TiO2nanotube arrays was first synthesized in two-step deposition method. In this study, the morphology, elements, crystal structure and photoelectric property testing of the three-component photocatalyst were characterized by scanning electron microscope (SEM) and fluorescence photoluminescence spectra (PL), etc. The three-component photocatalyst was applied to the photodegradation 2,4-dichlorophenoxyacetic acetic acid (2,4-D). The photocatalytic degradation experiment results of 2,4-D have shown that its 100% removal rate can be achieved within 140 minutes. The unique two-step excitation process in the three-component In2S3-Ag/TiO2NTs system leads to the significant improvement of photocatalytic ability. The experiments indicate that different values of pH and the concentration of 2,4-D have significant effect on degradation. The preliminary results show that the photocatalytic reactions are optimized at pH 4.23, higher or lower pH levels will reduce the removal rate due to the phase change of 2,4-D molecules. The photocatalytic degradation mechanism was also analyzed with equations and model diagrams.
photocatalysis; In2S3-Ag/TiO2; the two-step deposition method; the two-step excitation process
2015-03-15
国家“十一五”水体污染控制与治理科技重大专项 (2009ZX07423-004)
余 健(1964-),男,湖南益阳人,湖南大学教授
†通讯联系人,E-mail:jianyu@hnu.edu.cn
1674-2974(2015)12-0107-08
X5
A

