芦丁铅的合成及清除自由基活性研究*
郭胜男,翟广玉,渠文涛,张丽雪,王 艳**
(1.郑州大学 护理学院,河南 郑州 450001;2.郑州大学 药学院,河南 郑州 450001)
芦丁铅的合成及清除自由基活性研究*
郭胜男1,翟广玉1,渠文涛2,张丽雪1,王 艳1**
(1.郑州大学 护理学院,河南 郑州 450001;2.郑州大学 药学院,河南 郑州 450001)
芦丁与铅离子在室温下可以生成性能稳定的配合物。通过紫外光谱、红外光谱分析对其结构进行了表征。通过DPPH法测定了芦丁铅清除自由基的能力,实验结果显示,芦丁铅清除自由基的能力没有芦丁强。在日常生活中经常食用一些含有芦丁的黄酮类食物,如柑橘、草莓、银杏、荞麦等,可清除体内的自由基,使机体免受自由基的损伤,对降低人体内重金属离子的含量起着重要的作用。
芦丁;芦丁铅配合物;合成;表征;清除;自由基
前言
铅是对人体无任何生理功能且对人体健康有严重危害的重金属元素[1]。铅被广泛应用于交通制造业、工业、印刷及化妆品等众多领域,随着全球现代化工业和交通的快速发展,自然界中空气、水源、土壤、食物等均不同程度地受到铅污染[2]。日常生活中接触铅的机会很多,如用含铅的锡壶烫酒,儿童啃咬涂过铅油漆的玩具、铅笔、家具,含铅的食品如皮蛋、爆米花,用含铅彩色釉的瓷器装食品,特别是酸性食品,使用含铅汽油汽车尾气,含铅电池等[3]。铅对全身各系统和器官均有毒性作用,主要是神经、造血、消化、肝、肾及心血管系统。中毒时常常会出现头晕、头痛、肌肉关节酸痛、全身乏力、失眠多梦、低血红蛋白性贫血、腹胀、腹痛、便秘等多种症状[4]。环境铅污染已成为当今亟待解决的突出问题,应引起广泛关注[5]。
芦丁(槲皮素—3—芦丁糖苷,图1)广泛分布在多种植物中[6],如荞麦籽、中草药、水果,特别是柑橘类水果(橙子、葡萄柚和柠檬)。芦丁对人们的健康有重要作用,它具有显著的清除自由基的功能[7],如清除羟基自由基、氧自由基、过氧化氢自由基等,这些自由基可导致人体多种疾病。芦丁具有多方面的生理活性和药学性质,具有抗氧化[8]、抗炎[9]、抗癌[10],保护心脑血管的作用[11],还是有效的自由基清除剂和金属离子螯合剂[12]。螯合治疗是减缓重金属中毒的首选疗法[13],螯合剂能与引起中毒的重金属离子牢固地结合成螯合物,从体内排泄出去,达到解毒的目的。芦丁分子内有强配位的氧原子和合适的空间构型,能与许多金属离子形成稳定的螯合物,已经报道合成的芦丁金属螯合物有:Al(Ⅲ)、Zn(Ⅱ)[14]、Cu(Ⅱ)[15]、Co(Ⅱ)[16]、Fe(Ⅱ)、Fe(Ⅲ)[17]、Mn(Ⅱ)[18]、Au[19]。经常食用一些含有芦丁的黄酮类的食物,如柑橘、草莓、荞麦等,可清除体内的自由基,使机体免受自由基的损伤,对降低人体内重金属离子的含量起着重要的作用[20]。
本文的目的是研究芦丁与铅的螯合性质,及芦丁铅配合物清除自由基的性能。
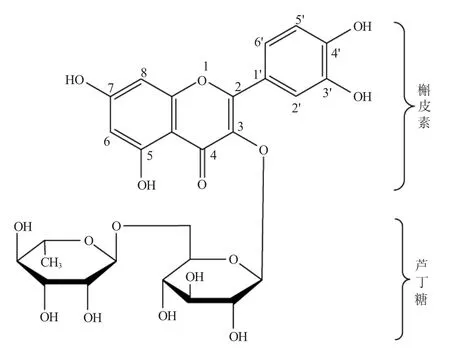
图1 芦丁的化学结构Fig.1 The chemical structure of rutin
1 实验
1.1 药品和仪器
药品:芦丁(纯度>95%),河南平舆馨星生化有限公司;硝酸铅,分析纯,二苯基苦基肼(DPPH,1、1-二苯基-2-苦基肼基自由基),上海晶纯实业有限公司;其它试剂均为分析纯。
仪器:iS10 FT-IR型红外光谱仪,美国尼高力,KBr压片;UV-2550型紫外-可见分光光度计,日本岛津公司;RE-52AA型旋转蒸发仪,上海亚荣生化仪器厂。
1.2 实验
按照文献[21]的方法进行改进。取1mmol(610mg)芦丁,加入25mL甲醇,搅拌使其完全溶解。加入预先溶于25mL甲醇中的硝酸铅 [1mmol Pb(NO3)2(331mg)]溶液,用适量甲醇钠调节pH=8.5。在磁力搅拌器上反应6h。用硅胶G板监控反应进程,待反应完成时停止。过滤,滤液在旋转蒸发仪上蒸干,得棕色固体,用甲醇冲洗三次,真空干燥器中干燥,得深棕色固体。收率67%。
1.3 清除DPPH自由基实验
溶液的配制:1×10-4mol/L的DPPH溶液的配制:准确称取10mg DPPH,置于干净的小烧杯中,用少量无水乙醇溶解,转入容量瓶中,用无水乙醇定容至刻度,混匀,避光,置于冰箱保存。供试液的配制:精密取各样品适量,以乙醇为溶剂,分别配制100mg/L、80mg/L、60mg/L、40mg/L、20mg/L的待测溶液。参照文献[22]方法,有所改进,准确吸取不同浓度的样品溶液各1mL,分别与3mL 1×10-4mol/L的DPPH溶液混合,避光放置30min,在517nm处测吸光度Ay。以相应溶剂代替样品作为空白对照,吸光度为As,相应样品溶液的吸光度为A0。DPPH自由基清除活性按下式计算:
Ay—1ml样品溶液与3mLDPPH溶液混匀后的吸光度值;As—1ml乙醇溶液与3ml DPPH溶液混匀后的吸光度值;A0—1mL样品溶液与3mL乙醇溶液混匀后的吸光度值,计算自由基半数清除率。
2 结果与讨论
2.1 紫外光谱分析
芦丁有两个吸收峰,359nm吸收带由肉桂酰生色团产生,为带Ⅰ,属于π→π*(B环)电子跃迁;257nm吸收带由苯甲酰生色团产生,为带Ⅱ,属于n→π*(A环)电子跃迁[23]。
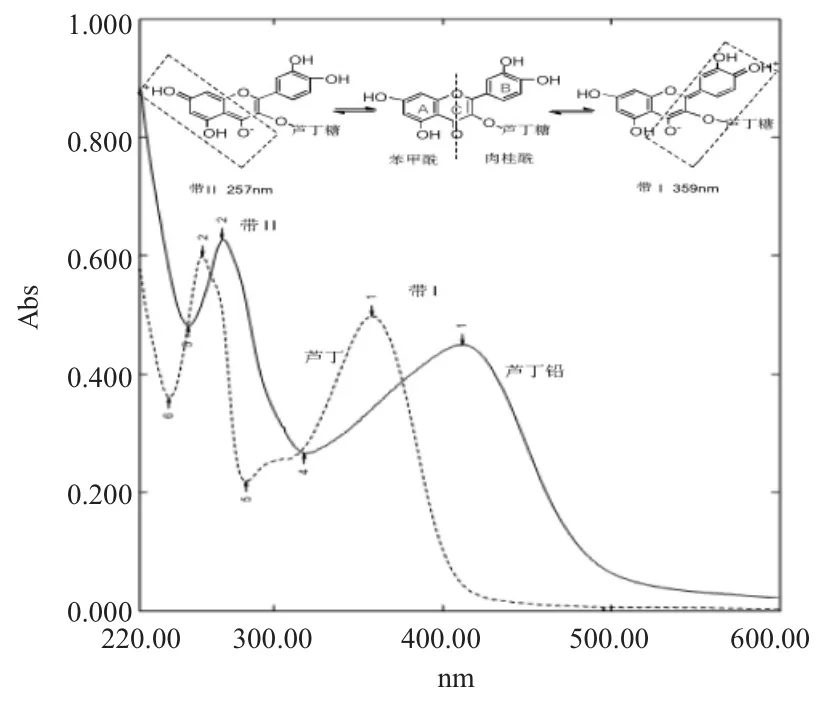
图2 芦丁和芦丁铅的紫外光谱图Fig.2 The UV-visible absorption spectrum of rutin and rutin-Pb complex
当芦丁与铅形成配合物后,共轭体系增大,电子跃迁需要的能量较低,紫外吸收光谱向长波方向移动,即发生红移。从图2可以看出,芦丁铅的带Ⅰ向红移至413nm,红移了55nm,而峰带Ⅱ向红移至270nm,移动的较少。芦丁铅的UV发生了红移,说明芦丁铅配合物的形成。带Ⅱ是苯甲酰基的吸收峰,带Ⅰ是肉桂酰基的吸收峰,配合物带I红移的多,这正说明在B环处形成了螯合环,共轭体系增大所导致的。
2.2 红外光谱分析
芦丁分子主要官能团红外吸收峰分别是:3423.42cm-1是-OH的伸缩振动,2937.69cm-1是-CH2的反对称伸缩振动,1361.52cm-1是-CH3的弯曲振动,1655.03cm-1是α、β不饱和酮的C=O伸缩振动,1603.69cm-1、1504.96cm-1、1456.11cm-1是苯环的骨架振动。1295.67cm-1、1063.13cm-1、1013.17cm-1是=C-O-C的反对称和对称伸缩振动,1203.68cm-1是酮的面内摇摆,807.88cm-1是对位取代苯面外弯曲振动[24]。
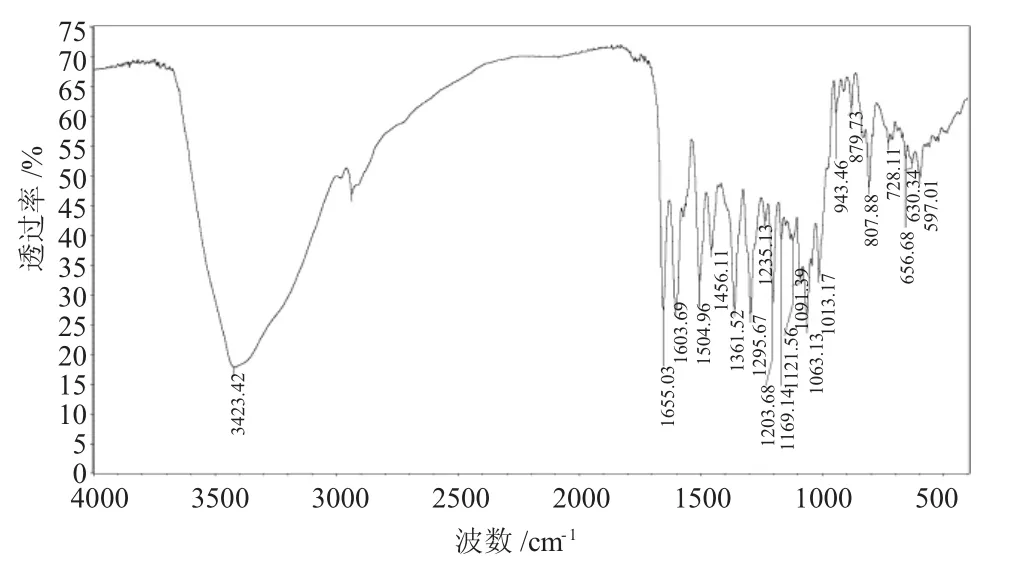
图3 芦丁的红外光谱Fig.3 The IR spectrum of rutin
芦丁铅主要官能团红外吸收峰分别是:羰基υC=O1654.87cm-1;苯环骨架振动频率υC=C1604.81cm-1、1504.95cm-1、1455.60cm-1;羟基υ-OH3416.06cm-1。
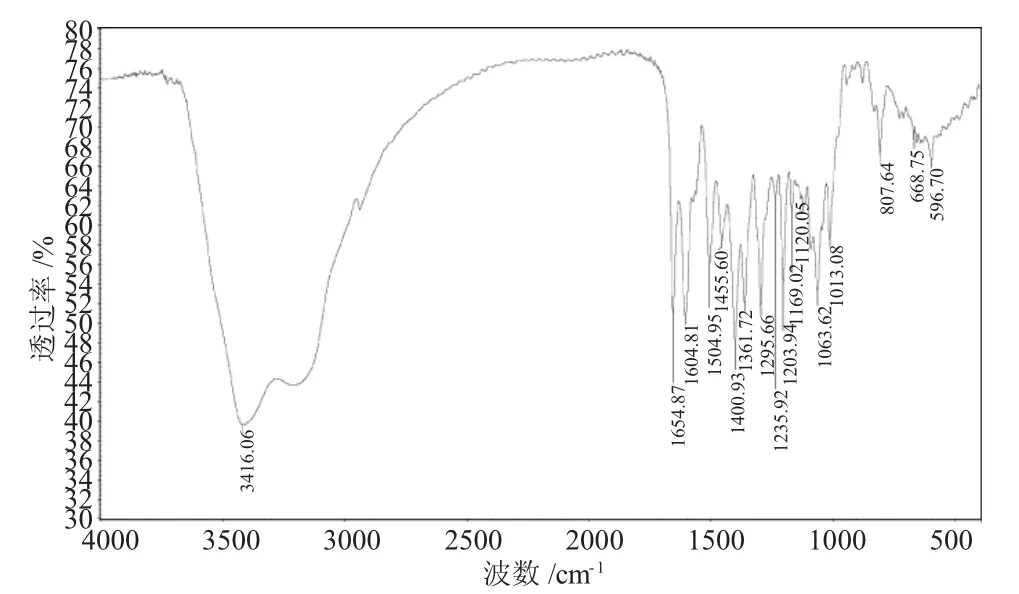
图4 芦丁铅的红外光谱Fig.4 The IR spectrum of rutin-Pb complex
通过图3和图4中的数据比较可以发现:
(1)芦丁铅υ(O-H)在3600~3000cm-1处表现出一个宽峰,说明了配合物中有水的存在[13]。
(2)芦丁的υ(C=O)出现在1655.03cm-1,当形成配合物后该振动频率是1654.87cm-1,羰基的吸收峰几乎没有发生变化,这说明配合物在羰基处没有形成配位键。
(3)芦丁在1456.11cm-1和1295.67cm-1处的吸收峰是酚羟基的C-O键伸缩振动与O-H键面内弯曲振动偶合所致,配合物中,这两个峰中间又出现了一个新的吸收峰1400.93cm-1,并且强度增大,说明酚羟基参与了配位成键。
(4)芦丁υ(C-O-C)振动频率是1203.68cm-1,芦丁铅是1203.66cm-1,配合物中此峰几乎没有变化,这进一步说明吡喃环中的氧原子没有参与配位。
(5)υ(Pb-O)伸缩振动峰在668.75cm-1的出现,说明了金属配位键的形成[25],而芦丁没有此峰。
2.3 芦丁铅体外清除DPPH自由基的作用
DPPH在有机溶剂中是一种稳定的自由基,其乙醇溶液在517nm处有最大吸收,当有自由基清除剂存在时,由于DPPH自由基的单电子被配对,从而使得在517nm处的吸光度减小,因此该法常被用来评价样品的抗氧化能力[22]。
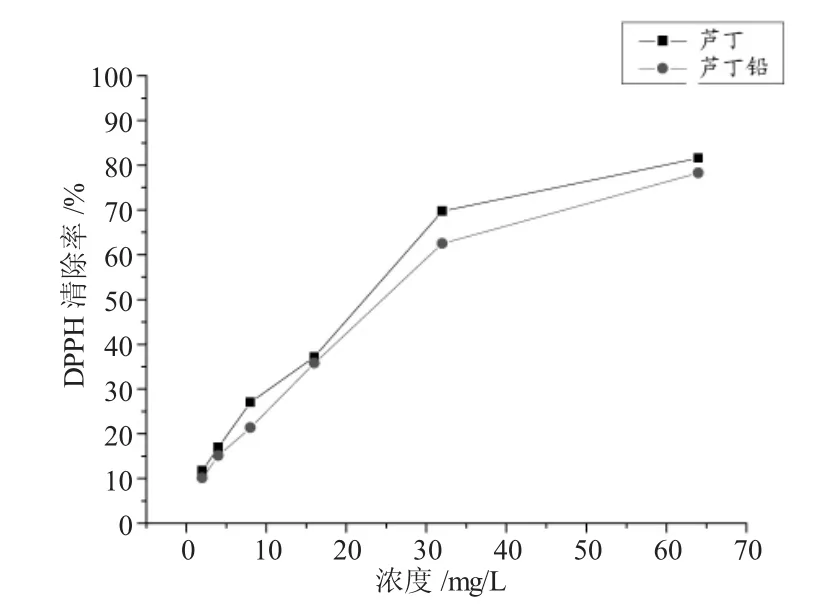
图5 芦丁和芦丁铅对DPPH自由基的清除作用Fig.5 The scavenging effect on DPPH radical of rutin and rutin-Pb
从图5可见,芦丁和芦丁铅都随着浓度的增大,对DPPH自由基的清除率也增大,但是很明显芦丁与铅离子形成配合物后,其对DPPH自由基的清除能力有所降低,这可能是由于芦丁的药效团3’,4’-二羟基与铅离子形成配位导致的。
3 结 论
(1)芦丁与铅离子在室温下就可以生成性能稳定的芦丁铅配合物。
(2)UV显示带Ⅰ红移的多,说明芦丁B环上共轭体系增大,电子跃迁需要的能量减少。
(3)IR显示羰基吸收峰几乎没有变化,邻二酚羟基吸收峰红移,668nm处有金属键特征吸收峰。
(4)清除自由基实验显示:芦丁铅没有芦丁清除自由基能力大,可能是邻二酚形成配合物后,接受电子的能力降低引起的。
(5)黄酮具有多方面的生理和药理活性,主要存在于多种蔬菜、水果、饮料和中草药中。
(6)在日常饮食中多食用含有黄酮类的食物如芦丁等,一方面可以清除体内的自由基,使机体免受自由基的侵袭,减少疾病;另一方面可以与体内的重金属离子结合成螯合物排出体外,减少重金属离子对人体的损伤。
[1] 陆贞玉,李文智.铅中毒[J].中国校医,2009,23(5):600~602.
[2] 张安星.铅在环境中的化学行为及防治措施[J].贵州化工,2009,34(6):33~35.
[3] 秦俊法,楼蔓藤,李国文.对铅中毒认识的三次重大飞跃[J].广东微量元素科学,2010,17,(3):1~13.
[4] CHEN J,TONG Y,XU J,et al.Environmental lead pollution threatens the children living in the Pearl River Delta region,China[J].Environ Sci Pollut Res Int.,2012,19(8):3268~3275.
[5] IQBAL MP.Lead pollution-a risk factor for cardiovascular disease in Asian developing countries[J].Pak J Pharm Sci.,2012,25(1):289~294.
[6] HENRYK ZIELINSKI.Antioxidant Properties and Rutin Content of High Pressure-Treated Raw and Roasted Buckwheat Groats[J].Food Bioprocess Technol,2013(6):92~100.
[7] HUI-HUI HAO,ZHU-MIN SHAO,DAO-QUAN TANG,et al.Preventive effects of rutin on the development of experimental diabetic nephropathy in rats[J].Life Sciences,2012,91(19~20): 959~967.
[8] MINA GHIASI,MAJID M HERAV.Quantum mechanical study of antioxidative ability and antioxidative mechanism of rutin(vitamin P)in solution[J].Carbohydrate Research,2011,346(6): 739~744.
[9] IGOR B AFANAS’EV,ELENA A OSTRAKHOVITCH,ELENA V
MIKHAL’CHIK.Enhancement of antioxidant and anti-inflammatory activities of bioflavonoid rutin by complexation with transition metals[J].Biochemical Pharmacology,2001,61:677~684.
[10] LIN JP,YANG JS,LIN JJ,et al.Rutin inhibits human leukemia tumor growth in a murine xenograft model in vivo[J].Environ Toxicol,2012,27(8):480~485.
[11] C MANACH,A MAZUR,A SCALBERT.Polyphenols and prevention of cardiovascular diseases[J].Curr.Opin.Lipidol.,2005, 16:77~84.
[12] AFANAS’EV,A DOROZHKO,A BRODSKI,et al.Chelating and free radical scavenging mechanisms of inhibitory action of rutin and quercetin in lipid peroxidation[J].Biochemical Pharmacology,1989,38:1763~1769.
[13] GHOLAMREZA DEHGHAN,ZAHRA KHOSHKAM.Tin(II)-quercetin complex:Synthesis,spectral characterization and antioxidant activity[J].Food Chemistry,2012,131:422~426.
[14] RUBENS F V DE SOUZA,WAGNER F DE GIOVANI.Synthesis,spectral and electrochemical properties of Al(III)and Zn(II)complexes with flavonoids[J].Spectrochimica Acta Part A,2005,61:1985~1990.
[15] MEDVIDOVIC-KOSANOVICMARTINA,SAMARDZICMIRELA, MALATESTI NELA,et al.Electroanalytical Characterization of a Copper(II)-Rutin Complex[J].International journal of electrochemical science,2011,6(4):1075~1084.
[16] LU-MING LIN,HAN-YING WU,WEI-SHUEN LI,et al.Kinetic studies of the oxidation of quercetin,rutin and taxifolin in the basic medium by(ethylenediaminetetraacetato)cobalt(III)complex[J].Inorganic Chemistry Communications,2010,13:633~635.
[17] NOWAK DOROTA,KUZNIAR ANNA,KOPACZ MARIA.Solid complexes of iron(II)and iron(III)with rutin[J].STRUCTURAL CHEMISTRY,2010,21(2):323~330.
[18] FRANZOI ANA CRISTINA,PERALTA ROSELY A,NEVES ADEMIR,et al.Biomimetic sensor based on Mn(III)Mn(II)complex as manganese peroxidase mimetic for determination of rutin[J].Talanta,2009,78(1):221~226.
[19] A P SADKOV,S A GOLOVANOVA,N V LARIONTSEVA.Protective properties of gold in the composition of nanoparticles and Au-rutin complexes[J].Russian Chemical Bulletin,2011,60(4):667~670.
[20] FRANCISCO PEREZ-VIZCAINO,JUAN DUARTE.Flavonols and cardiovascular disease[J].Molecular Aspects of Medicine,2010, 31:478~494.
[21] SELVARAJ STALIN,KRISHNASWAMY SRIDHARAN,DEVASHYAVENKAPPAYYA,etal.Synthesis,characterizationandDNA binding properties of rutin-iron complex[J].RSC ADVANCES, 2012,2(7):2797~2802.
[22] MANJALY J AJITHA,SMITHA MOHANLAL,CHERUMUTTATHU H SURESH,et al.DPPH Radical Scavenging Activity of Tricin and Its Conjugates Isolated from“Njavara”Rice Bran: A Density Functional Theory Study[J].Journal of Agricultural and Food Chemistry,2012,60(14):3693~3699.
[23] PAOLO MATTEINI,ANDREA GOTI,GIOVANNI AGATI.Theoretical conformational analysis of rutin[J].Monatsh Chem,2010,141:793~800.
[24] 周群,孙素琴,杜德国,等.芦丁热稳定性的红外光谱法实时原位跟踪[J].光谱学与光谱分析,2000,20(2):195~198.
[25] SERGIO A PAYÁN-GÓMEZ,NORMA FLORES-HOLGUÍN, ANTONINO PÉREZ-HERNÁNDEZ.Computational molecular characterization of the flavonoid rutin[J].Chemistry Central Journal,2010,4:12:2~8.
Synthesis and Free Radical Scavenging Activity of Pb(Ⅱ)-Rutin Complex
GUO Sheng-nan1,ZHAI Guang-yu1,QU Wen-tao2,ZHANG Li-xue1and WANG Yan1
(1.College of Nursing,Zhengzhou University,Zhengzhou 450052 China;2 College of Pharmacy,Zhengzhou University,Zhengzhou 450052,China)
The complex of Pb(II)with rutin was prepared at room temperature.The UV-visible,IR spectrum was used to characterize the structure of the complex.The free radical scavenging activity of the complex was evaluated by using 1,1-diphenyl-2-picrylhydrazyl(DPPH)radical scavenging method.The experiment showed that the free radical scavenging activity of Pb(II)-rutin complex was less effective than that of the rutin.Supplementing diet which is rich in rutin and other flavonoids in daily life,such as citrus,strawberry,ginkgo,buckwheat,etc.,could be contribut to removing free radicals and heavy metal ions in our body and made the body be safe from the damage of free radical.
Rutin;Pb(II)-rutin complex;synthesis;characterization;free radical
R 979.3
A
1001-0017(2015)02-0125-04
2014-12-08 *基金项目:郑州大学国家大学生创新创业训练计划项目(编号:2014xjxm316)
郭胜男(1992-),女,河南郑州人,学士,从事药物与护理研究。
**通讯联系人:王艳(1969-),女,河南新乡人,副教授。从事中草药有效成分的结构优化、药物化学合成及教学工作。E-mail:Zhaiguangyu1@sina. com

