酸水解-气相色谱法测定奶粉中的二十二碳六烯酸
邵仕萍, 相大鹏, 李 双, 奚星林, 陈文锐
(广东出入境检验检疫局检验检疫技术中心, 广东 广州 510623)
技术与应用
酸水解-气相色谱法测定奶粉中的二十二碳六烯酸
邵仕萍*, 相大鹏, 李 双, 奚星林, 陈文锐
(广东出入境检验检疫局检验检疫技术中心, 广东 广州 510623)
建立了盐酸水解,索氏提取总脂肪酸,氢氧化钾甲醇溶液甲酯化,硫酸氢钠处理,气相色谱测定奶粉中二十二碳六烯酸(DHA)含量的方法。采用三因素三水平正交试验对氢氧化钾甲醇溶液甲酯化条件进行了优化,得到最优反应条件为:1 mol/L氢氧化钾在25 ℃反应5 min。甲酯化衍生液经硫酸氢钠处理,在SP-2560气相色谱柱(100 m×0.25 mm×0.20 μm)上进行55 min程序升温测定DHA含量。DHA在5.0~300 mg/L范围内呈良好线性,相关系数为0.999 9。DHA质量浓度为10、50、100 mg/L时目标峰峰面积的相对标准偏差(RSD)分别为3.4%、1.2%和1.1%。方法检出限为2 mg/kg,回收率为90.4%~93.5%。该法用于实际样品的检测,结果令人满意。
气相色谱;二十二碳六烯酸;奶粉;酸水解
二十二碳六烯酸(docosahexenoic acid, DHA),俗称脑黄金,是一种对人体非常重要的多不饱和脂肪酸。婴幼儿缺乏DHA可能造成发育迟缓、智力障碍、皮肤异常鳞屑等不良后果[1-5]。婴幼儿奶粉作为宝宝的主要食物来源,是模拟母乳制作的配方粉,其DHA平均含量为总脂肪酸的0.2%。DHA含有6个双键,易受光、氧、热、金属离子的作用而变质[6],且具有鱼腥味,所以DHA原料供应商常用纤维素、蛋白质等材料包埋DHA,以满足人体的营养需要,并解决味觉上的不适应。目前,关于DHA含量检测技术的研究主要集中于人体血液中DHA含量的测定[7-10]和食品中DHA含量的测定[11-18],通常是先对DHA进行衍生化,然后进行色谱检测。中国国家标准GB 5413.27-2010《食品安全国家标准婴幼儿食品和乳品中脂肪酸的测定》[15]规定了奶粉中DHA的测定方法,但随着食品工业的发展,DHA包埋技术不断更新,国家标准规定的DHA检测方法和先前文献报道的方法已不能有效地测定各类奶粉中DHA的含量。这就需要发展新的DHA检测技术,以适应食品工业的进步。本文所建立的方法可以有效地测定各类奶粉中DHA的含量。
1 实验部分
1.1 仪器与试剂
7890A气相色谱,配7683B自动进样器、氢火焰离子化检测器(FID)及B04.01数据处理系统(安捷伦公司); SOXTEC 2050索氏提取仪(FOSS公司)。DHA标准品(纯度>99%)、DHA甲酯标准品(纯度>99%)(上海安谱科学仪器有限公司);电子天平,感量0.1 mg(Sartorius公司);异辛烷(色谱纯);盐酸、氢氧化钾、甲醇、正己烷、无水硫酸氢钠(分析纯);实验用水为去离子水;
DHA标准储备液的配制(1 g/L): 0.1 g DHA标准品溶于100 mL异辛烷中;其他各级DHA标准使用液根据需要逐级稀释,最大稀释比不大于1 000∶1; DHA甲酯标准储备液的配制(1 g/L): 0.1 g DHA甲酯标准品溶于100 mL异辛烷中;其他各级DHA甲酯标准使用液根据需要逐级稀释,最大稀释比不大于1 000∶1;氢氧化钾甲醇溶液(1 mol/L): 5.6 g氢氧化钾溶于100 mL的甲醇中;氯化钠溶液:40 g氯化钠溶于100 mL水中;盐酸溶液:向50 mL水中加入盐酸100 mL,摇匀。
1.2 样品前处理
总脂肪提取:称取5 g奶粉于100 mL三角烧瓶中,加入50 mL的盐酸溶液,于100 ℃水浴1 h。过滤,并用少许热水冲洗烧瓶,用沸水漂洗过滤器及其内容物,直到滤液中性。在室温下过夜(至少12 h),干燥内容物。用正己烷索氏提取总脂肪酸,称重,备用。
甲酯化:称取0.1 g上述总脂肪酸于试管中,加入2 mL异辛烷,振摇混匀。加入0.2 mL 1.0 mol/L氢氧化钾甲醇溶液,立即盖上盖子,25 ℃下剧烈振摇5 min,静置分层,加入2 mL氯化钠溶液短暂振摇。将异辛烷层转移到样品管,加入1 g硫酸氢钠并且振摇样品管,静置分层后取异辛烷层过0.45 μm滤膜后用于上机测定。
1.3 色谱条件
色谱柱:Supelco SP-2560气相色谱柱(100 m×0.25 mm×0.20 μm);升温程序:140 ℃保持5 min,以4 ℃/min升至240 ℃,保持25 min;载气(N2)流速0.80 mL/min,压力212.2 kPa,进样量0.5 μL;分流比:20∶1;进样口温度:250 ℃; FID温度:260 ℃。
1.4 结果计算
DHA的测定结果采用外标法计算,结合提取液的体积以及总脂肪酸的质量求得DHA在总脂肪酸中的含量。结合奶粉中总脂肪酸的测定结果,求得相应奶粉中DHA的含量。
2 结果与讨论
2.1 目标峰位置的确定
DHA标准品按照1.2节所述的操作进行甲酯化,再按照1.3节所述的条件进行色谱检测,所得色谱图中出现多个色谱峰,不易确定DHA甲酯所对应的目标峰,因此用DHA甲酯标准溶液进行色谱检测确定目标峰。取50 mg/L的DHA甲酯标准溶液按照1.3节所述的条件进行色谱检测,所得色谱图简洁明了,DHA甲酯所对应的目标峰的保留时间为50.350 min,如图1所示。

图1 (a)DHA标准品和(b)奶粉样品的气相色谱图Fig.1 GC chromatograms of (a) DHA standard and (b) a milk powder sample containing DHA
2.2 总脂肪酸的提取条件
奶粉中总脂肪酸的提取通常是先将奶粉样品进行水解,然后以正己烷为提取剂进行索氏抽提。因所用试剂的不同,水解方式分为碱水解和酸水解两种[12,17,19,20]。考虑到奶粉进入人体要被胃液消化,然后再被吸收,本方法模拟胃液使用盐酸溶液对奶粉样品进行酸水解,然后索氏提取总脂肪酸。
2.3 DHA甲酯化条件的优化
甲酯化是DHA检测的关键步骤,通常使用氢氧化钾(或氢氧化钠)甲醇溶液作为甲酯化试剂在指定的时间和温度下完成。虽然相同原理的甲酯化在多篇文献[11,14-16,21]中均有提及,但具体条件有显著差异。为了获得DHA甲酯化的最佳反应条件,设计了三因素三水平L9(33)正交实验,对反应温度、反应时间及甲酯化试剂KOH浓度进行优化。任意选取了某一婴儿奶粉的总脂肪酸提取物作为实验样品,相关因素的考察水平来源于GB/T 5009.168-2003[11]、GB 5413.27-2010[15]和ES ISO 12966-2:2012[21]。实验条件及结果见表1和表2。
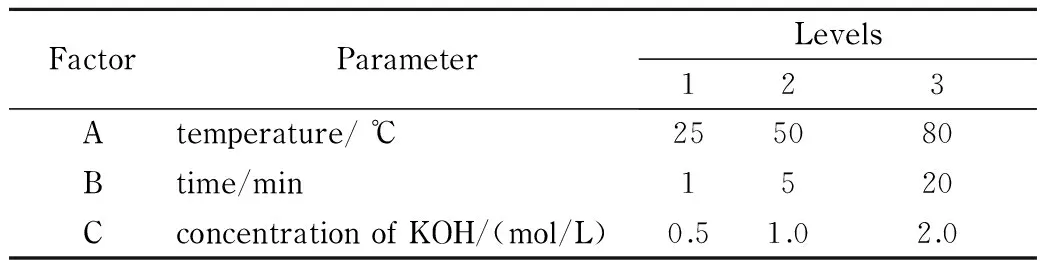
表1 正交实验的因素和水平
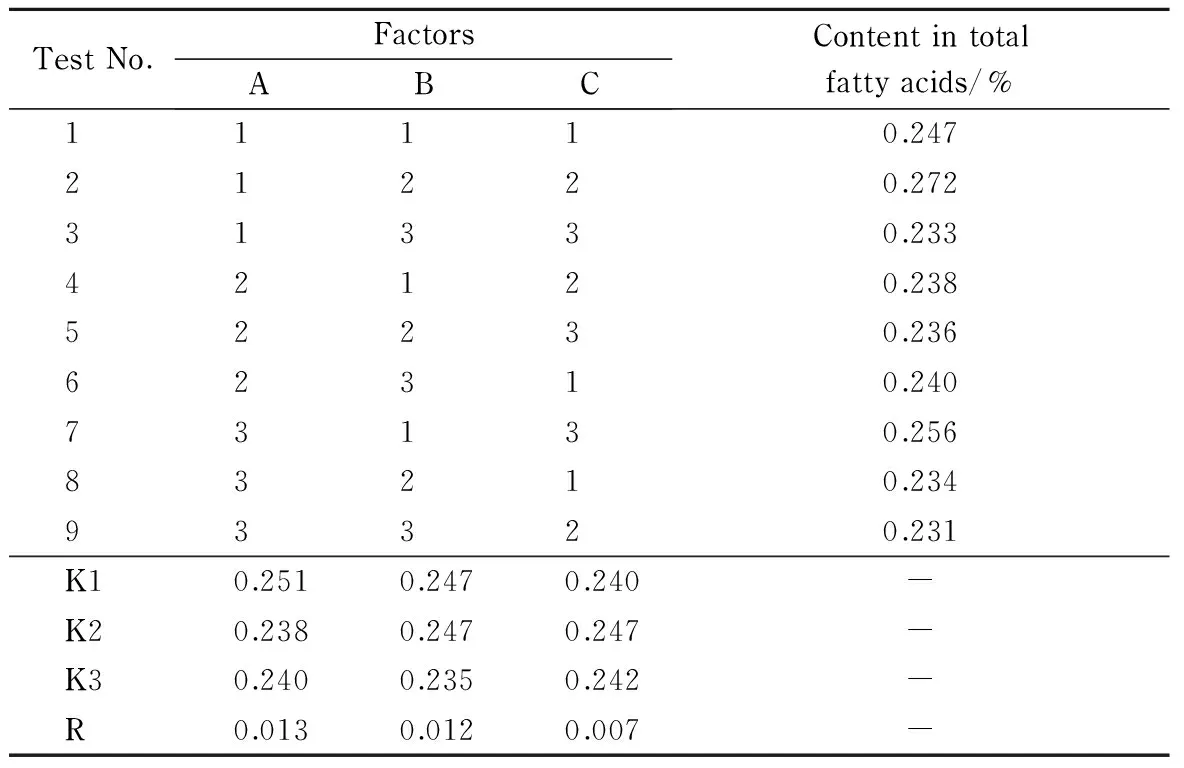
表2 实验条件的选择L9(33)正交表
-: blank.
由表2可知,反应温度是甲酯化反应的主要影响因素,且温度较低时效果更好,主要是因为DHA中含有6个双键,高温时易变质;反应时间不宜过长,否则也会因为DHA变质而致使效率降低;KOH浓度对反应影响相对较小。根据主要从优,兼顾成本效率的原则,确定A1B2C2为最佳试验条件,即2#试验所对应的条件,具体为1 mol/L氢氧化钾甲醇溶液在25 ℃反应5 min。使用最佳试验条件进行5次验证性试验,其结果(DHA在总脂肪酸中的含量)为0.270%、0.273%、0.274%、0.271%和0.273%,与2#试验结果相近,最佳试验条件可靠。
2.4 线性范围与检出限
取DHA标准储备液逐级稀释成500、400、300、200、100、80、60、40、20、10、5.0、2.0、1.0 mg/L的系列DHA标准溶液,按照1.2节所述的操作进行甲酯化,再按照1.3节所述的条件进行色谱检测,以DHA质量浓度为横坐标(X, mg/L),以目标峰面积为纵坐标(Y),绘制工作曲线。结果表明DHA质量浓度在5.0~300 mg/L范围内线性关系良好,线性方程为Y=0.349 4X+0.821 0,相关系数为0.999 9。仪器检出限为1 mg/L (S/N=3),奶粉中DHA的检出限为:0.2 mg/100 g。
2.5 精密度与回收率
取10、50、100 mg/L的DHA标准溶液2 mL各7份,按建立的方法进行甲酯化和色谱检测,考察方法的精密度,得到对应的相对标准偏差(RSD)分别为3.4%、1.2%和1.1%,表明本法具有良好的重复性。取婴儿奶粉、较大婴儿奶粉和幼儿奶粉样品各一种,分别进行7次测定,得出DHA平均含量分别为:50.4、40.7和8.2 mg/100 g,用上述3种奶粉样品作基体进行加标回收试验,结果如表3所示。
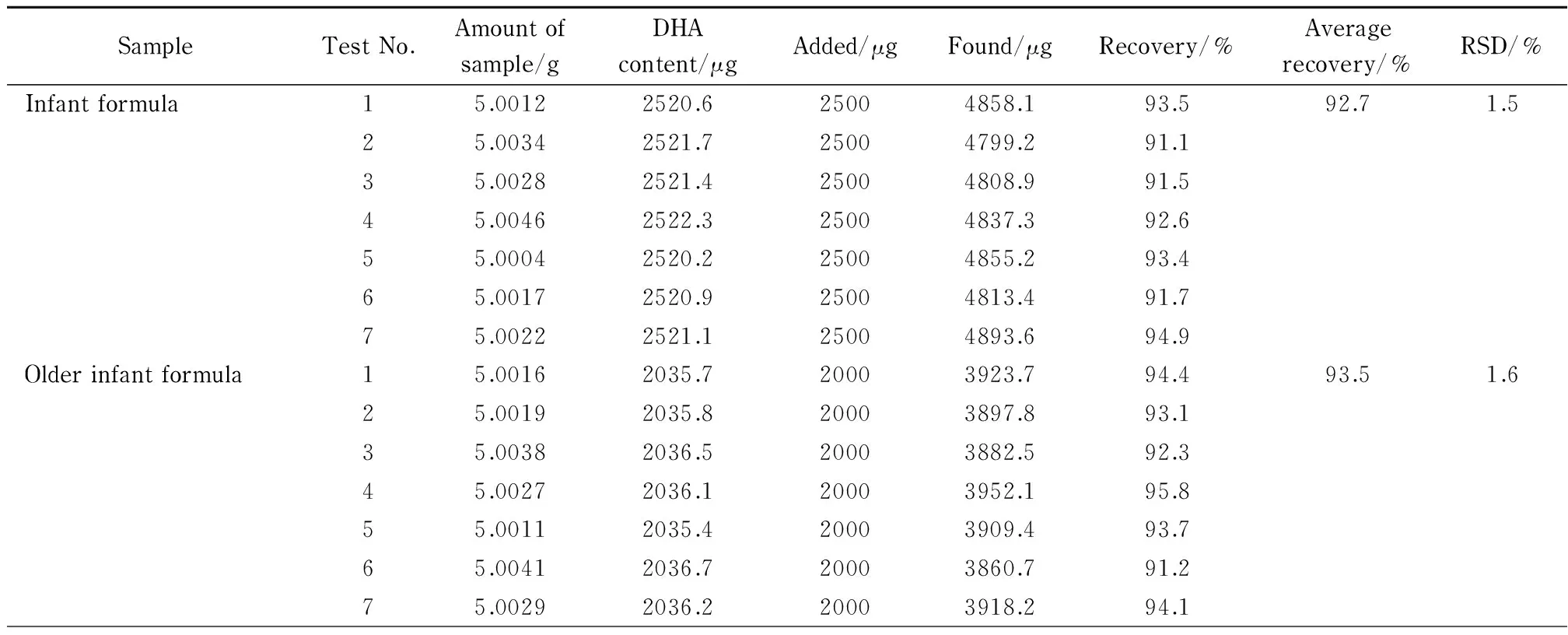
表3 加标回收率试验结果
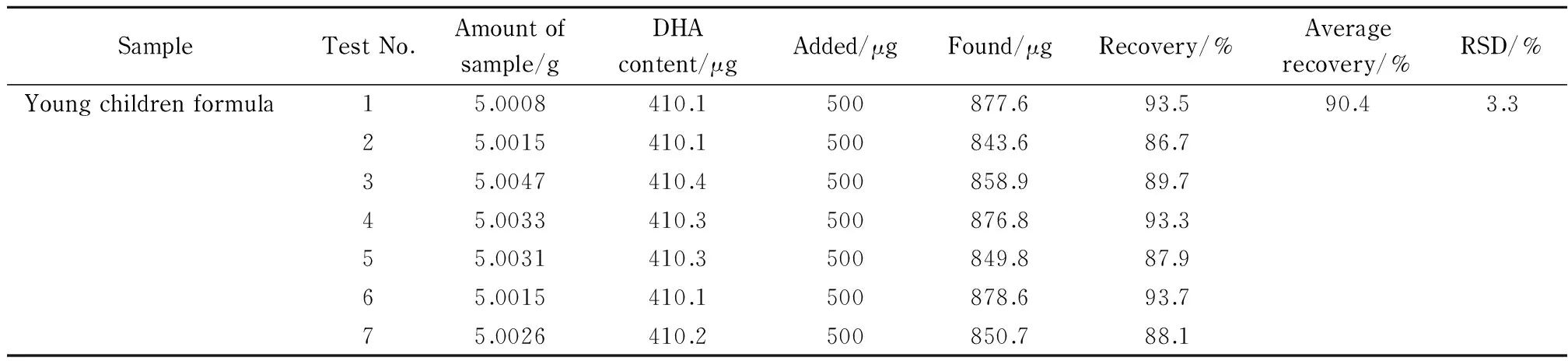
表3 (续)
由表3可知3种奶粉样品的加标回收率为90.4%~93.5%,且对应的相对标准偏差在1.5%~3.3%范围内,说明本方法准确度高。
2.6 实际样品测定
用国家标准方法GB 5413.27-2010[15](第一法乙酰氯-甲醇甲酯化法)和本方法分别对18个奶粉样品进行DHA含量的测定,结果如表4所示。由表4可知本方法的测定结果与样品的标签值十分接近,而国标方法的测定结果往往与样品的标签值有较大差异,甚至会出现无法检出的现象。
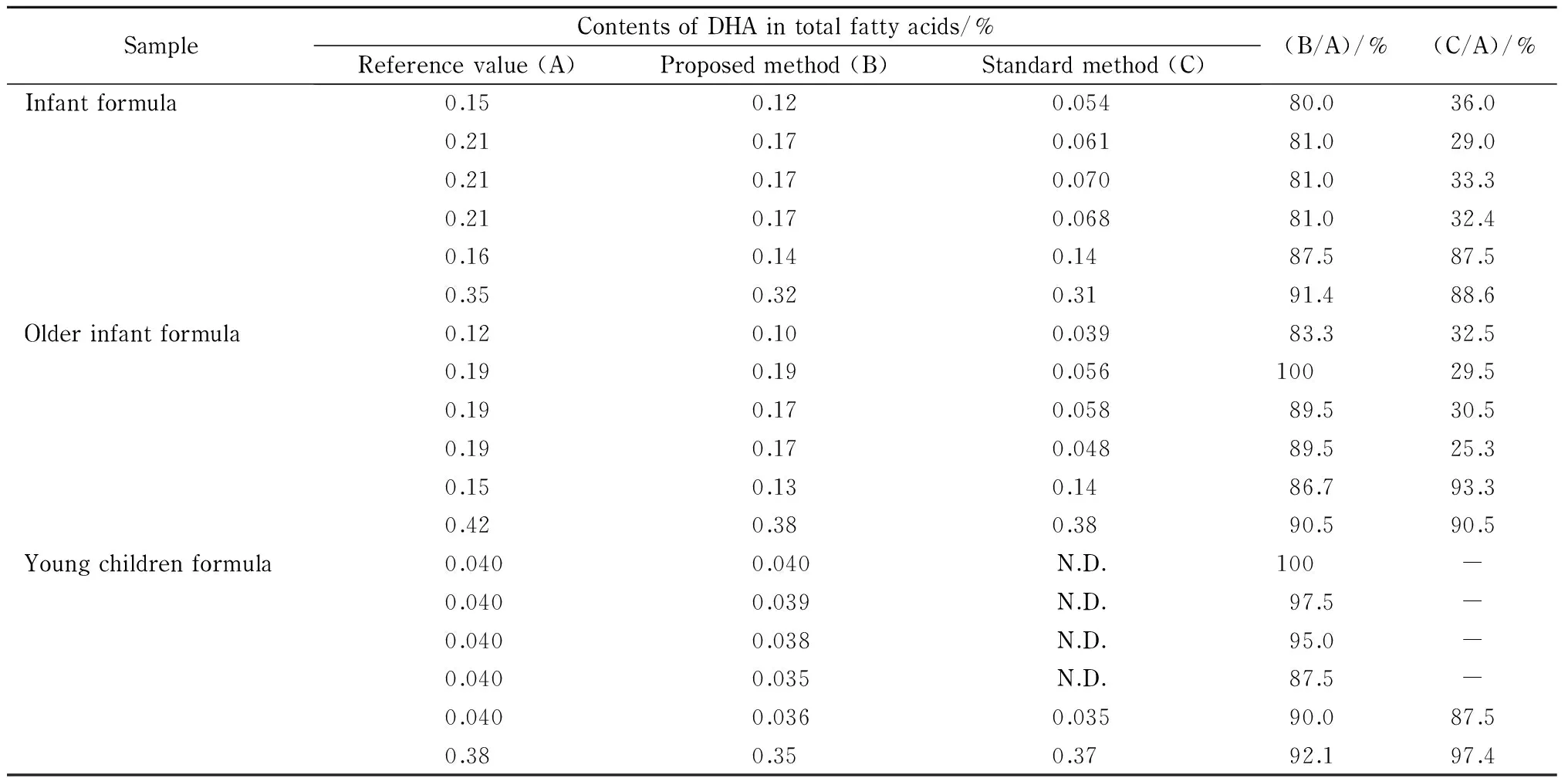
表4 奶粉中DHA的测定结果
N.D.: not detected; -: blank.
3 结论
本文建立的酸水解-气相色谱测定奶粉中二十二碳六烯酸含量的方法国内外未见相关报道,用酸水解代替碱水解提取脂肪,一方面能破解包埋材料,另一方面模拟人体胃液环境,更为科学实用。对于各类实际奶粉样品中DHA含量的测定结果表明本方法明显优于国标方法。另外,方法中用到的无水硫酸氢钠不能用其他试剂(如无水硫酸钠)替代,具体原理有待进一步研究。
[1] Willatts P, Forsyth J S, DiModugno M K, et al. Lancet, 1998, 352(9129): 688
[2] Uauy R, Hoffman D R, Peirano P, et al. Lipids, 2001, 36(9): 885
[3] Ding H P, Li Y H, Ding Q, et al. Chinese Journal of Clinical Nutrition (丁慧萍, 李艳红, 丁倩, 等. 中华临床营养杂志), 2011, 19(2): 129
[4] Wang Y N, Hou D Y, Xin G, et al. Journal of Anshan Normal University (王月囡, 侯冬岩, 辛广, 等. 鞍山师范学院学报), 2012, 14(4): 50
[5] He L Y, Zhang X M. Laboratory Medicine and Clinic (何俐莹, 张孝明. 检验医学与临床), 2014, 11(5): 666
[6] Zhu L N, Zhang Z G, Zhang M, et a1. China Dairy Industry (朱丽娜, 张志国, 张敏, 等. 中国乳品工业), 2009, 37(2): 45
[7] Bailey-Hall E, Nelson E B, Ryan A S. Lipids, 2008, 43(2): 181
[8] Kangani C O, Kelley D E, DeLany J P. J Chromatogr B, 2008, 873(1): 95
[9] Bowen C L, Kehler J, Evans C A. J Chromatogr B, 2010, 878(30): 3125
[10] Wang J, Wang D, Zhang H, et al. Chinese Journal of Chromatography (王静, 王丹, 张华, 等. 色谱), 2013, 31(8): 734
[11] GB/T 5009.168-2003
[12] Ma W H, Zhang Y, Xue G, et al. Food Research and Development (马文宏, 张燕, 薛刚, 等. 食品研究与开发), 2007, 28(8): 142
[13] Loukas V, Dimizas C, Sinanoglou V J, et al. Chem Phys Lipids, 2010, 163(3): 292
[14] Petrovic M, Kezic N, Bolanca V. Food Chem, 2010, 122(1): 285
[15] GB 5413.27-2010
[16] Tang S, Qin C, Wang H, et al. J Supercrit Fluid, 2011, 57(1): 44
[17] Lin Y Z, Chen S Y. Food Research and Development (林玉宙, 陈士勇. 食品研究与开发), 2012, 33(2): l43
[18] Peng H W, Zhang B, Yang X C, et a1. China Pharmacy (彭宏伟, 张博, 杨小川, 等. 中国药房), 2010 (13): 1228
[19] Decree of 8 September 1977 on the Official Methods of Analysis of Dietary and Diet Products. [2015-05-10]. http://www.legifrance.gouv.fr/affichTexte.do?cidTexte=JORFTEXT000000666765
[20] GB/T 5009.6-2003
[21] ES ISO 12966-2: 2012, Animal and Vegetable Fats and Oils—Gas Chromatography of Fatty Acid Methyl Esters—Part 2: Preparation of Methyl Esters of Fatty Acids. Ethiopian Standard

《色谱》论文中可直接使用的缩略词
《色谱》多位编委获得2015年中国分析测试协会科学技术奖
《色谱》副主编江桂斌,责任副主编刘虎威,编委汪海林、林金明、梁鑫淼、李彤获得2015年“中国分析测试协会科学技术奖”。该奖简称“CAIA奖”,经国家科学技术奖励工作办公室批准,由中国分析测试协会设立,旨在奖励分析测试领域新方法、新技术、新应用研究中取得优秀成果的科技工作者和组织,促进我国分析测试技术水平的不断提高。根据《中国分析测试协会科学技术奖(CAIA奖)评奖细则》,特等奖奖励具有国际领先水平或特大社会经济效益的重大成果;一等奖奖励具有国际水平或显著社会经济效益的成果;二等奖奖励具有国内领先水平或具有较好社会经济效益的成果;三等奖奖励具有国内先进水平或应用中有显著效果的成果;青年奖奖励在基础研究或应用推广中具有较显著成效的成果。
本届评奖范围针对于2013年1月1日到2015年7月间取得的、在分析测试新技术、新方法和新应用方面的创新性成果。本届共收到申请项目73项,内容涉及面广泛,有农产品与食品安全、生命科学与医学、能源与环境、仪器新技术及其应用等多个重点学科和热点领域。按照《中国分析测试协会科学技术奖(CAIA奖)评奖细则》,中国分析测试协会聘请有关方面的专家、学者组成评审委员会,从创新程度、科学价值、主要论文发表刊物或著作的影响力、应用推广程度、已获经济或社会效益等五方面对申报项目进行评审。经过形式审查、函评、初评和终评,完成了2015年“中国分析测试协会科学技术奖(CAIA奖)”评审工作,共评出特等奖2项,一等奖8项,二等奖12项,三等奖12项,青年奖6项。
Determination of docosahexaenoic acid in milk powder by gas chromatography using acid hydrolysis
SHAO Shiping*, XIANG Dapeng, LI Shuang, XI Xinglin, CHEN Wenrui
(InspectionandQuarantineTechnologyCentre,GuangdongEntry-ExitInspectionandQuarantineBureau,Guangzhou510623,China)
A method to determine docosahexenoic acid (DHA) in milk powder by gas chromatography was established. The milk powder samples were hydrolyzed with hydrochloric acid, extracted to get total fatty acids by Soxhlet extractor, then esterified with potassium hydroxide methanol solution to form methyl esters, and treated with sodium hydrogen sulfate. The optimal experiment conditions were obtained from orthogonal experiment L9(33) which performed with three factors and three levels, and it requires the reaction performed with 1 mol/L potassium hydroxide solution at 25 ℃ for 5 min. The derivative treated with sodium hydrogen sulfate was separated on a column of SP-2560 (100 m×0.25mm×0.20 μm), and determined in 55 min by temperature programming-gas chromatography. Good linearity was obtained in the range 5.0-300 mg/L with the correlation coefficient of 0.999 9. The relative standard deviations (RSDs) were 3.4%, 1.2% and 1.1% for the seven repeated experiments of 10, 50 and 100 mg/L of DHA, respectively. The limit of detection was 2 mg/kg, and the recoveries of DHA were in the range of 90.4%-93.5%. The results are satisfactory through the tests of practical samples.
gas chromatography (GC); docosahexenoic acid (DHA); milk powder; acid hydrolysis
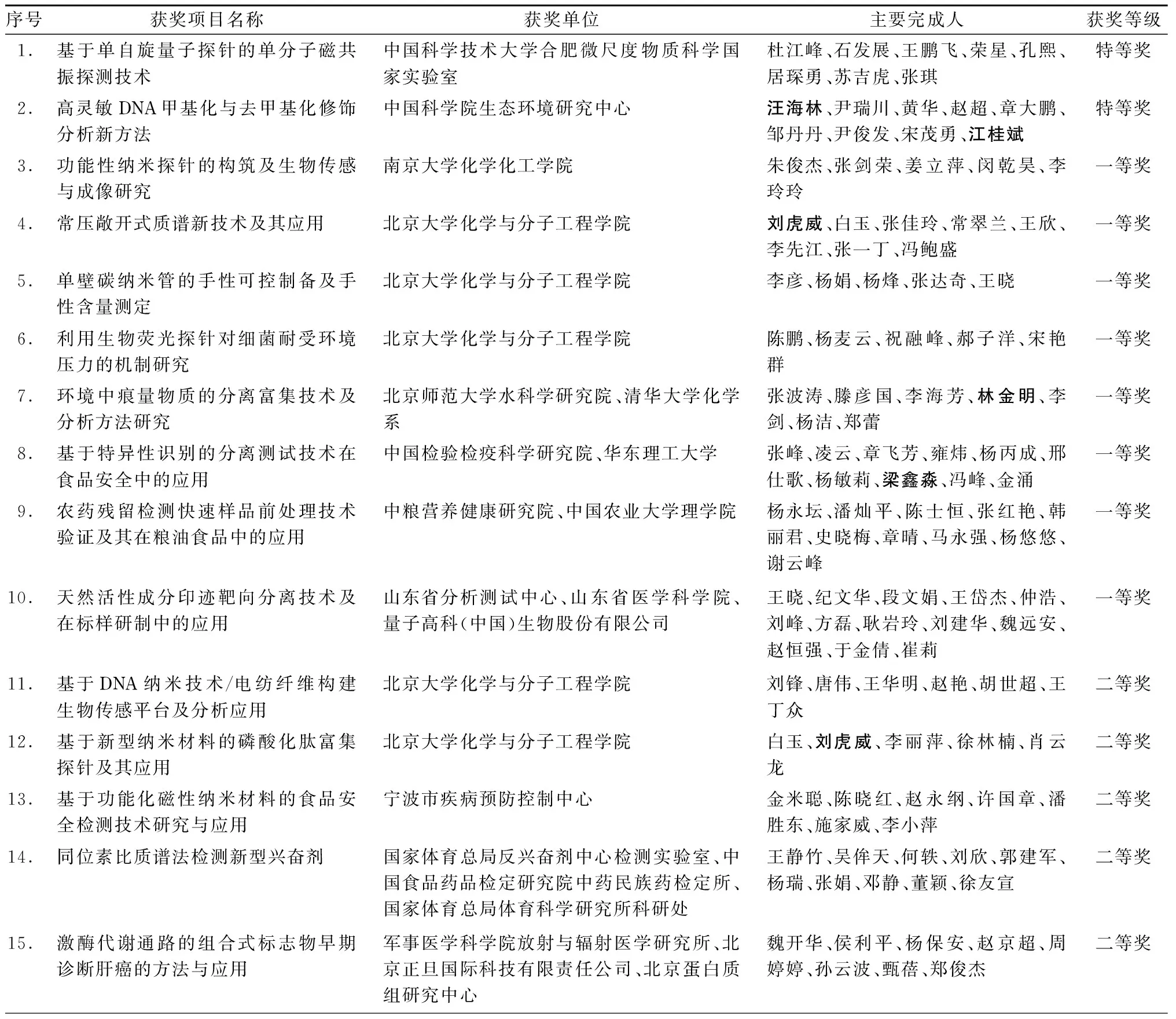
2015年中国分析测试协会科学技术奖获奖者名单

续
10.3724/SP.J.1123.2015.06022
广东省广州市科技计划项目(12S496140081).
2015-06-17
O658
:A
:1000-8713(2015)11-1214-05
*通讯联系人.Tel:(020)38290331,E-mail:shipingshao@163.com.