磁共振灌注成像对脑胶质瘤放疗后复发与放射损伤的价值*
内蒙古医科大学附属医院MRI室(内蒙古 呼和浩特 010050)
张 颖 牛广明 韩晓东 郭冬玲 苗燕平 白雪菲 吴 琼 吴 慧 高 阳
神经胶质瘤是颅内最常见的原发肿瘤,因其浸润性的生长方式导致肿瘤切除后复发的概率相当高,因此目前的治疗方式一般为手术切除结合放化疗,包括全脑放疗或伽马刀治疗[1]。这种方案虽然在一定程度上减少了肿瘤的复发,却不可避免地出现了放射治疗所引起的脑坏死。而复发的胶质瘤及放射性脑改变在磁共振上存在一定的相似性:常规扫描均表现为高信号,周边有水肿带,增强扫描可明显强化,有占位效应等。因此导致神经外科医师很难判断患者应该再次手术还是继续放疗,造成病情延误或过度医疗。
磁共振灌注成像(Perfusion Weighted Imaging, PWI)能通过组织反映微血管的分布,测得对比剂通过毛细血管网时周围组织在局部磁场内的短暂变化,通过磁共振信号的改变来显示,提供血液动力学方面的信息[2,3]。本研究旨在通过磁共振灌注成像技术鉴别经过手术的脑胶质瘤患者放疗后复发与放射性损伤。
1 资料与方法
1.1 资料.1 收集我院自2012年8月~2013年12月经手术病理证实为脑胶质瘤并进行放射治疗28~30天的患者60例,其中的46例符合入组要求,男性32例,女性14例,年龄23~72岁,平均46±10.5岁,每位患者分别在放疗放疗后每隔三个月行磁共振常规和灌注成像检查。
1.2 检查方法 使用美国GE公司3.0T Signa HDx超导型MR扫描仪(GE-Signa HDx,Milwaukee,US.),8NV-Head线圈,以头部线圈作为发射和接受线圈。所有患者在扫描前进行心理疏导,减少患者的恐惧心理;摘掉假牙及身上所有的金属物品,必要时更换衣服。扫描时先进
行磁共振常规头颅扫描,然后进行灌注及增强扫描。

表1 胶质瘤复发与放射性脑损伤
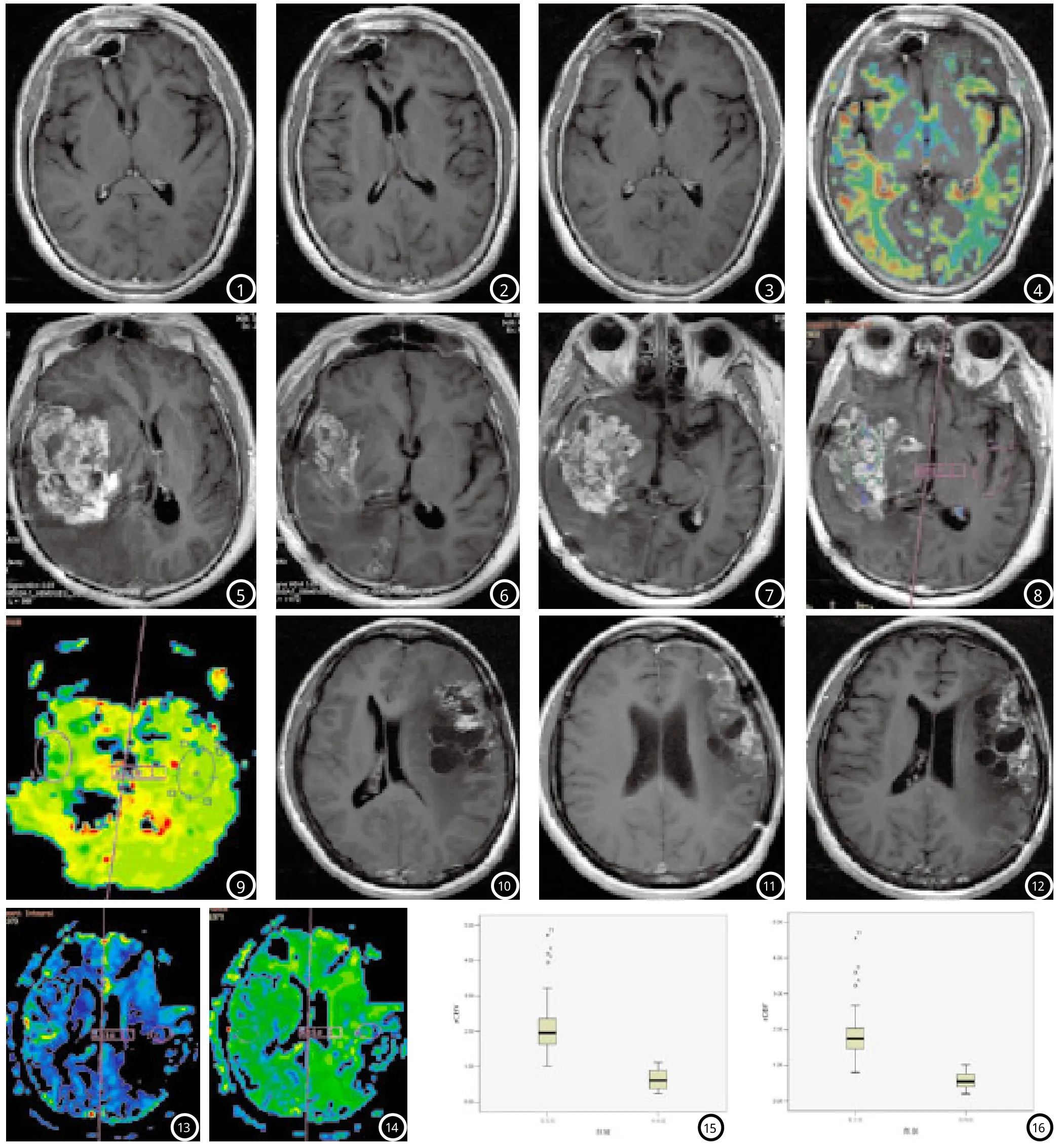
图1-4 患者,女,52岁,术后病理证实为胶质瘤Ⅱ级,常规放疗后进行复查。图1-3 为放疗后一个月、三个月、六个月轴位T1WI增强图像,未见异常强化病灶;图4 为放疗后六个月灌注图像,未见异常高灌注区。图5-95-9 患者,男,43岁,术后病理证实为胶质瘤Ⅳ级,常规放疗后进行复查。图5-6 为放疗后一个月、三个月复查图像显示右侧室旁异常强化区(为术后残留)范围缩小;图7 示放疗后六个月轴位T1WI增强图像,可见右侧基底节区异常强化病灶,病变范围向下累积;图8-9 为放疗后九个月灌注图像,并可见右侧基底节区异常高灌注区,二次手术证实复发。图10-14 患者,女,34岁,术后病理证实为胶质瘤Ⅲ级,常规放疗后进行复查。图10-11 为放疗后一个月、三个月轴位T1WI增强图像,可见左侧额顶叶条状强化,三个月后占位效应减轻,考虑放射性脑损伤,建议隔期复查;图12 为放疗后十二个月复查图像;图13-14 为放疗后十二个月灌注图像,左侧额顶叶病变区呈可见低灌注状态。图15-1615-16 盒图(boxplot)示数据离散程度和偏向。
1.3 数据采集 相关扫描序列及参数如下:
1.3.1 常规检查序列包括轴位T2加权成像(T2WI)、T1加权成像(T1WI)、弥散加权成像(DWI)和矢状位T1WI,以平行前后联合的水平进行全脑轴位扫描,平行中线的水平进行全脑矢状位扫描。
1.3.1.1 T2WI扫描参数:TR/TE=6280/104ms,层厚:5mm,间隔:l.5mm,NEX:1,FOV:24×24cm,Matrix:320×320,扫描层数为19层,扫描时间为82秒。
1.3.1.2 T1WI扫描参数:TR/TE=2825/24ms,层厚:5mm,间隔:l.5mm,NEX:1,FOV:24×18cm,Matrix:320×320,扫描层数为19层,扫描时间为99秒。
1.3.1.3 DWI扫描参数:TR/TE=4450/72.9ms,层厚:5mm,间隔:1.5mm,NEX:2,FOV:24×24cm,Matrix:128×l28,b=1000s/mm,扫描层数为19层,扫描时间为40秒。
1.3.1.4 矢状位T1WI扫描参数:TR/TE=2825/24ms,层厚:5mm,间隔:1.5mm,NEX:1,FOV:24×24cm,Matrix:420×224,扫描层数为19层,扫描时间为75秒。
1.3.2 PWI序列扫描,采用梯度回波-平面回波成像(GREEPI)脉冲序列行动态增强扫描。参数:TR/TE=1600/40ms,层厚:5mm,间隔:1.5mm,FOV:24×24cm,Matrix:128×128,从下向上采集,扫描范围包括全脑,采集层数为19层,时间为80秒。扫描时先出两组图像然后打药,用高压注射器通过留置静脉针以团注的方法给药,造影剂使用北京北陆药业集团生产的磁显葡胺(GD-DTPA),用量0.2ml/kg,速度4ml/s,造影剂注射完毕,再用等量的生理盐水冲洗导管。灌注扫描后,进行T1WI轴矢冠三个位置的增强扫描。
1.4 数据处理 本研究所有的磁共振原始数据均在G E Advantage 4.4工作站进行后处理,采用去卷积灌注软件进行分析。首先构建每一扫描层面的伪彩色图像,即相对脑血容量(relative cerebral blood volume,rCBV)图、相对脑血流量(relative cerebral blood flow,rCBF)和相对平均通过时间(relative mean transit time,rMTT)参考图,然后在rCBV图和rCBF图显示病灶范围最大的层面上人工勾画感兴趣区(ROI),测量病灶最大rCBV值、最大rCBF值,再测量健侧相应部位脑白质及脑皮质rCBV值、rCBF值,计算病灶及健侧灰质最大rCBV值、最大rCBF值的比值。为尽量减少人为因素影响,测量3次取平均值。
1.5 统计学处理 研究数据采用SPSS13.0统计软件处理。因数据为非正态分布,对胶质瘤复发和放射性脑损伤不同区域的rCBV值、rCBF值、rMTT值分别进行秩和检验,p<0.05为差异有统计学意义。
2 结 果
60例经手术切除后,病理确诊为胶质瘤的患者,放疗28天,随访半年以上(图1-4)。后临床证实30例为术后复发(10例经2次手术病理证实,15例在随访过程中病灶强化范围扩大,占位效应加重;5例经过一段时间病人死亡)(图5-9),10例为放射性脑损伤(图10-14)。
通过PWI检查,胶质瘤复发组rCBV、rCBF明显高于放射性脑损伤组,与临床结果接近(p<0.05,有统计学意义),见表1。
3 讨 论
3.1 磁共振灌注成像技术(PWI) PWI) PWI是反映组织的微血管分布和血流灌注情况的磁共振检查技术,可提供血液动力学方面的信息。应用高压注射器经静脉团注对比剂GD-DTPA后,以足够高的快速MR成像序列对目标器官进行连续多层面多次扫描,检测组织信号强度随时间的变化来反应组织的血流动力学。对比剂首次通过受检组织时,顺磁性对比剂进入毛细血管床引起周围组织内磁场的短暂变化,进而使邻近氢质子共振频率改变,导致质子失相位,T2值缩短,T2信号强度降低,后者反应组织中对比剂的浓度变化,即代表血流动力学变化[4,5]。另外,对比剂首过期间主要存在于血管内,血管外较少,血管内外浓度梯度最大,信号的变化受扩散因素影响很小,故能反映组织血液的灌注情况。根据对比剂首过局部脑组织所引起的信号强度变化与时间的关系,绘制出信号强度-时间曲线,从而获得部分血液动力学参数的相对值,通过工作站可绘制各种血液动力学指标图像(如:rCBV、rCBF和rMTT),无创地评价脑灌注情况[6]。
3.2 脑胶质瘤复发与放射性损伤的的磁共振表现 脑胶质瘤治疗后,影像学检查最关键的是鉴别肿瘤复发或放疗后损伤。复发的肿瘤多见于原发肿瘤区或附近;放射性损伤多分布于病变侧脑白质区,与照射范围基本一致。在MRI上二者均表现为片状、斑片状异常信号,增强后部分病例有环形或部分环形强化以及不均匀强化,周边不规则地图样强化。这些改变无特异性, 临床上对二者误诊的病例报道也很多见[7-9]。
常规MR增强扫描主要反映血脑屏障的破坏程度,例如低灌注的放射性脑坏死、手术后残腔、脑脓肿等强化较明显,而某些高灌注的脑肿瘤强化并不明显[10,11],因为血脑屏障的破坏可由肿瘤生长破坏正常的毛细血管或新生异常血管的血管壁病理重建引起,可伴有或不伴有血管增生[12]。因此,常规的磁共振检查技术在鉴别放射性脑损伤与胶质瘤复发中具有一定的局限性[13]。
3.3 PWI对脑胶质瘤术后复发与放射性损伤的鉴别诊断价值肿瘤细胞的生长与更新导致其新陈代谢需求增加,使肿瘤局部处于低血糖和缺氧状态,会刺激机体产生血管生长的活性物质,导致肿瘤内部新血管生成。恶性肿瘤具有较丰富的新生血管,不仅为肿瘤生长提供营养,而且新生血管本身就是肿瘤向周围及远处扩散的重要通道,其丰富程度是判断肿瘤组织分级、良恶性程度及肿瘤放、化疗或术后复发与否的重要指标[14,15]。
本研究中30例经放疗后肿瘤复发患者,病灶最大rCBV值、rCBF值较健侧皮质明显升高,rCBV图、rCBF图清楚显示病灶新生血管的不均匀性。通过与手术或穿刺病理结果比较,笔者认为rCBV图、rCBF图所示数值最大的区域是肿瘤生长最活跃、恶性程度最高的部位。另外,12例放射性脑坏死患者的病灶最大rCBV值、rCBF值较健侧皮质明显减低,是由于放疗导致内皮细胞和小血管的损伤,使局部组织缺血坏死,其血管分布程度减低,血流呈低灌注状态[16]。
3.4 PWI在脑胶质瘤放疗后研究中的优势与不足 除了PWI,磁共振波谱(MRS)对脑肿瘤放疗后复发和放射性脑坏死的鉴别也有重要价值[17-19]。但MRS存在检查时间较长、不能准确反映病变的空间分布等缺点[20]。PWI可以更好地显示病灶的空间分布,明确表明病灶的实质区、坏死区、边缘及水肿区;且检查时间较短,对于难以耐受较长时间检查的患者,更易接受。
很多参数影响PWI的测量结果,如:样本数的大小,对比剂注射流率、剂量,后处理中参数计算方法等,影响各研究结果间的可比性[21],因此需要制定一种标准化的PWI方案。
4 小 结
放射性脑坏死灶内缺乏新生血管,测量局部脑血流量图可以见到坏死灶的rCBV明显降低,由此可以精确的与肿瘤复发相鉴别。PWI以其较高的时间和空间分辨率,从微血管形成的数量和程度研究病变灌注情况,弥补了病理检查的有创性及检查结果依赖于组织取材准确性等缺点,可以了解肿瘤及其周边血供情况,避免了血-脑屏障破坏的影响,较好地无创性鉴别放射性坏死和肿瘤复发,也有助于下一步治疗方案的制定。
1.Beaucbesne PD,Taillandier L.Concurrent radiotherapy:fotemustine combination for newly diagnosed malignant glioma patients,a phase Ⅱstudy Cancer Chemothempy and Pharmacology,2009;64(11):74-76.
2.Kleihues P, Louis DN, Scheithauer BW, et al.The WHO classification of tumors of the nervous system[J].J Neuropathol Exp Neurol, 2002; 61(3):215-225.
3.Marquet G, Dameron O, Saikali S, et al.Grading glioma tumors using OWL-DL and NCI Thesaurus[J].AMIA Annu Symp Proc, 2007;11:508-512.
4.Rousseau A, Mokhtari K, Duyckaerts C.The 2007 WHO classification of tumors of the central nervous system----what has changed? [J].Curr Opin Neurol,2008; 21(6):720-7.
5.何景扬,林瑞蔼.恶性胶质瘤手术后放疗的临床疗效及预后影响因素[M].中外医学研究,2012;10(21):26.
6.吴开福,徐培坤,吴运等.6例胶质瘤术后放射性脑病误诊为胶质瘤复发的临床分析[M].中国微创外科杂志.2012;12(2):138.
7.Barbara Bobek-Billewicz, Gabriela Stasik-Pres, Henryk Majchrzak,?ukasz Zarudzki.Folia Neuropathologica 2010; 48 (2):82.
8.陈大朝,陈龙华,金吴东等.放射性脑损伤的MRI诊断[J].中国现代医学杂志,2006, 16(18): 2815-2818.
9.石岩,张玉强,黄爱军等.放射性脑损害误诊为胶质瘤复发1例[M].中国临床神经外科杂志,2010,15(2):128.
10.Law M, Young RJ, Babb JS, et al.Gliomas: predicting time to progression or survival with cerebral blood volume measurements at dynamic susceptibility- weighted contrast-enhanced perfusion MR imaging.Radiology, 2008; 247(2):490-498.
11.Emblem KE, Scheie D, Due-Tonnessen P, et al.Histogram analysis of MR imaging-derived cerebral blood volume maps:combined glioma grading and identifi cation of low-grade oligodendroglial subtypes[J].AJNR Am J Neuroradiol, 2008;29(9): 1664-1670.
12.Hoefnagels FWA, Lagerwaard FJ,Sanchez E, et al.Radiological progression of cerebral metastases after radiosurgery: assessment of perfusion MRI for differentiating between necrosis and recurrence[J].J Neurol, 2009; 256(6):878-887.
13.Barajas RF, Chang JS, Sneed PK,et al.Distinguishing recurrent intra-axial metastatiCTumor from radiation necrosis following gamma knife radiosurgery using dynamic susceptibilityweighted contrast-enhanced perfusion MR imaging[J].AJNR Am J Neuroradiol.2009; 30(2): 367-372.
14.Danchaivijitr N, Waldman AD,Tozer DJ, et al.Low-Grade Gliomas: Do Changes in rCBV Measurements at Longitudinal Perfusionweighted MR Imaging Predict Malignant Transformation? [J].Radiology, 2008; 247(1): 170-178.
15.Alessandro Stecco ,Carla Pisani,et al.DTI and PWI analysis of peri-enhancing tumoral brain tissue in patients treated for glioblastoma[J].J Neurooncol.2011; 102(2): 261-271.
16.Shah R, Vattoth S,Jacob R,et al.Radiation Necrosis in the Brain: Imaging Features and Differentiation from Tumor Recurrence radiographics[J].Radiographics,2012; 32(5):1343-1359.
17.Bisdas S, Kirkpatrick M,Giqlio P,et al.Cerebral Blood Volume Measurements by Perfusion-Weighted MR Imaging in Gliomas:Ready for Prime Time in Predicting Short-Term Outcome and Recurrent Disease? [J].AJNR Am J Neuroradiol, 2009; 30(4):681-688.
18.徐俊玲,陈传亮,连建敏等.磁共振灌注加权成像鉴别脑胶质瘤术后放疗后复发的价值[M].中华放射肿瘤学杂志,2012;21(4):306-309.
19.王玉林, 有慧, 张爱莲等.MR灌注成像在鉴别胶质瘤复发与放射性脑损伤中的价值[J].中华放射学杂志,2011; 45(7): 618.
20.Stupp R, Roila F.Malignant glioma: ESMO clinical recommendations for diagnosis, treatment and follow-up[J].Ann Oncol,2008; 19 Suppl 2: ii83-85.
21.Mitsuya K, Nakasu Y,Horiguchi S,et al.Perfusion weighted magnetic resonance imaging to distinguish the recurrence of metastatic brain tumors from radiation necrosis after stereotactic radiosurgery[J].J Neurooncol, 2010; 99(1): 81-88.

