液相色谱-串联质谱法测定水环境中的十氯酮
周 丽, 董 亮, 史双昕, 张利飞, 张秀蓝, 杨文龙, 李玲玲, 黄业茹
(国家环境分析测试中心,北京100029)
十氯酮(kepone,chlordecone)又名开蓬,是一种人工合成的有机氯杀虫剂,具有持久性有机污染物(POPs)的特性,目前已被列入《关于持久性有机污染物的斯德哥尔摩公约》禁用名单[1]。目前关于十氯酮的研究地区主要集中在美国弗吉尼亚州Hopewell市和法国法属西印度群岛(French West Indies)[2,3]。因此十氯酮在环境介质中的数据还很缺乏,亟待补充。尽管目前没有关于生产和使用十氯酮的报告,但不能排除有些国家仍在生产十氯酮或将其用作农业杀虫剂。十氯酮在国内的生产、使用状况未见详细报道。由于十氯酮是灭蚁灵的降解产物,且工业级的灭蚁灵中含有十氯酮[1,3],而我国到2009年5月为止尚未停止生产和使用灭蚁灵,尤其在江苏地区,因此可能存在十氯酮的污染[4]。国内对十氯酮的相关研究较少,仅有几篇相关的文献。为了更好地履行公约,我国需加快开展对十氯酮的研究,调查十氯酮在我国的生产和使用情况及其在各种环境介质中的污染现状,从而准确评估我国的污染状况,以保护环境和人类的健康。
与其他有机氯农药不同,由于羰基的存在,十氯酮在水溶液中容易形成水合物,生成偕二醇。Harless等[5]同时采用核磁共振(NMR)、红外光谱(IR)和质谱(MS)证实了其在甲醇中以半缩醛的形式存在。目前十氯酮的分析测定多采用气相色谱-电子捕获检测器(GC-ECD)和气相色谱-质谱(GCMS)[6-8]的方法,但亦有使用气相色谱-串联质谱(GC-MS/MS)[9,10]、高 效 液 相 色 谱-串 联 质 谱(HPLC-MS/MS)和近红外反射光谱法[9](NIRS,near infrared reflectance spectroscopy)进行分析检测的报道。国内孙翠香等[11]和王艳洁等[12,13]分别采用GC-MS和GC-ECD 的方法测定十氯酮。相比其他检测方法,HPLC-MS/MS具有定性定量准确、适用于极性化合物的测定等特点,目前尚未检索到国内采用HPLC-MS/MS测定十氯酮的相关报道。鉴于十氯酮是极性化合物及其在有机溶剂中的存在形式,本文建立了使用HPLC-MS/MS测定水环境中十氯酮的分析方法,并考察了净化方式。
1 实验部分
1.1 仪器和试剂
Agilent 7890-5975C 气相色谱-质谱联用仪,HPLC1200 液相色谱仪-6410A 串联质谱仪(美国Agilent公司);旋转蒸发浓缩仪(Buchi公司,瑞士) 十氯酮是纯度为99.9%的固体,购于美国AccuStandard公司,内标13C10-kepone的标准溶液购于美国Cambridge Isotope Laboratories(CIL)公司,丙酮、正己烷、二氯甲烷(农残级,美国J T Baker公司);甲醇、乙腈(HPLC 级,美国Honeywell公司)。
1.2 标准溶液的配制
称取1 mg十氯酮,用丙酮溶解、定容至10 mL,配制成100 mg/L十氯酮标准储备液。准确量取50 μL上述标准储备液,用丙酮稀释定容至5 mL,配制成1 mg/L十氯酮标准使用液,用此溶液配制工作溶液,作定量校正曲线。准确量取50μL 100 mg/L13C10-kepone,用丙酮稀释定容至5 mL,配制成1 mg/L13C10-kepone内标使用液。
1.3 样品前处理
摇匀水样,量取1 000 mL水样(萃取所用水样体积根据水质情况可适当增减),倒入2 000 mL的分液漏斗中,加入50μL1 mg/L13C10-kepone和30 mL二氯甲烷,振摇10 min,静置分层,收集有机相,重复萃取3 遍,合并有机相,旋转蒸发浓缩至约5 mL时加入15 mL 正己烷继续浓缩,提取后进行净化。
将浓缩液定容至6 mL左右,加入2 mL乙腈进行液液分配,提取乙腈相,然后氮吹浓缩,用乙腈定容,上机测定。如果是饮用水和地下水的萃取液可不经过净化。
1.4 液相色谱-质谱条件
色 谱 柱:Eclipse plus C18 柱(100 mm×2.1 mm,3.5μm);流速:0.3 mL/min;柱温:30 ℃;进样量:10μL;流动相:A 为水相,B 为乙腈;梯度洗脱条件:0~1.0 min,50%B;1.0~3.0 min,50%B~100%B;3.0~6.0 min,100%B;6.0~8.0 min,100%B~50%B;8.0~9.0 min,50%B。电喷雾负离子模式(ESI-);毛细管电压4 000 V;雾化器压力241 kPa(35 psi);干燥器流速10 L/min;干燥器温度350 ℃。十氯酮的监测离子对质谱条件见表1。

表1 十氯酮监测离子对质谱条件Table 1 MRM transitions and MS operating parameters selected for the analysis of kepone
2 结果与讨论
2.1 分析仪器的选择
本研究分别使用了气相色谱-质谱和液相色谱-串联质谱分析了十氯酮。气相色谱-质谱采用Agilent 7890-5975C 气相色谱-质谱联用仪,色谱柱为DB-5MS(30 m×0.25 mm×0.25μm,J&W)。程序升温为60 ℃保持1 min,以50 ℃/min 升温至180℃保持1 min,以5℃/min升温至240℃保持2 min,以30 ℃/min升温至300 ℃保持5 min。不分流进样,进样量为2μL;载气流速为1.55 mL/min;进样口温度为260℃;接口温度为280℃;质谱的电离方式为电子轰击源(EI),采集方式为选择离子(SIM)模式。经研究发现十氯酮采用气相色谱-质谱分析有以下缺点(见图1):容易拖尾,本实验使用了不同品牌的DB-5MS及1701色谱柱均会产生拖尾现象;容易降解,在分析样品一段时间后,发现十氯酮降解,进样系统需保持清洁(比如衬管和色谱柱)。所以十氯酮不适用气相色谱或气相色谱-质谱分析,因此本研究采用液相色谱-串联质谱法进行分析。
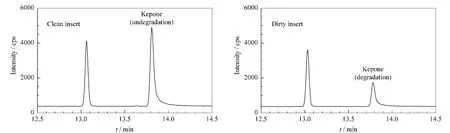
图1 100μg/L十氯酮标准溶液的SIM 图Fig.1 Total ion chromatograms of 100μg/L kepone standard solution by GC-MS
2.2 十氯酮在溶剂中的存在形式
十氯酮在甲醇和丙酮/乙腈两种溶剂中的存在形式不一样。通过全扫描模式(MS2Scan)分析,在甲醇溶剂的标准溶液中得到十氯酮的母离子质荷比(m/z)是520.8,而丙酮/乙腈溶剂中得到的母离子m/z 为506.7。这充分说明十氯酮在甲醇中以半缩醛的形式存在,而在丙酮/乙腈中以偕二醇的形式存在。在甲醇中得到母离子m/z 为520.8,而十氯酮的相对分子质量是489.6,如果以半缩醛的形式存在则是在其结构式上连接一个-CH3OH,当采用ESI-模式电离时,则变成[M+CH3OH-H]-,因此从520.8→489.6丢失的质荷比为31.2,这一过程证实了十氯酮在甲醇中以半缩醛的形式存在(见图2)。在丙酮/乙腈溶剂中得到母离子m/z 为506.7,如果以偕二醇的形式存在并采用ESI-模式时,则是[M+H2O-H]-,从506.7→489.6丢失的质荷比为17,这一过程说明了十氯酮偕二醇的存在形式。此结论证实了Harless等[5]关于十氯酮在有机溶剂中以不同形式存在的报道。考虑到前处理的方式,本实验采用丙酮溶剂的十氯酮标准溶液。
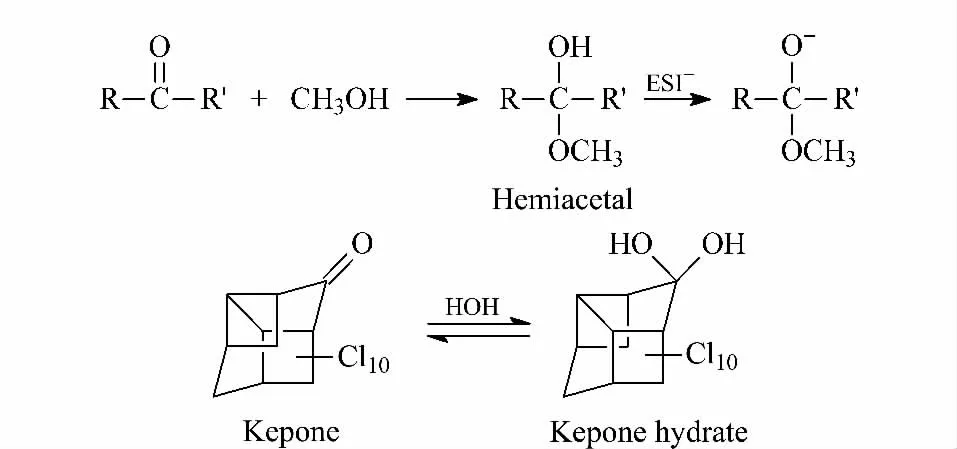
图2 十氯酮在甲醇(上)和丙酮/乙腈(下)中的存在形式Fig.2 Existing forms of kepone in methanol(up)and acetone/acetonitrile(down)
2.3 流动相的选择
由于十氯酮在不同溶剂中的存在形式不一样,因此实验中考察了乙腈/水和甲醇/水两种流动相对十氯酮的影响。对丙酮溶剂的十氯酮标准溶液进行全扫描模式分析,结果表明,在甲醇/水中出现两个化合物,而在乙腈/水中出现一个化合物(见图3),再一次证实了十氯酮在甲醇和丙酮/乙腈中的存在形式不同。因此本实验采用乙腈/水流动相。
2.4 净化条件的选择
2.4.1 柱色谱净化和酸净化
实验中参考Moseman等[7]研究的方法,填充了6 g的硅胶柱,结果表明需要200 mL含2%(v/v)甲醇和10%(v/v)甲苯的正己烷才能完全洗脱十氯酮,说明十氯酮在净化柱上有很强的保留,采用一般的淋洗液很难洗脱,Saleh 等[6]也报道了十氯酮在Florisil柱上保留性强的特点。这种净化方式使用的洗脱溶剂量大,极性强,因此净化效果一般。本实验也尝试了使用硫酸进行净化,结果显示十氯酮不耐受硫酸。
2.4.2 液液分配净化
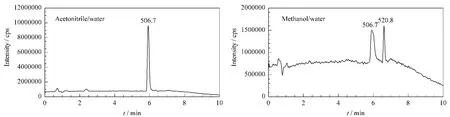
图3 不同流动相体系下1 mg/L十氯酮标准溶液的总离子流图Fig.3 Total ion chromatograms of kepone standard solution(1 mg/L)by HPLC-MS/MS in different mobile phase systems
在200 mL农夫山泉水样中加入50 ng十氯酮的标准溶液(丙酮溶剂),加入20 mL二氯甲烷萃取两次,合并萃取液,旋转蒸发浓缩至约5 mL时加入15 mL正己烷继续浓缩至6 mL左右,加入2 mL乙腈进行液液分配,提取乙腈相,然后氮吹浓缩,用乙腈定容,上机测定(目的是除去非极性化合物)。十氯酮的回收率为75%左右,考虑到净化时十氯酮的损失,采用同位素稀释法,即在样品萃取时加入50 μL1 mg/L13C12-kepone用来定量。
2.4.3 加NaCl对萃取效率的影响
萃取时,分别在空白水样中加入0、1%(质量分数)和3%的NaCl,然后加入40 ng十氯酮的标准溶液,按上述步骤进行液液萃取和浓缩,结果显示加入NaCl对萃取效率没有影响。
2.4.4 旋转蒸发和氮吹浓缩的影响
在50 mL左右丙酮溶液中加入40 ng十氯酮标准溶液,经旋转蒸发浓缩后进行测定。另外,在10 mL丙酮溶液中加入50 ng十氯酮标准溶液,经氮气吹扫浓缩后进行测定。其回收率分别约为107%和103%(n=3),所以旋转蒸发和氮吹浓缩对十氯酮没有影响。
2.5 质谱条件的选择
根据十氯酮的结构特征,本实验选择电喷雾离子源负离子模式(ESI-),通过对采集时间、干燥气流速、碰撞能量等参数进行调整,获得了优化后的选择监测离子参数;适当提高干燥气流速可以优化色谱峰形,对应的LC-MS/MS 的MRM 色谱图见图4。
2.6 方法检出限和线性方程
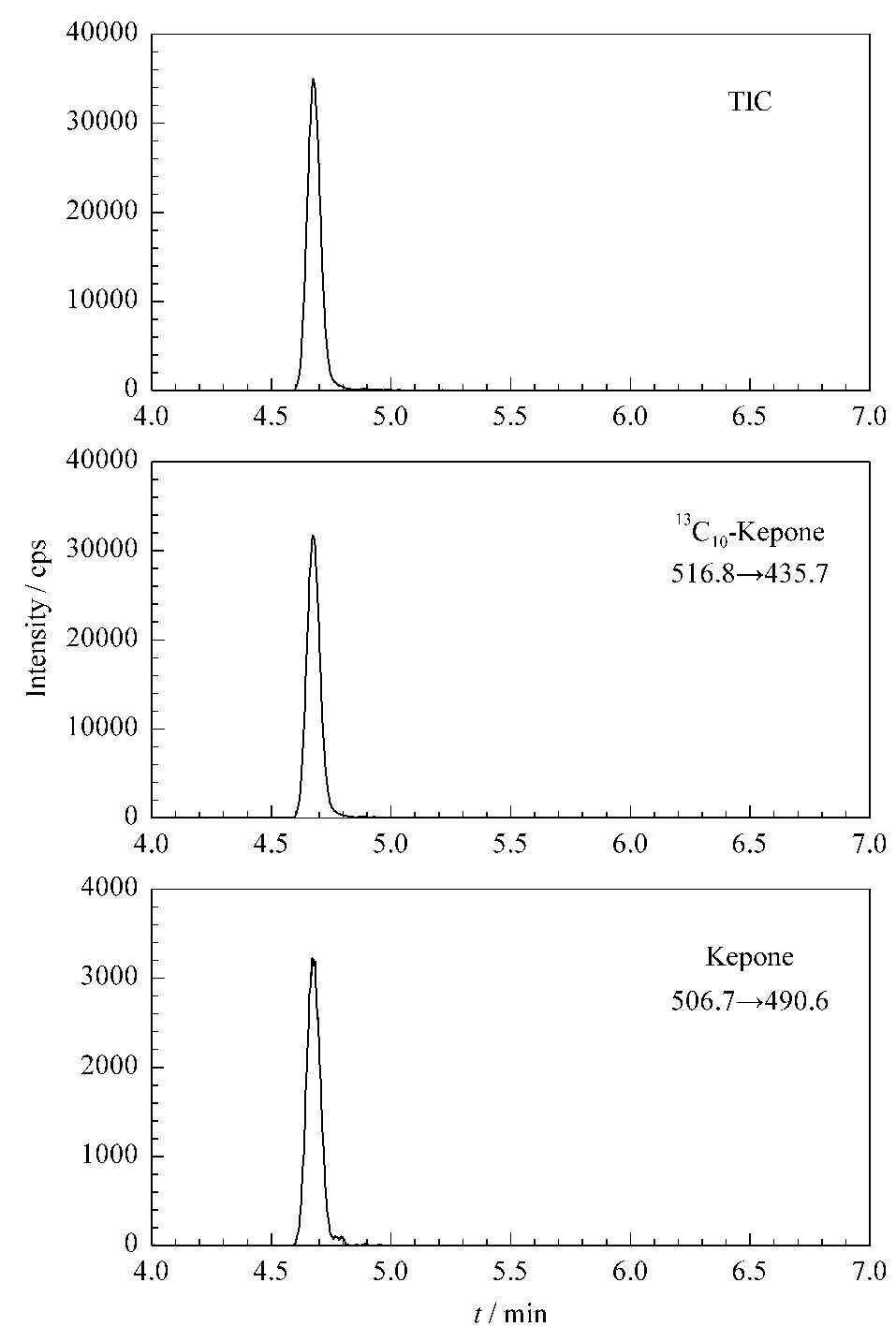
图4 十氯酮的MRM 色谱图Fig.4 MRM chromatograms of kepone
精确量取1.2节所述的标准溶液,逐级稀释,配制成不同浓度的混合标准工作溶液,进样体积为10 μL。采用同位素稀释法定量,结果表明十氯酮在5~100μg/L范围内有良好的线性关系,相关系数r2=0.999,仪器检出限为0.01 ng。方法检出限按照HJ168-2010(环境监测分析方法标准制修订技术导则)规定,采用空白样品加标的方法计算。向1 L空白水样(选用农夫山泉作为空白水样)中加入5 ng十氯酮标准溶液,平行做7个样品,对经过萃取、净化、浓缩、上机分析的全过程空白样品加标结果进行统计计算,其检出限及定量限分别为0.70 ng/L 和2.8 ng/L。
2.7 方法的回收率和精密度
为验证方法的准确度和精密度,按HJ168-2010规定,分别对5、40和100 ng/L 3 个不同浓度添加水平的样品,按全程序进行测定,每个水平分别做6次平行实验,本方法的回收率为95.1%~98.9%,精密 度(以 相 对 标 准 偏 差 计)为4.72%、3.85% 和4.45%。
2.8 实际样品分析
采集了北京市地表水和景观水共6个实际样品进行分析,每份样品取两份平行样,按照所建立的方法进行分析,结果表明在所有样品中均未检出十氯酮。
3 小结
本研究利用液相色谱-串联质谱联用技术测定环境水样品中的十氯酮,结果表明十氯酮在甲醇和丙酮/乙腈溶剂中的存在形态不同。在甲醇中十氯酮以半缩醛的形式存在,而在丙酮/乙腈中以偕二醇的形式存在。由于十氯酮极性较强,在净化时难以洗脱,且不耐酸,所以不能与其他有机氯农药一起分析。本研究所开发的液相色谱-串联质谱联用技术的仪器检出限为0.01 ng,在水环境中检出限及定量限分别为0.70 ng/L和2.8 ng/L。
[1] United Nations Enviroment Programme(UNEP),2007.Re-port of the Persistent Organic Pollutants Review Committee on the Work of Its Third Meeting. [2012-04-25].http://www.pops.int/documents/meetings/poprc/POPRC3/POPR C3_Report_e/POPRC3_Report_add10_e.pdf
[2] Zhou L,Huang Y R,Yang S,et al.Environmental Chemistry(周丽,黄业茹,杨盛,等.环境化学),2013,32(5):762
[3] Huggett R J,Bender M E.Environ Sci Technol,1980,14(8):918
[4] Wang B,Iino F,Yu G,et al.Chemosphere,2010,79:299
[5] Harless R L,Harris D E,Sovocool G W,et al.Biomed Mass Spectrom,1978,5(3):232
[6] Saleh F Y,Lee G F.Environ Sci Technol,1978,12(3):297
[7] Moseman R F,Crist H L,Edgerton T R,et al.Arch Environm Contam Toxicol,1977,6(1):221
[8] Hodgson D W,Kantor E J,Mann J B.Arch Environm Contam Toxicol,1978,7(1):99
[9] Brunet D,Woignier T,Lesueur-Jannoyer M,et al.Environm Pollut,2009,157(11):3120
[10] Bordet F,Thieffinne A,Mallet J,et al.Intern J Environ Anal Chem,2007,87:985
[11] Sun C X,Gao Y X,Liu T L,et al.Ecology and Environmental Sciences(孙翠香,高原雪,刘婷琳,等.生态环境学报),2011,20(4):727
[12] Wang Y J,Na G S,Wang Z,et al.Chinese Journal of Chromatography(王艳洁,那广水,王震,等.色谱),2012,30(8):847
[13] Wang Y J,Na G S,Wang Z,et al.Chinese Journal of Analytical Chemistry(王艳洁,那广水,王震,等.分析化学),2013,41(3):412

