内镜黏膜下剥离术治疗胃黏膜下肿瘤
陈晓东,郭长青
郑州大学第一附属医院消化内科郑州450052
#通讯作者,男,1966年10月生,博士,教授,主任医师,研究方向:消化道肿瘤及肝病,E-mail:cqguo6610@hotmail.com
消化道黏膜下肿瘤(submucosal tumor,SMT)泛指一类来自黏膜层以下(非黏膜组织)的消化道病变[1]。近年来,随着内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)设备改善、技术创新及经验累积,国内外逐渐开展ESD 治疗消化道早期癌、癌前病变及黏膜下肿瘤。ESD 可以一次切除较大的病变并提供更准确的病理检查结果[2]。但ESD 治疗消化道SMT 时易并发出血及穿孔,尤其是治疗来源于固有肌层的SMT,限制了ESD 治疗消化道SMT 的推广。2012年7月至2013年6月,作者应用头端弯曲的针形切开刀对35例胃SMT 行ESD,取得了较好的治疗效果,现报道如下。
1 对象与方法
1.1 研究对象 35例患者中,男13例,女22例,年龄25~77(58.7±17.1)岁。内镜检查前35例均有腹胀、上腹部不适、呃逆等非特异消化道症状。肿瘤位于贲门部2例,胃底部15例,胃体部8例,胃窦部10例。经内镜超声检查,23例位于固有肌层,12例位于黏膜下层。经16 层CT 平扫加增强检查,16例病灶被检查出。所有病例均于术前签署知情同意书,并告知手术方法、手术相关益处和风险。
1.2 器械 采用Olympus GIT-H260J 型胃镜,EUME1 内镜超声系统,超声探头采用UM-DP20-25R,频率为20 MHz。其他器械有NM-200L-0423 注射针、D-201-11804 先端透明帽、FD-410LR 热活检钳、KD-620-LR 型HOOK 刀、KD-610L 型IT 刀、SD-230U-20 圈套器、HX-610-135 止血夹、ERBE ICC-200 高频电切装置和APC300 氩气凝固器。
1.3 ESD 操作方法 全部病例均施行气管插管下全身静脉麻醉。ESD 操作步骤包括以下5 步。①标记:氩气刀沿隆起病灶边缘约5 mm 环周电凝标记。②黏膜下注射:于隆起病灶边缘标记点外侧,多点黏膜下注射含肾上腺素、亚甲蓝、甘油果糖混合注射液(注射液配制:200 mL 甘油果糖、2 mg 肾上腺素、0.2 mL 亚甲蓝)。③切开病灶外侧缘黏膜:应用HOOK 刀环形切开病灶外侧缘黏膜。④剥离肿瘤:应用IT 刀逐步剥离肿瘤,直至瘤体剥离完整,有时剥离接近结束时采用圈套器于病变根部圈套病变完整电切。⑤创面处理:切除病变后对于创面所有可见的小血管,应用氩气凝固器及热活检钳处理,较大裸露血管应用止血夹夹闭,最后用含去甲肾上腺素冰生理盐水冲洗创面。但创面较大或穿孔时,应用金属钛夹或尼龙绳封闭创面。ESD 操作步骤及剥离后的肿瘤见图1。
1.4 ESD 术后处理 瘤体随镜取出后,用甲醛溶液固定并送病理检查,同时进行CD34、CD117、CK、SMA、DOG-1、S-100 蛋白免疫组化染色。
术后禁食2 d,部分创面较大或穿孔病例给予留置胃管以持续胃肠减压,常规补液并给予质子泵抑制剂、抗生素,观察腹部体征及胃肠引流液,观察有无延迟出血及穿孔。术后第3 天,如无出血、腹痛,可进流食;术后第4 天,可进软食。术后1~12 个月进行内镜检查,观察创面愈合情况、金属夹是否脱落以及肿瘤有无残留或复发。
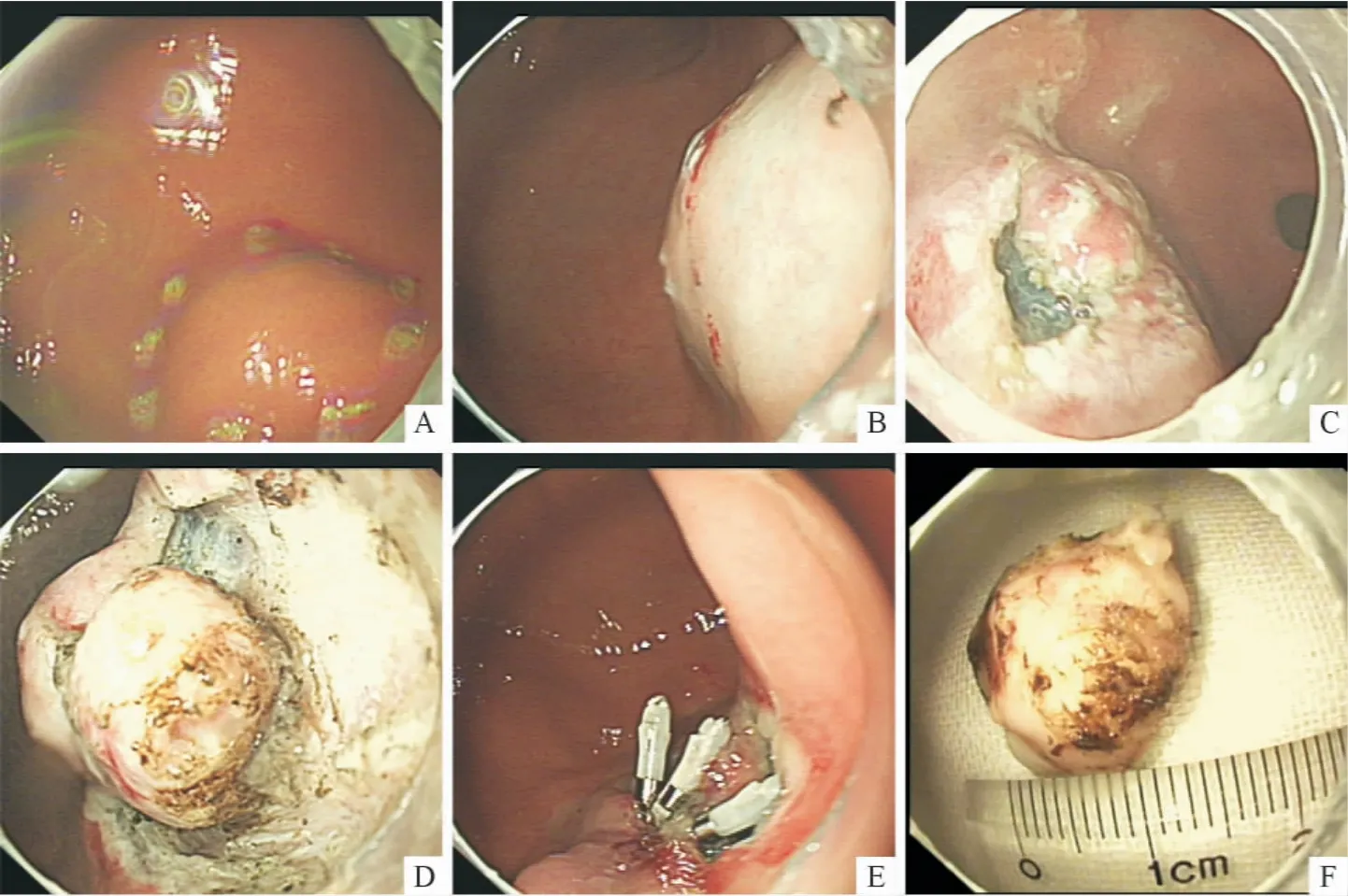
图1 ESD 操作步骤及剥离后的肿瘤
2 结果
35例胃SMT 均一次完整剥离,完整剥离率为100%,剥离肿瘤最大直径为0.8~3.0(1.5±0.6)cm,操作时间(自黏膜下注射至完整剥离肿瘤)35.0~100.0(56.0±14.6)min。切除标本病理及免疫组化染色结果显示:间质瘤11例,11例中CD34、CD117、DOG-1 表达阳性率均为100% (11/11);平滑肌瘤10例,10例中SMA、S-100 表达阳性率分别为100% (10/10)、40% (4/10);腺瘤2例(CK 均阳性表达,可见腺泡样结构),脂肪瘤5例(可见较多脂肪组织),异位胰腺7例(可见较多胰腺腺泡)。
ESD 治疗中创面均有少量渗血(<100 mL),均经电凝和凝固器处理成功止血。1例胃体腺瘤因剥离过程中切断小动脉大出血,内镜下应用金属钛夹夹闭血管止血成功。全组未见ESD 术后延迟出血。术中穿孔5例:4例均为来源于胃底固有肌层的间质瘤,剥离后可见胃壁裂孔,应用多枚金属钛夹成功将裂孔夹闭(其中1例应用金属钛夹联合尼龙绳缝合裂孔);1例为来源于胃窦黏膜下层的异位胰腺,因瘤体位置较深、与固有肌层粘连、胃壁瘢痕形成,剥离瘤体后发现胃壁裂孔,应用多枚金属钛夹成功夹闭裂孔。
术后随访12例,复查内镜,可见创面瘢痕样改变,5例有金属钛夹残留,无复发。
3 讨论
圈套器勒除术、内镜下黏膜切除术(EMR)、ESD等内镜切除方法均可用于治疗胃SMT。治疗胃SMT 时,圈套器容易滑脱,对于较大的肿瘤(直径>1 cm),难以一次性完整套扎,肿瘤残留、复发等发生率较高,需多次应用圈套器治疗。EMR 对于局限于黏膜内的带蒂的消化道肿瘤效果较好,但相关文献[3]报道,EMR 对直径>2 cm 的病变整体切除率约为30%,该研究中ESD 的完整剥离率为100%。与EMR 相比,ESD 最大的特点是能控制病灶切除的范围和大小,即使是累及黏膜下层的部分溃疡病灶也能被切除,这些都是EMR 难以克服的困难[4]。但ESD 的操作难度较EMR 高,且出血、穿孔等并发症的发生率较EMR 高,所以在一定程度上限制了ESD 的推广,同时要求ESD 操作者灵活运用ESD 治疗的器材及充分掌握ESD 的操作方法。
ESD 的难易程度主要与病变大小、部位、是否合并溃疡及有无瘢痕形成等有关[5]。根据作者的手术体会,以下2 种情况ESD 操作较难:①位于食管胃连接部(贲门部)、胃底部、中上部胃体大弯侧ESD 操作相对比较困难。②位于黏膜下层的胃异位胰腺,往往与固有肌层紧密接合,剥离较为困难。ESD 的操作难易程度直接影响ESD 的手术时间及并发症的发生率,该研究中35例胃SMT 的手术时间为(56.0±14.6)min,较相关研究[]中的手术平均时间稍长,这可能与该研究中位于胃底部、源于固有肌层的病灶较多有关。
ESD 治疗的主要并发症为出血和穿孔。在剥离肿瘤过程中,难免发生出血,需及时找到出血点进行止血,保证视野清晰;对于少量渗血,可用冰生理盐水(含去甲肾上腺素)冲洗创面,但应避免切除过程中反复冲洗;对于小血管的出血,应用凝固器、热活检钳、金属钛夹止血等可成功止血。该组1例胃体腺瘤病变剥离过程中切断小动脉,出现喷射性出血,及时应用金属钛夹将小动脉夹闭成功止血。所以剥离过程中应密切留意瘤体周围的小血管,及时发现并电凝血管,以避免切断血管引起大出血。为预防术后出血,创面裸露的小血管应马上处理,多采用热活检钳、凝固器、金属钛夹等,可明显降低出血率[6]。
穿孔是ESD 最严重的并发症,操作越困难的病变穿孔率越高[7]。Onozato 等[8]的回顾性研究显示ESD 治疗的穿孔率为5%,该组术中发生穿孔5例,4例为来源于胃底固有肌层的间质瘤。所以对于来源于固有肌层的SMT 应慎行ESD 治疗,尤其是胃底部,或对胃底部源于固有肌层的SMT 行ESD 治疗时,应更加注意操作技巧,术后应仔细观察有无穿孔。术中出现的穿孔一般可经内镜下金属钛夹闭合,该组中1例因裂孔较大,应用金属钛夹联合尼龙绳成功闭合裂孔。对于较大的裂孔亦可采取“吸引-夹闭-缝合”法,即适当吸引胃腔内气体,充分缩小穿孔,利用多个金属钛夹夹闭穿孔[9]。
因此,清晰的手术视野、精细的操作技巧以及术者对器械特性的熟知等是减少出血和穿孔的关键因素[10]。虽然该研究中穿孔及出血发生率仍偏高,但均可通过内镜控制,无1例因术中或术后并发症而需转外科手术,并不影响ESD 的治疗效果。术后35例胃SMT 均获得明确的病理学诊断。所以ESD 作为一种新型的微创手术方式,可以安全、有效地完整切除较大的、来源于黏膜下层及固有肌层的胃SMT,并可提供完整的病理学资料。
[1]周平红,姚礼庆,徐美东,等.内镜黏膜下剥离术治疗消化道黏膜下肿瘤[J].中国微创外科杂志,2007,7(11):1063
[2]Kakushima N,Fujishiro M.Endoscopic submucosal dissection for gastrointestinal neoplasms[J].World J Gastroenterol,2008,14(19):2962
[3]Saito Y,Fukuzawa M,Matsuda T,et al.Clinical outcome of endoscopic submucosal dissection versus endoscopic mucosal resection of large colorectal tumors as determined by curative resection[J].Surg Endosc,2010,24(2):343
[4]Hoteya S,Iizuka T,Kikuchi D,et al.Benefits of endoscopic submucosal dissection according to size and location of gastric neoplasm,compared with conventional mucosal resection[J].J Gastroenterol Hepatol,2009,24(6):1102
[5]方志恒,汪全红,钟萍,等.内镜黏膜下剥离术(ESD)治疗消化道病变[J].胃肠病学和肝病学杂志,2012,21(4):322
[6]Okada K,Yamamoto Y,Kasuga A,et al.Risk factors for delayed bleeding after endoscopic submucosal dissection for gastric neoplasm[J].Surg Endosc,2011,25(1):98
[7]卢忠生,令狐恩强,黄启阳,等.内镜黏膜下剥离术治疗消化道早期癌及癌前病变[J].中华消化内镜杂志,2008,25(11):578
[8]Onozato Y,Ishihara H,Iizuka H,et al.Endoscopic submucosal dissection for early gastric cancers and large flat adenomas[J].Endoscopy,2006,38(10):980
[9]周平红,姚礼庆,秦新裕,等.无腹腔镜辅助的内镜全层切除术治疗源于固有肌层的胃黏膜下肿瘤[J].中华消化内镜杂志,2009,26(12):617
[10]高飞,麻树人,张宁,等.玻璃酸钠、去甲肾上腺素、靛胭脂混合溶液在内镜黏膜下剥离术中的临床应用[J].解放军医学杂志,2011,36(7):733

