早期脑梗死患者血清中Hcy、hs-CRP、LDL与IR的相关性研究
徐巧绒,赵掌权,康 玲,唐文艳,李 欢(中铁二十局中心医院神经内科,咸阳 7000;西安市北方医院心内科; 通讯作者,E-mail:yujian.baihe@gmail.com)
脑血管病是中老年人的常见病和多发病,脑梗死是最常见的脑血管疾病,占脑卒中的70%以上,具有较高的致残率及病死率,找到能早期预测脑梗死形成的指标,是降低其危害的关键。目前认为脑梗死是多种危险因素共同作用的结果,中国高血压防治指南中把C反应蛋白(hs-CRP)、低密度脂蛋白(LDL)、糖尿病列入心脑血管疾病的危险因素[1],高血压为脑梗死的重要病因,它们在脑梗死发病中具有一定作用。本研究采用病例对照研究,探讨这四个因素在早期脑梗死中的关系及临床应用价值。
1 资料与方法
1.1 标本来源
选择2010-03~2012-12在中铁二十局中心医院神经内科住院且发病时间小于72 h的65例早期脑梗死患者,其中男性35例,女性30例,平均年龄(59.72±4.89)岁;所有病例均符合全国第四届脑血管病学术会议脑血管病诊断标准[2],并经CT或MRI证实。对照组为同期门诊体检健康者65例,男性31 例,女性34 例,平均年龄(57.94 ±5.06)岁。两组病例发病前3个月内均未使用叶酸、B族维生素、抗血小板聚集药物、降脂药物及卡马西平、苯妥英钠、异烟肼等药物。排除标准:①急慢性感染;②严重的肝肾功能不全;③急性心肌梗死或严重的慢性心衰(LVEF<30%);④糖尿病;⑤恶性肿瘤;⑥自身免疫性疾病;⑦近2个月有服用性激素史者。
1.2 研究方法
1.2.1 一般临床资料采集 记录对照组与脑梗死组中受试者一般资料,如姓名、年龄、性别、有无吸烟、高血压等。
1.2.2 实验室指标测定 130例病例均隔夜禁食12 h后采集静脉血,检测空腹血糖(FPG)、空腹胰岛素(FINS)、低密度脂蛋白(LDL),根据HOMA模型公式IRI=[FINS(mU/L)×FPG(mmol/L)]/22.5,计算 IRI。分析高 Hcy(Hcy>10 μmol/L)、高 hs-CRP(hs-CRP>1 mg/L)、高LDL(LDL>3.37 mmol/L)、IR(IRI>9.82 mIU/L)的发生率。
同时将采集的静脉血置于另外的抗凝管中,分离出血清,-20℃冻存备用,以检测Hcy、hs-CRP水平。用化学发光法检测Hcy水平;采用免疫投射比浊法检测hs-CRP。
1.3 统计学分析
采用SPSS13.0统计软件对实验结果进行统计学分析,计量资料如服从正态分布用±s表示;组间比较采用单因素方差分析(ANOVA),多变量间关系用多元回归分析和Logistic回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 一般临床资料比较
早期脑梗死组与对照组在年龄、性别构成比、吸烟、高血压发生方面差异无统计学意义(均P>0.05)。而早期脑梗死组高 Hcy、CRP、LDL及IR的发生率高于对照组,两组间差异具有统计学意义(均 P <0.01)。
2.2 实验室检查比较
早期脑梗死组病例组中 hs-CRP、Hcy、LDL、IRI较对照组均明显升高,且差异具有统计学意义(P<0.05),FPG与对照组比较差异无统计学意义(P>0.05,见表2)。

表1 对照组与早期脑梗死组临床资料比较Table 1 Com parison of clinical data between early cerebral infarction group and control group
表2 两组患者hs-CRP、Hcy、LDL、FPG、FINS、IRI比较(±s)Table 2 Comparison of hs-CRP,Hcy,LDL,FPG,FINS,IRI between early cerebral infarction group and control group(±s)

表2 两组患者hs-CRP、Hcy、LDL、FPG、FINS、IRI比较(±s)Table 2 Comparison of hs-CRP,Hcy,LDL,FPG,FINS,IRI between early cerebral infarction group and control group(±s)
与对照组比较,*P <0.05,**P <0.01
组别 n hs-CRP/(mg/L)Hcy/(μmol/L)LDL/(mmol/L)FPG/(mmol/L)FINS/(mmol/L)IRI早期对照组 65 5.1 ±0.5 12.4 ±1.9 2.2 ±0.1 5.4 ±0.7 7.0 ±1.8 1.7 ±0.2早期脑梗死组 65 10.4 ±1.2** 19.6 ±2.8* 2.5 ±0.2* 5.5 ±0.7 10.3 ±1.1** 2.5 ±0.4**
2.3 早期脑梗死患者危险因素分析
以病例中患有脑梗死为因变量,以 hs-CRP、Hcy、LDL、IRI各参数为自变量进行Logistic回归分析,结果表明早期脑梗死的发生与 hs-CRP、Hcy、LDL、IRI有关,血清hs-CRP、Hcy、LDL、IRI升高是早期脑梗死的独立危险因素(见表3)。
2.4 IRI与其他参数的相关性分析
以 IRI为因变量,分别以 Hcy、hs-CRP、LDL为自变量进行多元线性回归分析,结果显示Hcy(R2=0.527)、hs-CRP(R2=0.379)、LDL(R2=0.288)均与IRI具有相关性(均 P<0.05),是影响 IRI的重要因素。
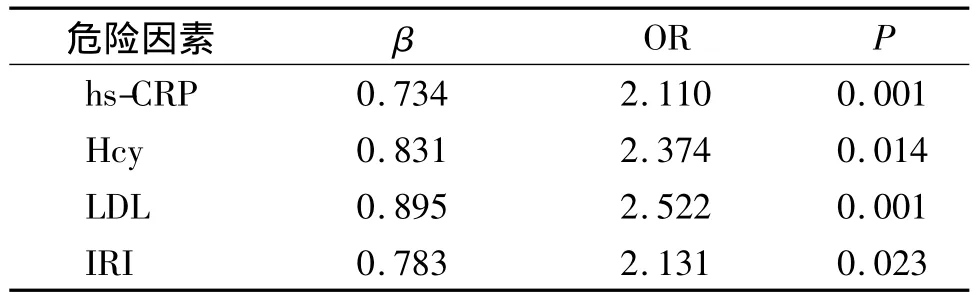
表3 Logistic回归分析早期脑梗死患者的危险因素Table 3 Logistic regression analysis of risk factors for early cerebral infarction
3 讨论
动脉粥样硬化是脑梗死的主要病因,临床研究显示,Hcy、hs-CRP、LDL的升高及IR是许多心脑血管疾病最重要的发病机制之一,脑梗死在居民所患脑血管病中所占比重相当大,其发生与这些指标的异常密切相关[3-6]。
Hcy是人体必需的含硫氨基酸,是蛋氨酸代谢的中间产物,有资料显示,过多的Hcy损伤血管的主要机制为:损伤具有舒张血管活性的内皮活性物质NO,同时抑制胶原蛋白合成,导致血管壁功能障碍[7];其氧化生成过量Hcy二聚体时产生过氧化氢,释放氧自由基对血管内皮有直接细胞毒作用,促进血管平滑肌细胞增殖[8,9]。在一项对大鼠的研究中发现,体内过量的Hcy可以缩短血小板生存时间、促进血小板聚集和黏附,还可以增加凝血因子Ⅴ、Ⅹ的活性,抑制组织纤溶酶和抗血栓形成因子Ⅲ、Ⅶ活性[10];促进动脉壁将 LDL氧化为氧化型LDL(ox-LDL),巨噬细胞吞噬ox-LDL后成为泡沫细胞,成为动脉粥样硬化的始动环节。本研究结果发现与健康体检者比较,早期脑梗死病例组中患者的Hcy明显升高(P<0.05),说明Hcy参与早期脑梗死的发病过程,并具有促进作用。
hs-CRP为体内炎性反应、组织损伤的敏感指标,而动脉粥样硬化和脑梗死的形成和发展均与持续反复的慢性炎性反应有关[11]。hs-CRP与vWF增强相关,vWF是内皮活化的标志物,内皮细胞功能障碍是动脉粥样硬化的起始环节,在脑梗死的病变过程中发挥着重要的作用。本实验中发现,早期脑梗死患者中 hs-CRP升高(P<0.05),说明 hs-CRP参与动脉硬化及脑梗死的发病过程。
血浆LDL中含量约占血浆总胆固醇的一半以上,许多基础实验与临床大规模荟萃分析显示,LDL对动脉粥样硬化发病的临床意义等于甚至高于血浆总胆固醇对动脉粥样硬化的作用,并且研究发现冠状动脉粥样硬化的发生与LDL关系更为密切。所以临床常将血浆LDL的水平作为冠心病二级预防和药物疗效判断的主要参考指标。绝大多数研究认为,体内过量的ROS能将 LDL氧化为氧化型LDL(oxydized LDL,ox-LDL)[12,13],ox-LDL 促使白细胞向血管内皮黏附、单核细胞进入内皮下层[12]、抑制斑块中巨噬细胞返回血液循环、促进巨噬细胞摄取LDL速度增加,导致大量泡沫细胞形成;ox-LDL还具有刺激炎性细胞因子分泌基质金属蛋白酶(Matrix metalloproteinase,MMP)、加速纤维帽处细胞基质降解,即增加了斑块的不稳定性和易损性,导致脏器血栓栓塞症状,如心肌梗死、脑梗死等。本实验中早期脑梗死患者与同期健康体检者比较,LDL升高较为明显,差异有统计学意义(P<0.05)。说明在对动脉粥样硬化及脑梗死的预防过程中,降低体内过多的LDL具有重要的作用。
胰岛素抵抗(IR)分为原发性和继发性,原发性主要与遗传因素有关,继发性胰岛素抵抗与肥胖、长期高血糖、高游离脂肪酸血症、某些药物如糖皮质激素、某些微量元素缺乏如铬和钒缺乏、妊娠和体内胰岛素拮抗激素增多等有关。有关研究表明,胰岛素抵抗通过一系列的信号转导途径促进炎症、内皮功能障碍等动脉粥样硬化病因的发生及进展[14],且胰岛素抵抗与它们相互促进,共同导致血小板激活,血小板的激活又在MS中起着核心作用[15]。本研究发现,早期脑梗死患者出现不同程度的胰岛素抵抗,说明胰岛素抵抗在脑梗死的发病过程中起到一定的作用。
最后将胰岛素抵抗指数(IRI)与hs-CRP、Hcy、LDL之间的相关性做了分析,研究表明 Hcy、hs-CRP、LDL均与IRI具有相关性,是影响IRI的重要因素。
IR的产生继而可以引起一系列的代谢综合征,是本病发生发展的关键。
本研究显示,早期脑梗死患者血清中hs-CRP、Hcy、LDL及 IRI明显高于同期门诊健康体检者(P <0.05)。说明 hs-CRP、Hcy、LDL 及空腹血糖、胰岛素水平在脑梗死形成过程中具有重要作用,早期对这些指标的检测、及时治疗对脑梗死的诊断及预防具有重要意义。
总之,IR、高 Hcy、CRP、LDL 水平,是早期脑梗死的独立的危险因素。因此在早期脑梗死诊治过程中,除关注血糖、血压、血脂等指标达标外,还应监测Hcy、CRP水平,评估病情的进展,并可采用相应的干预措施,通过降低IR和炎症因子水平,防治脑梗死等心脑血管意外的发生。
[1]中国高血压防治指南修订委员会.中国高血压防治指南[J].中华高血压杂志,2011,39(7):579-616.
[2]全国第四届脑血管病学术会议.各类脑血管病诊断要点[J].中华神经科杂志,1996,29(6):379-380.
[3]张江,王大力,张文彦,等.高敏 C反应蛋白与脑梗死危险因素的相关性研究[J].中华老年心脑血管病杂志,2006,8(6):391-393.
[4]Tseng YL,Chang YY,Liu JS,et al.Association of plasma homocysteine concentration with cerebral white matter hyperintensity on magnetic resonance images in stroke patients[J].J Neurol Sci,2009,284(1):36-39.
[5]Kuriyama N,Nagakane Y,Hosomi A,et al.Evaluation of factors associated with elevated levels of platelet-derived microparticles in the acute phase of cerebral infarction[J].Clin Appl Thromb-Hem,2010,16(1):26-32.
[6]Amarenco P,Lavallée PC,Labreuche J,et al.Coronary artery disease and risk of major vascular events after cerebral infarction[J].Stroke,2013,44(6):1505-1511.
[7]Oda E,Kawai R.Comparison between high-sensitivity C-reactive protein(hs-CRP)and white blood cell count(WBC)as an inflammatory component of metabolic syndrome in Japanese[J].Intern Med,2010,49(2):117-124.
[8]Sen U,Mishra PK,Tyagi N,et al.Homocysteine to hydrogen sulfide or hypertension[J].Cell Biochem Biophys,2010,57(2/3):49-58.
[9]Cunha A,Scherer E,Cunha M,et al.Acute hyperhomocysteinemia alters the coagulation system and oxidative status in the blood of rats[J].Mol Cell Biochem,2012,360(1/2):1-2.
[10]Sibrian-Vazquez M,Escobedo JO,Lim S,et al.Homocystamides promote free-radical and oxidative damage to proteins[J].Proc Natl Acad Sci,2010,107(2):551-554.
[11]Wieberdink RG,Koudstaal PJ,Hofman A,et al.Insulin resistance and the risk of stroke and stroke subtypes in the nondiabetic elderly[J].Am J Epidemiol,2012,176(8):699-707.
[12]陈瑗,周玫.氧化应激-炎症在动脉粥样硬化发生发展中作用研究的新进展[J].中国动脉硬化杂志,2008,16(10):757-762.
[13]Stocker R,Keaney JF.Role of oxidative modifications in atherosclerosis[J].Physiol Rev,2004,84(4):1381-1478.
[14]Kim B,Sullivan KA,Backus C,et al.Cortical neurons develop insulin resistance and blunted Akt signaling:a potential mechanism contributing to enhanced ischemic injury in diabetes[J].Antioxid Redox Sign,2011,14(10):1829-1839.
[15]Santilli F,Vazzana N,Liani R,et al.Platelet activation in obesity and metabolic syndrome[J].Obes Rev,2012,13(1):27-42.

