磁共振水成像在人工耳蜗植入术中的应用
陈治白,邱建新,张标新,吴 俊
(安徽医科大学第一附属医院耳鼻咽喉头颈外科,安徽合肥 230022)
近年来,随着人工耳蜗植入技术的不断发展,患者适应证的选择、术前检查、手术操作及术后护理都不断完善,人工耳蜗植入手术也越来越多的在各级医院开展起来。但由于人工耳蜗价格昂贵、人体内耳解剖结构复杂和术后康复治疗不规范等原因,并且术者对每一位患者综合评估也有所不同,使人工耳蜗植入术具有一定的风险性,因此,每一位患者在术前都需要充分的完善检查[1]。了解每一位患者的内耳及其周围解剖情况,耳蜗有无骨化或者纤维化、耳蜗有无畸形、内听道有无狭窄、蜗神经发育是否正常、面神经是否高位及颅内有无病变等,对确保手术成功率具有极其重要的意义。术前除了耳科专项检查和听力学评估以外,影像学检查以其直接的优势成为其中必不可少的一项,而MRI检查在其中占首要地位。计算机断层扫描(Compute Tomography,CT)可以发现耳蜗硬化等一些病变,但对内耳道狭窄、耳蜗严重发育畸形等不如磁共振成像(Magnetic resonance imaging,MRI)检查,同时对颅内病变显示较差,不能排除一些人工耳蜗植入的禁忌证,但磁共振检查却可以发现一些CT检查漏诊的病变。本文拟对比MRI内耳水成像和CT在检测内耳畸形的差异,从而探讨前者在人工耳蜗植入术前应用价值。
1 资料与方法
1.1 临床资料 收集2011年2月—2012年12月期间在我院行人工耳蜗植入术患者的影像学资料,包括头颅内听道MRI和颞骨CT,收集其中由我院单一影像学医师诊断的病例共200例,所有患者均由单一手术医师完成,其中男性113例,女性87例,年龄最小8个月,最大45岁,平均4.52岁。134例耳蜗植入选择右侧,其余选择左侧。植入体类型包括:澳大利亚Neuclear24M型弯电极108例,美国AB人工耳蜗90k型55例,奥地利 Med-EL40+型25例,pusal型 6例,sonata型4例,国产耳蜗诺尔康CS-10A 2例。
1.2 MRI检查 取仰卧位,头部取正中位,两耳对称,可以合作儿童检查前无需特殊处理,对于较小患儿,除检查前减少睡眠外,一般在检查前半小时使用镇静剂,一般使用鲁米那钠按体重计算出剂量肌注,扫描范围包括颞骨岩部、头部,应用美国G.E公司生产的3.0T HDx MR仪,8通道头颅线圈,行三维高级快速自旋回波(Fast Advanced Spin Echo,FASE)序列行横断扫描,内耳水成像扫描参数:TR=6.5 ms,TE=2.5 ms。FOV为16 mm×16 mm,扫描矩阵448 mm×256 mm,2 次采集,层厚为0.8 mm,间距为 -0.4 mm,(重叠0.4 mm,)层数为64,并对颞骨扫描的原始图像在工作站上应用最大密度投影(maximum intensity projection,MIP)法将图像进行三维重建,获得内耳MIP图像,删除周围低信号组织,仅留取双侧内耳,每30°旋转一次至180°,从而获得多轴面,多视角的内耳三维水成像。
1.3 统计学处理 以SPSS 19.0统计学软件包,以χ2检验分析比较CT、MRI和CT、MRI联合对内耳畸形检出率的差异,P<0.05为有统计学意义。
2 结果
200 例(400耳)患者均成功完成手术,14例(28耳)前庭倒水管扩大患者的CT和MRI检查均能发现。耳蜗畸形中5例(10耳)共腔畸形,8例(16耳)Mondini畸形,其中CT发现异常10例,另外3例漏诊,而MRI全部诊断出。内听道狭窄4例(4耳,均为单耳),CT发现异常2例,MRI全部发现异常(见图1和图2),耳蜗纤维化3例(3耳,均为单耳),MRI均发现异常,而CT未见明显异常,以上7例病人均在健侧行人工耳蜗植入,手术顺利完成,MRI和CT术前检查结果具体见表1。

图1 Mondini畸形

图2 耳蜗硬化
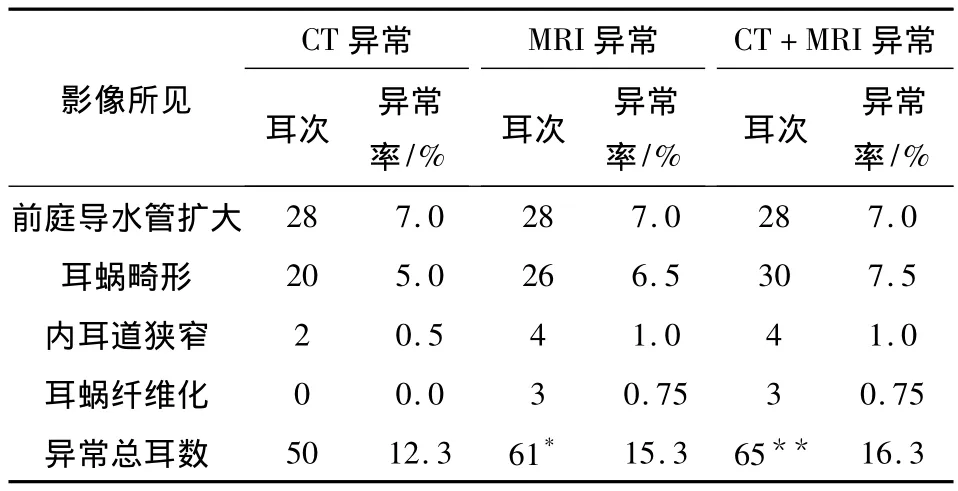
表1 400耳CT与MRI检查结果比较
在MRI和CT检查结果发现,CT、MRI、CT与MRI联合检查发现异常的出现率分别为12.5%(50/200)、15.3%(61/400)、16.3%(65/400),MRI在诊断内耳畸形中优于CT检查(P<0.05),两者联合检出百分率最高。
3 讨论
3.1 磁共振水成像 磁共振水成像用标准头部正交线圈或圆形表面线圈置于双耳,利用静态或缓慢流动的液体成像原理[2],其原理是利用长重复时间(time of repetition,TR),长回波时间(time to echo,TE)的重T2加权和脂肪抑制技术,获得重T2WI,使含水结构信号强度明显增强,从而与周围组织的低信号形成鲜明对比。并最大密度投影和三维重建,内耳膜迷路内充满淋巴液,属于相对静止的液体,因此可以在重T2加权上清晰地勾勒出耳蜗的形态结构,而周围骨性部分为低信号,形成鲜明对比,而不含水的组织信号随回波时间的延长而明显衰减,相当于内耳造影的效果,可测量内耳正常结构及显示解剖变异,直接显示内耳膜迷路及内外淋巴管和淋巴囊,发现内耳小的肿瘤如神经鞘瘤、血管瘤、听神经瘤等,为耳外科提供了细微解剖结构的影像学依据,为手术提供了重要的参考作用。同时又无需造影剂,在耳蜗纤维化及内听道狭窄等病变中的发现率优于其他常规检查,对CI手术患者的选择、术耳及电极的选择等均有重要的参考作用,所以已被越来越多地应用于人工耳蜗植入患者的术前检查中。也越来越来的受到耳外科医师的高度评价。MRI检查应用颞骨还包括以下三种检查方法,二维自旋回波为MRI最常用的基本序列,增强T1加权像可用于诊断内耳道小听神经瘤,三维梯度回波翻转角20°~30°,层厚1.0~1.3 mm,可用头部线圈,两侧同时扫描,三维积极干预稳态梯度回波为重T2加权像,用于显示膜迷路及内听道内面神经,在脑膜炎或颞骨骨折的病人,能够发现HRCT不能发现耳蜗受累的真正边界[3-4],也给耳蜗植入术前评估提供了一个新的方法,三维快速自旋回波,T2加权像,由于MRI相对的厚层扫描、较长的采集时间,常规的自旋回波序列不能够满足内耳检查的需要,为了克服上述两大技术缺陷,三维快速自旋回波能够获得比较满意的内耳图像,可清楚显示内耳膜迷路。
3.2 MRI在内耳部分病变中的诊断 内耳正常MRI表现,内听道:内听道位于颞骨深部,在重T2加权上呈管状或锥状高信号,直径约5 mm左右,两侧大小间差不多,内听道内脑脊液高信号,可清晰的显示神经走行及与邻近血管关系;半规管:半规管呈C形,边缘光滑规则,椭圆囊的半规管脚处略膨大,其余部分大小一致;耳蜗:呈典型的盘旋的“蜗牛”状,椭圆囊与球囊结构完整显示,呈高信号。先天行内耳畸形,内耳不发育或发育不良在MRI图像中表现为影像缺失,如Michel畸形、Mondini畸形、耳蜗发育不全性聋和蜗管球囊发育不全性聋等。大前庭水管综合征:表现为内淋巴管和内淋巴囊的扩大,在MRI的T2W1上内淋巴管位于颅后窝的乙状窦前方,内淋巴囊为位于内耳道后方硬脑膜外的高信号结构[5],在可以测量的内耳中,内淋巴管中点的宽度在0.1~1.4 mm范围内,MRI在诊断内淋巴囊扩大的标准为内淋巴囊骨内部分中点的最大宽度大于1.5 mm。该畸形术中可伴有搏动性脑脊液漏,甚至出现井喷[6]。听神经瘤是桥小脑角区最常见的肿瘤,MRI可显示内听道或桥小脑角占位性病变或桥脑多发性硬化,可作为诊断听神经瘤的金标准。MRI表现为肿块以内耳道为中心生长,常伴有囊变、坏死、出血、钙化等,肿瘤于T1WI上呈等或稍低信号,T2WI上呈高信号,囊变、坏死区域T1信号更低,T2信号更高,陈旧性出血、钙化T1、T2均为低信号。对于较大的听神经瘤,MRI一般能做出定性诊断,在通过增强扫描,能清楚的显示其大小及范围,内耳道内微小听神经瘤表现为T1WI在低信号脑脊液的衬托下出现管内软组织影,T2WI上肿瘤信号有所增高,但仍可在管内高信号脑脊液对比下显示充盈缺损,增强扫描呈球状、小结节状、线状,蜗神经的大小与螺旋神经节细胞的数量有关。蜗神经通过内耳道底进入内耳道,蜗神经位于内听道前下方,面神经位于前上部,前庭上神经和前庭下神经位于后部,蜗神经发育异常包括蜗直径减少、微小肿瘤甚至神经缺失等,在垂直内听道轴向的斜矢状面,蜗神经较内听道内其它神经小为蜗神经缺陷,在横断面、冠状面和斜矢状面均不能辩认者称蜗神经缺失,蜗神经缺矢广义上包括小神经、微细神经、神经确实缺失三种情况,发生原因主要包括先天性蜗神经缺陷和蜗神经损伤后发生继发性病变。先天性蜗神经缺陷而内听道正常,可能在子宫内或围产期内听道形成后才发生蜗神经损害。蜗神经缺失可能的原因是内听道发育不良,后天主要由于蜗神经损伤后发生继发性病变,声创伤、机械性损伤、和耳毒性抗生素使用等可使神经元数量减少至5%~10%[7]。Kang等[8]认为蜗神经的大小决定是否能行人工耳蜗植入的关键因素,蜗神经缺失是人工耳蜗植入的绝对禁忌证,而颞骨CT无法显示蜗神经结构,对于诊断蜗神经病变有一定的局限性,MRI则具有很好的空间分辨率和软组织分辨率,能清晰的显示内听道的神经结构,对蜗神经病变诊断有较大的优势,从而避免漏诊和误诊[9]。
3.3 MRI与HRCT 虽然HRCT在显示骨性病变方面较MRI有较大优势,但它对软组织鉴别能力非常低,而MRI能够提供重要的信息来帮助确定术侧的选择以及预计手术将会遇到的困难。CT或MRI在成人、儿童人工耳蜗植入术前筛选评估方面的作用曾有报道。但有关小儿患者中二者联合应用的报道较为少见,在了解内耳的骨性结构,乳突的气化情况及面神经的情况方面,HRCT优于MRI,硬化型耳蜗给手术带来较大风险,人工耳蜗电极插入比较困难。同时,HRCT对面神经走向及其变异情况的显示较好,有助于术者在手术操作中把握尺度,减少面神经损伤。而MRI有助于分辨耳蜗内的液体,在确定耳蜗是否纤维化有明显优势,而且对内耳道内神经的分辨优于CT[10]。另外值得一提的是HRCT对脑膜瘤、转移瘤、鼓室乳突胆脂瘤、骨纤维结构不良有较好的显示。
通过对本组200例患者的磁共振和CT结果分析得出如下结论。在人工耳蜗植入术前影像学评价中,MRI内耳水成像及耳蜗三维重建技术具有独特优势,是CT和其他影像学不能所取代的,能提供有关内耳膜迷路和蜗神经发育情况的可靠解剖信息,头颅MRI能发现颅内病变,对脑白质及脑瘫患者术后康复疗效起到评估作用,同时对人工耳蜗病例的选择、左右耳选择以及植入体电极型号的选择提供重要的帮助,是人工耳蜗植入术前必不可少的检查手段。
[1] 李玉洁,张道行.1396例人工耳蜗植入围手术期并发症讨论[J].临床耳鼻咽喉头颈外科杂志,2010,24(10):433 -435.
[2] 王云玲,贾 琳,王 红,等.MRH在内耳成像及病变诊断中的应用研究[J].磁共振成像,2012,3(1):15 -18.
[3] Aschendorff A.Imaging in cochlear implant patients[J].GMS Curr Top Otorhinolaryngol Head Neck Surg,2011(10):7.
[4] Miyasaka M,Nosaka S,Morimoto N,et al.CT and MR imaging for pediatric cochlear implantation:emphasis on the relationship between the cochlear nerve canal and the cochlear nerve[J].Pediatr Radiol,2010,40(9):1509 - 1516.
[5] 李坤军,邱建新.大前庭水管综合征患者的人工耳蜗植入[J].安徽医药,2011,15(6):719 -720.
[6] 方哲明,娄 昕,兰 兰,等.大前庭水管综合征内淋巴囊体积与听力损失相关性分析[J].中华耳科学杂志,2010,8(2):153-156.
[7] 马德菊.calpain1在卡那霉素致毒豚鼠耳蜗中的表达[J].安徽医药,2011,15(7):812 -814.
[8] Kang WS,Hyun SM,Lim HK,et al.Normative diameters and effects of aging on the cochlear and facial nerves in normal-hearing Korean ears using 3.0-tesla magnetic resonance imaging[J].Laryngoscope,2012,122(5):1109 -1114.
[9] 李幼瑾,杨 军,李 蕴.感音神经性聋患儿中先天性内耳畸形的构成、影像学及临床听力学特征[J].临床耳鼻咽喉头颈外科杂志,2011,25(1):1 -5.
[10] 曹雯君,李玉华.小儿蜗神经发育不良与蜗神经管的关系:CT和 MRI研究[J].放射学实践,2012,27(12):1324 -1327.

