替米沙坦激活PPARγ改善衰老大鼠脑血管内皮依赖性舒张功能
张黎黎,杨震,刘爱东,黄鸣清,周鹏,王沛坚*
(1.成都医学院第一附属医院神经内科,成都 610500;2.成都医学院第一附属医院心血管内科,成都 610500;3.福建中医药大学药学院,福州 350122)
目前我国超过60岁的老龄人口约2亿,提示我国已经进入老龄化社会。年龄增长导致血管老化是心脑血管疾病如脑卒中、冠心病、高血压等的重要危险因素[1,2]。血管老化最初的特征主要表现为血管内皮功能障碍[3]。由于血管老化往往缺乏典型的临床症状,目前对老年人群单纯的血管老化现象并未引起足够重视,缺少相应的防治措施[1]。此外,我国老年人口高血压的患病率已高达49%[4],因此寻求既能降低血压又能改善血管功能,防止血管老化的药物显得尤为重要。
替米沙坦为血管紧张素II受体(AT1型)拮抗剂,是临床常用的降压药物,可改善高血压患者预后。但近年研究显示,替米沙坦不但可拮抗AT1受体,还可作为过氧化物酶增殖物受体γ(PPARγ)和过氧化物酶增殖物受体β(PPARβ)的激动剂。替米沙坦通过激活PPARγ具有改善血管内皮依赖性舒张功能的作用[5,6];通过激活PPARβ具有改善高脂喂养小鼠的胰岛素抵抗,降低高脂喂养的高血压大鼠的体质量和血压[7,8]。更为重要的是,替米沙坦还可增加内皮细胞一氧化氮(NO)水平,延缓内皮细胞衰老[9]。目前研究已证实替米沙坦可降低血压并防止血管内皮细胞衰老,但替米沙坦对衰老相关的脑血管内皮功能障碍的作用及机制尚未明确。本实验利用自然衰老的大鼠模型,观察替米沙坦对衰老大鼠模型血压、心率及脑动脉血管功能的影响,在此基础上分离脑基底动脉,观察PPARγ和PPARβ的阻断剂对替米沙坦作用的影响,从而初步揭示替米沙坦对衰老大鼠脑动脉血管内皮依赖性舒张功能的作用机制。
1 材料与方法
1.1 实验动物及分组
24月龄雄性SD大鼠(12只)和6月龄雄性SD大鼠(6只)[1],分为年轻对照组(6只)、衰老模型组(6只)、衰老-替米沙坦组(6只,灌胃给药,5mg/kg/d)。替米沙坦以生理盐水混悬后灌胃给药,衰老组和对照组给予等体积生理盐水灌胃,1次/d,干预时间为1月。
1.2 仪器及试药
1.2.1 仪器 二氧化碳培养箱 (TC2323型,SHELDON,USA);去离子水过滤器 (Millipore,德国);PH 计(ф320 型,Beckman,德国);多导电生理记录仪 (Powerlab/8SP,ADI,Australia);微血管张力测 定 仪 (Wire Myograph,DMT 620M 型,Denmark)。
1.2.2 试药 替米沙坦(上海勃林格殷格翰药业有限公司);DMEM培养基、抗生素、胎牛血清等购于美国GIBCO公司;乌拉坦 (上海SCRC国药集团化学试剂公司);氯化钾 (KCl,重庆北碚化学试剂厂);GSK0660、GW9662、二甲基亚砜(DMSO)、L-硝基-精氨酸甲脂(L-NAME)、5-羟色胺(5-HT)、乙酰胆碱 (Ach)均购于Sigma公司;硝酸甘油 (NTG,山西康宝生物制品股份有限公司)。
1.3 脑基底动脉的体外培养[1,10]
SD大鼠以10%乌拉坦腹腔注射麻醉后断头处死,在解剖显微镜下分离脑基底动脉,立即转移至超净工作台放至盛有DMEM培养基的六孔板中进行培养。分组:衰老组,衰老+替米沙坦(Telmi,10 μM)组,Telmi+GSK0660 (1μM)组,Telmi+GW9662(1μM)组,干预时间为24h。
1.4 血管功能评价
1.4.1 参照既往建立的方法[1,11]在解剖显微镜下将血管环悬于两根钢丝之间,血管环于浴槽中平衡60min并调初张力致2mN,稳定后加入60mM KCl溶液预激3次,开始以下实验:1)内皮依赖性舒张功能(endothelium dependent relaxation,EDR)评估:于浴槽加入5-HT (10-5mmol/L)收缩血管,血管张力达平台后分别加入不同浓度的Ach(10-9~10-5mmol/L),观察血管对 Ach的反应性,每一浓度的加入均在上一浓度的反应到达平台后加入。2)非内皮依赖性 舒张 功能的评估:以5-HT (10-5mmol/L)预收缩血管,待反应达平台后加入不同浓度的 NTG (10-9~10-5mmol/L),观察血管对 NTG的反应性,每一浓度的加入均在上一浓度的反应到达平台后加入。
1.4.2 舒张反应的计算方法 Ach或NTG所引起的最大舒张幅度与5-HT引起的最大收缩幅度之比值。将数据输入Prism 3.0软件,制作拟合曲线,通过软件计算最大舒张反应[Emax(%)],并进行组间比较。
1.5 统计学方法
以SPSS 13.0统计分析软件进行数据录入及处理,数据以均数±标准差(±s)表示,采用非配对t检验进行组间比较,Prism 3.0软件制图,以P<0.05为差异有统计学意义。
2 结果
2.1 替米沙坦对衰老大鼠模型血压、心率的影响
衰老大鼠(24月龄)模型的血压、心率与对照组大鼠(6月龄)比较,差异无统计学意义(P>0.05);替米沙坦(5mg/kg/d)灌胃给药对血压和心率无显著影响,组间比较,差异无统计学意义(P>0.05)(见图1A和图1B)。
2.2 PPARγ和PPARβ阻断剂对替米沙坦作用的影响
替米沙坦(Telmi,10μM,24h)孵育可显著改善衰老大鼠脑动脉EDR,与衰老组比较,差异有统计学意义(P<0.01)。PPARγ的阻断剂 GW9662(1 μM,24h)可显著阻断替米沙坦对EDR的改善作用(P<0.05);PPARβ的阻断剂 GSK0660(1μM,24 h)虽有轻度的减弱作用,但差异无统计学意义(P>0.05),提示替米沙坦改善衰老大鼠脑动脉EDR的作用依赖于PPARγ(见图2)。
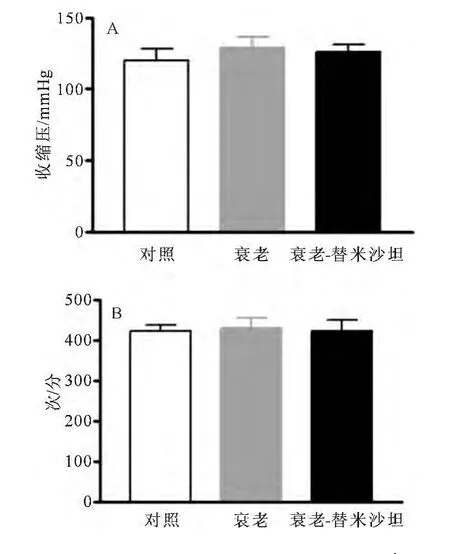
图1 替米沙坦对衰老大鼠模型血压、心率的影响
2.3 替米沙坦对自然衰老大鼠模型血管功能的影响
与对照组大鼠比较,衰老大鼠脑基底动脉Ach诱导的EDR显著下降(P<0.01),替米沙坦可改善衰老大鼠脑动脉Ach诱导的EDR(P<0.05)。但以LNAME(100μM,30min)预孵后比较,差异无统计学意义(P>0.05)。两组大鼠NTG诱导的非内皮依赖性舒张功能比较,差异无统计学意义(P>0.05)。上述结果提示,替米沙坦可显著改善衰老大鼠脑基底动脉Ach诱导的EDR(见图3A、图3B和图3C)。

图2 替米沙坦体外孵育对衰老大鼠EDR的作用及PPARγ和PPARβ阻断剂的影响与衰老组比较,**P<0.01;与衰老-替米沙坦组比较,#P<0.05
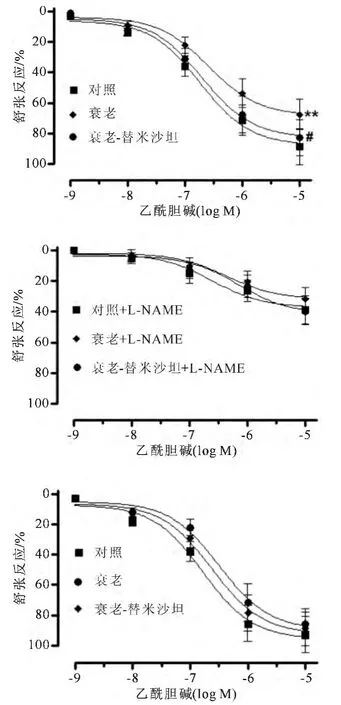
图3 替米沙坦对自然衰老大鼠模型血管功能的影响
3 讨论
衰老是脑卒中的重要危险因素,其主要原因可能与衰老导致机体氧化应激水平的显著升高,进而导致血管内皮功能受损有关,其机制可能与活性氧簇(ROS)在衰老的进程中显著升高有关。ROS不但直接损伤血管内皮细胞,还通过失活具有内皮保护作用的舒张因子-NO,直接介导了EDR受损[12]。
目前用于研究衰老的病理生理特征及相关的干预策略的动物模型主要有D-半乳糖诱导的衰老模型、自然衰老模型、臭氧吸入制作的自由基损伤模型等[1,13]。通常认为自然衰老模型能较好地模拟自然衰老进程,其病理特点与人体的衰老较为类似,是目前常用的研究衰老的重要模型[14]。本研究采用24月龄SD大鼠作为研究对象,衰老SD大鼠血压和心率与6月龄的对照大鼠比较,差异无统计学意义,与既往的研究一致。
替米沙坦是临床常用的抗高血压药物,有研究[15]发现,其还有改善血管内皮功能的作用。在本研究中,衰老大鼠在灌胃给予替米沙坦1月后,其脑动脉Ach诱导的EDR得到显著改善,而对NTG诱导的非内皮依赖性舒张功能未见明显影响。近年研究[7,8]提示,替米沙坦对肥胖相关的血压升高不但具有降压作用还能改善代谢,包括改善葡萄糖代谢、减轻体质量和胰岛素抵抗,但上述作用却不依赖于AT1受体的阻断作用,而是依赖于PPARβ。另有研究[16,17]显示,替米沙坦通过激活 PPARγ具有显著心血管代谢的保护作用。为分析替米沙坦对脑动脉EDR改善作用依赖于PPARγ抑或是PPARβ,根据既往建立的体外培养血管组织的方法,观察了PPARβ和PPARγ的阻断剂对替米沙坦作用的影响。结果发现,PPARγ的阻断剂GW9662可显著阻断替米沙坦的作用,而PPARβ的阻断剂GSK0660则不能,提示替米沙坦改善老龄鼠脑动脉EDR依赖于PPARγ。
综上所述,传统的降压药物替米沙坦不但具有显著的抗高血压作用,对于非高血压的老龄个体,替米沙坦则具有改善脑血管内皮功能的作用。故推测对于老龄高血压患者,替米沙坦的应用可能更有利于预防脑卒中的发生,但需进一步深入开展基础及临床研究。
[1]Pu Y,Zhang H,Wang P,et al.Dietary curcumin ameliorates aging-related cerebrovascular dysfunction through the ampk/uncoupling protein 2pathway [J].Cell Physiol Biochem,2013,32(5):1167-1177.
[2]Chen RL,Balami JS,Esiri MM,et al.Ischemic stroke in the elderly:an overview of evidence[J].Nat Rev Neurol,2010,6(5):256-265.
[3]Fleenor BS,Sindler AL,Marvi NK,et al.Curcumin ameliorates arterial dysfunction and oxidative stress with aging[J].Exp Gerontol,2013,48(2):269-276.
[4]Fukutomi M,Kario K.Aging and hypertension [J].Expert Rev Cardiovasc Ther,8(11):1531-1539.
[5]Kobayashi N,Ohno T,Yoshida K,et al.Cardioprotective mechanism of telmisartan via PPAR-gamma-eNOS pathway in dahl salt-sensitive hypertensive rats [J].Am J Hypertens,2008,21(5):576-581.
[6]Yamagishi S,Takeuchi M.Telmisartan is a promising cardiometabolic sartan due to its unique PPAR-gammainducing property [J].Med Hypotheses,2005,64(3):476-478.
[7]Feng X,Luo Z,Ma L,et al.Angiotensin II receptor blocker telmisartan enhances running endurance of skeletal muscle through activation of the PPAR-delta/AMPK pathway [J].J Cell Mol Med,2011,15(7):1572-1581.
[8]He H,Yang D,Ma L,et al.Telmisartan prevents weight gain and obesity through activation of peroxisome proliferatoractivated receptor-delta-dependent pathways [J].Hypertension,2010,55(4):869-879.
[9]Scalera F,Martens-Lobenhoffer J,Bukowska A,et al.Effect of telmisartan on nitric oxide--asymmetrical dimethylarginine system:role of angiotensin II type 1receptor gamma and peroxisome proliferator activated receptor gamma signaling during endothelial aging [J].Hypertension,2008,51(3):696-703.
[10]Tian XY,Wong WT,Xu A,et al.Uncoupling protein-2 protects endothelial function in diet-induced obese mice [J].Circ Res,2012,110(9):1211-1216.
[11]Sun J,Pu Y,Wang P,et al.TRPV1-mediated UCP2 upregulation ameliorates hyperglycemia-induced endothelial dysfunction[J].Cardiovasc Diabetol,2013,12:69.
[12]Silva RA,Chu Y,Miller JD,et al.Impact of ACE2deficiency and oxidative stress on cerebrovascular function with aging[J].Stroke,2012,43(12):3358-3363.
[13]王喆.衰老动物模型的研究进展 [J].中国比较医学杂志,2013,23(3):67-70.
[14]曾祥贵,谭忠庆,张浩,等.自然老龄小鼠与D-半乳糖衰老模型小鼠的比较 [J].现代预防医学,2001,28(4):416-417.
[15]Benndorf RA,Appel D,Maas R,et al.Telmisartan improves endothelial function in patients with essential hypertension[J].J Cardiovasc Pharmacol,2007,50(4):367-371.
[16]Yamagishi S,Nakamura K,Matsui T.Potential utility of telmisartan,an angiotensin II type 1receptor blocker with peroxisome proliferator-activated receptor-gamma (PPAR-gamma )-modulating activity for the treatment of cardiometabolic disorders[J].Curr Mol Med,2007,7(5):463-469.
[17]Yamagishi S,Takeuchi M.Telmisartan is a promising cardiometabolic sartan due to its unique PPAR-gammainducing property [J].Med Hypotheses,2005,64(3):476-478.

