替吉奥联合奥沙利铂与替吉奥联合多西他赛治疗晚期胃癌的临床观察
智俊娜,吴婷婷,赵本慧,陈丁丁,陆建伟
(1.中国药科大学,南京 210009;2.江苏省肿瘤医院,南京 210009)
在消化道肿瘤中,胃癌是最常见的恶性肿瘤,且其在癌症相关死亡中位列第2[1]。而在我国,胃癌的发病率和病死率位于首位[2]。虽然晚期胃癌是不可治愈的,但是规范的化疗可缓解患者临床症状,延长生存期,因此化疗已成为晚期胃癌治疗中必不可少的部分[3]。近年来新药不断涌现且组合成新的化疗方案(以口服氟尿嘧啶类联合铂类或紫杉类为主),其客观缓解率多已超过40%。为此,本研究旨在观察替吉奥联合奥沙利铂与替吉奥联合多西他赛治疗晚期胃癌的疗效以及毒副反应,现将结果报道如下。
1 资料与方法
1.1 临床资料
2012年9月~2013年11月,我科收治43例晚期或术后复发性的胃癌患者,均符合以下标准:1)经我院组织学或细胞学证实为不可手术或手术后复发的转移性胃腺癌患者;2)年龄18~75岁,性别不限,可口服给药;3)有客观可测量肿瘤病灶;4)一般状况采用行为状态量表(Ckarnofsky performance status,KPS)评分≥70,预计生存期>3个月;5)骨髓储备及肝肾功能基本正常;6)无其他恶性肿瘤病史。其中男性30例,女性13例;年龄26~73岁,中位年龄57岁。分为两组:替吉奥联合奥沙利铂组(OXA组)26例,初治26例,复治0例;替吉奥联合多西他赛组(TXT组)17例,初治13例,复治4例。两组的临床分期、年龄、性别等一般资料比较差异无统计学意义(P>0.05),具有可比性(见表1)。
1.2 治疗方法
OXA组:替吉奥胶囊:40mg/m2,口服,2次/d,第1~14天,3w为1周期;OXA:130mg/m2,静滴,第1天,3w为1周期。TXT组:替吉奥胶囊:40mg/m2,口服,2次/d,第1~14天,3w 为1周期;TXT:60mg/m2,静滴,第1天,3w 为1周期,至少完成2个周期。TXT组患者化疗前1d开始口服地塞米松7.5mg,2次/d,连服3d,进行预处理,并常规予5-羟色胺Ⅲ亚型受体(5-HT3)拮抗药止吐。定期查血常规和肝、肾功能,若治疗中出现3/4级骨髓抑制,则使用细胞集落刺激因子(GCSF),必要时输注红细胞、血小板治疗。若患者在口服替吉奥时出现严重毒副反应,给予对症药物治疗,同时停止口服替吉奥,或病情进展时,停止化疗,最多接受6个周期。
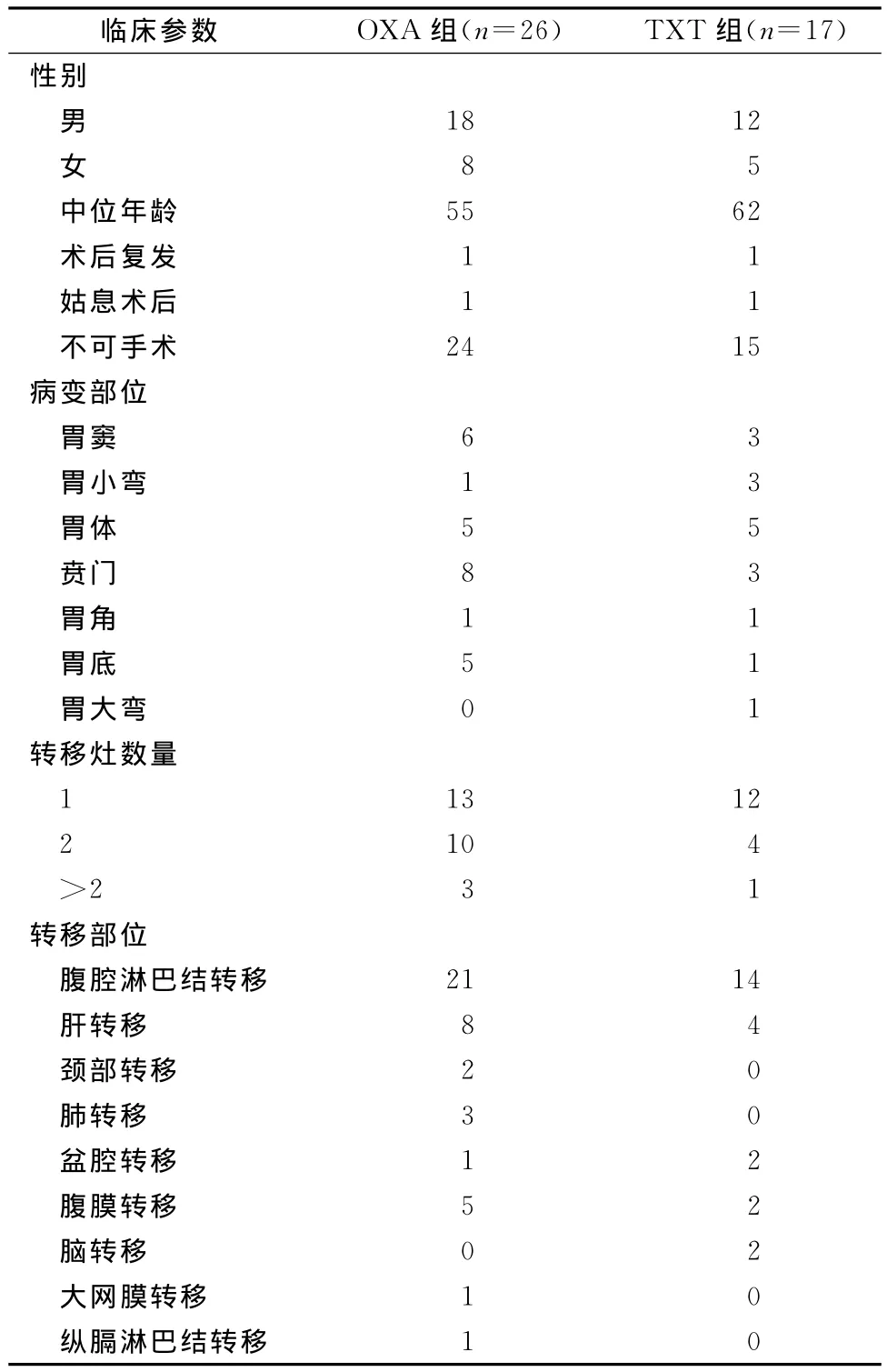
表1 43例晚期胃癌患者的临床病理特征
1.3 评价标准
每2个周期按照实体瘤疗效评价标准RECIST 1.1标准判定近期疗效,分完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD),有效率(RR)=CR+PR,疾病控制率(DCR)=CR+PR+SD。毒副反应按照美国通用毒性标准3.0(NCI-CTC 3.0)分为0~4级,每周期进行评价。生活质量的评价采用KPS评分,显著改善:增加≥20分,改善:增加≥10分,稳定:增加<10分,降低:减少≥10分,在化疗前、化疗进展或化疗结束时进行评分。生活质量改善率=改善率+稳定率。
1.4 统计学方法
采用SPSS 17.0软件进行统计学分析,计数资料采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 近期疗效
晚期胃癌42例患者,均至少完成2个化疗周期,共160个周期,平均每个患者完成3.8个周期,其中TXT组1例患者因出现严重毒副反应,无法评价疗效。OXA组获CR 0例,PR 15例,SD 6例,PD 5例,RR为57.7%,DCR为80.8%;TXT 组获CR 0例,PR 4例,SD 6例,PD的为6例,RR为31.3% ,DCR 62.5%。OXA组的有效率高于TXT组,但差异无统计学意义(P=0.096)(见表2)。

表2 治疗晚期胃癌各化疗方案的近期疗效
2.2 毒副反应
43例患者均可评价毒副反应,以I~II级为主(见表3)。TXT 组白细胞减少(94.1%)、口腔炎(35.3%)和便秘(76.5%)的总发生率明显高于OXA组(73.1%、3.8%、38.5%),差异有统计学意义(P=0.019、0.006、0.015);OXA 组的神经毒性发生率(53.8%)显著高于 TXT 组(17.6%),差异有统计学意义(P=0.018)(见表3)。

表3 治疗晚期胃癌的毒副反应情况
2.3 生活质量
42例晚期胃癌患者治疗后,OXA组KPS评分显著改善0例,改善10例,稳定11例,降低5例,改善率为38.5%;TXT组KPS评分显著改善0例,改善6例,稳定5例,降低5例,改善率为37.5%,两组比较差异无统计学意义(P=0.950)(见表4)。

表4 42例患者治疗前后生活质量改善情况
3 讨论
替吉奥是第四代氟尿嘧啶类抗肿瘤药,是由替加氟 (Tegafur,FT-207)、吉美 嘧 啶 (Gimeracil,CDHP)和奥替拉西钾(Oteracil Potassium,Oxo)以1∶0.4∶1摩尔比组成的复方制剂。替加氟口服吸收后经肝微粒体的细胞色素P-450酶系作用而转化为氟尿嘧啶,从而起到抗癌的作用;吉美嘧啶可通过抑制二氢嘧啶脱氢酶(DPD),延长氟尿嘧啶的作用时间,提高疗效;奥替拉西钾通过抑制氟尿嘧啶磷酸化,减少胃肠道反应[4]。替吉奥胶囊由于其方便、安全和良好等特点,被广泛用于胃癌的一线治疗[5]。
奥沙利铂作为第三代铂类,由于疗效好,毒副反应小,可耐受,被广泛用于晚期胃癌治疗。Koizumi等[6]研究表明替吉奥联合顺铂(DDP)疗效高于替吉奥单药。日本推荐替吉奥联合DDP为治疗晚期胃癌的一线标准方案,但很多患者因为DDP毒副反应大而终止治疗。Montagnani等[7]的meta分析结果表明与联合DDP相比,联合OXA不仅可得到更高的生存效益,而且毒副反应小,可以耐受,尤为适用于老年患者。Oh和Park等[8,9]报道了替吉奥联合OXA治疗晚期胃癌的有效率分别为53.7%和61%,常见的III~IV级毒副反应分别为血小板减少(39%)、中性粒细胞减少(28%)和恶心呕吐(12.2%)和腹泻(4.9%)。
TXT是一种半合成的紫杉类抗肿瘤药,可单药或联合其它抗肿瘤药来治疗多种肿瘤。Koizumi等[6,10]研究表明,TXT与氟尿嘧啶类药物有协同作用,替吉奥联合TXT比替吉奥单药效率更高,分别为38.8%和26.8%;替吉奥联合TXT中,中性粒细胞减少发生率较高(29.0%vs 4.5%,P<0.05),但是患者可以耐受。Yoshida等[11]报道了替吉奥联合TXT治疗晚期胃癌的有效率为56.3%,发生率较高的III~IV级毒副反应为中性粒细胞减少(58.3%)和白细胞减少(41.7%)。
本研究应用替吉奥分别联合OXA和TXT治疗晚期胃癌,其近期有效率分别是57.7%和31.3%,疾病控制率分别为80.8%和62.5%,与国内外相关研究结果相近。在毒副反应方面,两组多以I~Ⅱ级为主,均无Ⅳ度骨髓抑制、肝肾损害等严重毒副反应,患者均可耐受。TXT组白细胞减少、口腔炎和便秘的总发生率明显高于OXA组,差异有统计学意义(P<0.05);OXA组的神经毒性发生率(53.8%)显著高于 TXT 组(17.6%),差异有统计学意义(P<0.05)。
综上所述,替吉奥联合OXA治疗晚期胃癌与替吉奥联合TXT相比,疗效相当,毒副反应TXT组略高于OXA组。但由于多西他赛组病例较少,使结果存在一定偏差,所以需要大样本实验进一步验证。
[1]Kamangar F,Dores GM,Anderson WF.Patterns of cancer incidence,mortality,and prevalence across five continents:defining priorities to reduce cancer disparities in different geographic regions of the world[J].Journal of Clinical Oncology,2006,24(14):2137-2150.
[2]王罡,张俊华.胃癌外科治疗的新进展[J].中国医药导报,2009,6(5):11-13.
[3]金懋林,陈强,程凤歧,等.奥沙利铂联合亚叶酸钙和5-氟尿嘧啶治疗晚期胃癌的研究[J].中华肿瘤杂志,2003,25(2):172-174.
[4]Chu QS,Hammond LA,Schwartz G,et al.Phase I and pharmacokinetic study of the oral fluoropyrimidine S-1on a once-daily-for-28-day schedule in patients with advanced malignancies[J].Clinical Cancer Research,2004,10(15):4913-4921.
[5]Huang J,Cao Y,Wu L,et al.S-1-based therapy versus 5-FU-based therapy in advanced gastric cancer:a meta-analysis[J].Medical Oncology,2011,28(4):1004-1011.
[6]Koizumi W,Narahara H,Hara T,et al.S-1plus cisplatin versus S-1alone for first-line treatment of advanced gastric cancer(SPIRITS trial):aphase III trial[J].The Lancet Oncology,2008,9(3):215-221.
[7]Montagnani F,Turrisi G,Marinozzi C,et al.Effectiveness and safety of oxaliplatin compared to cisplatin for advanced,unresectable gastric cancer:a systematic review and metaanalysis[J].Gastric Cancer,2011,14(1):50-55.
[8]Oh SY,Kwon HC,Jeong SH,et al.A phase II study of S-1 and oxaliplatin(SOx)combination chemotherapy as a firstline therapy for patients with advanced gastric cancer[J].Investigational New Drugs,2012,30(1):350-356.
[9]Park I, Lee JL, Ryu MH,et al. Phase I/II and pharmacokinetic study of S-1and oxaliplatin in previously untreated advanced gastric cancer[J].Cancer Chemotherapy and Pharmacology,2010,65(3):473-480.
[10]Koizumi W,Kim YH,Fujii M,et al.Addition of docetaxel to S-1without platinum prolongs survival of patients with advanced gastric cancer:a randomized study(START)[J].Journal of Cancer Research and Clinical Oncology,2014,140(2):319-328.
[11]Yoshida K,Ninomiya M,Takakura N,et al.Phase II study of docetaxel and S-1combination therapy for advanced or recurrent gastric cancer[J].Clinical Cancer Research,2006,12(11):3402-3407.

