门冬氨酸鸟氨酸注射液工艺质量研究
顾大业,王成永,汪洪湖,陈文婕,戴荣欢
(1.安徽中医药大学药学院,合肥230001;2.安徽蚌埠丰原医药科技发展有限公司,安徽 蚌埠233000)
门冬氨酸鸟氨酸注射液于20世纪70年代最先在德国应用于临床,于1991年收载入德国药典,同时并被美国FDA 批准用于治疗肝性脑病。门冬氨酸鸟氨酸是由门冬氨酸与鸟氨酸聚合形成稳定的二肽聚合物,鸟氨酸是通过肝脏鸟氨酸循环来加速尿素的合成,促进氨的代谢,因而达到降低血氨浓度。天门冬氨酸则是间接参与三羧酸循环以及核酸的合成,从而有利于对受损肝细胞进行修复,也促进了肝细胞内的能量生成[1]。门冬氨酸鸟氨酸注射液在我国也是首个用于临床具有解毒、护肝、能量三效合一的新药,其主要有效成分是门冬氨酸鸟氨酸,化学名称为(S)-2,5-二氨基戊酸(s)-2-氨基丁二酸盐,分子式:C9H19N3O6,相对分子质量:265.27[2]。临床主要应用于急、慢性肝病的治疗,其包括肝硬化、脂肪肝以及肝炎所引起的血氨升高症状,其中对肝性脑病尤其有效[3]。
一 材料与方法
为筛选优化工艺参数,实验以溶液PH 值、配液温度以及充氮压力为考察因素,以样品中门冬氨酸鸟氨酸和鸟氨酸内酰胺盐的含量为考察指标,,选用L9(34)正交表进行试验,优选出该注射液的最佳配制工艺参数,按照筛选出的最佳工艺参数配制出的样品经留样观察和仪器分析检测表明各项指标均符合门冬氨酸鸟氨酸注射液质量标准要求,从而确保了该产品的质量可靠与稳定。
试药及物料。门冬氨酸鸟氨酸原料药(批号:120824,含量:99.62%,水分3.2%,自制);门冬氨酸鸟氨酸对照品(中国药品生物制品检定所),鸟氨酸内酰胺盐对照品(120827,自制),氨水(江苏彤晟化学试剂有限公司,分析纯);磷酸(江苏强盛化工有限公司,分析纯);乙腈(分析纯),微孔滤膜(0.22um,PALL公司);玻璃安瓿(10mL棕色,兆丰(丹阳)新型药用包材有限公司)。
仪器及设备。磁力搅拌器(江苏金坛市金城国胜实验仪器厂),KQ3200B型超声波清洗器(昆山市超声仪器有限公司);安瓿拉丝灌封机(上海远东制药机械总厂);TU-1901双光束紫外可见分光光度计(北京普析通用仪器有限责任公司);高效液相色谱仪(waters)。
二 配置方法
(一)考察指标的确定与检测方法
通过查阅相关文献和一些预实验发现,门冬氨酸鸟氨酸在偏碱的溶液体系中鸟氨酸会降解,引起鸟氨酸内酰胺盐增加。又根据预实验发现,门冬氨酸鸟氨酸随着温度升高颜色加深,含量降低且鸟氨酸内酰胺盐增加。所以选择门冬氨酸鸟氨酸含量和鸟氨酸内酰胺盐为主要考察指标,参照国家药品监督管理局标准YBH04442011门冬氨酸鸟氨酸质量标准,采用HPLC法测定注射液样品中门冬氨酸鸟氨酸含量和鸟氨酸内酰胺盐。
(二)相关因素与水平的确定
通过查阅相关文献和一些预实验发现,配制溶液温度越高,门冬氨酸鸟氨酸溶解越完全,但温度过高,不利于主药的稳定。充氮量越少,溶液中的残留空气越多,越不利于主药稳定,但通氮量过大,会引起溶液温度迅速下降,也不利于主药完全溶解,故影响其含量。PH 值越大,鸟氨酸越不稳定,杂质含量也越偏高。因此,结合原有工艺参数,选取注射液配制时的PH 值、温度以及充氮压力为考察因素,每个因素选三个水平进行L9(34)正交表平行试验,采用综合评分法对数据进行分析(其权重系数分别为0.6,0.4),优选最佳配液工艺,因素水平见表1。
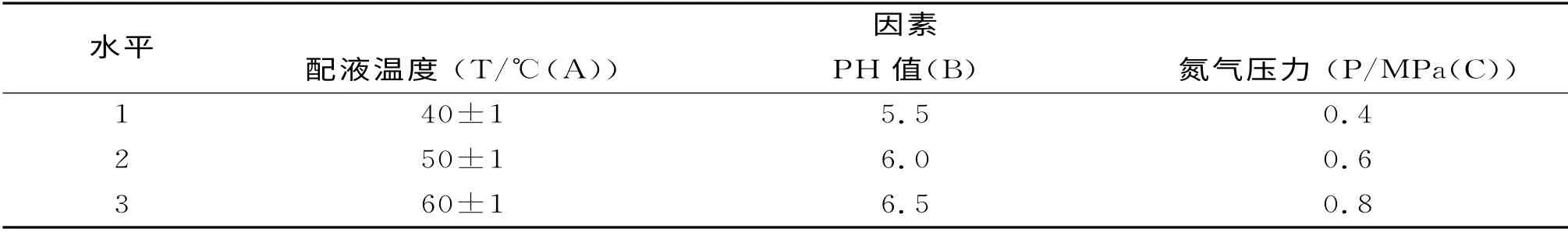
表1 因素水平
(三)正交试验设计
按照正交设计的试验条件来进行样品的配制,称取门冬氨酸鸟氨酸约100g若干份,分别置250ml烧杯中加入100ml注射用水放入相应温度的水浴锅中匀速搅拌30min至全溶,然后定容至200ml,样品配制好后进行过滤、灌封、灭菌,然后留样观察,并按国家食品药品监督管理局门冬氨酸鸟氨酸质量标准检验门冬氨酸鸟氨酸与鸟氨酸内酰胺盐的含量。正交试验设计见表1,试验结果见表2,方差分析见表3。
(四)门冬氨酸鸟氨酸及鸟氨酸内酰胺盐含量的测定[4,5]
色谱条件。Waters 1525-2487-TCM-717Alltima Amino色谱柱(4.6mm×250mm,5 um);流动相:乙腈-0.05mol/L 磷酸二氢钾溶液(50∶50);检测波长:210nm;流速:1.0mL/min;柱温:30 ℃。
对照品溶液的制备。取门冬氨酸鸟氨酸对照品适量,精密称定,加流动相溶解并稀释制成每毫升含1mg的溶液,即得对照品溶液。
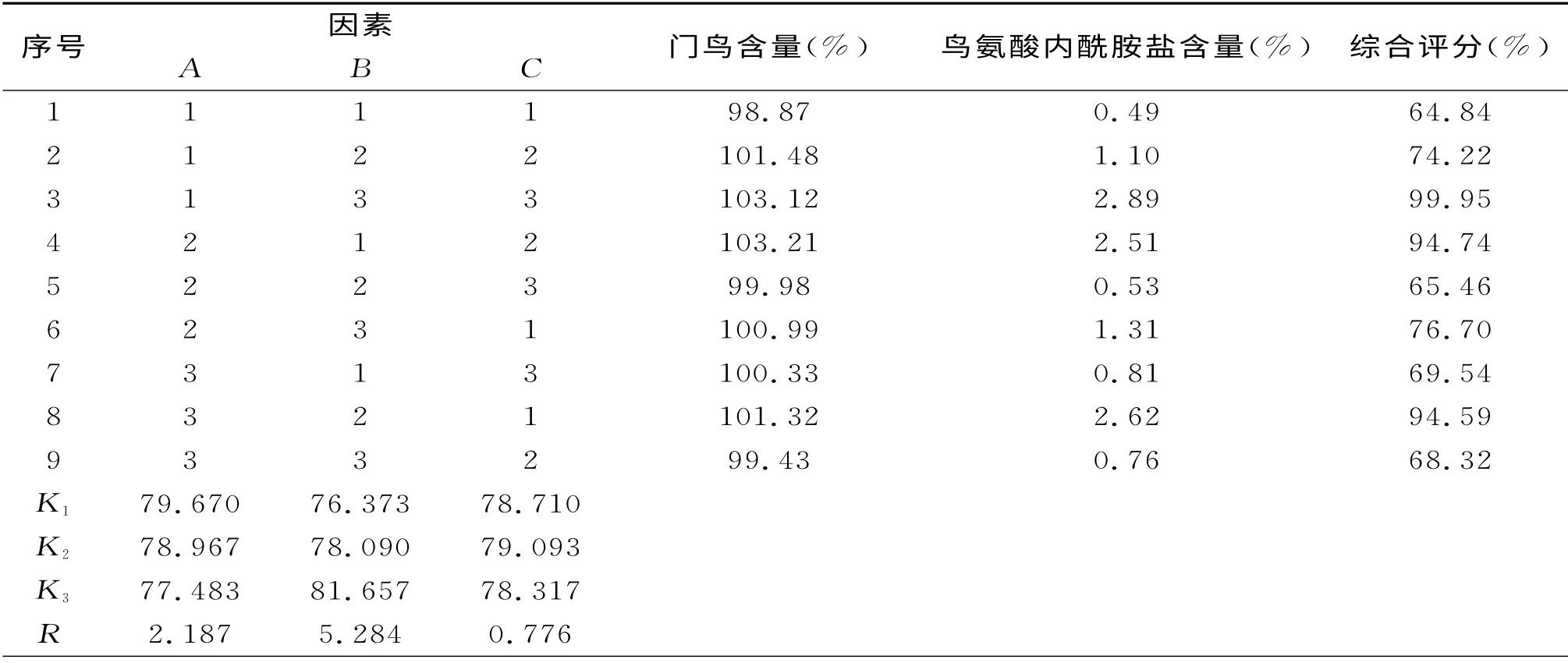
表2 正交试验结果
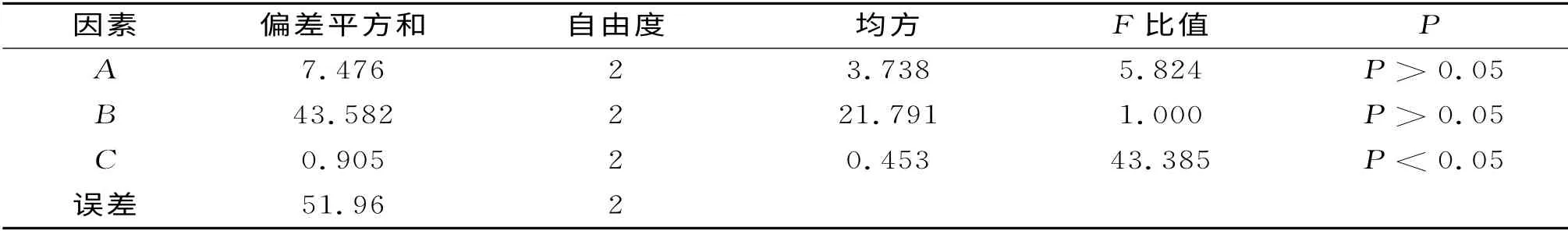
表3 方差分析表
供试品溶液的制备。精密量取门冬氨酸鸟氨酸注射液0.2ml,置100ml量瓶中,加流动相稀释至刻度,摇匀,滤过,取续滤液,即得供试品溶液。
含量测定。精密量取供试品和对照品20ul注入HPLC仪,记录色谱图,按外标法计算门冬氨酸鸟氨酸含量,面积归一化法计算鸟氨酸内酰胺盐含量。

(1)式中:As为供试品中门冬氨酸鸟氨酸的峰面积;Cr为门冬氨酸鸟氨酸对照品的浓度,mg/ml;Ar为对照品中门冬氨酸鸟氨酸的峰面积;Cs为供试品中门冬氨酸鸟氨酸的标示浓度,mg/ml。
三 结果分析
通过对表2直观分析表明,以综合评分为标准,在所选的因素水平范围内,各因素作用顺序为B>A>C,最佳提取组合为:A1B3C2,即:溶解温度为40°,PH 值为6.0,充氮压力为0.6 MPa。通过对表3的方差分析表明,只有因素C(充氮压力)有显著性影响(P<0.05),而因素A(溶解温度)、因素B(PH 值)对试验结果均无显著影响(P>0.05),考虑到生产上的节能和经济性问题,优选因素水平组合为A1B2C2,即溶解温度为40°,PH值为6.0,充氮压力为0.6MPa。
四 最佳工艺验证
分别称取5份门冬氨酸鸟氨酸原料药约100g置250ml烧杯中加100ml纯化水至40°水浴锅上加热搅拌30min后冷却,然后定容至200ml,用1mol/L NaoH-HCL 调PH 到6.0,再过滤充氮灌封,实验结果表明门鸟平均含量为100.93%;鸟氨酸内酰胺盐的平均含量为0.397%。实验结果见表4。
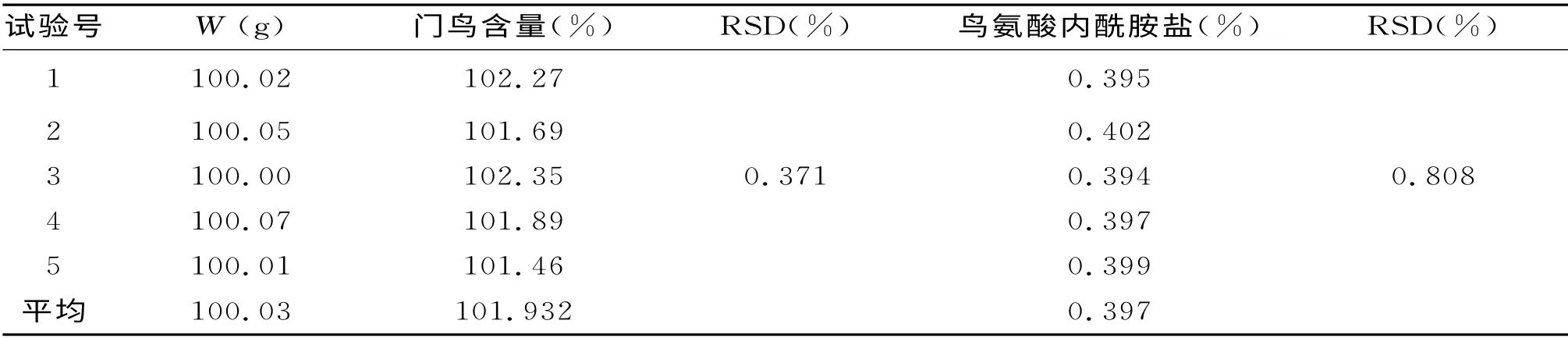
表4 工艺验证试验
通过表4工艺验证试验结果表明5个平行样门冬氨酸鸟氨酸含量的RSD 为0.371%小于限度2%,鸟氨酸内酰胺盐含量的RSD 为0.808%小于限度20%,因此表明该方案A1B2C2的重现性较好,说明此小试工艺的条件稳定可行。
五 讨论
门冬氨酸鸟氨酸是由鸟氨酸和天门冬氨酸通过成盐反应生成的二肽聚合物,其性质不稳定,注射液在高温、光照、偏碱环境中鸟氨酸易成环,颜色加深,导致含量降低,杂质偏大。因此优选适宜的配制工艺参数对其质量影响作用重大,本文是通过正交试验法优选出了门冬氨酸鸟氨酸注射液配制工艺参数,按筛选出的工艺条件来制备样品并检测样品中门冬氨酸鸟氨酸含量和鸟氨酸内酰胺盐量,结果显示根据筛选的工艺参数配制的注射液性质稳定,质量可靠。
本研究是从优化工艺参数的角度来进行筛选,可用于指导实际生产。但改善门冬氨酸鸟氨酸注射液的质量还可以从筛选处方着手。因为门冬氨酸鸟氨酸注射液长期贮存有不稳定现象,所以可以考虑通过加入合适的PH 调节剂和抗氧剂来提高溶液的稳定性。故可以通过对门冬氨酸鸟氨酸注射液的处方和生产工艺来进行优化,解决产品在贮存过程中的不稳定现象,甚至可以耐受终端灭菌等现实问题,将有利于提高门冬氨酸鸟氨酸注射液的品质。
[1]陈孝治.瑞甘[J].中南药学,2004,2(4):254-255.
[2]蒋音,陈良,巫善明.门冬氨酸鸟氨酸的药理作用与临床应用[J].世界感染杂志,2007,7(5):415-418.
[3]何昌武,张彦秋.门冬氨酸-鸟氨酸治疗病毒性肝炎胆红素升高的疗效观察[J].中国自然医学杂志,2009,11(1):74-75.
[4]王荣梅.高效液相色谱法测定盐酸精氨酸注射液的含量[J].中国生化药物杂志,2003,24(6):296-297.
[5]缪宁梅,马婕.高效液相色谱法测定门冬氨酸鸟氨酸注射液的含量[J].中国生化药物杂志,2007,28(1):52-53.

