替米考星肠溶微丸的制备及其评价
韩萌萌,李沙沙,孙朋超,梁 倩,李敏营,张娜娜,赵永星
(郑州大学药学院,郑州450001)
替米考星是由泰乐菌素的水解产物半合成的一种大环内酯类抗生素,对防治畜禽由胸膜肺炎放线杆菌、巴氏杆菌、支原体等感染引起的肺炎、禽支原体病及泌乳动物的乳腺炎有良好的效果[1]。由于替米考星在酸性环境中不稳定,目前国内外上市的替米考星剂型仅有替米考星预混剂、注射液等[2],这些剂型不仅成本高,而且给药不方便。微丸属于口服多剂量剂型,不仅给药方便,而且药物的体内吸收速度均匀且个体间生物利用度差异较小[3]。为了解决替米考星在酸性环境中不稳定[4],口服在胃中易被破坏以及药物味苦[1]的问题,本实验将替米考星制备成肠溶微丸制剂,并对其进行了表征和初步评价。
1 材料与方法
1.1 材料 替米考星和花生壳粉(河南官渡兽药制造有限公司)、微晶纤维素(安徽山河药辅料股份有限公司)、药用淀粉和药用糊精(曲阜市药用辅料有限公司)、十二烷基硫酸钠(山东聊城安信药用辅料有限公司)、欧巴代®肠溶薄膜包衣预混剂(上海卡乐康包衣技术有限公司)。
1.2 仪器设备 E-50挤出滚圆设备(重庆英格造粒包衣技术有限公司)、Mini DPL 0.2型流化床(重庆精工机械)、RCZ-8B溶出仪(天大天发科技有限公司)、Nikon Eclipse 80i型荧光显微镜(日本Nikon公司)、UV-2450紫外分光光度计(日本岛津)、Nicolet 380-红外分光光度计(美国赛默飞世尔科技)、DSC-200F3差示扫描量热仪(德国耐驰科学仪器贸易上海有限公司)。
1.3 制备方法
1.3.1 微丸的制备 按处方量称取药物与辅料,过100目筛,混合均匀,以1%羟丙基甲基纤维素为粘合剂制软材,用孔径1.0 mm的筛网以30 r/min的挤出速度挤出,挤出后在滚圆机内以800 r/min的速度滚转1.5 min,微丸于60℃流化床干燥1 h,筛分后取16~24目的微丸作为合格的微丸。
1.3.2 微丸的包衣 用80%的乙醇配制浓度为10%的肠溶包衣液,磁力搅拌1 h,使其充分溶解,过100目筛备用。将合格的微丸置于流化床中,设置进风温度为70℃,物料温度为60℃。风机频率25 Hz,雾化压力0.06 MPa,蠕动泵流速2 mL/min,包衣结束后,固化 30 min[5],得替米考星肠溶微丸。
1.4 替米考星含量测定 紫外分光光度计扫描替米考星溶液,结果显示其在292 nm波长处有最大吸收。在此波长下测系列浓度的供试品溶液和各供试品溶液的吸光度[6]。以样品吸光度(A)对浓度(C)进行线性回归,得直线方程 A=0.0559C-0.0045 (R2= 0.9999) 。 结果显示替米考星浓度在6~45 μg/mL范围内与吸光度有良好的线性关系,可用于替米考星的含量测定。
取替米考星微丸适量,研细,精密称取适量(约相当于替米考星25 mg),置于100 mL容量瓶中,加水至使其完全溶解,定容至刻度。量取10 mL稀释至100 mL,作为供试品溶液。同法称取原料药适量,制得25 μg/mL的替米考星作为对照品溶液,在292 nm的波长下,分别测定吸光度,计算得到替米考星微丸相对含药量为103.00%。
1.5 替米考星微丸释放度的测定 参照2010版《中国药典》附录 XD释放度测定法第二法[7],以900 mL 0.l mol/L盐酸溶液作为溶出介质,设置温度(37士0.5)℃,各取1 g微丸投入溶出杯中,采用桨法,转速 100 r/min,分别于 20、40、60、80、100、120 min取样,取样量2 mL,10 mL容量瓶定容。结束后,弃去酸液,立即加入pH 6.8的磷酸钠缓冲溶液继续运转,分别于 130、140、150、160 min 取样,取1 mL溶出液至10 mL容量瓶定容,紫外测定吸光度,计算药物的累积释放量[8]。
1.6 替米考星微丸的确证 将药物、药物与辅料的物理混合物和替米考星肠溶微丸进行红外扫描,比较其红外光谱图,可以判断药物在微丸中的变化,由替米考星主要官能团的特征峰的变化,进一步确定药物在制剂中的存在状态。另外,差示扫描量热仪分别测3组物质的熔点,根据其熔点的变化,可以推断药物在制备的过程中药物存在形式的变化。
2 结果
根据预实验结果和文献报道[9],影响微丸成型的因素主要是微晶纤维素的处方量,而包衣增重对微丸释放度影响较大。因此,本文就这两个因素进行考察,结果如下。
2.1 不同处方量的微晶纤维素对微丸成型性的影响 保持其他因素不变,通过改变填充剂花生壳粉和微晶纤维素的量来制备微丸。结果如图1所示,微晶纤维素的处方量分别是15%、25%、30%时,在电子显微镜下观察,4倍镜下微丸的形状分别如图1中A、B、C所示;40倍镜下微丸的表面分别如图1中 D、E、F 所示。
2.2 包衣增重量对微丸释放度的影响 肠溶微丸的溶出度主要受到肠溶包衣材料性质的影响,肠溶包衣材料的厚度在一定程度上决定着微丸的释放速率[10]。固定处方中原辅料的量,考察不同包衣增重(5%、10%、15%)对药物释放的影响。由图2可知,在酸性介质中,包衣增重不同的微丸2 h后释放度分别达到67.46%、9.98%、5.97%。在pH 6.8的磷酸缓冲盐介质中,最终累积释放量分别达到94.00%、90.78%、69.60%。
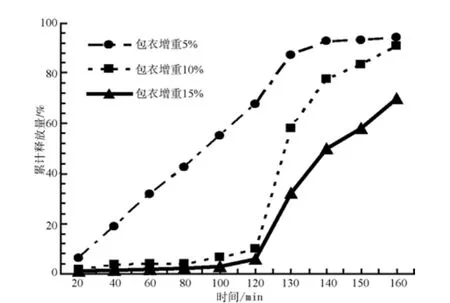
图2 包衣增重量对微丸释放度的影响
2.3 替米考星微丸的确证
2.3.1 红外分析 替米考星、替米考星与辅料的物理混合物、替米考星微丸红外光谱见图3所示。根据参考文献[11]其中在特征区 3450 cm-1,指纹区1200 cm-1是叔醇羟基的特征峰,2960 cm-1、2920 cm-1是甲基、亚甲基的伸缩振动峰,1650 cm-1是叔胺中碳氮键的伸缩振动峰,1050~1100 cm-1是六元单氧环中碳氧单键伸缩振动峰。
2.3.2 差示扫描量热分析 替米考星、替米考星与辅料的物理混合物、替米考星微丸DSC图谱见图4所示。替米考星为单峰,熔点为101.2℃;替米考星和辅料物理混合物的熔点在105.1℃;替米考星微丸在100℃没有固定的熔点。
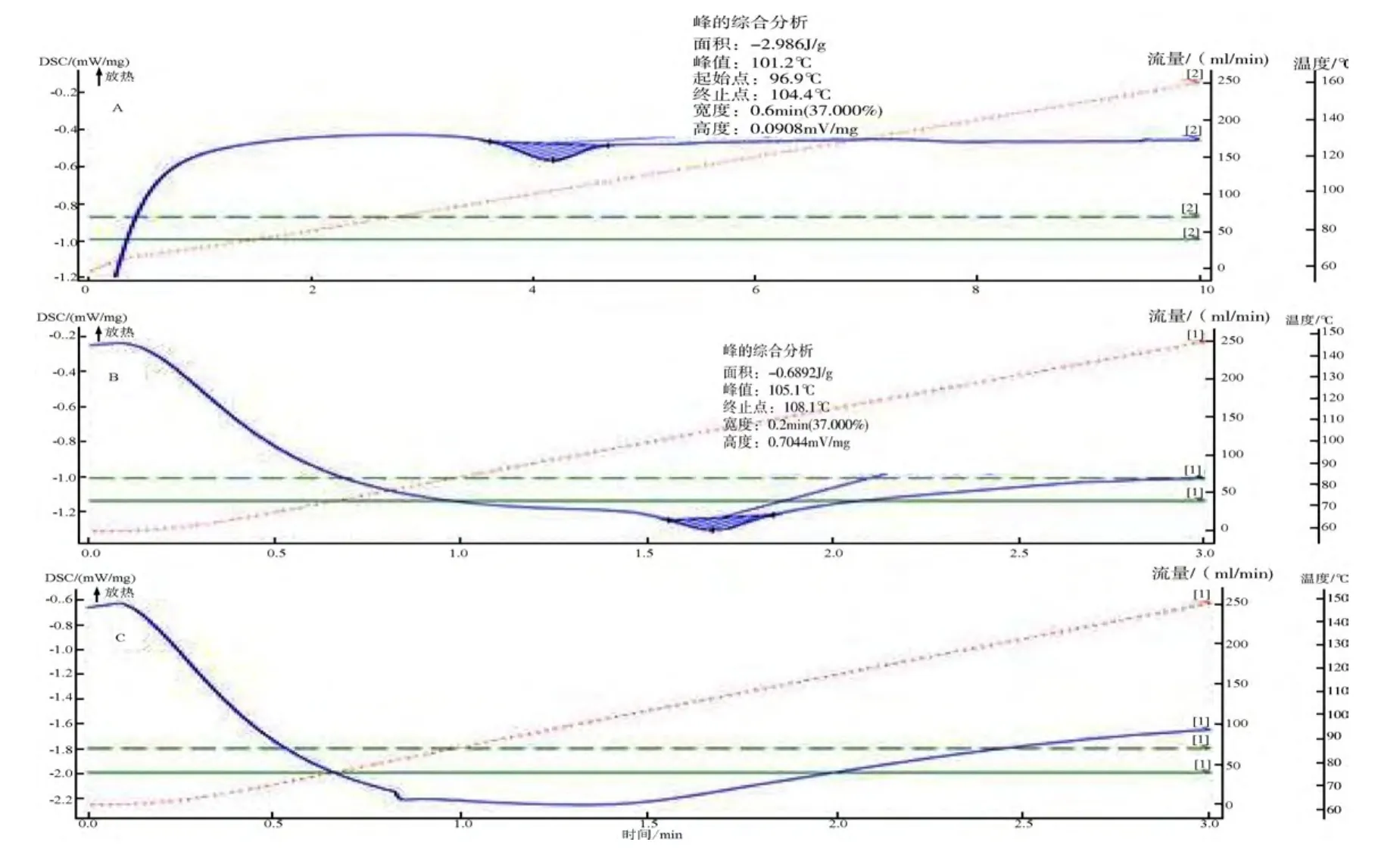
图4 替米考星(A)、替米考星与辅料的物理混合物(B)和替米考星微丸(C)的DSC图谱
3 讨论
本实验考察微晶纤维素用量与替米考星微丸成型性的关系,15%的微晶纤维素成型性最差,滚圆后成不规则状,表面粗糙;30%的微晶纤维素成型性相对较好,微丸粒径也比较均匀,表面光滑。结果表明微晶纤维素用量越大,微丸越圆整、成型性越好、收率也越高。包衣膜增重对替米考星释放的影响显著,且随着包衣增重的增加,药物在酸性释放介质中的释放度逐渐降低,随着时间的延长,在缓冲盐释放介质中包衣膜出现不同程度的溶解,导致释放速率增大。包衣增重5%的处方在酸中释放较快,2 h内药物释放量达到60%以上,140 min后在磷酸盐中释放量达到90%以上;包衣增重15%的处方在酸中释放缓慢,在磷酸盐中释放不足70%;包衣增重10%的处方在酸中2 h内释放不超过10%,在缓冲盐介质释放实验中,药物达到肠溶的效果,160 min后药物释放达到90%以上。按照肠溶制剂的要求[7],肠溶制剂在酸中释放量不超过10%,在磷酸盐中释放不低于70%。因此包衣增重10%的微丸在肠道中溶解释放的效果最好。
挤出滚圆法是制备球形微丸一种比较理想的方法,其设备操作简单,生产能力强、成本低,制得的含药微丸载药量高[12]。红外图谱结果显示:A、B在3450 cm-1的位置出现强的-OH伸缩振动峰,但C中此特征峰消失,说明药物中的-OH被掩盖起来,同时在1050~1100 cm-1处,A、B中有明显的药物中六元单氧环的特征峰,但在C中此官能团的特征峰消失,初步证明了替米考星制成微丸后是以固体分散体的形成存在[13]。结合差示扫描量热分析实验结果,替米考星微丸图C与物理混合物图B相比,峰形发生比较大的变化,其中100℃左右的峰完全消失,也没有形成新峰,进一步证实替米考星以无定型固体共沉淀物的形式形成固体分散体。可能是在制备微丸过程中,药物经混合、制软材、挤出滚圆等一系列处方工艺后,药物高度分散在微丸中,以无定型固体共沉淀物的形式得到稳定的固体分散体,有利于药物的溶出[14]。结合释放度实验,在缓冲盐中药物释放量明显增大,可以达到肠溶释放的效果且有利于增加药物的吸收,提高药物的生物利用度。因此,本实验制备替米考星肠溶微丸的方法具有可行性。
[1]江海洋,沈建忠,胡顶飞.兽用抗菌药替米考星[J].中国兽药杂志,2002,36(8):28-31.
[2]何凤艳,邓旭明,刘明春,等.替米考星对内毒素炎症小鼠存活率和细胞因子的影响[J].中国兽医学报,2009,9(29):1186-1188.
[3]Florian Priese, Bertram Wolf.Development of high drug loaded pellets by Design of Experiment and population balance model calculation[J].Powder Technology,2013, 241: 149-157.
[4]X F Wang, S L Zhang, L Y.Enhancement of antibacterial activity of tilmicosin against Staphylococcus aureus by solid lipid nanoparticles in vitro and in vivo[J].The Veterinary Journal, 2012,1 (191):115-120.
[5]Fridrun Podczeck, John Michael Newton.Influence of the standing time of the extrudate and speed of rotation of the spheroniser plate on the properties of pellets produced by extrusion and spheronization[J].Advanced Powder Technolog.In Press, http://dx.doi.org/10.1016/j.apt.2013.10.011.
[6]P E Knight, F Podczeck, J M Newton.The rheological properties of modified microcrystalline cellulose containing high levels of model drugs[J].J Pharm Sci,2009, 98 : 2160-2169.
[7]中国药典国家药典委员会.中华人民共和国药典2010年版第二部附录[S].
[8]陈宝妮,冯宝仪,李美娣,等.替米考星肠溶微丸的质量评价[J].中国兽药杂志, 2010, 44(5): 19.
[9]Pan Chen.Novel compaction techniques with pellet containing granules[J].Eur J Pharm Biopharm,2010, 3(75): 436-442.
[10]李连闯,车文实.微丸成型工艺研究进展[J].安徽医科大学报,2013, 48(4): 453-455.
[11]李仲谨,韩春鹏,苗宗成,等.替米考星β-环糊精聚合物微球的制备与表征[J].安徽农业科学, 2011, 39(2):1067-1078.
[12]佟 杰,王东凯.罗红霉素包衣缓释微丸的体外释放研究[J].中国药剂学杂志,2005,3(1):6.
[13]杜向党,连明香,陈玉霞,等.恩诺沙星聚合物胶束的制备及体外释放[J].中国兽医学报,2012, 3(32):432-436.
[14]Akhgari A,Abbaspour M R,Moradkhanizadeh M.Combination of Pectin and Eudargit RS and Eudragit RL in the Matrix of PelletsPrepared by Extrusion-Spheronization for Possible Colonic Delivery of 5-Amino Salicylic Acid[J].Jundishapur Journal of Natural Pharmaceutical Products,2013, 8(2): 86-92.

