毛细管电泳法分离6种手性化合物
吕迎春,樊竹青,侯云洪
(普洱学院 生命科学系,云南普洱665000)
毛细管电泳(capillary electrophoresis,CE)是20世纪80年代崛起的一种分离分析技术。从1985年Gassmann E.[1]首次应用于手性分离以来,由于该技术具有分离效率高、分析时间短、样品耗费少等优点,已被迅速应用于手性分离[2-7]。环糊精分子呈笼状结构并含有多个手性中心,它能与客体分子形成超分子化合物,从而对客体分子产生多重的分子识别能力[8]。因此,环糊精类手性选择剂是目前毛细管电泳手性分离应用得最广的手性选择剂。
氧氟沙星属于第三代氟喹诺酮类广谱抗菌药,其分子结构中具有一个手性碳原子,从而产生S-(-)和R-(+)两种光学异构体。近年来研究证明,左旋氧氟沙星抗革兰氏阳性菌及阴性菌的活性是右旋的8~128倍,是氧氟沙星外消旋体的2倍[9],其不良反应比氧氟沙星外消旋体低。因此,获取抗菌能力强且毒副作用小的左氧氟沙星有着重要意义。布洛芬属于非甾体抗炎镇痛药,具有镇痛、退热等作用,它主要通过可逆性的抑制环氧化酶来抑制作为炎症介质的各种前列腺素的生成,起到解热镇痛抗炎的药理作用。其分子结构中在β位有一个手性碳原子,存在一对光学异构体S-构型和R-构型,其中只有S-布洛芬具有主要的生理活性作用,而R-构型不仅活性低且有副作用。
1 实验部分
1.1 仪器与试剂
CL1020高效毛细管电泳仪(UV紫外检测器波长范围190~700 nm)和HW-2000色谱数据工作站,北京彩陆科学仪器有限公司;未涂层熔融石英毛细管(50 cm×50 um,有效长度41 cm),河北永年光导纤维厂;羟丙基-β-环糊精(HP-β-CD)购于Sigma公司;氢氧化钠、磷酸均为国产分析纯试剂。实验所用6种对映体标准品均购于中国药品生物制品检定所。分子结构见图1。
1.2 实验方法
1.2.1 溶液的配制
将手性化合物分别溶于10 mmol/L NaOH溶液中,配制成浓度为4 mmol/L的溶液后进行超声溶解并保存于4℃环境中,在分析前再用背景电解质溶液进行适当稀释。
于70 mmol/L H3PO4溶液中加入pH分别为1.0、2.1、2.5、3.0、3.8、4.3、5.0、6.0 和 7.0 的缓冲溶液,将一定量的HP-β-CD溶于其中。样品和缓冲溶液用0.45 μm滤膜(水系)过滤,使用前在超声波上脱气5~10 min。
1.2.2 电泳条件
毛细管使用前分别用0.5 mol/L NaOH溶液、水及缓冲溶液各冲洗3 min。采用压力进样,进样压力 3.06 kPa,进样时间 3 s,分离温度25℃。

图1 6种手性化合物的结构Figure 1 Structures of 6 chiral compounds
2 结果与讨论
2.1 氧氟沙星对映体的分离
在分离氧氟沙星对映体时,如果背景电解质溶液的pH值大于4.3,则峰形变差。选择pH为2.1,羟丙基-β-环糊精的浓度为40 mmol/L,分离电压为10 kV,检测波长为254 nm时,可在短时间内对氧氟沙星实现手性分离且重现性好。
在利用毛细管电泳分离氧氟沙星对映体的基础上,将左旋的氧氟沙星标准品加入到其对映体混合物中,对其谱图进行研究分析表明:对映体出峰的顺序为S-(-)-氧氟沙星先出峰,R-(+)-氧氟沙星后出峰,如图2-A所示。
2.2 特布他林对映体的分离
羟丙基-β-环糊精的浓度为40 mmol/L,分离电压为10 kV,检测波长为210 nm,调节磷酸盐缓冲溶液的pH对出峰时间有明显影响。pH值为6.0的出峰时间明显比pH为2.5时的出峰时间短,其对应谱图分别为图2-B(1)、图2-B(2)所示。
2.3 克伦特罗对映体的分离
磷酸盐缓冲溶液pH值为2.5,羟丙基-β-环糊精溶液浓度为40 mmol/L,检测波长254 nm。调节电压分别为10、12、15 kV时,其CE谱图分别为2-C(1)、图2-C(2)和图2-C(3)所示。分析谱图显示随着电压的增大,出峰时间明显缩短,但峰高也变矮,因此选择电压12 kV时分离效果比较理想。
2.4 美托洛尔的分离
选取浓度为40 mmol/L的羟丙基-β-环糊精溶液,电压为10 kV,检测波长为204 nm时,研究了改变磷酸盐缓冲溶液(70 mmol/L)pH对美托洛尔对映体分离效果的影响。实验结果表明在pH值为6.0缓冲溶液环境下能实现美托洛尔的基线分离(图2-D)。
2.5 扁桃酸的分离
选择浓度为40 mmol/L的羟丙基-β-环糊精溶液,电压为15 kV,检测波长为206 nm时,改变磷酸盐缓冲溶液(70 mmol/L)pH分别为2.5、5.0、6.0、7.0时,对扁桃酸对映体分离的研究。结果显示磷酸盐缓冲溶液pH=6.0时,能实现对扁桃酸的分离(见图2-E)。
2.6 苯基丁二酸
选取浓度为40 mmol/L的羟丙基-β-环糊精溶液,电压为10 kV,检测波长为254 nm时,改变磷酸盐缓冲溶液(70 mmol/L)pH分别为2.5、5.0、6.0、7.0时,对扁桃酸对映体分离的研究。结果显示磷酸盐缓冲溶液pH=6.0时,能实现苯基丁二酸的手性分离(见图2-F)。
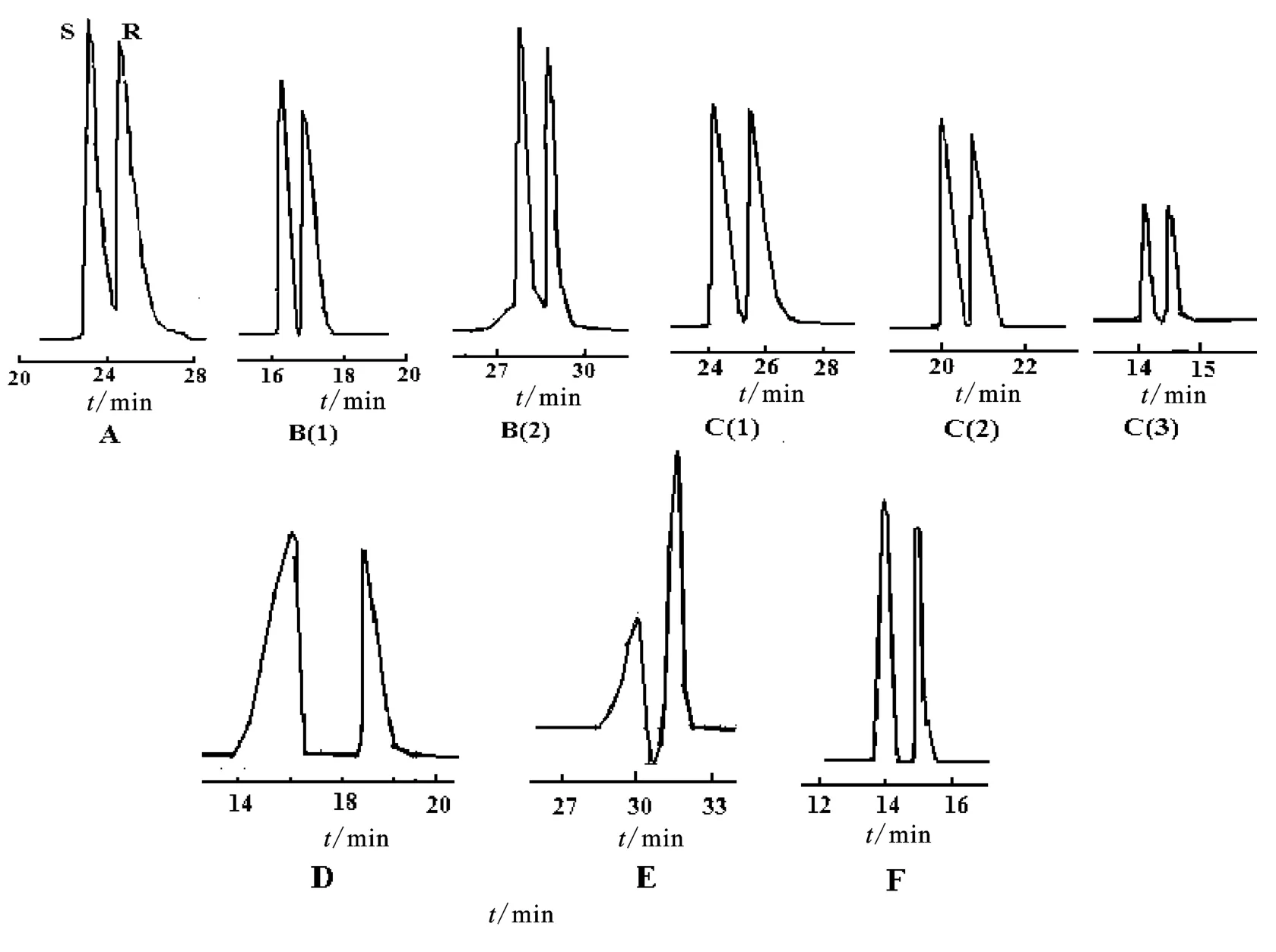
图2 各手性化合物拆分的电泳图Figure 2 Electropherograms of chiral compounds
3 结论
从上述结果得出,羟丙基-β-环糊精是一种理想的CE手性添加剂。以40 mmol/L的羟丙基-β-环糊精溶液、磷酸盐缓冲溶液(70 mmol/L)pH为6.0、电压10 kV,分离温度为25℃时,仅改变检测波长分别为254、210、204时,可同时实现苯基丁二酸、特布他林、美托洛尔等3种对映体的手性分离;以40 mmol/L的羟丙基-β-环糊精溶液,电压10 kV,分离温度为25℃,检测波长为254 nm时,仅改变磷酸盐缓冲溶液(70 mmol/L)pH值分别为2.1、2.5时就能实现氧氟沙星、克伦特罗的手性分离。因此,仅对少数影响分离条件的调整,即可实现几种对映体的分离,从而提高了工作效率。同时,氧氟沙星对映体出峰顺序的确定可为与氧氟沙星结构相似的对映体毛细管电泳分离提供定性分析的依据。
[1]Gassmann E,Kuo J E,Zare R N.Electrokinetic separation of chiral compounds[J].Science,1985,230:813-814.
[2]Arai T,Nimura N,Kinoshita T.Investigation of enantioselective ofloxacin-albumin binding and displacement interactions using capillary affinity zone electrophoresis[J].Biomedical chromatograpiiy,1995,9:68-74.
[3]Zhou S,Ouyang J,Baeyens W R,et al.Chiral separation of four fluoroquinolone compounds using capillary electrophoresis with hydroxypropyl-β-cyclodextrin as chiral selector[J].Chromatogr.A,2006,1130:296-301.
[4]王伟,张永利,董英茹,等.毛细管电泳法手性分离5种碱性药物[J].药物分析杂志,2007,27:1984-1987.
[5]俞犄,王义明,罗国安.俞氧氟沙星对映体的毛细管电泳手性分离[J].药学学报,1997,32:203-206.
[6]韦寿莲,邓光辉.手性药物的毛细管电泳拆分[J].分析测试学报,2007,26:907-910.
[7]Abushoffa A M,Fillet M,Hubert P,et al.Chiral separation of basic drugs capillary electrophoresis with carboxymethylcyclodextrins[J]. Chromatogr. A,2002,948:321-329.
[8]袁黎明.手性识别材料[M].北京:科学出版社,2010.
[9]Hayakawa I,Atarashi S,Yokohama S,et al.Synthesis and antibacterial activities of optically active ofloxacin[J].Antimicrob.Agents Chemother.,1986,29:163-164.

