奥美沙坦联合前列地尔对糖尿病伴微量白蛋白尿的干预分析
严连喜,周玉坤,李康峰
(第二军医大学长征医院南京分院肾内科,江苏南京,210015)
糖尿病肾病(DKD)病程长,因早期起病隐匿多不被重视和发现。根据Mogensen[1]分型,当患者出现临床大量蛋白尿,DKD处于临床Ⅳ期,为不可逆状态,肾小球滤过率(GFR)将以每月1 mL/min下降。因此,对临床出现微量白蛋白尿(mAlb)的Ⅲ期DKD的控制是延缓DKD进程最为关键的阶段。有实验已证实,奥美沙坦较其他ARB类药物有明显预防糖尿病伴微量白蛋白尿的作用[2]。本文探讨分析奥美沙坦联合前列地尔短期内治疗对糖尿病伴微量白蛋白尿的影响。
1 资料与方法
1.1 一般资料
选择2012年11月—2013年11月在本科室确诊为2型糖尿病(2次空腹血糖>7.0 mmol/L,餐后 2 h 血糖 >11.1 mmol/L[3])40 例伴高血压(血压大于140/90 mmHg)的患者,其中男18例,女22例。平均年龄(45.23±7.31)岁,同时排除消化道出血、脑出血等脏器出血疾病及感染状态。确诊糖尿病时间(4.34±2.31)年。所有患者行3次以上尿常规检查,尿蛋白定性:±~+。入选患者24h尿蛋白定量<1.0 g,尿比浊法测定晨尿mAlb均超标>20 mg/L(参考值0~20 mg/L)。
1.2 分组方法
将40例患者分为A组20例,单用奥美沙坦(第一三共制药)20 mg/d口服;B组20例奥美沙坦20 mg/d口服,联合前列地尔(本溪恒康制药)10μg/d稀释为20 mL生理盐水静脉注射。2组患者均排除肾功能异常,A组血肌酐(62.23±9.42)mol/L,B组血肌酐(58.68 ±10.16)μmol/L。入选患者均采用精蛋白锌重组赖脯胰岛素混和注射液控制血糖,优泌乐25/50(美国礼来公司)控制血糖达标。治疗时间2周。
1.3 临床数据检测及eGFR值计算
观察2组治疗前后晨尿 mAlb、计算 eGFR(K/DOQI推荐应用简化MDRD公式评估GFR值)[4]、血压、高敏 C 反应蛋白(hs-CRP)(正常范围0~10 mg/L)、凝血酶原时间(PT)(9~13 s),以及活化部分凝血活酶时间(APTT)(20~40 s)变化。
1.4 统计学处理
应用统计软件SPSS 13.0软件进行分析,所有数据均以均数±标准差表示。计数资料采用t检验,计量资料用χ2检验,P <0.05表示差异有统计学意义。
2 结果
2.1 2组患者治疗前后实验室指标比较
2组患者治疗前实验室检查肾功能及肾小球滤过率比较差异无统计学意义。经过短期(2周)治疗结果显示:A组可降低尿微量白蛋白,但差异无统计学意义;却可降低肾小球高灌注、高滤过状态,有效降低eGFR(P<0.05)。B组治疗2周疗程,则可显著降低尿微量白蛋白(P<0.01);改善肾小球高灌注、高滤过(P<0.01)。见表1。2组对糖尿病伴高血压治疗结果显示,对收缩压、舒张压干预的降压效果差异有统计学意义(P<0.01);对糖尿病微炎症状态影响,2组治疗前后hs-CRP的改变差异均有统计学意义(P<0.01);而对凝血功能影响差异无统计学意义。见表1。
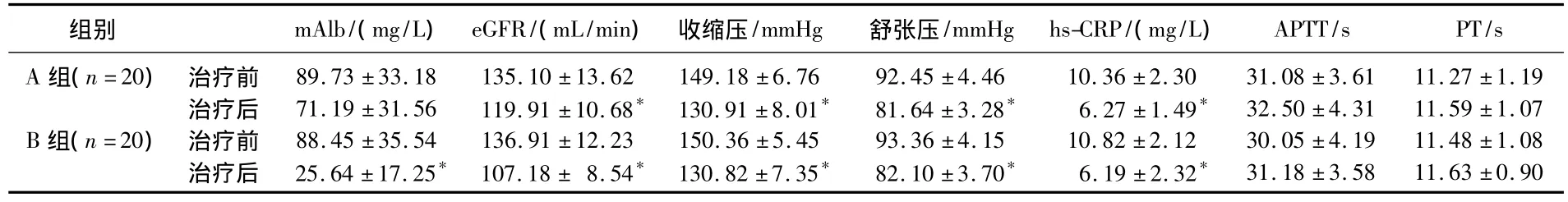
表1 2组患者治疗前后实验室指标的比较
2.2 2组不良反应发生情况
2周治疗观察期间,未见出血不良反应。其中B组1例在静脉注射前列地尔过程中出现注射部位的疼痛、潮红,经减慢推注速度、对症治疗后缓解。
3 讨论
微量白蛋白尿对于临床早期诊断糖尿病肾病或糖尿病合并慢性肾脏病具有很高的实用价值。尿微量白蛋白是指尿液中白蛋白一直处于20~200 mg/min的持续排泄浓度,或者晨尿的白蛋白量在20 ~200 mg/L 之间[5]。ROADMAP 研究[2]表明,目前不仅是对糖尿病伴微量白蛋白尿的治疗,而是重在预防,与目前的循证医学(EBM)理念相一致。由于公共卫生资源有限,对疾病的预防可以减轻对后续疾病治疗资源的浪费。本文观察在某种程度上是ROADMAP研究的延续,B组对糖尿病伴微量白蛋白尿的影响短期内可见其效果较A组明显,其原因可能在于糖尿病肾小球血流动力学异常除与肾素血管紧张素系统有关外,还与前列腺素代谢异常有关,即血栓素A2与前列环素平衡失调[6]。前列地尔是把前列腺素E1包裹在0.2μm脂微球内的新型靶向制剂,脂微球的包裹减少其在肺内的灭活,延迟了代谢,可高浓度聚集于肾小球,维持长时间靶向治疗的药效,更好地发挥效果[7]。血管紧张素转化酶抑制剂或血管紧张素受体抑制剂需要4~8周时间才能在肾脏的局部发挥抗RAS系统的作用。本研究A组虽然短期内尿微量白蛋白减少,但差异无统计学意义。而B组可在短期内减少尿微量白蛋白,体现出1+1>2的效应;对血压的控制及肾小球率过滤改变差异有统计学。前列地尔有抑制血小板活化、减少血小板聚抑制[8]、改善微循环的作用,但对PT、APTT无明显影响,即大大提高其临床适用范围,确保临床的安全性。此外,血管紧张素受体抑制剂对于糖尿病肾病的独立于降压之外的肾保护作用系其非血流动力学效应所致,但确切的机制目前仍不清楚[9-11]。本组观察发现,奥美沙坦或联合前列地尔对hs-CRP的改变差异有统计学意义,提示奥美沙坦独立于降压以外的降低尿微量白蛋白作用可能与改变微炎症状态有关。而2型糖尿病是一种亚临床型慢性炎症性疾病,慢性炎症是其持续进展的关键因素[12-13]。总之,奥美沙坦联合前列地尔对糖尿病伴微量白蛋白尿的治疗短期内既可以见其疗效,而且安全有效。其机制与传统血管紧张素受体抑制剂类药物可抑制肾素-血管紧张素系统(RAS),降低肾脏高灌注、高滤过。联合前列地尔除能抑制肾脏局部血小板聚集、改善肾脏局部高凝状态外,亦与奥美沙坦抑制微炎症,延缓糖尿病慢性炎症的进程相关。
[1]林善锬.糖尿病肾病[M].3版.北京:人民卫生出版社,2008:1414.
[2]Ritz E G,Viberti C L,Ruilope M A,et al.Determinants of urinary albumin excretionwithin the normal range in patients with type 2 diabetes:the Randomised Olmesartanand Diabetes Microaluminuria Prevention(ROADMAP)study[J].Diabetologia,2010,53(1):49.
[3]程桦.糖尿病[M].7版.北京:人民卫生出版社,2008:770.
[4]黄颂敏.糖尿病肾病[M].北京:人民卫生出版社,2008:70.
[5]Blouza S,DakMi S.Efficacy of low-dose oral sulodexide in the management of diabetic nephropathy[J].J Nephrol,2010,23(4):415.
[6]欧亚萍.前列地尔治疗糖尿病肾病蛋白尿的疗效观察[J].药物与临床,2008,5(20):75.
[7]王海燕.前列地尔对糖尿病肾病蛋白尿的影响[J].医学综述,2011,17(18):2843.
[8]邹继红,寿伟璋,阎福岭.前列地尔对糖尿病肾病尿清蛋白排泄率、血小板活化和血脂的影响[J].中国新药与临床杂志,2004,23(7):409.
[9]Brownlee M.The pathobiology of diabetic complications:a unifying mechanism[J].Diabetes,2005,54(6):1615.
[10]万军,王文耕,欧冬梅,等.依帕司他联合前列地尔治疗早期2型糖尿病肾病的疗效观察[J].实用临床医药杂志,2010,14(8):77.
[11]刘钢铁.前列地尔对早期糖尿病肾病血流变的影响[J].中华全科医学,2011,9(9):1404.
[12]陈云亚.前列地尔对早期糖尿病肾病患者血清相关炎症因子的影响[J].海南医学院学报,2013,19(12):1685.
[13]马咏梅,费小薇,徐邦奎.前列地尔联合甲钴胺治疗糖尿病周围神经病变的临床观察[J].实用临床医药杂志,2011,15(19):103.

