阿司匹林与氟尿嘧啶协同抑制结肠癌细胞生长增殖的机制研究*
刘 宇, 高 东, 钟静静, 万岩岩, 李翔英, 靳广毅, 王晓冬
氟尿嘧啶是一种目前临床上常用的广谱抗肿瘤药物,对结肠癌有较好的效果,对其它消化系统癌症、宫颈癌、卵巢癌等也有效[1-2]。氟尿嘧啶主要通过抑制脱氧胸苷酸合成酶,阻断脱氧尿苷酸甲基化转变为脱氧胸苷酸,进而干扰DNA的合成以发挥抗肿瘤效果,属于抗代谢类抗肿瘤药物。但氟尿嘧啶本身毒性较大,用药后患者易发生严重的不良反应,如骨髓抑制、胃肠道及神经系统损害等。阿司匹林是一种历史悠久的解热镇痛药,近年来研究表明阿司匹林能显著降低结肠癌、食管癌、前列腺癌、胰腺癌等肿瘤发病的危险性[3],并具有抑制结肠癌细胞生长增殖的作用[4]。本研究主要通过MTT法观察阿司匹林与氟尿嘧啶协同抑制结肠癌细胞生长增殖的作用,旨在采用低浓度的药物协同作用发挥药效并减低不良反应,并且通过Hoechst染色、caspase活性测试、流式细胞术、real-time PCR、Western blotting等方法探讨其作用机制,为今后可能的临床应用奠定基础。
材料和方法
1 主要试剂
阿司匹林、氟尿嘧啶、噻唑蓝(MTT)、二甲亚砜(DMSO)和碘化丙啶(PI)购自 Sigma-Aldrich;Hoechst 33258、casapse-3、caspase-8、caspase-9 试剂盒和BCA蛋白定量试剂盒购自碧云天生物技术有限公司;RNA提取试剂盒和实时荧光定量PCR试剂盒(SYBR Premix Ex Taq)购自 TaKaRa;Bcl-2、Bax、βactinⅠ抗及相应Ⅱ抗购自Santa Cruz;RPMI-1640培养基和胎牛血清购自HyClone,其它常规试剂均为国产分析纯。
2 细胞培养和实验分组
人结肠癌细胞株HCT-116和SW620为本实验室保藏并常规传代培养,生长于含有10%灭活胎牛血清、青霉素(1×105U/L)和链霉素(100 mg/L)的RPMI-1640培养基中,于37℃、5%CO2、饱和湿度的培养箱内培养;细胞常规每3~4 d传代1次,所有实验采用对数生长期细胞。
体外培养的结肠癌细胞分成4组进行处理:空白对照组(control group),用RPMI-1640完全培养基进行培养;阿司匹林组(aspirin group),用含 100 μmol/L阿司匹林的培养基进行培养;氟尿嘧啶组(5-fluorouracil,5-Fu),用含 0.3、1、3、10、30 或 100 μmol/L氟尿嘧啶的培养基进行培养;氟尿嘧啶+阿司匹林组(5-Fu+aspirin),用同时含有不同浓度的氟尿嘧啶与100 μmol/L阿司匹林的培养基进行培养。
3 方法
3.1 MTT法 HCT-116或SW620细胞常规胰酶消化成单细胞悬液,1×108/L细胞接种于96孔板,培养箱内孵育过夜;次日每孔加入含100 μmol/L阿司匹林和0.3、1、3、10、30、100 μmol/L 氟尿嘧啶的培养基;作用一定时间后,每孔加入5 g/L MTT 20 μL,继续孵育4 h,弃上清每孔加入100 μL DMSO,室温振荡摇匀,酶标仪检测490 nm处吸光度,并计算不同药物作用下细胞的存活率。
3.2 Hoechst 33258染色法 1×108/L HCT-116细胞接种于24孔板,加入含100 μmol/L阿司匹林和1、3、10、30、100 μmol/L 氟尿嘧啶的培养基作用48 h 后,弃上清,4%甲醛固定10 min;弃上清,Hoechst 33258染色5 min;荧光显微镜观察细胞核状态并拍照。
3.3 Caspase-3、-8、-9活性的检测 1×108/L HCT-116细胞接种于6孔板,加入含100 μmol/L阿司匹林和1、3、10、30、100 μmol/L 氟尿嘧啶的培养基作用48 h后,收集细胞,并按照试剂盒操作说明进行活性检测。
3.4 流式细胞术 1×108/L HCT-116细胞接种于6孔板,加入含100 μmol/L阿司匹林和100 μmol/L氟尿嘧啶的培养基作用48 h后,收集细胞,PBS洗涤并重悬,加入RNase A 37℃作用30 min,再加入PI于4℃作用30 min,流式细胞术检测细胞周期。
3.5 Real-time PCR 1×108/L HCT-116细胞接种于6孔板,加入含100 μmol/L阿司匹林和100 μmol/L氟尿嘧啶的培养基作用48 h后,收集细胞提取RNA并逆转录成cDNA。实时荧光定量PCR按照试剂盒操作说明进行,引物序列见表1,具体反应条件为:预变性95 ℃ 1 min,95 ℃ 15 s,59 ℃ 20 s,40 个循环。不同样本目的基因表达的相对差异量用2-ΔΔCt法计算。
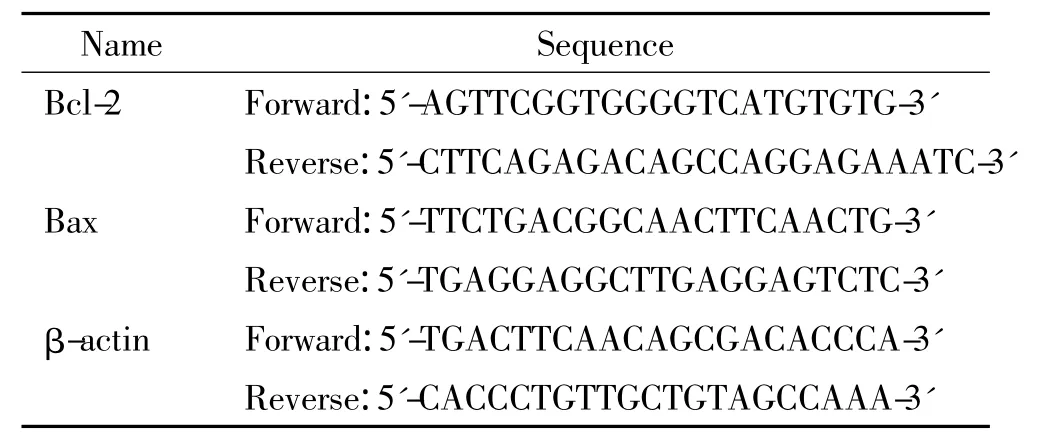
表1 引物序列Table 1.Sequences of the primers
3.6 Western blotting 1×108/L HCT-116细胞接种于6孔板,加入含100 μmol/L阿司匹林和100 μmol/L氟尿嘧啶的培养基作用48 h后,收集细胞,提取总蛋白并用BCA法进行蛋白定量。样品于SDS-PAGE分离后转印至PVDF膜上,5%BSA封闭1 h,Ⅰ抗4℃过夜,Ⅱ抗1 h,ECL法显色。
4 统计学处理
数据均用数±标准差(mean±SD)表示,采用SPSS 17.0统计软件分析,组间均数比较采用t检验或方差分析,以P<0.05为差异有统计学意义。
结 果
1 阿司匹林与氟尿嘧啶协同抑制结肠癌细胞生长增殖
单独应用氟尿嘧啶对HCT116细胞的生长增殖具有抑制作用,且作用效果呈时间及浓度依赖性。单独应用100 μmol/L阿司匹林对HCT116细胞增殖没有明显的抑制效果,但将100 μmol/L阿司匹林与不同浓度的氟尿嘧啶协同应用于HCT116细胞时,细胞增殖能力被更有效地抑制,且此种协同抑制同样具有时间及浓度依赖性,见图1及表2。同时,协同应用阿司匹林与氟尿嘧啶于SW620结肠癌细胞时,出现相似的实验结果,见表2。

Figure 1.Changes of HCT116 cell viability after treatment with various concentrations of 5-Fu and 100 μmol/L aspirin for 24,48 and 72 h.Mean±SD.n=3.*P<0.05 vs control group;#P<0.05 vs 5-Fu group.图1 5-Fu与阿司匹林对HCT116细胞存活率的影响

表2 5-Fu单独作用或在阿司匹林协同下对结肠癌细胞增殖的IC50值Table 2.The IC50values of 5-Fu alone or combined with aspirin(100 μmol/L)for the proliferation of colon cancer cell lines(μmol/L.Mean±SD.n=3)
2 阿司匹林与氟尿嘧啶协同诱导结肠癌细胞出现凋亡形态
HCT116细胞用Hoechst 33258染色后通过荧光显微镜观察可见,未经处理组活细胞核呈均匀荧光,药物处理组则表现出不同程度的浓染致密颗粒状荧光,即发生细胞凋亡的典型特征。单独应用100 μmol/L氟尿嘧啶48 h后可见凋亡形态,单独应用30 μmol/L氟尿嘧啶则凋亡形态不明显。不同浓度氟尿嘧啶与100 μmol/L阿司匹林协同作用48 h后,细胞核皱缩碎裂、染色质浓缩等凋亡形态均更加显著,见图2。

Figure 2.Nuclear morphology of HCT116 cells treated with 5-Fu and aspirin for 48 h (Hoechst 33258 staining,×200).A:control;B:30 μmol/L 5-Fu;C:30 μmol/L 5-Fu+100 μmol/L aspirin;D:100 μmol/L 5-Fu;E:100 μmol/L 5-Fu+100 μmol/L aspirin.图2 5-Fu与阿司匹林对HCT116细胞核形态的影响
3 阿司匹林与氟尿嘧啶协同应用激活结肠癌细胞caspase酶活性
HCT116细胞用不同浓度氟尿嘧啶刺激48 h后,caspase-3、-8、-9酶活性均有所提高,且活性增强呈浓度依赖性,但单独应用100 μmol/L阿司匹林则对caspase酶活性几无影响。100 μmol/L阿司匹林与氟尿嘧啶协同应用后,相对于单用氟尿嘧啶,细胞的caspase酶活性明显增加。100 μmol/L氟尿嘧啶与阿司匹林合用后,caspase-3、-8、-9酶活性分别由1.7、3.2和2.8倍提高到2.2、4.0和3.4倍,见图3。
4 阿司匹林与氟尿嘧啶协同应用影响结肠癌细胞周期
HCT116细胞药物作用48 h后,流式细胞术检测发现100 μmol/L氟尿嘧啶显著提高了sub-G1及S期的比例。单用100 μmol/L阿司匹林对细胞周期无明显影响。100 μmol/L阿司匹林与氟尿嘧啶协同作用后,与单用氟尿嘧啶相比,细胞凋亡(sub-G1期)比例有所增加,G0/G1期及S期变化则无显著差异,见图4、表3。
5 阿司匹林与氟尿嘧啶协同应用影响Bcl-2和Bax mRNA水平
如图5所示,单独应用阿司匹林对Bcl-2 mRNA水平无明显影响,单独应用氟尿嘧啶则抑制Bcl-2 mRNA水平,2种药物协同应用更显著下调 Bcl-2 mRNA水平,但阿司匹林和氟尿嘧啶对Bax mRNA水平均无明显影响。
6 阿司匹林与氟尿嘧啶协同应用影响Bcl-2和Bax蛋白表达
如图6所示,单独应用阿司匹林对蛋白表达无明显影响,单独应用氟尿嘧啶抑制Bcl-2表达,协同应用后抑制Bcl-2表达效果更显著,但2种药物对Bax表达水平无明显影响。
讨 论

Figure 3.Changes of caspase-3,caspase-8 and caspase-9 activity in HCT116 cells after 5-Fu treatment for 48 h with or without 100 μmol/L aspirin.Mean ± SD.n=3.*P<0.05 vs control group;#P<0.05 vs 5-Fu group.图3 5-Fu与阿司匹林对HCT116细胞caspase酶活性的影响
氟尿嘧啶和阿司匹林是临床上常用的2种药物。氟尿嘧啶主要用于治疗结肠癌在内的多种肿瘤,且文献显示氟尿嘧啶可以诱发肿瘤细胞凋亡以达到抗肿瘤的效果[5]。阿司匹林是一种常用的非甾体抗炎药,主要临床作用为解热、镇痛、抗炎等。近期研究发现阿司匹林可以预防结肠癌等肿瘤发生,且对肿瘤细胞凋亡也有一定的影响[6-7]。已有文献报道将阿司匹林与氟尿嘧啶联合应用于HT-29结肠癌细胞,通过诱发凋亡取得较好的肿瘤抑制效果[8]。本课题则将2种药物联合应用于HCT116及SW620结肠癌细胞,证明2药均采用较低的药物浓度可以达到单药高浓度时的抑制肿瘤效果,并研究其相关机制。另外,之前研究结果仅证明无明显细胞毒性的低浓度氟尿嘧啶与高浓度阿司匹林联合应用的效果,而本研究则主要探讨低浓度阿司匹林对氟尿嘧啶毒性的增强作用。

Figure 4.The cell cycle of HCT116 cells after treatment with 100 μmol/L 5-Fu or 100 μmol/L aspirin for 48 h.Debris represented the apoptotic cells(sub-G1phase).A:control;B:100 μmol/L aspirin;C:100 μmol/L 5-Fu;D:100 μmol/L 5-Fu+100 μmol/L aspirin.图4 5-Fu与阿司匹林对HCT116细胞周期的影响

表3 5-Fu与阿司匹林对HCT116细胞周期的影响Table 3.Effects of 5-Fu and aspirin on cell cycle of HCT116 cells(%.Mean±SD.n=3)

Figure 5.Relative mRNA expression levels of Bcl-2 and Bax in HCT116 cells after treatment with 100 μmol/L 5-Fu or 100 μmol/L aspirin for 48 h.Mean ±SD.n=3.*P <0.05 vs control group;#P<0.05 vs 5-Fu group.图5 5-Fu与阿司匹林影响Bcl-2和Bax mRNA的表达
阿司匹林采用对细胞生长增殖几乎没有影响的浓度(100 μmol/L)与氟尿嘧啶协同应用,结果表明与单用氟尿嘧啶相比,抑制HCT116和SW620结肠癌细胞增殖的效果明显增强,IC50显著降低,且上述效果具有时间和浓度依赖性。Hoechst 33258染色及流式细胞术检测发现100 μmol/L阿司匹林协同作用后,氟尿嘧啶可以诱发HCT116细胞产生更明显的凋亡形态(细胞核皱缩、碎裂等)及细胞凋亡(sub-G1期)比例增加,越高浓度的氟尿嘧啶诱发凋亡的作用越明显。另外,氟尿嘧啶是一种周期特异性药物,可以将肿瘤细胞有效阻滞在S期[9]。阿司匹林也有报道较大浓度时诱导肿瘤细胞G0/G1期比例增高[10]。流式细胞术检测结果发现氟尿嘧啶作用下,HCT116细胞的S期比例确有明显提高。但低浓度阿司匹林协同作用对于S期及G0/G1期比例没有明显效果,即2种药物协同杀伤HCT116细胞的主要作用机制在于诱发细胞凋亡,协同影响S期、G0/G1期效果甚微。

Figure 6.Relative protein expression levels of Bcl-2 and Bax in HCT116 cells after treatment with 100 μmol/L 5-Fu or 100 μmol/L aspirin for 48 h.Mean ± SD.n=3.*P<0.05 vs control group;#P<0.05 vs 5-Fu group.图6 5-Fu与阿司匹林影响Bcl-2和Bax蛋白的表达
经典的细胞凋亡包括外源性途径和内源性途径两种,外源性途径(死亡受体途径)caspase级联反应包括上游凋亡启动因子caspase-8和下游凋亡执行因子caspase-3,内源性途径(线粒体途径)则包括上游凋亡启动因子caspase-9和下游凋亡执行因子caspase-3[11]。已有文献表明氟尿嘧啶可以通过上述2种途径诱发肿瘤细胞凋亡[12-13]。Caspase活性测试结果表明,单用氟尿嘧啶导致HCT116结肠癌细胞caspase-3、-8、-9 激活,协同应用 100 μmol/L 阿司匹林后caspase-3、-8、-9活性更为提高,且此种激活能力具有浓度依赖性。Bcl-2蛋白家族是调控细胞凋亡的主要因素之一,包括以Bcl-2为代表的抗凋亡蛋白和以Bax为代表的促凋亡蛋白。Bax主要负责在线粒体的外膜上形成通透性转运孔道,使细胞色素C等物质进入细胞质并引发凋亡,Bcl-2则可以结合并抑制促凋亡蛋白,使凋亡不会发生[14]。Real-time PCR及Western blotting检测证明氟尿嘧啶抑制抗凋亡bcl-2基因的转录及翻译,进而诱导HCT116细胞发生凋亡,且阿司匹林具有协同效果,但药物对于促凋亡bax基因则影响微弱。
上述实验表明在无明显细胞毒性的低浓度阿司匹林作用下,氟尿嘧啶诱发结肠癌细胞凋亡的作用显著增强,且外源性及内源性凋亡途径均发挥效果。两药合用的抗肿瘤效果与抑制Bcl-2表达呈正相关,但与Bax表达无明显关系。总之,氟尿嘧啶和阿司匹林可以通过诱发细胞凋亡途径,协同发挥抑制结肠癌细胞生长增殖的效果。
[1] Chue AL,Fernando IN,Hussain SA,et al.Chemotherapy related encephalopathy in a patient with Stage IV cervical carcinoma treated with cisplatin and 5-fluorouracil:a case report[J].Cases J,2009,2:8526.
[2] Lee HJ,Kim HS,Park NH,et al.Feasibility of oxaliplatin,leucovorin,and 5-fluorouracil(FOLFOX-4)chemotherapy in heavily pretreated patients with recurrent epithelial ovarian cancer[J].Cancer Res Treat,2013,45(1):40-47.
[3] Sutcliffe P,Connock M,Gurung T,et al.Aspirin for prophylactic use in the primary prevention of cardiovascular disease and cancer:a systematic review and overview of reviews[J].Health Technol Assess,2013,17(43):1-253.
[4] Pathi S,Jutooru I,Chadalapaka G,et al.Aspirin inhibits colon cancer cell and tumor growth and downregulates specificity protein(Sp)transcription factors[J].PLoS One,2012,7(10):e48208.
[5] Wyatt MD,Wilson DM 3rd.Participation of DNA repair in the response to 5-fluorouracil[J].Cell Mol Life Sci,2009,66(5):788-799.
[6] Jana NR.NSAIDs and apoptosis[J].Cell Mol Life Sci,2008,65(9):1295-1301.
[7] Raza H,John A,Benedict S.Acetylsalicylic acid-induced oxidative stress,cell cycle arrest,apoptosis and mitochondrial dysfunction in human hepatoma HepG2 cells[J].Eur J Pharmacol,2011,668(1-2):15-24.
[8] Ashktorab H,Dawkins FW,Mohamed R,et al.Apoptosis induced by aspirin and 5-fluorouracil in human colonic adenocarcinoma cells[J].Dig Dis Sci,2005,50(6):1025-1032.
[9] 朱玉萍,何 超,朱洪波,等.结肠癌细胞获得性5氟尿嘧啶耐药的机制研究[J].中国病理生理杂志,2007,23(10):2007-2011.
[10]李 盛,严 浩,黄志琨.阿司匹林诱导人宫颈癌He-La细胞凋亡及机制[J].中国医院药学杂志,2012,32(9):675-678.
[11] Xu G,Shi Y.Apoptosis signaling pathways and lymphocyte homeostasis[J].Cell Res,2007,17(9):759-771.
[12] Can G,Akpinar B,Baran Y,et al.5-Fluorouracil signaling through a calcium-calmodulin-dependent pathway is required for p53 activation and apoptosis in colon carcinoma cells[J].Oncogene,2013,32(38):4529-4538.
[13]Lei X,Lv X,Liu M,et al.Thymoquinone inhibits growth and augments 5-fluorouracil-induced apoptosis in gastric cancer cells both in vitro and in vivo[J].Biochem Biophys Res Commun,2012,417(2):864-868.
[14] Shamas-Din A,Kale J,Leber B,et al.Mechanisms of action of Bcl-2 family proteins[J].Cold Spring Harb Perspect Biol,2013,5(4):a008714.

