新型查尔酮类衍生物的合成
侯 玲,李依南,刘若灿,张 波,杨 迪,蔡志强
(沈阳工业大学石油化工学院,辽宁辽阳 111003)
查尔酮类化合物是广泛存在于植物界中的一类天然产物,尤其是甘草、红花等植物中含量较高。研究发现该物质是一类具有多种生物活性的化学物质,具有抗心血管疾病活性、抗炎活性、抗寄生虫活性、抗氧化活性、抗血小板凝聚活性、抗肝脏病毒活性、抗菌活性及抗肿瘤活性等[1-4]特性,同时也是植物体内合成黄酮类化合物的重要物质。
已有研究证实查尔酮类化合物具有能抑制细胞信号传导过程的酪氨酸蛋白激酶、细胞周期蛋白激酶等的活性,另外在体外、体内药理筛选实验中也具有显著抑制肿瘤细胞的增殖、诱导肿瘤细胞凋亡、对正常细胞毒性轻微等特点[5]。为此,近几年,有关查尔酮类化合物抗肿瘤作用的研究受到国内外专家、学者的广泛关注。
查尔酮类化合物结构简单,其基本化学结构为1,3-二苯基-2-丙烯-1-酮(见下式)。
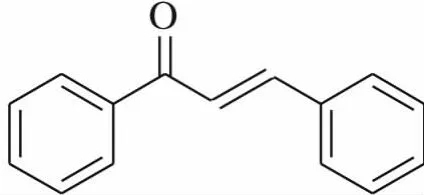
其衍生物主要是在两个苯环上引入不同的取代基或使碳链局部发生改变(羰基、双键、环化等)[6]。本文设计的目标化合物1,3-二苯基-4-羟基-2-丁烯-1-酮相当于在查尔酮基本结构的β位引入一个羟甲基,文献[7]中报道了具有类似 1,3-二苯基-4-羟基-2-丁烯-1-酮化合物母核结构的查尔酮衍生物有望成为抗HIV药物的先导化合物,因此,本文设计并合成此化合物,并对其必需的中间体进行了工艺优化。
1 实验部分
1.1 试剂与仪器
苯乙酮、无水乙醇、氯化亚砜(SOCl2)、过氧化苯甲酰(BPO)、N-溴代丁二酰亚胺(NBS)、乙酸钠、乙酸乙酯、石油醚均为分析纯。
X-4显微熔点测定仪;ZF-20D暗箱式紫外分析仪;DF-101B集热式恒温加热器;Bruker ARX-400 NMR型核磁共振仪(DMSO-d6为溶剂,TMS为内标);Agient 1100四级杆液质联用仪;Perkin-Elmer Spcetrum-FTIR型红外光谱仪(KBr压片)。
1.2 实验方法
为完成目标产物的合成,合成路线如下:
上述工艺中较难控制的操作是苯乙酮的自身缩合反应,因其在发生两分子缩合的主产物同时,还会发生三分子缩合的副产物[8]。为此如何控制缩合反应条件是本文研究重点。
1.2.1 (E)-1,3-二苯丁-2-烯-1-酮的合成[9-10]将苯乙酮、无水乙醇加入圆底烧瓶中,室温搅拌,缓慢滴加二氯亚砜与无水乙醇混合液。反应一定时间,TLC检测。当反应结束时,加入饱和Na2CO3溶液,用乙酸乙酯萃取2次,合并有机相,无水硫酸镁干燥,蒸干溶剂,所得固体柱层析纯化,得到淡黄色油状液体(E)-1,3-二苯丁-2-烯-1-酮。
1.2.2 (Z)-4-溴-1,3-二苯丁-2-烯-1-酮的合成 将(E)-1,3-二苯丁-2-烯-1-酮(11.10 g,50 mmol)、N-溴代丁二酰亚胺(8.9 g,50 mmol)、过氧化苯甲酰(0.30 g,1.2 mmol)溶解在50 mL 的四氯化碳中,加热回流,反应5 h,冷却至室温,过滤,蒸干溶剂。加入水和二氯甲烷萃取3次,合并有机相,无水硫酸镁干燥,蒸干溶剂。残余物经柱层析纯化[石油醚∶乙酸乙酯=1∶100],得到淡黄色针状晶体(Z)-4-溴-1,3-二苯丁-2-烯-1-酮 3.5 g,收率为23.27%。m.p.96~98℃,FTIR:1 620 cm-1(— C C—),1 695 cm-1(— C O),1H NMR(CDCl3,400 MHz)δ:5.02(s,2H,CH2),7.040 ~8.05(m,11H,ArH),ESI-MS(m/z):301[M+H]+。
1.2.3 (Z)-4-羟基-1,3-二苯丁-2-烯-1-酮的合成将 (Z)-4-溴-1,3-二 苯 丁-2-烯-1-酮 (2.5 g,8.3 mmol)和乙酸钠(1.37 g,16.6 mmol)的无水甲醇(30 mL)溶液置于100 mL单口瓶中,加热回流反应过夜。蒸干溶剂,加水和二氯甲烷萃取3次,合并有机相,无水硫酸镁干燥,蒸干溶剂。残余物经柱层析纯化(石油醚∶乙酸乙酯=1∶20),得到淡黄色油状物(Z)-4-羟基-1,3-二苯丁-2-烯-1-酮 0.20 g,收率为10.11%。FTIR:1 601 cm-1(— C C—),1 684 cm-1(— C O),1H NMR(CDCl3,400 MHz)δ 5.50(s,2H,CH2),7.16 ~7.57(m,9H,ArH),8.00~8.01(d,J=4 MHz,2H,ArH);ESI-MS(m/z):239[M+H]+。
2 结果与讨论
2.1 SOCl2加入量对羟醛缩合反应的影响
SOCl2加入量对羟醛缩合反应的影响见表1。

表1 SOCl2加入量对产品收率的影响Table1 Effect of thionyl chloride on yield
由表1可知,催化剂SOCl2加入量(或物料比)对反应取向有很大影响,随着SOCl2的增多,收率增大,但加入量过多会导致副反应产物(1,3,5-三苯基苯)明显增加。故适宜的物料摩尔比是苯乙酮∶氯化亚砜接近 1.2∶1。
2.2 温度和时间对羟醛缩合反应的影响
温度和时间对羟醛缩合反应的影响见表2。

表2 温度和时间对产品收率的影响Table2 Effect of reaction temperature and time on yield
由表2可知,温度和时间对反应的主、副产物含量的影响较大,通过实验研究表明,较为适宜的温度是15℃,反应时间30 min。
3 结论
查尔酮衍生物(Z)-1,3-二苯基-4-羟基-2-丁烯-1-酮的合成可采用以下合成工艺:①SOCl2作催化剂,室温,苯乙酮与SOCl2摩尔比1.2∶1进行自身羟醛缩合;②缩合产物经柱层析纯化后,在BPO引发下,用等摩尔NBS溴代;③溴代产物与乙酸钠按1∶2摩尔比,加热发生水解生成目标产物。在上述工艺合成中苯乙酮易发生三分子自身羟醛缩合反应,生成1,3,5-三苯基苯副产物,条件较难控制,因此对此步反应进行了工艺优化,最佳反应条件为∶n(苯乙酮)∶n(氯化亚砜)=1.2∶1,反应温度为室温,反应时间为30 min,此时缩合产物收率达72%。
[1] 潘元,梁桂兆,杨善彬,等.查耳酮类似物的抗结核分支杆菌3D-QSAR 研究[J].分子科学学报,2009,25(1):5-9.
[2] 石玉,李祎亮,刘巍,等.2-羟基查耳酮类衍生物的合成与抗肿瘤活性筛选[J].现代药物与临床,2010,25(1):48-54.
[3] 关晓,姚伯龙.查尔酮类化合物药理作用研究进展[J].广东化工,2012,40(7):23-28.
[4] 方线文,周丽珍,成昭,等.含氮芥基查尔酮类衍生物的合成、晶体结构及抗肿瘤活性[J].有机化学,2013,33:523-529.
[5] 张爱平,郝娟,黄茜,等.三种查尔酮类化合物与人血清白蛋白相互作用及其构效关系研究[J].分析科学学报,2013,29(1):73-77.
[6] 张爽,刘新泳.查耳酮衍生物的结构修饰及生物活性研究进展[J].药学进展,2012,36(6):241-251.
[7] 高复兴,薛灵芬,陈光辉,等.取代羟基查尔酮化合物的合成与表征[J].化学世界,2012,5:294-296.
[8] 胡志国,刘军,董志兵,等.1,3,5-三苯基苯的简单合成方法[J].化学通报,2004,9:700-703.
[9] Jorn H H,Brendan T P,Philip P,et al.Rhodium(Ⅱ)-catalyzed cross-coupling of diazo compounds[J].Angew Chem Int Ed,2011,50(11):2544-2548.
[10] Yasuhiro N,Hisashi Y.Iron-catalyzed asymmetric epoxidation of β,β-disubtituted enones[J].J Am Chem Soc,2011,133(22):8432-8435.

