分散液-液微萃取分光光度法联用测水中铅
唐祝兴,朱 娜
(沈阳理工大学环境与化学工程学院,辽宁沈阳 110159)
引 言
铅是一种可以在人体内沉积的有毒重金属元素,在人体内起不到任何的生理作用,当人们的生活水平与科技水平日益的增高,铅的应用也越来越广泛,运输、涂料、农药和器皿中都可能存在铅的身影,使得空气、食品和水都受到严重的重金属污染。长期存在物质表面的铅很容易进入人的体内,并在体内积累[1],当人体内铅的含量达到一定量时,人的组织器官就会出现非正常反应,如贫血、神经紊乱、肾功能减退甚至诱发癌症,当儿童血液中铅质量浓度大于100μg/L时就会对身体造成伤害[2]。
因此,建立一种新的能够快速准确检测分析水中铅的方法具有重要的意义。目前,已有很多采用分光光度法、原子吸收光度法或原子荧光法等[3]对水中的铅进行分析检测。但是,随着科学水平不断提高,样品中铅的含量有时是微量,甚至是痕量的,对分析方法的要求也越来越高。因此,直接使用这些仪器分析复杂样品中的铅面临许多的问题,主要原因为检出限不够低。
为了提高检测分析方法的灵敏度和选择性,就要选择高效的前处理技术进行分离富集,分散液-液微萃取(DLLME)技术是以液相微萃取为基础而发展起来的一种新型分离富集方法[4],分散液-液微萃取技术就是采用极少量的萃取剂进行萃取,并使用分散剂使萃取剂在溶液中能够均匀的分散开,由于萃取剂分散成极小的液滴增大了萃取剂的表面积[5-6],使萃取剂与分析物的接触面积增大,这样使用极少的萃取剂就能快速的萃取更多的样品,通过离心沉淀,使已经分散开的萃取剂沉积到离心管底部,由于分散剂的作用提高了萃取剂的有效表面积,因此分散液-液微萃取有很好的富集倍数和萃取效率[7]。分光光度法分析具有操作简单、检测速度快等优点,本文把液液分散微萃取技术与分光光度法联用测定水中铅,目的是建立一种新的方法能够快速准确的检测环境水中微量铅。
1 实验部分
1.1 试剂
硝酸铅、2-[(5-溴-2-吡-)]偶氮-5-二乙氨基苯酚(5-Br-PADAP)、四硼酸钠、氢氧化钠、无水乙醇、甲醇、丙酮、四氯化碳、三氯甲烷、乙腈、盐酸,所有试剂均为分析纯。实验所用蒸馏水为二次蒸馏水。
1g/L铅储备液、0.2g/L铅标准工作液、1g/L 5-Br-PADAP溶液、0.2g/L 5-Br-PADAP溶液、硼砂-盐酸缓冲溶液、硼砂-氢氧化钠缓冲溶液。
1.2 实验仪器
721E型可见分光光度计(上海光谱仪器有限公司)、800型离心沉淀器(上海手术器械厂)、KQ3200E型超声清洗器(昆山市超声仪器有限公司)。
1.3 实验方法
移取0.2mL铅的标准工作液于10mL离心管中,依次加入0.6mL pH 为9.0的缓冲溶液,0.4mL 0.2g/L 5-Br-PADAP溶液,用蒸馏水稀释至10mL,静置 1min,加入 0.1mL CCl4,0.3mL 乙醇溶液,萃取1min,在3500r/min的转速下离心3min,移去上层清液,用甲醇将管底的沉淀物稀释至4mL,超声振动,成均一透明液体,用可见分光光度计,在波长为570nm处测定。
2 实验结果与讨论
2.1 最大吸收波长的确定
取两支离心管,按照1.3中实验方法操作,其中一支不加入CCl4和CH3CH2OH,萃取1min,离心沉淀。将离心后的溶液取出,移去上层清液,将管底的沉淀物以甲醇稀释至4mL,以超声振动摇匀,移至可见分光光度计,以蒸馏水为参比,在470~700nm范围测定其吸光度。结果如图1所示,最大吸收峰出现在λ=570nm处,即最大吸收波长为570nm。
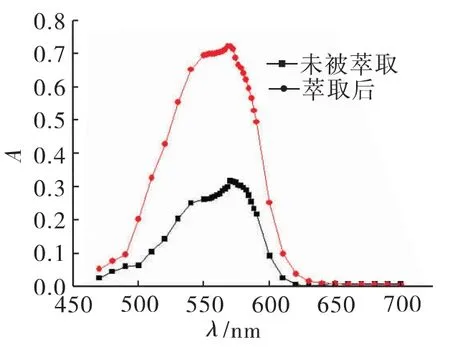
图1 吸收曲线
2.2 螯合剂用量的确定
在分散液-液微萃取的实验中,铅离子先与螯合剂反应生成螯合物,疏水的螯合物在萃取过程中,容易被萃取剂萃取出来,螯合剂也可以作为铅离子的显色剂,因此,螯合剂的用量,直接影响铅离子的萃取效率和分光光度法信号的强弱程度,按照1.3实验方法操作,只是改变螯合剂的用量,分别加入0.1、0.2、0.3、0.4、0.5 和 0.6mL 质量浓度为0.2g/L的5-Br-PADAP溶液,考察螯合剂的用量与吸光度的关系,结果如图2所示。由图2可以看出,当螯合剂小于0.5mL时,吸光度随着螯合剂的增加而增加,当螯合剂为0.5mL时吸光度达到最大,当螯合剂大于0.5mL时吸光值趋于平稳。因此,实验螯合剂最佳为0.5mL。
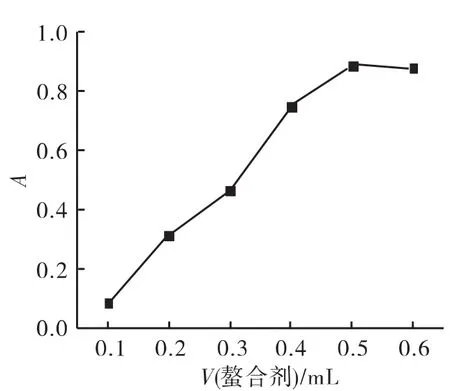
图2 螯合剂用量与吸光度关系
2.3 萃取剂选择与用量的确定
萃取剂的选择对液液萃取的效率有重要的影响,萃取剂应满足难溶于水,对待测离子不产生干扰,并且对待萃取物有较好的萃取能力。按照1.3实验方法,考察了CCl4、CHCl3对萃取效率的影响,结果如表1。由表1可以看出CCl4有更好的萃取效果。
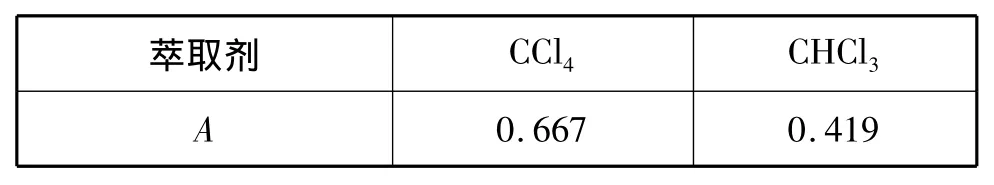
表1 萃取剂的种类与吸光度的关系
再按照1.3实验方法改变CCl4的用量,测定吸光度值,结果如图3所示。当萃取剂低于0.1mL时,吸光度与萃取剂用量成正比,当萃取剂达到0.1mL时,吸光度达到最大,继续增加萃取剂的用量,吸光度迅速下降。因此确定最佳萃取剂为0.1mL。
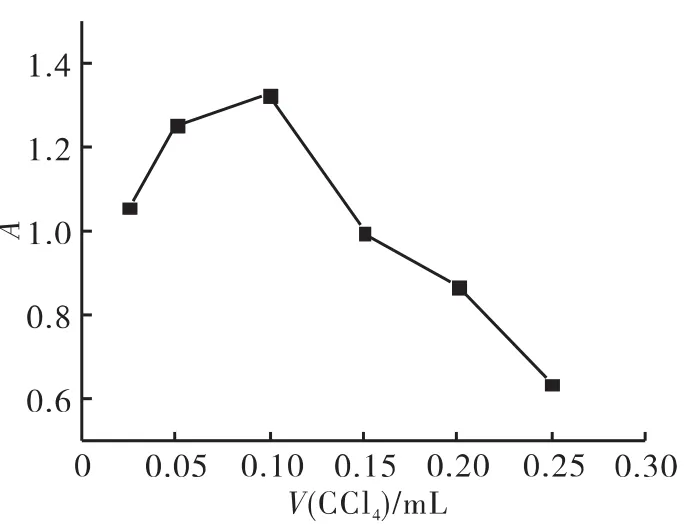
图3 萃取剂的用量与吸光度关系
2.4 分散剂的选择与用量的确定
分散剂对水和有机相都应具有良好的亲和性,按照1.3实验方法操作,考察甲醇、乙醇、丙酮和乙腈四种溶剂作为分散剂对萃取效率的影响。测量吸光度,结果如表2所示。乙醇为最优分散剂。再按照1.3实验方法考察分散剂用量与吸光度的关系,结果如图4所示。当乙醇小于0.3mL时,不能够很好的将螯合物分散开,吸光度随分散剂用量增加而增加,当乙醇达到0.3mL时,吸光度达到最大,继续增加乙醇的用量,能够使更多的螯合物溶解在水中,吸光度下降,因此,实验选择乙醇的最佳用量为0.3mL。

表2 不同分散剂与吸光度的关系
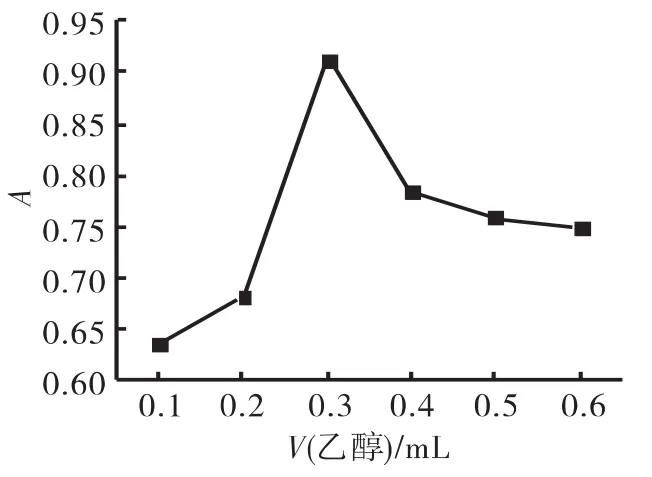
图4 分散剂的用量与吸光度的关系
2.5 稀释剂的确定
离心之后,离心管底部的沉淀物无法直接进行测量,需要选择合适的稀释剂对有机相进行溶解稀释,按照1.3实验方法,分别考察乙醇、甲醇和丙酮三种稀释剂对萃取效果的影响,结果如表3所示。由表3可知最优的稀释剂为甲醇。
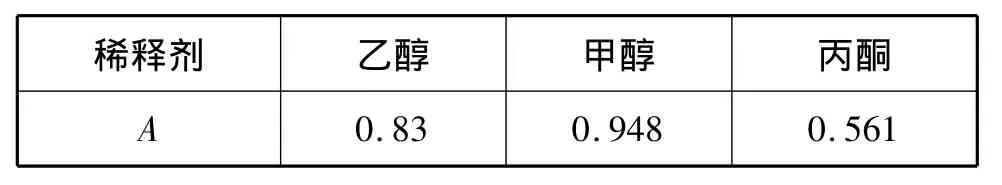
表3 不同稀释剂与吸光度的关系
2.6 萃取时间的确定
在液液微萃取中,萃取时间是指将萃取剂注入后离心之前的振荡时间,研究了不同萃取时间(0、0.5、1、1.5、2、2.5min)与吸光度的关系。结果如图5所示,当萃取t为1min时,吸光度达到最大值,当萃取t大于1min时,吸光度下降,可能由有机溶剂的挥发造成的,因此最佳的萃取t为1min。
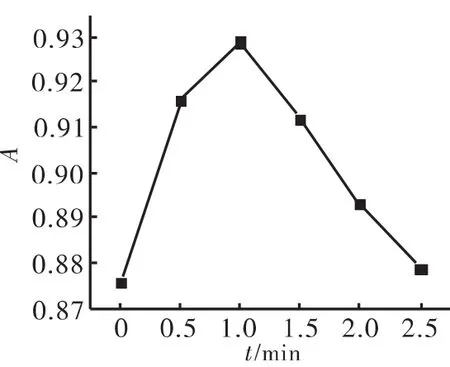
图5 萃取时间与吸光度关系
2.7 缓冲溶液pH的确定
要获得最好的萃取效果,就要在最佳溶液的pH处,使反应进行完全,按照1.3实验方法操作,考察pH 分别为6、7、8、9、10和11的缓冲液对萃取效率的影响,萃取结果如图6所示。由图6可知,当缓冲溶液的pH为9时,吸光度最大。

图6 缓冲溶液pH与吸光度的关系
2.8 干扰离子
在分散液-液微萃取的过程中,溶液中存在的某些离子可能与螯合剂形成疏水性螯合物,从而影响吸光度,影响铅的萃取效率。考察样品中常见的可能对铅存在干扰的离子 Na+、K+、、Ba2+、Mg2+、Al3+、Ca2+、Fe3+、Zn2+、Cu2+,溶液中干扰离子最大允许浓度倍数分别为:Na+是 1000,K+,Ba2+是 800,Mg2+,Al3+是400,Ca2+是500,Fe3+、Zn2+是10,Cu2+是15。
2.9 检出限与线性范围
检出限是指方法能够检测出的待测组分的最小浓度。一般为本底信号的3倍,该方法的检出限为0.1mg/L。
线性范围是该方法的校准曲线的直线部分所对应的待测物质的浓度(或量)的变化范围。通过对一系列浓度铅离子溶液进行分析测定,得到线性方程为 A=0.00472+0.16449x,相关系数 R=0.99214,其中 A是吸光度,x是铅离子质量浓度mg/L。本方法的线性范围为0.4~10mg/L。
2.10 富集倍数
富集倍数是指被萃取富集后的溶液浓度与未被处理前的浓度之比。分别测定萃取前后溶液的吸光度,得到该方法的富集倍数为94倍。
3 样品的测定
采用分散液-液微萃取分光光度法测定不同来源水中铅,样品分别为自来水、湖水和浑河水。取已处理好的三种样品按照1.3的实验方法在波长570nm处进行测定,并分别向已处理好的样品中加入一定量的铅标准溶液,用同样的方法进行测定,并计算回收率。结果如表4。
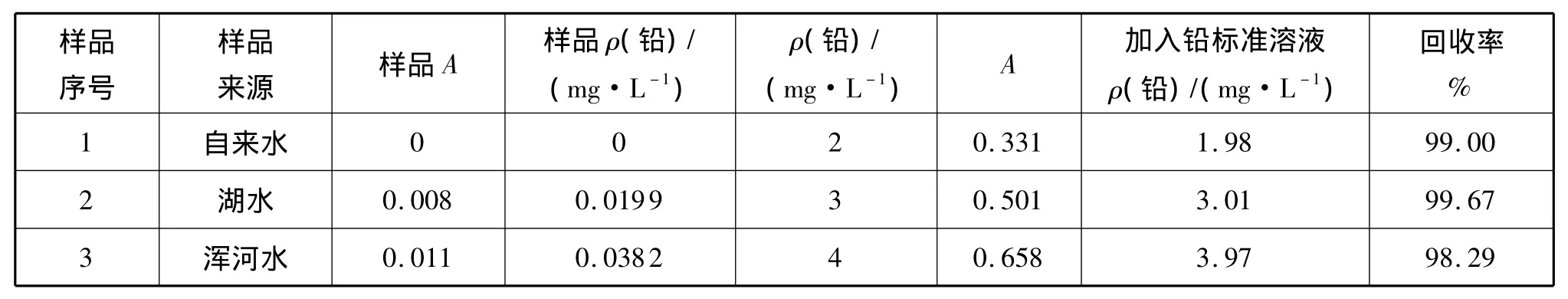
表4 样品测定及回收率
3 结论
采用分散液-液微萃取分光光度法测定环境水样中铅,检出限为0.1mg/L,富集倍数为94倍,加标回收率在90% ~110%之间,说明该方法的重现性好。该方法所需要的样品量少,操作步骤简单,分析速度快,与传统的测定方法相比,分散液-液微萃取分光光度法联用测定水中微量铅的方法具有操作简单、灵敏度高、重现性好且低成本消耗等优点。适用于环境样品分析的方法。
[1]袁宝珊.环境铅污染与儿童健康[J].微量元素与健康研究,1998,25(4):193-198.
[2]刘玉莹.环境铅污染的来源及对儿童的危害[J].职业与健康,2003,19(6):8-9.
[3]丁宗庆,刘光东.分散液液微萃取-分光光度法测定痕量钒[J].冶金分析,2009,29(4):54-56.
[4]陈秋生,孟兆芳.水中铅的测定方法研究进展[J].微量元素与健康研究,2008,25(3):66-68.
[5]臧晓欢,吴秋华,张美月,等.分散液相微萃取技术研究进展[J].分析化学,2009,37(2):161-168.
[6]Mohammad R,Yaghoub A,Mohammad R M H,et al.Determination of Organic Compounds in Water Using Dispersive Liquid-Liquid Microextraction[J].Journal of Chromatography A,2006,1116(1-2):1-9.
[7]Daneshfar A,Khezeli T,Lotfi H J.Determination of Cholesterol in Food Samples Using Dispersive Liquid-Liquid Microextraction Followed by HPLC-UV[J].Journal of Chromatography B,2009,877(4):456-460.

