全亲水无规共聚物P(NIPAM-co-AA)的pH 和温度双重刺激响应性水相自组装
陈韩婷 樊 晔 方 云
(江南大学化学与材料工程学院,食品胶体与生物技术教育部重点实验室,江苏无锡214122)
1 引言
双亲水性嵌段共聚物(DHBC)由两种或两种以上水溶性聚合物嵌段组成,1当环境条件改变时,若其中某一嵌段从亲水性转变为疏水性,则双亲水性嵌段共聚物会转化为典型的两亲性嵌段共聚物(ABC),产生环境响应性自组装.2-41998年Armes研究小组5第一次报道了一种DHBC分子聚(甲基丙烯酸-2-(N-吗啡基)乙酯)-b-聚(甲基丙烯酸-2-(二乙胺基)乙酯)(PMEMA-b-PDEAEMA)在稀水溶液中的聚集行为:当pH升高至8.5时,PDEAEMA嵌段因去质子化而疏水,形成了以PDEAEMA嵌段为核,PMEMA嵌段为壳的胶束;而在中性条件下加入电解质Na2SO4时,PMEMA嵌段因盐析而疏水,形成了以PMEMA嵌段为核,PDEAEMA嵌段为壳的胶束.以后又有基于pH值、温度、离子强度改变,或加入金属离子、小分子或高分子与其中某一嵌段络合等引起的刺激响应性自组装行为的报道,6-9DHBC作为智能材料在药物传递、10-13基因治疗13,14及金属胶体合成的纳米反应器15,16等方面均有潜在应用.但是合成DHBC常采用基团转移聚合(GCP)和可逆加成-断裂链转移聚合(RAFT)方法,对水非常敏感,故需要在真空下进行,反应条件苛刻并且所需的大分子链引发剂价格昂贵,1,17-22因而其实用性有限.无规共聚物比嵌段共聚物更易合成且低成本,在应用拓展上更具潜力,但其化学结构无规性导致自组装驱动力亦表现为“无规”,故目前仅有少量关于两亲性无规共聚物(ARC)在选择性溶剂中自组装行为的报道,如在二甲基甲酰胺/水、23,24二氧六环/水、25,26四氢呋喃/水、27,28二甲亚砜/水29等选择性溶剂中.该组装过程需将ARC溶于有机溶剂中,通过添加水使其中某一链段表现疏水性而收缩为疏水微区;另一链段表现为亲水性而形成亲水微区并富集于表面使组装体稳定;由于ARC一般不能在水中完全溶解,故目前尚未见有ARC在全水相中自组装的报道,因此有必要合成全亲水无规共聚物(HRC),研究其在全水相环境中的刺激响应性自组装行为,使其更贴近应用实际和绿色化学需求,并对理解和利用其自组装驱动力具有指导意义.
本课题组前期曾研究了分子结构与一种HRC分子聚(丙烯酰胺-co-丙烯酸)(P(AM-co-AA))相似的聚合物——部分水解丙烯酰胺(HPAM),利用其pH刺激响应性实现了全水相自组装.30,31由于HPAM在中性pH下具有较好的水溶性,通过调节pH值使丙烯酸(AA)链节或丙烯酰胺(AM)链节分别表现出不同的质子化状态,就能形成pH刺激响应性的氢键络合对,并成为疏水自组装的驱动力,从而使无规共聚物的自组装更趋绿色化和简单化.但是,丙烯酰胺单体的生物毒性限制了其在生物医药领域中的应用,因此本文选取生物相容性32-34的两种单体,即具有温度刺激响应性的N-异丙基丙烯酰胺(NIPAM)单体和pH刺激响应性的丙烯酸单体,合成了一种全亲水无规共聚物P(NIPAM-co-AA),并研究其对pH和温度刺激的双响应性水相自组装行为,以期揭示其在药物传递方面的潜在应用价值.
2 实验部分
2.1 试剂
N-异丙基丙烯酰胺,98%,TCI试剂公司,重结晶后使用;丙烯酸、偶氮二异丁腈(AIBN)及其它试剂均为分析纯,中国医药(集团)上海化学试剂公司,AIBN经重结晶后使用,AA经减压蒸馏后使用;超纯水(电阻率18.2 MΩ·cm)自制.
2.2 P(NIPAM-co-AA)的合成及表征
在圆底烧瓶中加入4.7 g的NIPAM和1.0 g的AA单体,并加入占单体质量5%的引发剂AIBN和66 mL的叔丁醇;通氮气驱赶空气30 min,70°C反应12 h.分别用400 mL正己烷沉淀两次,将沉淀物在40°C真空干燥箱中干燥至恒重,得到的白色粉末状固体即为低分子量目标产物——全亲水无规共聚物P(NIPAM-co-AA).该反应转化率为87%.FTIR图谱(FTLA2000-104,加拿大ABB Bomen公司,溴化钾压片)显示1647 cm-1处强吸收峰为酰胺中羰基(C=O)的伸缩振动,1090 cm-1处强吸收峰归属于酰胺中C―N的伸缩振动,1716 cm-1处的肩峰为羧基缔合时的伸缩振动,3364 cm-1处宽吸收峰为羧基中O―H的伸缩振动及酰胺中N―H的伸缩振动峰的叠加.酸碱滴定测得P(NIPAM-co-AA)中AA质量分数为19%;凝胶过滤色谱(Waters 600,美国Waters公司,流动相为0.05 mol·L-1LiBr的二甲基甲酰胺(DMF)溶液,标样为聚环氧乙烷(PEO)(106500,920000)和聚乙二醇(PEG)(4250,8580,58700),柱温为35°C)测得P(NIPAM-co-AA)的重均分子量Mw=3.1×104,数均分子量Mn=1.8×104,多分散系数Mw/Mn=1.7.差示扫描量热法(DSC)测试结果表明本文合成的聚合物只有一个玻璃化转化温度Tg(109.8°C),故P(NIPAM-co-AA)可视为无规共聚物.由于本文合成的无规聚合物相对分子质量只有104量级,故忽略产生类似嵌段共聚物的长序列链段并有显著影响.
2.3 P(NIPAM-co-AA)自组装体的制备及表征
将2 mL浓度为5 mg·mL-1的P(NIPAM-co-AA)水溶液用超纯水稀释至接近10 mL,在20°C及磁力搅拌下,以40 uL·min-1的速率加入 0.1 mol·L-1的HCl或NaOH,缓慢调节至所需pH值后用超纯水稀释至10 mL,得到1 mg·mL-1的P(NIPAM-co-AA)水溶液;在指定温度±0.1°C的水浴中恒温24 h,得到指定温度和指定pH值的P(NIPAM-co-AA)自组装体溶液.
恒温下将上述P(NIPAM-co-AA)自组装体溶液滴在铜网上,用滤纸吸掉多余溶液并稍干,重复3次,干燥,用透射电子显微镜(TEM,JEOLJEM2100,日本电子公司,加速电压200kV)对自组装体形貌进行TEM表征;上述溶液经0.8 μm滤膜过滤后用激光光散射仪(ALV-5022F,德国ALV公司),激光波长623.8 nm,散射角90°,扫描时间300 s,在指定温度±0.01°C下对流体动力学半径(Rh)进行DLS表征,Rh及其分布f(Rh)均由CONTIN非线性模拟得到,调整散射角为30°到150°条件下对均方根旋转半径(Rg)进行SLS表征;用zeta电位仪(Zetasizer 2000,英国Malvern公司)在(20.0±0.1)°C下测定其zeta电位,取5次测定平均值;用红外光谱仪(FTLA2000-104,加拿大ABB Bomen公司,硒化锌盐片涂片)测定其FT-IR谱图.
用0.1 mol·L-1的HCl或NaOH调节10 mg·mL-1的P(NIPAM-co-AA)水溶液的pH值,并用紫外-可见光分光光度计(T6,北京谱析通用仪器有限责任公司)在500 nm波长处测定吸光度表征其最低临界溶解温度(LCST),恒温精度±0.01°C.
3 结果与讨论
3.1 P(NIPAM-co-AA)自组装的驱动力
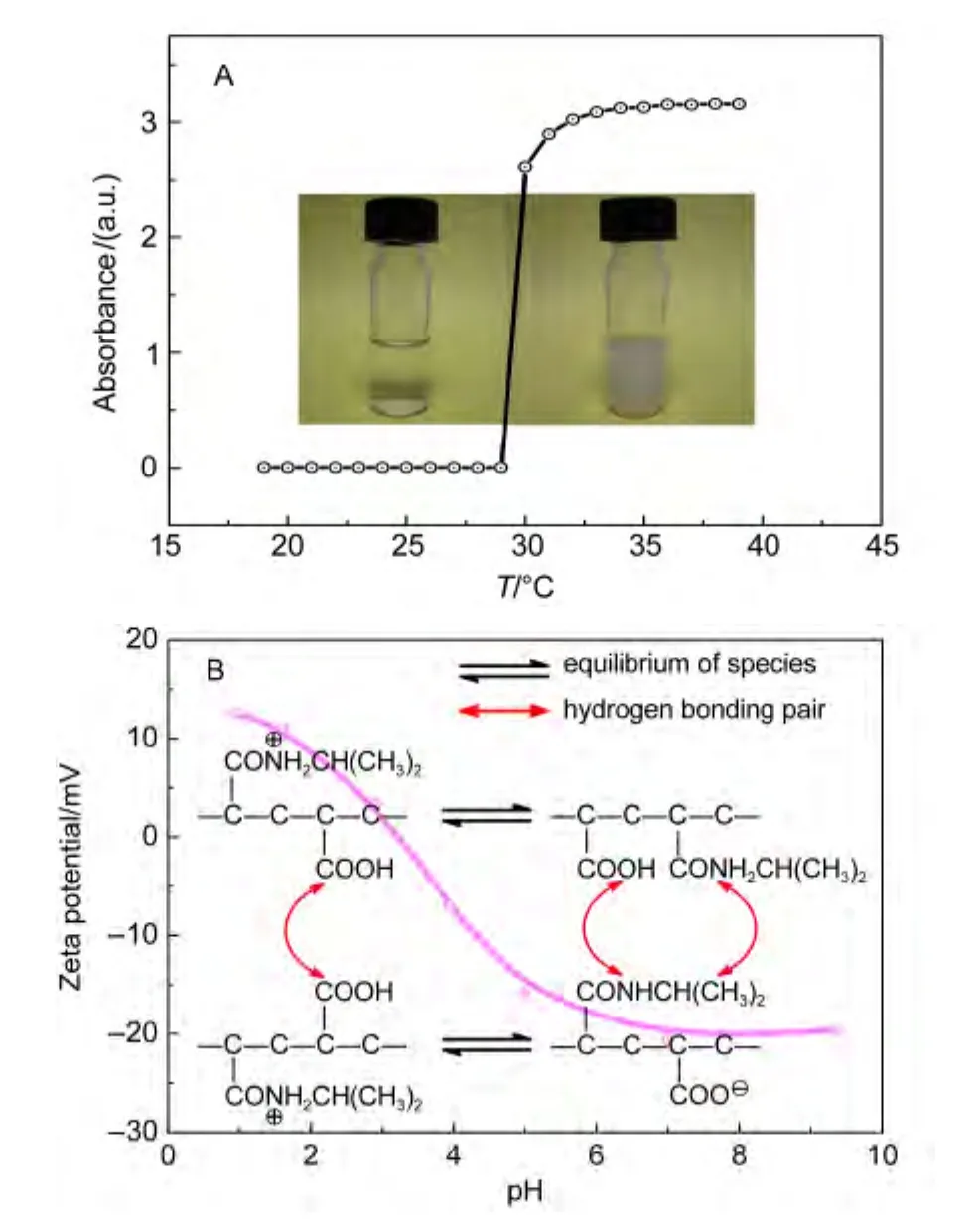
图1 P(NIPAM-co-AA)水溶液的LCST(A)以及pH刺激响应的P(NIPAM-co-AA)自组装体溶液的zeta电位与链节间氢键对的关系(B)Fig.1 LCST of P(NIPAM-co-AA)(A)and the relationship between zeta potential and pH stimuli-responsive hydrogen-bonding pairs of the assembled aqueous P(NIPAM-co-AA)solution(B)
测定10 mg·mL-1的P(NIPAM-co-AA)水溶液在不同温度下500 nm处的吸光度如图1A所示,表明其最低临界溶解温度(LCST)为29.6°C.在LCST以下温度,NIPAM链节上的酰胺基团亲水,与水分子间形成氢键使P(NIPAM-co-AA)溶于水而透明;在LCST以上温度,NIPAM链节与水分子间氢键被破坏,酰胺基团上异丙基的疏水作用占主导,NIPAM链段表现为疏水性从而使P(NIPAM-co-AA)溶液变浑浊.因此,P(NIPAM-co-AA)中NIPAM链节在LCST上下温度的疏水性-亲水性变化是其产生温度刺激响应性自组装的驱动力.
P(NIPAM-co-AA)自组装体溶液的zeta电位随pH的变化趋势如图1B所示,zeta电位零值出现在pH 3.0左右,表明此时P(NIPAM-co-AA)自组装体表面处于“等电点”而失去电性保护.当pH值从3.0向中性变化时,zeta电位由零转向负值并最终形成绝对值为20 mV的平台;此时NIPAM链节以非离子态存在,而AA链节中―COOH与―COO−达到解离平衡;相应地,富NIPAM链段形成的NIPAM-NIPAM疏水性氢键络合对以及酰胺基团上异丙基的疏水作用成为P(NIPAM-co-AA)疏水自组装的主要驱动力,而―COO−的静电排斥力及其与水分子间的水化作用成为稳定P(NIPAM-co-AA)自组装体表面的辅助驱动力.当pH值从3.0向酸性增大变化时,zeta电位由零转向正值并呈持续上升趋势;此时NIPAM链节质子化成―CONH2+CH(CH3)2状态,而AA链节以―COOH形式存在;相应地,富AA链段中形成的AA-AA疏水性氢键络合对以及酰胺基团上异丙基的疏水作用成为P(NIPAM-co-AA)疏水自组装的主要驱动力,而―CONH2+CH(CH3)2的静电排斥力及其与水分子的水化作用成为稳定P(NIPAM-co-AA)自组装体表面的辅助驱动力.因此,P(NIPAM-co-AA)中两种链节在等电点前后荷电状态的变化以及因此形成不同的疏水性氢键络合对是产生pH刺激响应性自组装的驱动力.
由于大分子自组装体是一个动力学稳定的体系,因此FT-IR图谱能够提供自组装体表面富集化学基团的信息,从而间接反映组装体内部疏水性氢键络合对的信息;将其与上述zeta电位分析结果相结合,就能进一步验证上述形成P(NIPAM-co-AA)的pH刺激响应自组装体的主次驱动力.pH 4.0时未经组装的P(NIPAM-co-AA)的FT-IR图谱如图2中部所示,IR特征峰为―COOH中C=O的伸缩振动峰(1716 cm-1(一肩峰)),酰胺I带(1647 cm-1)和酰胺II带(1558 cm-1)等.pH 1.3时P(NIPAM-co-AA)自组装体的FT-IR图谱如图2下部所示,与pH 4.0时未经组装的P(NIPAM-co-AA)相比,酰胺I带(1633 cm-1)和酰胺II带(1557 cm-1)均向低波数移动,这是酰胺基被质子化为―CONH2+CH(CH3)2的反映,并与图1B中zeta电位的测试结果相互印证,这说明离子化的富NIPAM链段位于自组装体的外表并伸展在水中形成带正电的保护层;同时,―COOH的C=O的伸缩振动峰(1717 cm-1)峰强增大,这是羧基间形成氢键的反映,说明富AA链段在自组装体内部构成疏水性氢键络合对.pH 6.0时P(NIPAM-co-AA)自组装体的FT-IR图谱如图2上部所示,与pH 4.0时未经组装的P(NIPAM-co-AA)相比,―COOH的C=O的伸缩振动峰消失,新形成的羧酸盐特征吸收峰与酰胺II带叠加(1561 cm-1),其峰强大大增大,这是AA链节离子化为―COO-的反映,并与图1B中zeta电位测试结果相互印证,这说明离子化的富AA链段位于自组装体的外表并伸展在水中形成带负电的保护层;相应地,未离子化的AA链节以及富NIPAM链段在自组装体内部构成疏水性氢键络合对.
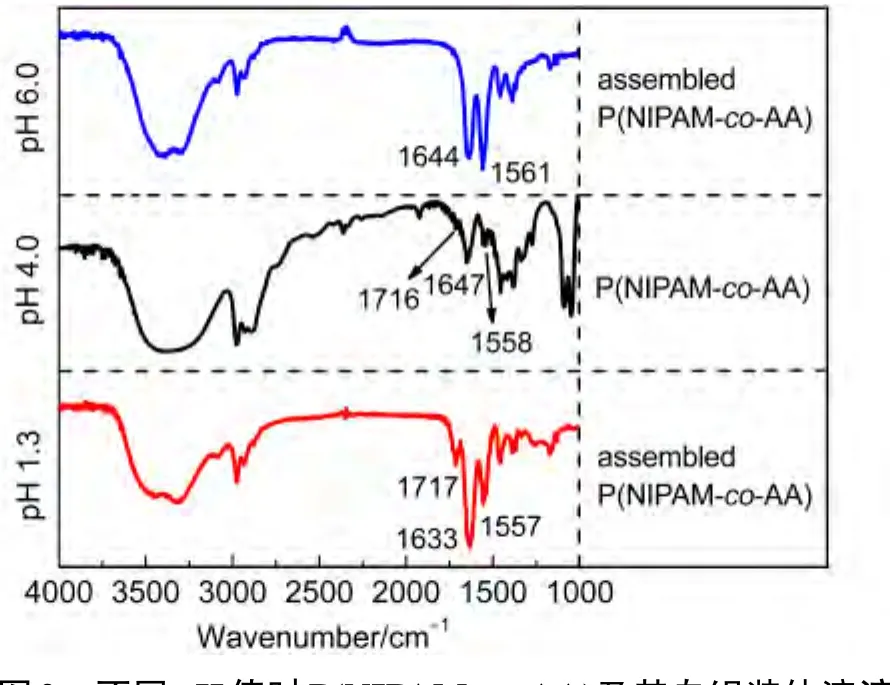
图2 不同pH值时P(NIPAM-co-AA)及其自组装体溶液的FT-IR光谱Fig.2 FT-IR spectra of P(NIPAM-co-AA)and the assembled aqueous solution of P(NIPAM-co-AA)at different pH values
3.2 P(NIPAM-co-AA)的双重响应性自组装体的形貌及粒径
不同pH值下P(NIPAM-co-AA)的LCST变化如图3A中曲线所示.本文先将pH恒定在P(NIPAM-co-AA)的自然pH条件(pH 4.0),考察其温度刺激响应性自组装行为,如图3A(a,b)所示;然后恒定在LCST以下温度(20°C),考察其pH刺激响应性自组装行为,如图3A(c,d,e)所示.各种条件下P(NIPAM-co-AA)自组装体的TEM影像如图3B所示.恒定pH时,在LCST以上,40°C时P(NIPAM-co-AA)自组装为图3B(a)中约20 nm左右的蠕虫状自组装体,60°C时P(NIPAM-co-AA)进一步收缩为图3B(b)中5 nm左右的小团块.恒定温度时,pH 1.3处P(NIPAM-co-AA)自组装为图3B(d)中约100 nm的棒状自组装体;pH 0.9处P(NIPAM-co-AA)自组装为图3B(c)中约100 nm的似矩形自组装体;继续升高pH至6.0处,P(NIPAM-co-AA)自组装为图3B(e)中长轴约1 μm,短轴约500 nm的椭圆形大囊泡.考察过AA组成为9%到68%的全亲水无规共聚物P(NIPAM-co-AA),发现其同样具有双重刺激响应性行为.由动态激光光散射(DLS)测得P(NIPAM-co-AA)在上述各温度和pH环境下形成的自组装体的粒径及粒径分布结果见图4,与TEM影像观察到的粒径大小相互印证.同时,表1中利用DLS与SLS相结合方式辅助判断聚集体的形貌,得到pH 4.0、40°C时蠕虫状自组装体的Rg/Rh为1.34;pH 0.9、20°C时似矩形自组装体的Rg/Rh为0.78,进一步证实了TEM影像与激光光散射结果的吻合性.35,36

图3 不同pH下无规共聚物P(NIPAM-co-AA)的LCST曲线(A)及pH和温度双响应性P(NIPAM-co-AA)自组装体的TEM图像(B)Fig.3 LCST curve of P(NIPAM-co-AA)at different pH values(A)and the TEM images of the dual pH-and thermoresponsive P(NIPAM-co-AA)assemblies(B)
3.3 P(NIPAM-co-AA)的双重响应性自组装体的微结构分析
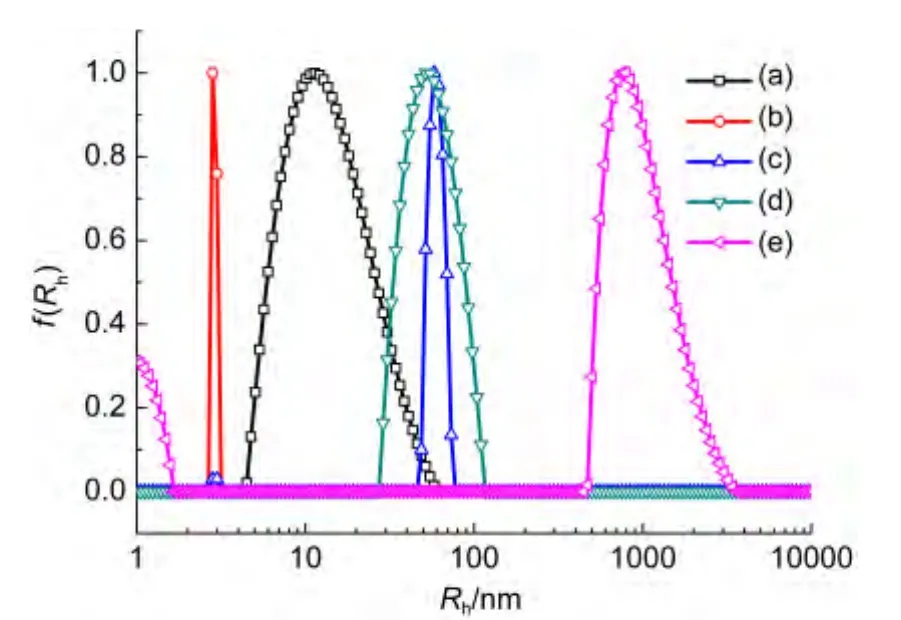
图4 pH和温度双重响应性P(NIPAM-co-AA)自组装体的粒径(Rh)及粒径分布(f(Rh))图Fig.4 Radius(Rh)and the radius distribution(f(Rh))of the dual pH-and thermo-responsive P(NIPAM-co-AA)assemblies
在温度刺激响应组装过程中,将pH值恒定在P(NIPAM-co-AA)的自然pH值(pH 4.0).当体系温度(20°C)低于LCST时,P(NIPAM-co-AA)中两种链节均溶于水,故表现为典型的全亲水无规共聚物(HRC),在水中为伸展的线团状,因此pH=4.0、T=20°C条件相应的聚合物的DSL图和TEM图没有明显的图像和影像.当温度(40°C)高于LCST时,富NIPAM链段因疏水而收缩,富AA链段因荷负电而亲水;由于无规共聚物具有链段分布弥散的特性,其自组装体不可能像嵌段共聚物那样形成界面清晰的疏水内核和亲水外壳,而是在富NIPAM链段的疏水微区中含有亲水的AA链节,同时在富AA链段的亲水微区中含有疏水的NIPAM链节,因此形成的自组装体具有内部富集NIPAM链节,从内到外NIPAM链节含量逐渐减少,而表面富集AA链节的链节梯度分布特征,且疏水微区与亲水微区相间共存的微结构.随着温度进一步升高(60°C),NIPAM链节与水分子间的氢键完全被破坏,富NIPAM链段的疏水性增强,使原来较为松散的蠕虫状自组装体(20nm)收缩塌陷为粒径更小(5 nm)、结构更为密实的小团块.该实验事实表明高温时低浓度(1 mg·mL-1)的P(NIPAM-co-AA)聚集体将以内部收缩为主,而不易发生聚集体间相互聚并.P(NIPAM-co-AA)的上述温度刺激响应性自组装体的微结构变化趋势如图5中垂直线所示.

表1 pH和温度双重响应性P(NIPAM-co-AA)自组装体的粒径参数Table 1 Radius of the dual pH-and thermo-responsive P(NIPAM-co-AA)assemblies
在pH刺激响应组装过程中,将温度恒定在低于LCST曲线的20°C.当体系pH值(pH 6.0)高于P(NIPAM-co-AA)的自然pH值(pH 4.0)时,P(NIPAM-co-AA)中富NIPAM链段的NIPAM-NIPAM链节之间因氢键相互作用形成了疏水性氢键络合对,并且与富NIPAM链段中异丙基的疏水作用共同导致链段收缩塌陷,而富AA链段中阴离子化的AA链节伸展在水中,因此构成了具有自组装体内部富集NIPAM链节、从内到外NIPAM链节含量逐渐减少、而表面富集AA链节的链节梯度分布特征的微结构.此时,在自组装体内部富NIPAM链段的疏水微区中还包含AA链节,它们之间的静电斥力会导致疏水微区上发生明显的微相分离,拉空形成了囊泡的囊腔,如图2B(e)所示.当体系pH值(pH 0.9)低于P(NIPAM-co-AA)的自然pH值时,P(NIPAM-co-AA)中富AA链段的AA-AA链节之间的氢键相互作用形成了疏水性氢键络合对,并且与包藏于富AA链段的NIPAM链节中的异丙基的疏水作用共同导致链段收缩塌陷,而富NIPAM链段中阳离子化的NIPAM链节伸展在水中,因此构成了自组装体内部富集AA链节,从内到外AA链节含量逐渐减少,而表面富集NIPAM链节的链节梯度分布特征,且疏水微区与亲水微区相间共存的微结构.此时,由于在自组装体内部富AA链段的疏水微区中还包含NIPAM链节,它们之间的静电斥力也可能会像pH 6.0时的情形相仿,导致疏水微区中发生微相分离,拉空形成小囊腔,但这需要进一步实验证实.P(NIPAM-co-AA)的上述pH刺激响应性自组装体的微结构变化趋势如图5中水平线所示.

图5 水溶液中pH和温度刺激响应性P(NIPAM-co-AA)自组装的微结构示意图Fig.5 Schematic illustration of the stimuli-responsive selfassembled microstructure of the dual pH-and thermoresponsive P(NIPAM-co-AA)in aqueous solution
4 结论
合成了一种全亲水无规共聚物P(NIPAM-co-AA),该聚合物在水相中能够产生pH或温度刺激响应性自组装.在本文实验范围内得到以下结论:(1)P(NIPAM-co-AA)中NIPAM链节在LCST上下温度的疏水性-亲水性变化是其产生温度刺激响应性自组装的驱动力;P(NIPAM-co-AA)中两种链节在等电点前后荷电状态的变化以及因此形成不同的疏水性氢键络合对是产生pH刺激响应性自组装的驱动力.(2)由于无规共聚物P(NIPAM-co-AA)具有链段分布弥散的特性,其自组装体不可能像嵌段共聚物那样形成界面清晰的疏水内核和亲水外壳,而是在富疏水链段的疏水微区中含有亲水链节,同时在富亲水链段的亲水微区中含有疏水链节,因此形成的自组装体具有内部富集疏水链节、从内到外疏水链节含量逐渐减少、而表面富集亲水链节的链节梯度分布特征,且疏水微区与亲水微区相间共存的微结构.并且由于环境刺激响应,在不同pH或温度条件下自组装体的亲/疏水链段将发生互换.(3)全亲水无规共聚物P(NIPAM-co-AA)的合成方法简单、具有pH和温度双重响应性,其在全水相中的刺激响应性自组装行为在药物释放等方面具有潜在的应用价值.
(1) Jiang,M.;Eisenberg,A.;Liu,G.J.;Zhang,X.Macromolecular Self-Assembly;Science Press:Beijing,2006;pp 137-181. [江明,艾森伯格,A.,刘国军,张 希.大分子自组装.北京:科学出版社,2006:137-181.]
(2) Liu,S.Y.;Billingham,N.C.;Armes,S.P.Angew.Chem.Inter.Edit.2001,40(12),2328.doi:10.1002/1521-3773(20010618)40:12<2328::AID-ANIE2328>3.0.CO;2-M
(3)Colfen,H.Macromol.Rapid Commun.2001,22,219.
(4) Gil,E.S.;Hudson,S.A.Prog.Polym.Sci.2004,29,1173.doi:10.1016/j.progpolymsci.2004.08.003
(5) Bütün,V.;Billingham,N.C.;Armes,S.P.J.Am.Chem.Soc.1998,120(45),11818.doi:10.1021/ja982295a
(6)Rodríguez-Hernández,J.;Lecommandoux,S.J.Am.Chem.Soc.2005,127(7),2026.doi:10.1021/ja043920g
(7)Chang,C.;Wie,H.;Feng,J.;Wang,Z.C.;Wu,X.J.;Wu,D.Q.;Cheng,S.X.;Zhang,X.Z.;Zhuo,R.X.Macromolecules 2009,42(13),4838.doi:10.1021/ma900492v
(8) Smith,A.E.;Xu,X.;Kirkland-York,S.E.;Aavin,D.A.;McCormik,C.L.Macromolecules 2010,43(3),1210.doi:10.1021/ma902378k
(9) Shih,Y.J.;Chang,Y.;Deratani,A.;Quemener,D.Biomacromolecules 2012,13(9),2849.doi:10.1021/bm3008764
(10)Wang,A.;Gao,H.;Sun,Y.F.;Sun,Y.L.;Yang,Y.W.;Wu,G.L.;Wang,Y.N.;Fan,Y.;Ma,J.B.Int.J.Pharmaceut.2013,441,30.doi:10.1016/j.ijpharm.2012.12.021
(11) Bian,J.;Zhang,M.Z.;He,J.L.;Ni,P.H.React.Funct.Polym.2013,73,579.doi:10.1016/j.reactfunctpolym.2012.12.010
(12) Joshi,R.V.;Nelson,C.E.;Poole,K.M.;Skala,M.C.;Duvall,C.L.Acta Biomater.2013,9,6526.doi:10.1016/j.actbio.2013.01.041
(13) Ganta,S.;Devalapally,H.;Shahiwala,A.;Amiji,M.J.Control.Release.2008,126,187.doi:10.1016/j.jconrel.2007.12.017
(14)Calejo,M.T.;Cardoso,A.M.S.;Kjøniksen,A.L.;Zhu,K.Z.;Morais,C.M.;Sande,S.A.;Caedoso,A.L.;Lima,P.D.;Jurado,A.;Nyström,B.Int.J.Pharmaceut.2013,448,105.doi:10.1016/j.ijpharm.2013.03.028
(15) Bronstein,L.M.;Sidorov,S.N.;Gourkova,A.Y.;Valetsky,P.M.;Hartmann,J.;Breulmann,M.;Cölfen,H.;Antonietti,M.Inorg.Chim.Acta 1998,280,348.doi:10.1016/S0020-1693(98)00208-4
(16) Li,L.Y.;He,W.D.;Li,W.T.;Zhang,K.R.;Pan,T.T.;Ding,Z.L.;Zhang,B.Y.J.Polym.Sci.Pol.Chem.2010,48,5018.doi:10.1002/pola.v48:22
(17)Mitsukami,Y.;Donovan,M.S.;Lowe,A.B.;McCormik,C.L.Macromolecules 2001,34(7),2248.doi:10.1021/ma0018087
(18) Patrickios,C.S.;Lowe,A.B.;Armes,S.P.;Billinghan,N.C.J.Polym.Sci.Pol.Chem.1998,36(4),617.
(19) Quek,J.Y.;Zhu,Y.;Roth,P.J.;Davis,T.P.;Lowe,A.B.Macromolecules 2013,46(18),7290.doi:10.1021/ma4013187
(20) Chiefari,J.;Chong,Y.K.;Ercole,F.;Krstina,J.;Jeffery,J.;Le,T.P.T.;Mayadunne,R.T.A.;Meijs,G.F.;Moad,C.L.;Moad,G.;Rizzardo,E.;San,H.T.Macromolecules 1998,31(16),5559.
(21)Lowe,A.B.;McCormick,C.L.Prog.Polym.Sci.2007,32(3),283.doi:10.1016/j.progpolymsci.2006.11.003
(22)Yang,P.;Ratcliffe,L.P.D.;Armes,S.P.Macromolecules 2013,46,8545.doi:10.1021/ma401797a
(23) Tao,Y.H.;Yang,Y.Q.;Shi,D.J.;Chen,M.Q.;Yang,C.;Liu,X.Y.Polymer 2012,53,1551.doi:10.1016/j.polymer.2012.02.001
(24)Tian,F.;Yu,Y.Y.;Wang,C.C.;Yang,S.Macromolecules 2008,41(10),3385.doi:10.1021/ma800142j
(25) Liu,X.Y.;Kim,J.;Wu,J.;Eisenberg,A.Macromolecules 2005,38(16),6749.doi:10.1021/ma050665r
(26) Liu,X.Y.;Wu,J.;Kim,J.;Eisenberg,A.Langmuir 2006,22(1),419.doi:10.1021/la0519610
(27)Li,N.;Li,Y.B.;Wang,X.G.Polymer 2012,53,3975.doi:10.1016/j.polymer.2012.07.001
(28) Li,N.;Wang,X.Acta Polym.Sin.2013,No.4,549.
(29)Wang,Y.;Wang,Y.;Wu,G.L.;Fan,Y.G.;Ma,J.B.Colloids and Surfaces B 2009,68(1),13.doi:10.1016/j.colsurfb.2008.08.026
(30) Fang,Y.;Pang,P.P.;Lai,Z.Y.Chem.Lett.2011,40(10),1074.doi:10.1246/cl.2011.1074
(31) Fang,Y.;Lai,Z.Y.;Pang,P.P.;Jiang,M.Acta Physico-Chimica Sinica 2011,27(7),1712. [方 云,赖中宇,庞萍萍,江 明.物理化学学报,2011,27(7),1712.]doi:10.3866/PKU.WHXB20110703
(32) Qian,J.;Wu,F.J.Mater.Chem.B 2013,1(28),3464.doi:10.1039/c3tb20527d
(33) Zhang,X.;Yang,P.;Dai,Y.Adv.Funct.Mater.2013,23(33),4067.doi:10.1002/adfm.v23.33
(34)Li,C.;Alam,M.M.;Bolisetty,S.Chem.Commun.2011,47(10),2913.doi:10.1039/c0cc05126h
(35) Zhang,Q.;Ye,J.;Liu,Y.;Nie,T.;Xue,D.;Song,Q.;Chen,H.;Zhang,G.;Tang,Y.;Wu,C.;Xie,Z.Macromolecules 2008,41,2228.doi:10.1021/ma702139b
(36) Liu,T.;Zhao,Z.;Wu,C.;Chu,B.;Schneider,D.K.;Nace,V.M.J.Phys.Chem.B 1997,101,8808.doi:10.1021/jp963810z
——拉曼光谱和密度泛函理论计算

