锂电池热点论文点评(2013.10.1—2013.11.30)
王 昊,闫 勇,徐凯琪,林明翔,唐代春,董金平,孙 洋,陈 彬,贲留斌,黄学杰
(中国科学院物理研究所,北京 100190)
1 正极材料
1.1 层状氧化物正极材料
Liu等[1]使用原位中子衍射研究了普通层状正 极材料Li(Ni1/3Mn1/3Co1/3)O2和富锂层状正极材料xLi2MnO3·(1–x)LiMO2(M=Ni,Mn,Co)在 x=0.5时电化学循环中的结构变化。富锂层状正极材料在第一周充放电过程中(2.0~4.7 V)发生不可逆容量损失,同时伴随着晶体晶面间距的变化。对于普通层状正极材料,其结构在第一周充放电过程中则发生完全可逆转变。Maugeri等[2]运用 XAS研究了 LiMnO2、LiMn0.65Cr0.35O2和 LiMn0.5Ni0.5O2的局部结构。LiMnO2有两种不同的Mn—O化学键,这和Jahn-Teller相变产生的MnO6八面体一致。在Ni和Cr掺杂的材料中Mn—O化学键只有一种,表明Jahn-Teller相变被抑制。同时作者还发现,Cr趋向于占据远离Mn的位置(长的Mn—Cr键),而Ni趋向于占据靠近 Mn的位置(短的 Mn—Cr键)。Mohanty等[3]用中子衍射和磁性测试技术研究了富锂材料Li1.2Mn0.55Ni0.15Co0.10O2的结构。分析表明,该材料可以表示为单斜相 Li2MO3(M=Co、Mn、Ni)(空间群C2/m),同时1%的Ni占据Li的4h位置;或者可以表示为50%单斜相Li2MnO3(空间群 C2/m)和 50%三斜相 LiMO2(M = Co、Mn、Ni)(空间群R3-m)的混合物,在混合物中Li/Ni有3%的互占位。Kim 等[4]用Sm2O3包覆Li(Li1/6Mn1/6Co1/6Ni1/6)O2正极材料,并且用 XRD、EIS、DSC研究了Sm2O3包覆的作用。XRD和TEM的结果表明,Sm2O3包覆并没有改变Li(Li1/6Mn1/6Co1/6Ni1/6)O2的层状结构。电化学测试结果表明,Sm2O3包覆的Li(Li1/6Mn1/6Co1/6Ni1/6)O2循环性能显著提高。EIS结果表明,Sm2O3包覆的 Li(Li1/6Mn1/6Co1/6Ni1/6)O2表面阻抗和电荷转移阻抗减小。DSC的结果表明,包覆后材料的热性质显著改善。Xiong等[5]使用NH4F使Li在LiNi0.8Co0.1Mn0.1O2表面富集。在循环时,原位沉淀的LiF作为抵御HF的保护层,故LiF修饰的LiNi0.8Co0.1Mn0.1O2倍率性能和循环性能显著提高。XRD、EDX、TEM、XPS的结果表明,LiF原位包覆在LiNi0.8Co0.1Mn0.1O2的表面。Kim等[6]采用喷雾热解法合成了纳米尺寸的0.6Li2MnO3·0.4LiCoO2复合物,XRD显示,800 ℃和900 ℃处理的复合物结晶度高,阳离子互占位少。900 ℃处理的样品具有高初始放电比容量(263 mA·h/g)和优异的循环 性能。
1.2 尖晶石正极材料
Cheng等[7]通过在前驱体 Mn0.79Ni0.21CO3表面包覆Al2O3,接着与Li2CO3混合,在900 ℃下烧结得到 LiAlO2包覆的 LiMn1.58Ni0.42O4材料。结果发现,在烧结的过程中 Al3+不仅与 Li2CO3反应生成LiAlO2,而且从表面迁移到体相。电化学测试表明,1% (摩尔分数)的LiAlO2包覆的LiMn1.58Ni0.42O4在 4 C 倍率下有 100.6 mA·h/g 的容量。在 55 ℃时与未包覆的材料相比容量衰减少5%。这表明通过在前驱体上包覆Al2O3以及后续烧结来形成LiAlO2是值得借鉴的方法。
Zhu等[8]通过原位XRD研究了Fd-3m空间群的LiNi0.5Mn1.5O4以及Cr掺杂的LiNi0.5Mn1.5O4。结果发现脱Li过程经过两个两相共存区域。通过对相图的分析以及文献中报道的不同结果,区分脱离化学计量比、应力场效应、阳离子有序程度以及非平衡效应影响的是内在性能还是与样品有关的性能。结果表明,Cr掺杂稳定晶格但不影响容量。Xiao等[9]研究了掺杂Cr的高电压LiNi0.5Mn1.5O4正极材料,充电过程中第一个和第二个两相反应的区域明显延伸。这种延伸的两相区域或者延伸的固溶区域减少了相界面而有利于Li+的快速移动。同时材料充电过程中的结构变化也因此减小。Guo等[10]通过稀硫酸水热处理EMD,使其从γ-MnO2转变为β-MnO2,并且去除了杂质离子,这样处理后得到的 β-MnO2作为合成LiMn2O4的前驱体,合成的LiMn2O4是具有有序微米尺寸的八角晶体。Jiang 等[11]采用 Mn3O4作为前驱体合成微米大小的球形LiMn2O4尖晶石纯相,并且比较不同烧结温度的晶体结构、形貌以及电化学性能,发现800 ℃合成的LiMn2O4具有优越的电化学性能。Zhao等[12]通过YPO4包覆LiMn2O4,与LiMn2O4比较发现质量分数为3% 的YPO4包覆的 LiMn2O4具有较好的循环性能。YPO4不但隔绝了电极活性物质与电解液,阻止了Mn离子的溶解,并且抑制了阻抗的增长,进一步提高了电极的热稳定性。
1.3 聚阴离子正极材料
Ni等[13]构建了 LiCoPO4/Li4Ti5O12全电池,该体系开路电压为 3.2 V,可逆容量为 122 mA·h/g,20 周循环后容量保持为76%。作者也指出若用改进的电解质或是掺杂Mn会提高体系的循环性能。Gutierrez等[14]探讨了影响过渡金属氧化还原电对 M2+/M3+在聚阴离子电极材料中电位高低的因素。研究表明,M2+/M3+的电位主要受到晶体结构与聚阴离子诱导作用(inductive effect)的影响。过渡金属离子与LiO4多面体共边的结构对电压有提升作用,而与PO4多面体共边的结构则会使电压降低。Lopez等[15]合成并研究了Ca与Fe掺杂的磷酸钛铝锂作为锂离子电池正极材料。电子顺磁共振(EPR)结果显示,掺杂后的Li2Ti1.5Ca0.5(PO4)3存在占据四面体中心位置的Ti3+缺陷。Ca2+本身虽然没有活性,但造成了M2位晶格扭曲使更多的Li+可以参与电化学反应,而Fe3+的引入提升了材料的充放电容量。所合成的Li1.2+xTi1.9–xFexCa0.1(PO4)3(x=0.1~0.4)容量为126~131 mA·h/g。Fan等[16]通过碳热还原的方法制备了LiFePO4/C(LFPC)和 LiFe1–2xTixPO4/C(LFTPC)。作者用不同比率的 TiO2掺杂 LiFePO4(LFP)来提高其电化学性质。研究表明,在LFPC中,最佳的碳含量为5%(质量分数)。LFTPC的晶体结构很稳定,并且其粒子尺寸比LFP小。在不同Ti掺杂率的LFTPC中,掺杂率为2%的LFTPC具有最好的倍率性能和循环性能。碳包覆和Ti掺杂的LFTPC电导率可达10–4S/cm。
2 负极材料
2.1 硅基负极材料
Zeilinger等[17]运用 XRD 研究了Al掺杂单晶Li15Si4材料。掺杂Al后材料中Li的晶体占据位置发生了变化。无掺杂的材料为亚稳态,在200 ℃发生分解放热反应,这个反应在400 ℃前缓慢进行。掺杂Al的Li15Si4结构相对稳定,在700 ℃才发生分解反应。这种稳定性的提高可能是由于电子浓度的提高以及费米面的移动造成的。Becker等[18]用原位 AFM 研究了相同高度不同直径的图形化硅柱子充放电过程的体积形变。直径大的样品循环第二周即出现裂纹,所有样品循环后均形成多孔、不稳定的结构。Cattaneo等[19]用6/7Li核磁共振谱研究了纳米硅首周充放电不可逆容量与嵌Li容量的关系。嵌Li容量至接近1000 mA·h/g时,Li15Si4就会在颗粒表面形成,嵌 Li量越高 Li15Si4越多,不可逆容量也越高,P掺杂的纳米硅Li15Si4形成量减少,不可逆容量也相对较少。Lee等[20]用XPS研究了不同嵌Li量的SiOx,分析了其产物的形式(主要是Li2O、Li15Si4和LiSiO4),从而研究嵌Li量对其动力学的影响。Li等[21]用PITT技术研究了用ALD包覆不同厚度 Al2O3硅薄膜的 Li+扩散系数。Stournara等[22]利用密度泛函、分子动力学以及飞行时间二次离子质谱研究了Si/Cu界面在嵌Li过程的界面变化,发现Li在界面富集,Li浓度比体相高20%,该结果使Si、Cu的附着力减少接近16%,从而影响Si的循环性能。Wang等[23]用Cu或Al2O3包覆的具有织纹结构的Si薄膜的循环性能有所提高,体积膨胀与收缩主要发生在平行于基底的方向,而垂直于基底方向的体积变化很小。Wong等[24]利用溶剂交换法制备了稳定均一的纳米硅石墨烯复合材料的悬浮液,提高了石墨烯作为导电剂和体积膨胀缓冲剂的作用。
2.2 其它负极材料
Choi等[25]研究了 Li4Ti5O12电极材料充放电过程中的力学行为。通过光学放大系统,可以探测到Li4Ti5O12嵌 Li变为 Li7Ti5O12过程中微弱的体积变化。放电到1 V以下发现体积变化非常明显,对应Li+进一步嵌入形成Li7+xTi5O12的过程。Fan等[26]在多孔铜集流体上通过电沉积制备了锡钴合金与碳纳米管的多孔复合物,并通过电镜研究了充放电前后材料的形貌变化,随着循环次数增多,材料内部孔洞减少,但没有明显脱落。Hori等[27]通过X射线光电子能谱和硬X射线光电子能谱研究了硬碳材料的嵌Li行为。对比硬碳不同嵌Li电位的光谱,可以指认出硬碳自身和表面SEI的光谱信号。光谱分析验证了硬碳的两种嵌 Li机制:Li嵌入硬碳石墨层间和纳米孔洞。Hwang等[28]在石墨烯的层状框架中镶嵌了纳米SnO2颗粒,通过共价键的作用SnO2被固定在石墨烯表面,有效抑制了充放电过程中SnO2的团聚。Liu等[29]通过化学法合成了 SnO2与石墨烯的复合材料,单晶 SnO2呈现纳米片状,均匀分散在石墨烯中。其中 SnO2含量为 87%(质量分数),透射电镜显示纳米片平均厚度约 5 nm。Wang等[30]通过微波水热在石墨烯表面负载SnO2,然后以纳米 SnO2颗粒为种子在石墨烯表面生长SnO2纳米棒,最后进行碳包覆,得到石墨烯/ SnO2/C的三明治结构,有效抑制了SnO2作为锂离子电池负极的容量衰减。Zhang等[31]通过溶剂热法制备了介孔Mn0.5Co0.5Fe2O4纳米小球与石墨烯的复合材料,其中大小为 5~15 nm的一次颗粒团聚成50~200 nm的小球。石墨烯含量为2.1%(质量分数)的样品表现出高容量和优秀的循环性能,200周循环容量保持为 886 mA·h/g。
Momma等[32]研究了Sn-O-C负极材料。这个材料放电容量在100周后为465 mA·h/g,保持了80%的起始容量。材料在放电50周后结构保持稳定,同时Sn在放电态发生Li0.4Sn的转变。Noh等[33]运用原位环境 TEM 研究了 Sn电极电化学循环中的变化。作者发现Sn在脱Li过程中产生的形变导致微观尺寸的空隙。脱嵌Li过程中的速率不对称性是由嵌Li过程中生成的SEI造成的。SEI在脱Li过程中发生部分溶解。作者指出充放电过程中SEI的形成和溶解是造成材料容量衰减的原因。Yun等[34]合成出具有大孔和介孔的多空碳材料,其比表面积高达1265.9 m2/g。在此材料中富含O、N、S元素,其含量分别为9.8%、7.3%和7.6%。将此材料作为锂电池负极材料,在第270周可逆容量递增至1090 mA·h/g。He等[35]利用不同的Li源(乙酸锂、氢氧化锂),通过水热法合成Li4Ti5O12来研究SEI形成的影响因素,得到的结论是不同的表面形貌与电解液接触会形成不同的 SEI,最终影响材料的循环性能。Jang等[36]在电解液中添加FEC,Sn-Fe-P合金经过循环后SEI中的LiF增加,而有机物成分减少,这可能是FEC能提高其循环性能的原因。Liu等[37]利用原位 TEM 首次直接观察到界面效应改变锂离子传输行为。通过在 Ge纳米线表面包覆几个纳米的Si后,嵌Li过程只能沿着Ge(111)方向进行。
3 电解质
3.1 固态电解质
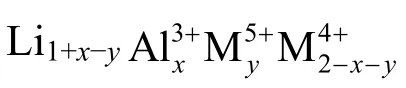
Morimoto等[42]合成了无定形的磷酸钛铝锂Li1+xAlxTi2−x(PO4)3(x=0.3)(a-LATP)和 NASICON结构的磷酸钛铝锂 Li1+xAlxTi2−x(PO4)3(x=0.3)(c-LATP),合成的c-LATP具有高室温电导率(10−4S/cm),可用其作为LiCoO2的表面修饰材料。修饰后的LiCoO2在截止电压为4.5 V时显示出较高比容量(180 mA·h/g)和较好的循环性能。
3.2 其它电解液/添加剂
Li等[43]通过使用 TMP(三甲基磷酸酯)为高电压电解液添加剂并用 Li1.2Mn0.54Ni0.13Co0.13O2作为正极的电池做测试。结果发现,添加1%TMP的电解液可以提高循环性能和倍率性能。在循环 100周之后有81.3%的容量保持以及5 C倍率下有150 mA·h/g的比容量。Cui等[44]以无氟 LiBOB 为 Li盐,γ-丁内酯(GBL)、环丁砜(SL)以及 DMC为溶剂用作5 V高电压电解液,其中GBL、SL具有较高的抗氧化分解能力,DMC可以降低黏度。通过测试分析表明 SL溶剂是提高电化学性能的主要因素,它不仅能提高电解液系统的抗氧化分解能力,而且减小了电极极化电阻。1 mol/L的LiBOB-SL/GBL/DMC与正极LiNi0.5Mn1.5O4和负极C的兼容性都较好。Hu等[45]以1 mol/L的LiPF6的FEC/F-EMC/F-EPE(3︰5︰2)溶液作为高电压电解液用于LiNi0.5Mn1.5O4/graphite全电池中。结果显示,这种电解液在55 ℃时比传统电解液的电压稳定性更好。通过测试循环过的正极发现在正极表面氟化电解液的分解产物起了很大作用。Schmuelling等[46]通过非原位以及原位 XRD研究了 Pyr14TFSI电解液中阴离子TFSI如何嵌入石墨中。结果发现,TFSI嵌入石墨存在一系列的阶相,而且用石墨作为正负极的放电容量受截止电压和温度的影响,阶的转变以及 TFSI嵌入石墨的成分与温度和截止电压都有关。
Sedlarikova等[47]研究了 LiClO4与 LiBF4在聚合物电解质中的热稳定性。研究发现,在惰性气体气氛下电解质相对稳定,而空气气氛下升温至450 ℃将发生电解液分解。含 LiClO4的电解质则发生爆炸,相比之下LiBF4则较为稳定。
Akita等[48]通过FT-IR(傅里叶变换红外光谱)分别研究了Li+在LiFePO4正极充、放电过程中的溶剂化和去溶剂化过程,采用的电解液为 1.0 mol/L的 LiPF6/EC +DEC(1︰1)。发现电压达到 4.3 V 时电解液还没有分解,而达到4.5 V时电解液分解形成 ROCOOLi、RCOOLi、Li2CO3和 CO2。
4 电池技术
4.1 锂空气电池
Itkis等[49]研究了锂空气电池放电产物正极上的超氧基团与碳的反应,其中碳包括活化的双键或者芳香基形成的环氧官能团和。这些反应产物都影响着锂空电池的可逆容量。有少量官能团的碳具有更好的稳定性。Luntz等[50]研究认为,锂空气电池中 Li2O2的电子传输分为极化子空穴隧穿与跃迁两种方式。前者不依赖于温度,但受绝缘的Li2O2层厚度影响很大,到达临界厚度后需要过电位才能实现隧穿;后者随温度升高传导速率明显提高,受Li2O2层厚度影响较小。通常情况下速率较快的极化子隧穿起主导作用,但因此导致较高的过电位;而电流密度较小且温度较高时,由于极化子跃迁贡献较大可以极大地减小过电位提高容量。按照这一理论,锂空气电池很难在大电流(高倍率)的情况下保持高容量。Kim等[51]制备了高导电炭黑和Co3O4的复合材料,并用聚多巴胺(polydopamine)进行了包覆,增加了Co3O4颗粒的均一性。将这种材料用作锂空气电池催化剂可以降低过电位,增强循环性能。Li等[52]在碳纸上电沉积纳米 Ni催化剂,在金属Ni的催化作用下通过CVD在碳纸上生长了碳纳米管阵列,将这种材料用作锂空气电池正极,既为反应物提供了载体,同时具有很好的催化活性,研究表明,其催化性能可以与 Pt催化剂媲美。Li等[53]以碳材料(carbon black N330)作为锂空气电池正极,研究发现,在不同气氛下进行热处理,能够增加材料的介孔,其对锂空气电池的放电容量有很大影响,因为放电产物在碳表面形成的膜有钝化作用。Zhai等[54]用大比表面积的碳材料作为锂空气电池正极,由于其多孔性,放电产物更易形成不均匀的LiO2,与Li2O2相比(4.2 V),它具有较低的电位(3.2~3.5 V)。实验表明,活性碳作为锂空电池正极既能够对放电产物进行一定的控制,又具有一定的催化活性。
5 电池表征、电池模型和测量技术
Catherino[55]提出了一种预测电化学电池热响应的方法,且其能够被系统控制得以很好地应用。此方法能够定量估计多个电池的热量产生速率、在电池产气时的热量产生率以及电池的健康状态等。Xiao等[56]通过新的模型与实验得出锂离子电池在放电过程中热量被释放,在充电过程中热量被吸收,不可逆热量主要由充放电过程中体系的熵变热(55%~70%)和焦耳热(30%~45%)提供,由离子浓度梯度造成的混合热的绝对值可达总不可逆热量的13%。Ebner等[57]报道了一种X射线拓扑成像技术,该技术可以对充放电过程中电极材料颗粒的形貌和组分进行 3D成像。使用该方法,他们发现SnO的嵌锂反应符合Core-Shell模型,并且观察到由于嵌锂后体积膨胀导致的电极颗粒开裂继而破碎的现象。Liu等[58]使用原位软 X射线衍射研究了Li(Co1/3Ni1/3Mn1/3)O2和 LiFePO4为正极的聚合物电池。通过比较这两个正极材料发现,LiFePO4在充放电过程中出现电滞后现象是由相变以及电极的导电性变化引起的。Han等[59]研究了晶界对 Li+扩散和Li脱出、嵌入引起应力的影响。作者采用 Voronoi晶界分布建模,计算显示,表观扩散系数随着晶界密度的增加而增大,这就提高了容量利用率;同时计算还表明,引入晶界减少了锂离子扩散的浓度梯度,从而减小了锂离子脱出、嵌入的应力。Illig等[60]分析了 18650型磷酸铁锂/石墨电池的阻抗谱,100~5 kHz 与集流体的电感相关,5 kHz~10 Hz 段与电解质相关,但主要来自于负极/电解质界面阻抗,与 SOC 无关,10 Hz~5 mHz低频段阻抗与SOC密切相关,主要贡献来自正极,与锂离子扩散行为有关。Ansean等[61]研究了高功率型磷酸铁锂电池的快速充电行为,对其研究的电池采用三段式快速充电,发现对电池寿命无害,即先以4 C充电至截止电压3.6 V,接着以1 C再次充电至截止电压,最后一步是恒压充电5 min,总用时20 min可充满电。
Kabitz等[62]研究了三元材料(LiNi1/3Mn1/3Co1/3O2)/石墨10 A·h软包电池随温度和充放电深度的衰减行为,10% DOD循环和搁置的性能衰减特性相当,电池内阻增加与负极膨胀和 SEI增厚较密切相关。Ponrouch等[63]在室温真空下利用碳棒的热蒸发来对锂电池电极材料进行碳包覆,这种非传统的碳包覆方式能够获得较好的碳包覆层,且能够利用沉积时间来有效控制碳包覆厚度。Remmlinger等[64]通过在线测量HEV电池内阻来估计HEV电池寿命,采用线性参数变量模型,较为简单实用。Waag等[65]基于内阻与输出电流能力相关性提出了一个在线估计电池组功率输出能力的方法,采用低成本16位单片机即可实现对电池的管理。Lee等[66]用一个多尺度多区域(multi-scale multi-domain,MSMD)的模型来模拟圆柱卷绕电池的热力学、电学及电化学性质。通过对不同结构电池充放电过程中电流与热流的模拟,发现如果电流接触点过少会引起电阻增大。更重要的是,如果电极接触点结构设计不合理,会引发电极动力学的不均一性,从而影响电池寿命。Wang等[67]提出了一个包括相干矢量机和一个有条件的三参数容量衰减模型的动力电池寿命模型,将容量衰减模型外推到一个故障阈值来估计电池寿命,该模型起始参数可随机选择,可反映容量随循环非线性衰减的趋势。
6 理论计算、界面反应及其它
Ali等[68]用有限元法模拟锂离子电池受到压力后的形变。该方法将电池各个部分用代表体积元表示,结合试验参数,可以模拟电池在受到不同应力情况下各个部分的褶皱和扭结等应变。An等[69]用一种有限元法模拟分析锂离子电池中的电极颗粒形变和物质扩散行为。该方法适用于体积形变较大的材料,如用于模拟硅负极、黏结剂与集流体构成的体系在充放电过程中的结构演化。Araujo等[70]计算研究了Li2FeSiO4的晶体结构和Li+扩散行为。结果表明,Li+在 Fe-Si-O层间沿之字形路径跃迁。GGA近似计算结果为 Li+沿二维通道传输,而GGA+U的结果则是一维通道。根据计算得到的离子跃迁活化能,室温下该材料的 Li+电导率为10−17~10−20S/cm。Hajiyani等[71]通过高通量计算研究了二元过渡金属掺杂的橄榄石结构正极材料LiMyM′1−yPO4(M,M′为过渡金属元素)的形成能、充放电电压和体积形变等性质。发现主要规律如下:随着 d轨道电子占据数的增多,Li+嵌入电位升高但材料的热稳定性随之变差。Ling等[72]计算研究了铁氰化铁中碱金属与碱土金属离子嵌入反应。结果表明,随着离子半径的增大,嵌入离子倾向占据的位置逐渐由面心变为体心,并且离子半径越大嵌入电压越高,但半径大的离子可能导致动力学性能变差。Preiss等[73]提出一个描述界面处电化学过程的渗透模型。模拟结果显示,充放电过程中电荷会在电极材料的外层积聚,类似于电化学双电层模型。该模型的建立有助于理解电荷转移动力学过程。Browning等[74]通过研究电极表面与电解液的固有化学反应,即未经过电化学循环测试,发现反应活性不仅与电极的化学性质有关还和电解液的配比有关。Filso等[75]提出一种粗略估计离子扩散通道的方法。该方法通过将晶胞内离子的电荷进行线性叠加,找出电荷密度较低的空间作为离子传输的近似通道。计算结果与文献报道的离子通道符合较好,说明该方法可用作离子导体的初步筛选。
[1] Liu H D,Fell C R,An K,et al.In-situ neutron diffraction study of the xLi2MnO3·(1-x)LiMO2(x=0,0.5;M = Ni,Mn,Co)layered oxide compounds during electrochemical cycling[J].Journal of Power Sources,2013,240:772-778.
[2] Maugeri L,Iadecolaa A,Simonelli L,et al.Study of local disorder in LiMn (Cr,Ni) O2compounds by extended X-ray absorption fine structure measurements[J].Journal of Power Sources,2013,242:202-207.
[3] Mohanty D,Huq A,Payzant E A,et al.Neutron diffraction and magnetic susceptibility studies on a high-voltage Li1.2Mn0.55Ni0.15Co0.10O2lithium ion battery cathode:Insight into the crystal structure[J].Chemistry of Materials,2013,25(20):4064-4070.
[4] Kim G Y,Park Y J.Enhanced electrochemical and thermal properties of Sm2O3coated Li (Li1/6Mn1/2Ni1/6Co1/6) O2for Li-ion batteries[J].Journal of Electroceramics,2013,31(1-2):199-203.
[5] Xiong X H,WangZ X,Yin X,et al.A modified LiF coating process to enhance the electrochemical performance characteristics of LiNi0.8Co0.1Mn0.1O2cathode materials[J].Materials Letters,2013,110:4-9.
[6] Kim M H,Kang Y C,Jeong S M,et al.Morphologies and electrochemical properties of 0.6Li2MnO3·0.4LiCoO2composite cathode powders prepared by spray pyrolysis[J].Materials Chemistry and Physics,2013,142(1):438-444.
[7] Cheng F Q,Xin Y L,Huang Y Y,et al.Enhanced electrochemical performances of 5V spinel LiMn1.58Ni0.42O4cathode materials by coating with LiAlO2[J].Journal of Power Sources,2013,239:181-188.
[8] Zhu W,Liu D,Trottier J,et al.In-situ X-ray diffraction study of the phase evolution in undoped and Cr-doped LixMn1.5Ni0.5O4(0.1≤x≤1.0)5 V cathode materials[J].Journal of Power Sources,2013,242:236-243.
[9] Xiao J,Yu X,Zheng J,et al.Interplay between two-phase and solid solution reactions in high voltage spinel cathode material for lithium ion batteries[J].Journal of Power Sources,2013,242:736-741.
[10] Guo D L,Chang Z R,Li B,et al.Synthesis of high-purity LiMn2O4with enhanced electrical properties from electrolytic manganese dioxide treated by sulfuric acid-assisted hydrothermal method[J].Journal of Solid State Electrochemistry,2013,17(11):2849-2856.
[11] Jiang J B,Du K,Cao Y B,et al.Syntheses of spherical LiMn2O4with Mn3O4and its electrochemistry performance[J].Journal of Alloys and Compounds,2013,577:138-142.
[12] Zhao S,BaiY,Ding L H,et al.Enhanced cycling stability and thermal stability of YPO4-coated LiMn2O4cathode materials for lithium ion batteries[J].Solid State Ionics,2013,247:22-29.
[13] Ni J F,Liu W,Liu J Z,et al.Investigation on a 3.2V LiCoPO4/Li4Ti5O12full battery[J].Electrochemistry Communications,2013,35:1-4.
[14] Gutierrez A,Benedek N A,Manthiram A.Crystal-chemical guide for understanding redox energy variations of M2+/3+couples in polyanion cathodes for lithium-ion batteries[J].Chemistry of Materials,2013,25(20):4010-4016.
[15] Lopez M C,Ortiz G F,Lavela P,et al.Tunable Ti4+/Ti3+redox potential in the presence of iron and calcium in NASICON-type related phosphates as electrodes for lithium batteries[J].Chemistry of Materials,2013,25(20):4025-4035.
[16] Fan C L,HanS C,Li L F,et al.Structure and electrochemical performances of LiFe1-2xTixPO4/C cathode doped with high valence Ti4+by carbothermal reduction method[J].Journal of Alloys and Compounds,2013,576:18-23.
[17] Zeilinger M,Baran V,Van W L,et al.Stabilizing the phase Li15Si4through lithium-aluminum substitution in Li15-xAlxSi4(0.4<x<0.8)single crystal X-ray structure determination of Li15Si4and Li14.37Al0.63Si4[J].Chemistry of Materials,2013,25(20):4113-4121.
[18] Becker C R,Strawhecker K E,Mcallister Q P,et al.In situ atomic force microscopy of lithiation and delithiation of silicon nanostructures for lithium ion batteries[J].Acs Nano,2013,7(10):9173-9182.
[19] Cattaneo A S,Dupke S,Schmitz A,et al.Solid state NMR structural studies of the lithiation of nano-silicon:Effects of charging capacities, host-doping, and thermal treatment[J].Solid State Ionics,2013,249:41-48.
[20] Lee J K,Kim B K,Yoon W Y.Irreversible behaviors and kinetics of lithiated products in SiOxanodes with inserting Li contents in Li ion batteries[J].Japanese Journal of Applied Physics,2013,52(10),doi:10.7567/jjap.52.10mb10.
[21] Li J C,Xiao X C,Cheng Y T,et al.Atomic layered coating enabling ultrafast surface kinetics at silicon electrodes in lithium ion batteries[J].Journal of Physical Chemistry Letters,2013,4(20):3387-3391.
[22] Stournara M E,Xiao X C,Qi Y,et al.Li segregation induces structure and strength cChanges at the amorphous Si/Cu interface[J].Nano Letters,2013,13(10):4759-4768.
[23] Wang Y H,Liu Y P,Zheng J Y,et al.Electrochemical performances and volume variation of nano-textured silicon thin films as anodes for lithium-ion batteries[J].Nanotechnology,2013,24( 42):doi:10.1088/0957 -4484/24/42/424011.
[24] Wong D P,Tseng H P,Chen Y T,et al.A stable silicon/graphene composite using solvent exchange method as anode material for lithium ion batteries[J].Carbon,2013,63:397-403.
[25] Choi Z,Kramer D,Monig R.Correlation of stress and structural evolution in Li4Ti5O12-based electrodes for lithium ion batteries[J].Journal of Power Sources,2013,240:245-251.
[26] Fan X Y,Shi Y X,Wang J J,et al.Electrochemical synthesis and lithium storage properties of three-dimensional porous Sn-Co alloy/CNT composite[J].Ionics,2013,19(11):1551-1558.
[27] Hori H,Shikano M,Kobayashi H,et al.Analysis of hard carbon for lithium-ion batteries by hard X-ray photoelectron spectroscopy[J].Journal of Power Sources,2013,242:844-847.
[28] Hwang Y H,Bae E G,Sohn K S,et al.SnO2nanoparticles confined in a graphene framework for advanced anode materials[J].Journal of Power Sources,2013,240:683-690.
[29] Liu H D,Huang J M,Xiang C J,et al.In situ synthesis of SnO2nanosheet/graphene composite as anode materials for lithium-ion batteries[J].Journal of Materials Science:Materials in Electronics,2013,24(10):3640-3645.
[30] Wang D N,Yang J L,Li X F,et al.Layer by layer assembly of sandwiched graphene/SnO2nanorod/carbon nanostructures with ultrahigh lithium ion storage properties[J].Energy & Environmental Science,2013,6(10):2900-2906.
[31] Zhang Z L,Wang Y H,Li D,et al.Mesoporous Mn0.5Co0.5Fe2O4nanospheres grown on graphene for enhanced lithium storage properties[J].Industrial & Engineering Chemistry Research,2013,52(42):14906-14912.
[32] Momma T,Jeong M,Yokoshima T,et al.Sn-O-C composite anode for Li secondary battery synthesized by an electrodeposition technique using organic carbonate electrolyte[J].Journal of Power Sources,2013,242:527-532.
[33] Noh K W,Dillon S J.Morphological changes in and around Sn electrodes during Li ion cycling characterized by in situ environmental TEM[J].Scripta Materialia,2013,69(9):658-661.
[34] Yun Y S,Jin H J.Electrochemical performance of heteroatom- enriched amorphous carbon with hierarchical porous structure as anode for lithium-ion batteries[J].Materials Letters,2013,108:311-315.
[35] He Y B,Liu M,Huang Z D,et al.Effect of solid electrolyte interface(SEI)film on cyclic performance of Li4Ti5O12anodes for Li ion batteries[J].Journal of Power Sources,2013,239:269-276.
[36] Jang J Y,Park G,Lee S M,et al.Functional electrolytes enhancing electrochemical performance of Sn-Fe-P alloy as anode for lithium-ion batteries[J].Electrochemistry Communications,2013,35:72-75.
[37] Liu Y,Liu X H,Nguyen B M,et al.Tailoring lithiation behavior by interface and bandgap engineering at the nanoscale[J].Nano Letters,2013,13 (10):4876-4883.
[38] Chiappone A,Jeremias S,Bongiovanni R,et al.NMR study of photo-crosslinked solid polymer electrolytes:The influence of monofunctional oligoethers[J].Journal of Polymer Science Part B:Polymer Physics,2013,51(21):1571-1580.
[39] Chiappone A,Nair J R,Gerbaldi C,et al.Nanoscale microfibrillated cellulose reinforced truly-solid polymer electrolytes for flexible,safe and sustainable lithium-based batteries[J].Cellulose,2013,20(5):2439-2449.
[40] Amiki Y,Sagane F,Yamamoto K,et al.Electrochemical properties of an all-solid-state lithium-ion battery with an in-situ formed electrode material grown from a lithium conductive glass ceramics sheet[J].Journal of Power Sources,2013,241:583-588.
[41] Hartmann P,Leichtweiss T,Busche M R,et al.Degradation of NASICON-type materials in contact with lithium metal:Formation of mixed conducting interphases(MCI)on solid electrolytes[J].Journal of Physical Chemistry C,2013,117(41):21064-21074.
[42] Morimoto H,Awano H,Terashima J,et al.Preparation of lithium ion conducting solid electrolyte of NASICON-type Li1+xAlxTi2-x(PO4)3(x=0.3)obtained by using the mechanochemical method and its application as surface modification materials of LiCoO2cathode for lithium cell[J].Journal of Power Sources,2013,240:636-643.
[43] Li Z D,Zhang Y C,Xiang H F,et al.Trimethyl phosphite as an electrolyte additive for high-voltage lithium-ion batteries using lithium-rich layered oxide cathode[J].Journal of Power Sources,2013,240:471-475.
[44] Cui X L,Zhang H M,Li S Y,et al.Electrochemical performances of a novel high-voltage electrolyte based upon sulfolane and gamma-butyrolactone[J].Journal of Power Sources,2013,240:476-485.
[45] Hu L B,Zhang Z C,Amine K. Fluorinated electrolytes for Li-ion battery:An FEC-based electrolyte for high voltage LiNi0.5Mn1.5O4/ graphite couple[J].Electrochemistry Communications,2013,35:76-79.
[46] Schmuelling G,Placke T,Kloepsch R,et al.X-ray diffraction studies of the electrochemical intercalation of bis (trifluoromethanesulfonyl) imide anions into graphite for dual-ion cells[J].Journal of Power Sources,2013,239:563-571.
[47] Sedlarikova M,Vondrak J,Musil M,et al.Explosivity of lithium perchlorate in gel polymer electrolytes[J].Polymer Composites,2013,34(11):1970-1974.
[48] Akita Y,Segawa M,Munakata H,et al.In-situ Fourier transform infrared spectroscopic analysis on dynamic behavior of electrolyte solution on LiFePO4cathode[J].Journal of Power Sources,2013,239:175-180.
[49] Itkis D M,Semenenko D A,Kataev E Y,et al.Reactivity of carbon in lithium-oxygen battery positive electrodes[J].Nano Letters,2013,13(10):4697-4701.
[50] Luntz A C,Viswanathan V,Voss J,et al.Tunneling and polaron charge transport through Li2O2in LiO2batteries[J].Journal of Physical Chemistry Letters,2013,4(20):3494-3499.
[51] Kim D S,Park Y J.Ketjen black/Co3O4nanocomposite prepared using polydopamine pre-coating layer as a reaction agent:Effective catalyst for air electrodes of Li/air batteries[J].Journal of Alloys and Compounds,2013,575:319-325.
[52] Li Y F,Huang Z P,Huang K,et al.Hybrid Li-air battery cathodes with sparse carbon nanotube arrays directly grown on carbon fiber papers[J].Energy & Environmental Science,2013,6(11):3339-3345.
[53] Li Y L,Li X F,Geng D S,et al.Carbon black cathodes for lithium oxygen batteries:Influence of porosity and heteroatom-doping[J].Carbon,2013,64:170-177.
[54] Zhai D Y,Wang H H,Yang J B,et al.Disproportionation in LiO2batteries based on a large surface area carbon cathode[J].Journal of the American Chemical Society,2013,135(41):15364-15372.
[55] Catherino H A.Estimation of the heat generation rates in electrochemical cells[J].Journal of Power Sources,2013,239:505-512.
[56] Xiao M,Choe S Y.Theoretical and experimental analysis of heat generations of a pouch type LiMn2O4/carbon high power Li-polymer battery[J].Journal of Power Sources,2013,241:46-55.
[57] Ebner M,Marone F,Stampanoni M,et al.Visualization and quantification of electrochemical and mechanical degradation in Li ion batteries[J].Science,2013,342(6159):716-720.
[58] Liu X S,Wang D D,Liu G,et al.Distinct charge dynamics in battery electrodes revealed by in situ and operando soft X-ray spectroscopy[J].Nature Communications,2013,4:doi:10.1038/ ncomms3568.
[59] Han S,Park J,Lu W,et al.Numerical study of grain boundary effect on Li+effective diffusivity and intercalation-induced stresses in Li-ion battery active materials[J].Journal of Power Sources,2013,240:155-167.
[60] Illig J,Schmidt J P,Weiss M,et al.Understanding the impedance spectrum of 18650 LiFePO4-cells[J].Journal of Power Sources,2013,239:670-679.
[61] Ansean D,Gonzalez M,Viera J C,et al.Fast charging technique for high power lithium iron phosphate batteries:A cycle life analysis[J].Journal of Power Sources,2013,239:9-15.
[62] Kabitz S,Gerschler J B,Ecker M,et al.Cycle and calendar life study of a graphite vertical bar Li(Ni1/3Mn1/3Co1/3)O2Li-ion high energy system.Part A:Full cell characterization[J].Journal of Power Sources,2013,239:572-583.
[63] Ponrouch A,Goni A R,Sougrati M T,et al.A new room temperature and solvent free carbon coating procedure for battery electrode materials[J].Energy & Environmental Science,2013,6(11):3363-3371.
[64] Remmlinger J,Buchholz M,Soczka-guth T,et al.On-board state-of-health monitoring of lithium-ion batteries using linear parameter-varying models[J].Journal of Power Sources,2013,239:689-695.
[65] Waag W,Fleischer C,Sauer D U.Adaptive on-line prediction of the available power of lithium-ion batteries[J].Journal of Power Sources,2013,242:548-559.
[66] Lee K J,Smith K,Pesaran A,et al.Three dimensional thermal-,electrical-,and electrochemical-coupled model for cylindrical wound large format lithium-ion batteries[J].Journal of Power Sources,2013,241:20-32.
[67] Wang D,Miao Q,Pecht M.Prognostics of lithium-ion batteries based on relevance vectors and a conditional three-parameter capacity degradation model[J].Journal of Power Sources,2013,239:253-264.
[68] Ali M Y,Lai W J,Pan J.Computational models for simulations of lithium-ion battery cells under constrained compression tests[J].Journal of Power Sources,2013,242:325-340.
[69] An Y H,Jiang H Q.A finite element simulation on transient large deformation and mass diffusion in electrodes for lithium ion batteries[J].Modelling and Simulation in Materials Science and Engineering,2013,21(7):doi:10.1088/0965-0393/21/7/074007.
[70] Araujo R B,Scheicher R H,Dealmeida J S,et al.First-principles investigation of Li ion diffusion in Li2FeSiO4[J].Solid State Ionics,2013,247:8-14.
[71] Hajiyani H R,Preiss U,Drautz R,et al.High-throughput ab initio screening of binary solid solutions in olivine phosphates for Li-ion battery cathodes[J].Modelling and Simulation in Materials Science and Engineering,2013,21(7):doi:10.1088/0965-0393/21/7/074004.
[72] Ling C,Chen J J,Mizuno F.First-principles study of alkali and alkaline earth ion intercalation in iron hexacyanoferrate:The important role of ionic radius[J].Journal of Physical Chemistry C,2013,117(41):21158-21165.
[73] Preiss U,Borukhovich E,Alemayehu N,et al.A permeation model for the electrochemical interface[J].Modelling and Simulation in Materials Science and Engineering,2013,21(7):doi:10.1088/0965-0393/21/7/074006.
[74] Browning K L,Baggetto L,Unocic R R,et al.Gas evolution from cathode materials:A pathway to solvent decomposition concomitant to SEI formation[J].Journal of Power Sources,2013,239:341-346.
[75] Filso M O,Turner M J,Gibbs G V,et al.Visualizing lithium-ion migration pathways in battery materials[J].Chemistry:A EuropeanJournal,2013,19(46):15535-15544.

