沉积物中汞的甲基化研究进展
阴皎阳,尹大强,王 锐
同济大学环境科学与工程学院 污染控制与资源化研究国家重点实验室,上海 200092
沉积物中汞的甲基化研究进展
阴皎阳,尹大强,王 锐*
同济大学环境科学与工程学院 污染控制与资源化研究国家重点实验室,上海 200092
汞是环境中存在的一种重要污染物质,其毒性与之化学形态密切相关。环境中的汞主要以无机汞形态存在,然而无机汞可以通过甲基化作用转化为毒性更强的甲基汞,从而给受到暴露的生物及人类带来更高的健康风险。沉积物是汞在水生环境系统中的主要分布相,也是无机汞甲基化过程发生的主要场所。沉积物中汞的甲基化过程受到生物种类、汞的生物可利用性等生物因素及温度、含硫化合物、有机质、氧化还原条件等环境理化性质的影响。本文对汞在沉积物中甲基化过程的作用机制及其影响因素的研究现状及最新进展进行了总结,并对未来更深入的研究进行了展望。
汞;沉积物;甲基化;生物可利用性
汞(Hg)是环境中天然存在的一种有毒有害重金属元素。1950年在日本暴发的水俣病事件[1,2]及1970年在伊拉克发生的杀虫剂污染稻米中毒事件[3],都是由汞引发的,随后,汞这一全球性污染物越来越受到人们的关注。2013年10月7日~10日,由联合国环境规划署主办的“汞条约外交会议”在日本熊本召开,会议最终表决通过了旨在控制和减少全球汞排放的《水俣公约》,包括中国在内的87个国家和地区的代表共同签署了该公约,标志着全球携手减少汞污染迈出第一步。
环境中的汞主要以元素汞、无机汞和有机汞三大类形态存在。无机汞毒性通常由职业暴露引起且主要积累在肾脏中,可导致肾毒性[4]。气态单质汞(Hg0)可通过呼吸作用进入人体并在大脑中产生蓄积[5]。与无机汞和单质汞相比,有机汞的毒性更甚。环境中的有机汞包含甲基汞(methylmercury, MeHg)、二甲基汞(dimethylmercury, DMHg)、甲基乙基汞(methylethylmercury, MEHg)、二乙基汞(diethylmercury, DEHg)等形态,其中以MeHg最为普遍。MeHg在海产品和淡水鱼中广泛存在,在鱼的肌肉组织中MeHg的含量占总汞的95%~97%[6]。MeHg在水生生态系统中可经食物链逐级放大,并最终通过人类食用鱼、虾、贝类而对人体健康造成威胁,例如MeHg可以穿过人体的血脑屏障,产生神经毒性,造成一系列的健康风险[7]。
当前,全球汞污染状况不容小视,并可通过大气汞进行跨国传输。大气汞的来源包括自然源和人为源,据估算,全球人为源(如化石燃料燃烧、金属冶炼等)每年约向大气中排放2 100 t汞,而自然源(如火山爆发、土壤和水体中汞挥发等)排放每年约为1 800~5 800 t[8]。大气中的汞主要以气态单质汞、活性气态汞和颗粒汞的形态存在,其中Hg0可随大气环流在全球范围内进行迁移,并通过干湿沉降进入水生和陆地生态系统。水体或沉积物中的Hg0被氧化为Hg2+后可以在生物或非生物的作用下转化为MeHg,且以沉积物中的生物甲基化过程最为显著。环境中各种形态的汞在大气循环、吸附/解吸、沉降/再悬浮等物理作用下进行迁移,并发生复杂的形态转化,经过一系列的生物地球化学循环(见图1),大部分汞最终分布于沉积物中。
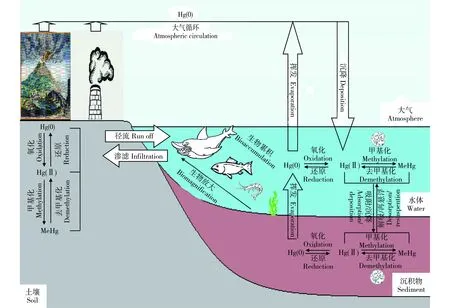
图1 汞的生物地球化学循环图 Fig. 1 Biogeochemical cycling of Hg
事实上,沉积物是汞在环境中的主要分布相,全球范围超过98%的汞存在于海洋沉积物中[9]。众多研究表明,沉积物中的汞对水生生态系统中的汞循环有着至关重要的作用:一方面,由于沉积物及悬浮颗粒物对汞具有很强的亲和势,水体中的汞通过颗粒物沉降等滞留在沉积物中[10,11],因而成为水生环境中汞最主要的汇;另一方面,沉积物又是许多水生生物(尤其是底栖生物)吸收汞的主要途径[12],在一些污染严重的地区,汞通过沉积物的再悬浮重新进入水体[13],使之成为水体汞的源。沉积物中的汞含量与沿岸汞排放历史密切相关,其浓度通常先随深度的增加而升高,在10~20 cm处达到最高,之后随深度的增加迅速降低[14-16]。在未受污染的地区,沉积物中总汞含量约为0.02~0.4 μg·g-1,而在城市、工业区及采矿区的沉积物中总汞含量可达100 μg·g-1[17]。一般而言,沉积物中MeHg含量约占总汞的1%~1.5%[17],但在沉积物的孔隙水中,该比例可达50%左右[18]。
由上可知,沉积物对于汞的生物地球化学循环,尤其是在汞的甲基化过程中扮演着重要角色。本文将介绍近几十年来关于沉积物中汞的甲基化研究历史及最新成果,并对甲基化的途径、机制及其影响因素进行总结,以期为今后进一步研究的开展提供参考。
1 无机汞在沉积物中的甲基化
沉积物中汞的甲基化包括生物甲基化和非生物甲基化,其中以生物甲基化为主导。甲基化反应的强弱通常用甲基化速率表征,甲基化速率越高,甲基化作用就越强,潜在的环境及生态风险也越大。沉积物甲基化速率的地区差异较大,低可低至0.2%·d-1甚至接近于零,高可高至5%·d-1,且其随沉积物深度[19,20]、含硫化合物[21,22]、有机质含量[23]、温度[24]等环境条件的变化而改变。
1.1 生物甲基化
汞的生物甲基化最早是由Wood证实的[25],他发现沉积物中的产甲烷菌利用甲基钴氨素将无机汞转化为MeHg。随后,有研究发现,一些革兰氏阳性菌和革兰氏阴性菌[26]及藻类[27]也可以甲基化无机汞。水生生态系统中汞的甲基化过程主要发生在沉积物中,以沉积物—水体交界面最为活跃,且甲基化速率随沉积物深度的增加迅速降低[28-30]。
大量研究表明[31-34],硫酸盐还原菌(sulfate reducing bacteria, SRB)是沉积物中汞甲基化的主要作用微生物。除SRB外,产甲烷菌(methanogens)和铁还原细菌(iron reducing bacteria, IRB)也被认为是沉积物中汞甲基化的重要生物媒介[32,34]。普遍认为,汞的生物甲基化是在微生物作用下将从无机汞转化为毒性更高的甲基汞的过程,而Hu[35]等的最新研究发现,在厌氧条件下,硫酸盐还原菌D. desulphuricans ND132可以直接氧化并甲基化元素汞(Hg0),D. alaskensis G20能氧化但不能甲基化Hg0,而铁还原细菌G. sulphurreducens PCA在有半胱氨酸存在的基质中可以氧化并甲基化Hg0, 这意味着甲基化和非甲基化细菌组成的微生物群落可以共同促进MeHg的生成。
通常认为,汞的甲基化是一种酶催化的细胞内反应。早期研究者认为[36],汞的甲基化过程是SRB细胞内乙酰辅酶A(acetyl coenzyme A, acetyl CoA)碳代谢途径的“代谢错误”现象。随后的研究发现[37],MeHg的产生并不局限于SRB的CoA代谢途径。SRB多以低分子量脂肪酸、醇类和H2作为电子供体[33],在还原硫酸盐的同时,对无机汞产生甲基化作用。然而,SRB甲基化过程的甲基转移酶或甲基供体目前还未能完全确定[38]。除了细胞内甲基化,一些研究者认为细胞外甲基化也可能发生,因为微生物代谢产生的甲基钴氨素可以在离体条件下自发地将溶解态的Hg2+甲基化[39-41]。Parkman等[42]发现,细胞外甲基化还可以通过细菌的胞外酶催化实现,同时伴随着有机质的分解。
由于汞的甲基化主要是一个细胞内过程,因而细胞对于无机汞的吸收是该反应的关键。环境中的无机汞通常不是以自由离子形式存在的,而是与各种有机或无机配体,如氢氧化物、氯化物、硫化物、有机质等相结合形成的复合物。近年的研究表明,汞的生物可利用性主要是由中性溶解态的汞形态控制的,在沉积物中,中性的Hg-S复合物被认为是汞可生物利用的主要形态。研究者在实地调查中发现,汞的甲基化速率与溶解的Hg-S复合物的浓度成正比,证实了该观点[43,44]。在实验室条件下,无机汞与硫醇形成的复合物Hg2+-thiol也可被生物甲基化,但该过程在自然条件下能否实现仍有待考察[45]。另外,通常认为HgS(s)是不可被生物利用的形态,但也有研究者发现,溶解的HgS可以被甲基化[46]。目前,关于甲基化细菌对汞的吸收过程与运输机制仍然不太清楚。
近来,研究者试图从基因的角度对生物甲基化过程的作用机理进行探索,并已取得重要进展。Parks等[47在脱硫弧菌ND132(Desulfovibrio desulfuricans, ND132)和地杆菌PCA(Geobacter sulfurreducens, PCA)中发现了两个基因簇——hgcA和hgcB,缺失两者中的任意一种都将导致微生物甲基化功能的丧失,修复后其甲基化功能则可获得不同程度的恢复。hgcA和hgcB分别编码了一种假定的类咕啉蛋白质HgcA和一种2[4Fe-4S]铁氧化还原蛋白HgcB,这两种蛋白质在SRB甲基化过程中分别作为甲基载体和类咕啉辅助因子还原的电子供体。在目前已测序的微生物中,hgcA和hgcB存在于所有甲基化微生物中,而在非甲基化微生物中则均不存在,这表明在已测序的甲基化微生物中存在一种普遍的汞甲基化路径。
1.2 非生物甲基化
相对于生物甲基化来说,汞的非生物甲基化途径对甲基化的贡献较小,只有前者的十分之一[48],且仅在存在适当的甲基供体时发生[49]。甲基碘化物、二甲基硫化物等小分子有机物和富里酸、腐殖酸等溶解态的大分子有机质可促进MeHg的产生,而甲基钴氨素、甲基铅、甲基锡等含甲基的物质则可以通过转甲基作用将无机汞转化为MeHg。
早期研究认为,利用甲基钴氨素发生的甲基化过程,必须在有诸如脱硫芽孢弧菌的严格厌氧菌存在的条件下,通过酶催化作用来完成[34,37,50]。但在实验室条件下,该反应可在无生物的条件下迅速进行[41,51],推测其反应方程式为:

(1)
甲基锡在环境中广泛存在,其对Hg2+的甲基化作用被证实是水环境中MeHg的一个重要非生物来源[52,53]。有研究者通过研究三甲基锡对Hg2+的转甲基作用速率,发现其为pH,氯化物浓度及离子强度的函数,并推测该反应方程式为[52]:
Me3Sn4++Hg2+→Me2Sn4++MeHg2+
(2)
相比甲基锡等物质,腐殖质在沉积物汞的甲基化过程中扮演着更为重要的角色,主要有以下依据:其一,腐殖质在环境中的含量很高,沉积物中也不例外;其二,腐殖质多与可利用的溶解态汞以络合物的形式相结合,使反应易于发生;其三,一些模型研究发现,腐殖质可有效地将Hg2+转化为MeHg[54]。
此外,无机汞与聚硅酮、环硅氧烷、聚二甲硅氧烷等含硅化合物反应,均可产生MeHg[55]。光化学反应诱发的无机汞离子与甲醇、乙醇、乙酸、丙酸等物质发生的烷基转移作用也可产生MeHg[56]。
2 甲基汞在沉积物中的去甲基化过程
汞的去甲基化经常与甲基化同时发生,但目前关于沉积物中汞的去甲基化研究远少于对甲基化的研究。已有研究普遍认为,MeHg在沉积物中的去甲基化过程是一个生物过程,主要包括两条生物途径:有机汞裂解酶催化途径和共代谢途径。有机汞裂解酶是一种由mer-B基因编码的MerR蛋白质,特异性地存在于对汞具有广谱抗性的细菌中。这类细菌可以在裂解酶的催化下,将MeHg的C-Hg链断开,随后生成的Hg2+又可以通过两种途径继续降解。一种是还原性mer途径,在mer-A操纵子的作用下编码的汞离子还原酶可以把MeHg断裂产生的Hg2+最终还原为Hg0,同时伴随着甲烷的产生。另一种是氧化途径,在该过程中,MeHg断裂产生的Hg2+不会被还原,且释放的甲烷被氧化为CO2,因而最终产物为Hg2+和CO2[17]。共代谢途径则是一种非有机汞裂解酶催化的过程。该过程中,细菌利用小分子有机物代谢过程中产生的能量来裂解MeHg生成Hg2+,甲烷和CO2都可能是该过程的最终产物[58]。硫酸盐还原菌或产甲烷菌都可能参与沉积物中MeHg的去甲基化过程,但具体何种微生物通过何种途径起主导作用取决于沉积物的环境条件[59]。
在水体中,光降解是环境中MeHg非生物去甲基化的主要途径,其中,与硫结合的甲基汞离子(CH3HgS-)可以被迅速地光降解,而甲基汞离子和甲基汞氢氧化物由于其光吸收率较低,不易发生光降解[60,61]。Sellers 等[61]认为MeHg在表层水中的光降解是水环境中汞的地球化学循环的重要过程,而在沉积物中,MeHg的去甲基化过程还是以生物途径为主[62]。除此之外,一些化学物质,如硒氨基酸,在实验室条件下也可使MeHg发生去甲基化[63],但该过程在环境中是否存在还有待探索。
3 无机汞在沉积物中甲基化过程的主要影响因素
近几十年来,关于沉积物中汞甲基化过程的大量研究发现,该过程受到一系列生物及理化因素的影响,如生物种类、汞的生物可利用性、温度、含硫化合物、有机质等,具体内容介绍如下。
3.1 生物因素
不同种类生物的甲基化效率不同。Schaefer等通过研究两种实验菌种,Geobacter sulfurreducens(IRB)和 Desulfovibrio desulfuricans ND132(SRB),发现当溶液中存在硫醇化合物时,SRB比IRB更易甲基化其摄入的无机汞。并不是所有的SRB都可以甲基化无机汞,具有甲基化能力的SRB有脱硫弧菌目(Desulfovibrionales)、脱硫杆菌目(Desulfobacterales)及除硫单胞菌目(Desulfuromonadales),研究者关注最多的是脱磷孤菌属(Desulfovibrio)[64-66]和地杆菌属(Geobacter)[35];能够利用醋酸的SRB较脱磷孤菌属有更高的甲基化效率[67];Macalady等[68]通过对比脱硫杆菌属和脱磷孤菌属,发现脱硫杆菌是湖泊沉积物中重要的甲基化生物,且数量更多。
微生物的生长阶段也是影响甲基化效率的一个重要因素,但现有研究结论存在差异。早期研究发现,处于生长期的细胞容易促进Hg0的形成,不再生长的活细胞易发生去甲基化,而死亡细胞则导致MeHg的生成[69]。近来,Biswas等[70]通过对脱硫弧菌的研究发现,处于对数生长中期和对数生长晚期的菌株的甲基化速率相近,而处于稳定期晚期的菌株甲基化效率为前两者的三倍,即稳定期的菌株更有利于MeHg的产生。也有研究者发现,生长期是菌株甲基化无机汞的主要阶段,进入稳定期后,MeHg的产生量会降低[35]。
汞的生物可利用性是影响其包括甲基化过程在内的生物地球化学循环的一个限制性因素。汞的生物可利用性是由环境理化因子、生物因素等多因素控制的,包括汞的化学形态、颗粒结合态与溶解态的比例、环境中存在的配体及电子受体、微生物群落的活性等[71]。Han等[72]发现,归一化为硫酸盐还原速率的甲基化速率与汞的颗粒物—水分配系数的对数成负线性相关,表明汞的生物可利用性是影响甲基化过程的一个重要因素。在四个北极圈的湖泊沉积物中,研究者发现甲基化速率与孔隙水中无机汞含量呈明显的正相关关系[73]。环境中存在的Hg2+是通过主动运输进入微生物细胞内的,而细胞外介质中存在的半胱氨酸及某些硫醇可以结合Hg2+,从而促进微生物对Hg2+的摄入和甲基化过程,而另一些硫醇则会起抑制作用[64,74]。利用稳定同位素示踪技术,Hintelmann等[75]发现汞的来源对其生物可利用性也有影响,实验中加入的示踪物199Hg2+比环境中原有的Hg2+更易于被生物利用,而新加入的Me202Hg与环境中原有的MeHg的去甲基化速率则没有明显差异。
生物间的相互作用也可能会影响MeHg的产生。Park等[50]研究发现,在无硫酸盐的条件下,脱硫弧菌与海藻甲烷球菌共生可以以较快的速率将Hg2+转化为MeHg,而这两种微生物在相同条件下单独作用时无法产生该效果。SRB可以通过氧化有机质增加H2和醋酸盐的活性,使其被产甲烷菌利用,从而与产甲烷菌共生[76]。通过对比在高硫酸盐含量(1~16 mmol·L-1)和硫酸盐缺乏(<100 μmol·L-1)两种不同地球化学条件下沉积物中MeHg的生成量,研究发现在硫酸盐缺乏的条件下,MeHg产生量更高[77],这可能是由于产甲烷菌和SRB相互作用的结果。此外,汞的生物地球化学循环还受到底栖生物活动的影响。研究者[78,79]认为,底栖生物通过两种方式促进微生物的活性,一是产生微小的氧化还原界面,增强SRB的活性和Hg2+的生物可利用性;二是促进了不稳定有机物向沉积物深层的传递及还原性代谢产物(如:硫化物)的移除。然而,底栖生物诱导高MeHg净产生量的主导因素究竟是甲基化过程的促进亦或是去甲基化过程的抑制,目前尚未明确。
3.2 温 度
多数研究者发现,夏季尤其是夏末沉积物中汞的甲基化效率最高[80-83],可能是由于温度变化所导致微生物的活性改变而引起的[84]。Yu等[80]研究发现,晚春时微生物的甲基化潜力较低,而在夏季后期较高;且春季去甲基化产物以CH4为主,夏季则以CO2为主。这表明,温度的变化不仅会影响MeHg的净产量,还可能影响反应过程的作用方式。孔隙水中的MeHg浓度也随季节发生变化,其在春季相对较低,随着温度的升高逐渐上升,到夏末秋初达到较高水平,且沉积物中的MeHg通量也在夏季达到峰值[81,82]。
然而,在不同的环境条件下,温度对汞的甲基化的影响可能截然不同。Marvin-DiPasquale等[85]考察了冬季末、春季、秋季三个季节的甲基化和去甲基化过程,发现在冬季末MeHg的产生速率与硫酸盐还原速率成正相关,MeHg的产生量也在该阶段达到最大,随后逐渐降低。推测这可能是由于两方面的原因造成的:其一,温度升高,MeHg的去甲基化作用加强;其二,在温暖的季节,孔隙水中的硫化物和固相中硫酸盐还原所产生的还原态硫会增加,并抑制汞的甲基化过程。
总的来说,温度对汞的甲基化及MeHg的去甲基化过程均有重要影响。一般而言,相对较高的温度可以通过增强微生物的活性而促进甲基化进程,去甲基化则在较低温度下作用更为明显,这可能是由于当温度升高时,甲基化作用较去甲基化作用增长更快[17]。
3.3 含硫化合物
沉积物中的含硫化合物是控制汞甲基化过程的一个重要因素[86,87]。高的甲基化速率通常与高的溶解性硫酸盐含量相一致[34,88],而高浓度的硫化物则会抑制甲基化过程。Hollweg等[88]发现,甲基化速率与孔隙水中的硫酸盐含量呈正相关,而与硫化物含量呈负相关。当向沉积物中加入硫化物后,硫酸盐的还原速率和MeHg的浓度随硫化物浓度的升高呈指数下降,这是由于:当硫化物浓度低于10-5mol·L-1时,溶解态的汞主要以HgS(0)(aq)的形态存在,其具有高的生物可利用性;而当硫化物浓度大于10-5mol·L-1时,溶解态的汞主要以HgSH2·的形态存在,其不易被生物利用[89]。也有研究者发现,在受污染的沉积物中,硫酸盐的生物可利用性与沉积物中MeHg的占比、MeHg浓度、甲基化速率并无明显关系[33],这可能是由于多种影响因素共同作用的结果。总的来说,当存在可被生物利用的硫酸盐、而硫化物浓度较低时,甲基化过程更容易进行。
3.4 有机质
沉积物中的有机质可以通过多种途径对汞的甲基化过程产生不同影响。一方面,溶解性有机质(dissolved organic matter, DOM)可以通过增强微生物的活性来促进MeHg的产生。高含量的有机质使沉积物维持较低的氧化还原电位,从而有利于甲基化的发生[90]。同时,有机质可以作为甲基化微生物的营养物质,以此增加其活性,使甲基化效率提高[91],并且,有研究发现Hg2+的甲基化速率随着DOM分子量的上升而提高[92]。另一方面,有机质可以改变汞的生物可利用性,进而影响甲基化过程。DOM与汞之间会发生强烈的相互作用,影响汞在水环境中的存在形态、溶解性、迁移性及其毒性,这种相互作用主要归因于汞与有机质上的还原态硫官能团的结合[93]。研究者发现,沉积物中有机硫的含量与甲基化速率呈负相关,其认为在有机硫含量较低的沉积物中,汞在固相中的分布较少,而多以溶解态存在,因而汞的生物可利用性增强,有利于甲基化的发生[88]。因此,在减少水体中营养物质以防止富营养化发生时,可能会致使沉积物中大量存在的汞的生物可利用性加强,从而加剧MeHg的生成[84]。然而,与DOM相比,环境中存在的硫化物对汞的结合力更强,这意味着硫化物可与DOM竞争结合汞,甚至可能会产生DOM-Hg-MS复合物,关于这三者之间的相互作用机制还有待进一步的研究[94]。
由此可知,有机质是汞甲基化过程中的重要影响因子,其与硫化物等其他因素的相互作用所产生的复合效应尤其值得关注和进一步的探索。
3.5 氧化还原条件
汞的甲基化过程在厌氧或好氧状态下均可发生, 但多数研究表明,其在厌氧条件下更为强烈[81, 88, 95]。厌氧条件下,几乎100%溶解态的无机汞都能被甲基化[81]。DeLaune等[95]在实验条件下对比了沉积物在厌氧和好氧状态下MeHg的产生量,发现当氧化还原电位从-200 mV(强还原状态)上升至+250 mV(中度还原状态)时,MeHg的产生量减少了95%。
许多研究者发现,在氧化还原交替地带,如沉积物—水体交界面、潮间带[96-98]等,甲基化过程最为活跃,MeHg的含量也最高。这主要是由于氧化还原条件的频繁变化可以增强包括甲基化生物在内的微生物的活性[99]。此外,一些人为活动也可以通过改变沉积物的氧化还原条件对甲基化过程产生影响。在航道沉积物中,孔隙水的更新和氧化还原状态的更替刺激了微生物的活性,使之具有较高的甲基化能力[97]。人类的疏浚活动会诱发沉积物颗粒再悬浮,新的营养物质进入孔隙水,随之而来的浮游生物暴发使得周围环境处于缺氧或厌氧状态,这都有利于汞的甲基化[100]。
与甲基化过程相反,去甲基化过程在好氧状态下更容易被加强[95]。但也有研究者认为,去甲基化速率在好氧状态下会降低[98,101]或几乎不受氧化还原条件影响[82,102]。
3.6 盐 度
大多数研究发现,汞的甲基化过程在海洋及河口沉积物中的强度低于淡水沉积物,而这一差异主要归因于盐度的不同[17,33103]。有研究发现,高盐度沉积物中的甲基化水平只有低盐度沉积物中甲基化水平的40%[103],有机淡水沉积物中汞的甲基化速率较矿化淡水沉积物及咸水沉积物高出2~5倍[33]。这可能是在盐度较高的条件下,部分汞以不易被生物利用的络合形态存在[17],此外盐度的差异改变了反应系统中甲基供体的电子密度及金属离子的亲电子性[104]。高盐度对甲基化过程的抑制作用在还原态条件下尤为显著,并可以增强MeHg的去甲基化[105]。然而,也有部分研究发现,随着沉积物盐度的上升,MeHg的浓度显著增加[106]。
3.7 pH
pH对汞的甲基化的影响通常表现为与其它环境条件(如氧化还原条件)的交互作用。例如,在好氧的表层沉积物及沉积物-水体交界面,随着pH的降低,甲基化速率提高[106-108],MeHg产量甚至可增加2~3倍[107];而在厌氧沉积物中,MeHg的产生量与pH的变化趋势相一致,即pH降低时,MeHg的产生量降低[109-110]。而pH单一因素则可能通过影响汞的生物可利用性和微生物摄入量来影响汞的甲基化。一方面,pH降低时,颗粒物对孔隙水中汞的吸附能力增加,因而可供生物利用的无机汞含量下降[109],导致MeHg生成量减少。另一方面,甲基化微生物对Hg2+的摄入量与pH值直接相关[111,112],即使在pH变化幅度很小的情况下(7.3~6.3),pH的降低也能大大促进微生物对Hg2+的摄入[111]。 在实际环境中,这两种机制可能同时存在,并与其它影响因素共同作用,从而综合影响汞的甲基化过程。
pH对汞的去甲基化过程的影响同样受到其它环境因素的影响,且往往与其对汞的甲基化的影响相反。在表层沉积物中,MeHg的去甲基化速率随着水体pH的降低而降低[113];而在厌氧沉积物中,去甲基化在低pH条件下会增强[109-110]。
3.8 其 他
除以上影响因素外,其他一些环境理化性质也会对汞的甲基化过程产生影响。Faganeli等[114]认为,汞的迁移转化受到其他元素的生物地球化学转化过程的强烈影响,尤其是那些对氧化还原敏感且又是微生物生长的必需元素,如Fe、Mn等。研究表明,Fe可以通过与环境中的硫化物作用(形成FeS沉淀)改变溶解态汞的含量,从而间接影响汞的甲基化过程[89, 115, 116]。Han等[89]通过向沉积物中加入Fe(II)(0~0.61 mmol·L-1)或Fe(III)(0~3.5 mmol·L-1)后发现,当加入的Fe浓度较低时,MeHg含量增加,而当加入的Fe浓度较高时,MeHg含量降低。
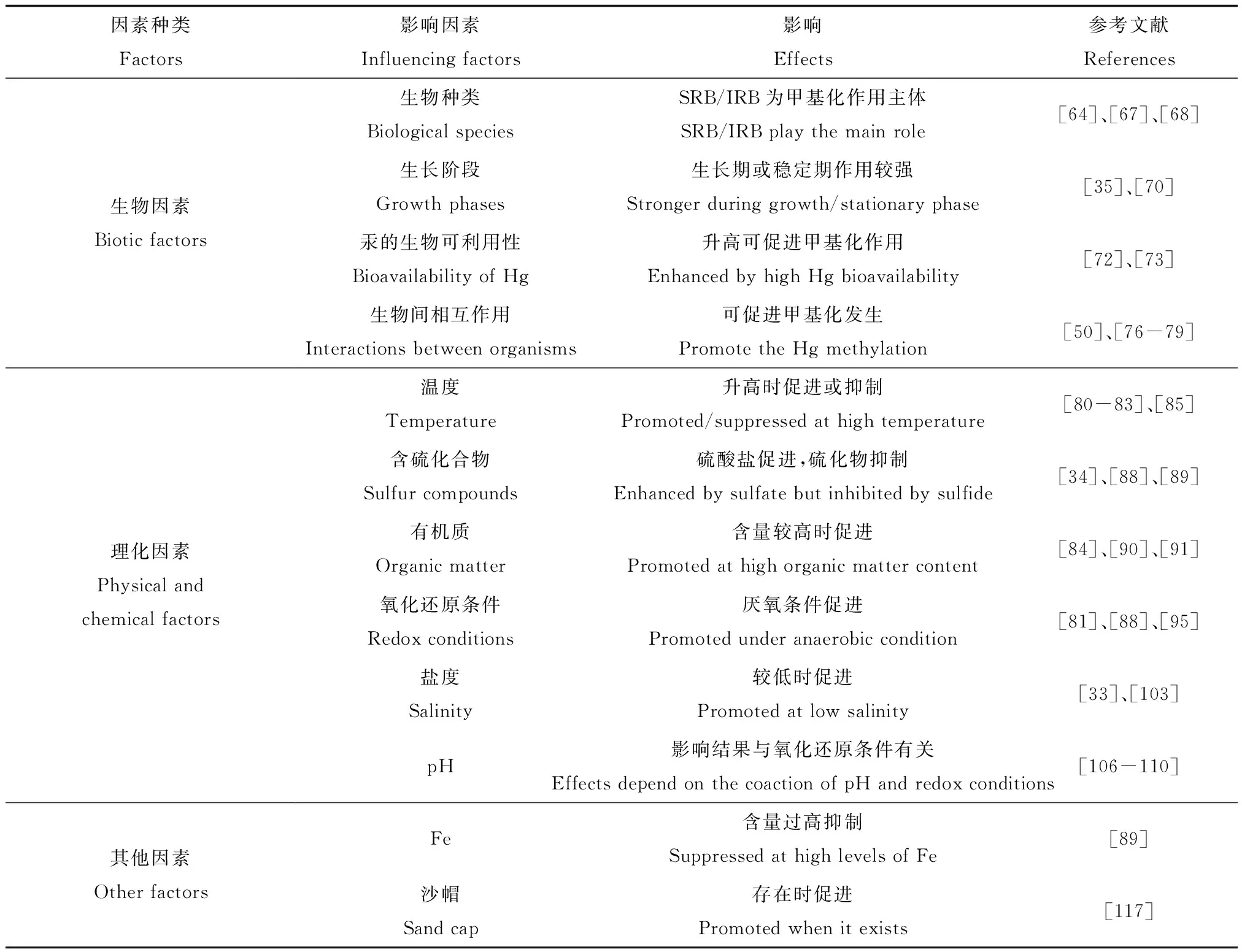
表1 沉积物中汞甲基化过程的影响因素Table 1 Influencing factors of mercury methylation in sediments
另外,Johnson等[117]研究发现,有沙帽(2~3 cm)的沉积物比无沙帽的沉积物中MeHg的含量高出50%,并认为沙帽的存在会增强包括SRB在内的厌氧微生物的活性,改变甲基化与去甲基化之间的平衡,并使MeHg的浓度升高,而当沙帽很薄或不稳定时,其物理封存作用的效果将无法体现。
至此可以看出,生物种类、汞的生物可利用性等生物因素及温度、含硫化合物、有机质等理化因素都会影响到沉积物中汞的甲基化过程(表1)。总的来说,在甲基化微生物广泛分布、温度较高、硫酸盐及营养物质丰富的厌氧沉积物中,无机汞的甲基化过程较为活跃。
4 结 语
沉积物中汞的甲基化包括生物甲基化和非生物甲基化两条途径,并以生物途径为主。硫酸盐还原菌是汞甲基化的主要微生物,产甲烷菌和铁还原菌也是重要的生物媒介。然而由于微生物甲基化过程的复杂性,关于细菌对汞的吸收机制、甲基化过程的生化机理目前依然没有定论。最近,Parks[47]等对甲基化微生物和非甲基化微生物基因层面的研究发现,基因簇hgcA和hgcB是微生物发生甲基化汞的两个必需基因,使得对人们对汞的生物甲基化机理的理解迈进了一大步。汞的非生物甲基化一方面可以由甲基碘化物、二甲基硫化物等小分子有机物和富里酸、腐殖酸等溶解态的大分子有机质而引发,另一方面可以通过甲基钴氨素、甲基铅、甲基锡等含甲基物质的转甲基作用来实现。有机汞裂解和氧化去甲基化是MeHg生物去甲基化的两种方式,厌氧菌或好氧菌都可能参与该过程。目前关于MeHg的去甲基化主要集中于在水体环境中的研究,对于自然条件下沉积物中MeHg的非生物去甲基化过程还缺乏研究。
新技术的发展推动了汞的甲基化机制及其影响因素的研究。稳定同位素的应用[23, 75]及X射线吸收精细结构谱[118]的发展为汞的甲基化过程研究提供了新的方法选择和技术手段,使得对汞元素的追踪和产物的分析成为可能;甲基化微生物的基因[47, 119]及蛋白质组学分析[118]成为从分子层面探索汞的甲基化机制的新思路;动力学模型[120]及统计分析软件的应用[21, 121]使甲基化过程影响因素的主因素分析获得了数据支撑。然而,由于甲基化过程的复杂性以及自然生态系统的多样性,目前不同生态系统沉积物中汞的甲基化机理及主要控制因素仍不明确,有待今后从以下两个方面继续探索:其一,继续对汞甲基化的单因素影响因子进行模拟研究,并结合化学及生物学研究手段,揭示生物及非生物的甲基化机制;其二,加强对自然生态系统中汞甲基化的影响因子间交互作用的研究,确定不同生态系统中汞甲基化的主要控制因素,从而为沉积物中甲基汞的修复提供理论依据。
[1] Harada M. Minamata disease: Methylmercury poisoning in Japan caused by environmental pollution [J]. CRC Critical Reviews in Toxicology, 1995, 25(1): 1-24
[2] Mcalpine D, Araki S. Minamata disease an unusual neurological disorder caused by contaminated fish [J]. The Lancet, 1958, 272(7047): 629-631
[3] Bakir F, Damluji S F, Amin-Zaki L, et al. Methylmercury poisoning in Iraq [J]. Science, 1973, 181(96): 230-241
[4] Clarkson T W. Human toxicology of mercury [J]. The Journal of Trace Elements in Experimental Medicine, 1998, 11(2-3): 303-317
[5] Magos L. Physiology and toxicology of mercury [J]. Metal Ions in Biological Systems, 1997, 34: 321-370
[6] Bloom N S. On the chemical form of mercury in edible fish and marine invertebrate tissue [J]. Canadian Journal of Fisheries and Aquatic Sciences, 1992, 49(5): 1010-1017
[7] Clarkson T W, Magos L. The toxicology of mercury and its chemical compounds [J]. CRC Critical Reviews in Toxicology, 2006, 36(8): 609-662
[8] Li P, Feng X B, Qiu G L, et al. Mercury pollution in Asia: A review of the contaminated sites [J]. Journal of Hazardous Material, 2009, 168(2-3): 591-601
[9] Clarkson T W, Hamada R, Amin-Zaki L. Mercury. Changing Metal Cycles and Human Health [C]. Springer-Verlag, Berlin, 1984, 285-309
[10] Balcom P H, Hammerschmidt C R, Fitzgerald W F, et al. Seasonal distributions and cycling of mercury and methylmercury in the waters of New York/New Jersey Harbor Estuary [J]. Marine Chemistry, 2008, 109(1): 1-17
[11] Kim D, Wang Q, Sorial G A, et al. A model approach for evaluating effects of remedial actions on mercury speciation and transport in a lake system [J]. Science of the Total Environment, 2004, 327(1): 1-15
[12] Fairbrother A, Wenstel R, Sappington K, et al. Framework for metals risk assessment [J]. Ecotoxicology and Environmental Safety, 2007, 68(2): 145-227
[13] Bloom N S, Moretto L M, Scopece P, et al. Seasonal cycling of mercury and monomethyl mercury in the Venice Lagoon (Italy) [J]. Marine Chemistry, 2004, 91(1): 85-99
[14] Tomiyasu T, Takenaka S, Noguchi Y, et al. Estimation of the residual total mercury in marine sediments of Minamata Bay after a pollution prevention project [J]. Marine Chemistry, 2014, 159: 19-24
[15] Abi-Ghanem C, Nakhlé K, Khalaf G, et al. Mercury distribution and methylmercury mobility in the sediments of three sites on the Lebanese Coast, Eastern Mediterranean [J]. Archives of environmental contamination and toxicology, 2011, 60(3): 394-405
[16] Yu X, Li H, Pan K, et al. Mercury distribution, speciation and bioavailability in sediments from the Pearl River Estuary, Southern China [J]. Marine pollution bulletin, 2012, 64(8): 1699-1704
[17] Ullrich S M, Tanton T W, Abdrashitova S A. Mercury in the aquatic environment: A review of factors affecting methylation [J]. Critical Reviews in Environmental Science and Technology, 2001, 31(3): 241-293
[18] Covelli S, Faganeli J, Horvat M, et al. Porewater distribution and benthic flux measurements of mercury and methylmercury in the Gulf of Trieste (Northern Adriatic Sea) [J]. Estuarine, Coastal and Shelf Science, 1999, 48(4): 415-428
[19] Hines M E, Poitras E N, Covelli S, et al. Mercury methylation and demethylation in Hg-contaminated lagoon sediments (Marano and Grado Lagoon, Italy) [J]. Estuarine, Coastal and Shelf Science, 2012, 113: 85-95
[20] Yan H, Li Q, Meng B, et al. Spatial distribution and methylation of mercury in a eutrophic reservoir heavily contaminated by mercury in Southwest China [J]. Applied Geochemistry, 2013, 33: 182-190
[21] Schartup A T, Balcom P H, Mason R P. Sediment-Porewater Partitioning, Total Sulfur, and Methylmercury Production in Estuaries [J]. Environmental Science & Technology, 2014, 48(2): 954-960
[22] Marvin-DiPasquale M, Windham-Myers L, Agee J L, et al. Methylmercury production in sediment from agricultural and non-agricultural wetlands in the Yolo Bypass, California, USA [J]. Science of The Total Environment, 2013, 484: 288-299
[23] Schartup A T, Mason R P, Balcom P H, et al. Methylmercury production in estuarine sediments: Role of organic matter [J]. Environmental science & technology, 2012, 47(2): 695-700
[24] St. Pierre K A, Chételat J, Yumvihoze E, et al. Temperature and the sulphur cycle control monomethylmercury cycling in high Arctic coastal marine sediments from Allen Bay, Nunavut, Canada [J]. Environmental Science & Technology, 2014, 48(5): 2680-2687
[25] Wood J M, Kennedy F S, Rosen C G. Synthesis of methyl-mercury compounds by extracts of a methanogenic bacterium [J]. Nature, 1968, 220: 173-174
[26] Hamdy M K, Noyes O R. Formation of methyl mercury by bacteria [J]. Applied Microbiology, 1975, 30(3): 424-432
[27] Vonk J W, Sijpesteijn A K. Studies on the methylation of mercuric chloride by pure cultures of bacteria and fungi [J]. Antonie van Leeuwenhoek, 1973, 39(1): 505-513
[28] Korthals E T, Winfrey M R. Seasonal and spatial variations in mercury methylation and demethylation in an oligotrophic lake [J]. Applied and Environmental Microbiology, 1987, 53(10): 2397-2404
[29] Matilainen T. Involvement of Bacteria in Methylmercury Formation in Anaerobic Lake Waters [M]//Mercury as a Global Pollutant. Springer Netherlands, 1995: 757-764
[30] Rudd J W, Turner M A, Furutani A, et al. The English-Wabigoon River system: I. A synthesis of recent research with a view towards mercury amelioration [J]. Canadian Journal of Fisheries and Aquatic Sciences, 1983, 40(12): 2206-2217
[31] Avramescu M L, Yumvihoze E, Hintelmann H, et al. Biogeochemical factors influencing net mercury methylation in contaminated freshwater sediments from the St. Lawrence River in Cornwall, Ontario, Canada [J]. Science of the Total Environment, 2011, 409(5): 968-978
[32] Warner K A, Roden E E, Bonzongo J C. Microbial mercury transformation in anoxic freshwater sediments under iron-reducing and other electron-accepting conditions [J]. Environmental Science & Technology, 2003, 37(10): 2159-2165
[33] Drott A, Lambertsson L, Björn E, et al. Do potential methylation rates reflect accumulated methyl mercury in contaminated sediments?[J]. Environmental Science & Technology, 2007, 42(1): 153-158
[34] Fleming E J, Mack E E, Green P G, et al. Mercury methylation from unexpected sources: Molybdate-inhibited freshwater sediments and an iron-reducing bacterium [J]. Applied and Environmental Microbiology, 2006, 72(1): 457-464
[35] Hu H Y, Lin H, Zheng W, et al. Oxidation and methylation of dissolved elemental mercury by anaerobic bacteria [J]. Nature Geoscience, 2013, 6(9): 751-754
[36] Choi S C, Bartha R. Cobalamin-mediated mercury methylation by Desulfovibrio desulfuricans LS [J]. Applied and Environmental Microbiology, 1993, 59(1): 290-295
[37] Ekstrom E B, Morel F M M, Benoit J M. Mercury methylation independent of the acetyl-coenzyme A pathway in sulfate-reducing bacteria [J]. Applied and Environmental Microbiology, 2003, 69(9): 5414-5422
[38] Graham A M, Bullock A L, Maizel A C, et al. Detailed assessment of the kinetics of Hg-cell association, Hg methylation, and methylmercury degradation in several Desulfovibrio species [J]. Applied and Environmental Microbiology, 2012, 78(20): 7337-7346
[39] Ridley W P, Dizikes L J, Wood J M. Biomethylation of toxic elements in the environment [J]. Science, 1977, 197(4301): 329-332
[40] Neujahr H Y, Bertilsson L. Methylation of mercury compounds by methylcobalamin [J]. Biochemistry, 1971, 10(14): 2805-2808
[41] Imura N, Pan E S S K, Nagao K, et al. Chemical methylation of inorganic mercury with methylcobalamin, a vitamin B12 analog [J]. Mercury Poisoning, 1973, 2: 30
[42] Parkman H, Ostlund P, Samuelsson M, et al. Methylmercury in A Permanently Stratified Fjord [M]. 1995
[43] Hammerschmidt C R, Fitzgerald W F, Balcom P H, et al. Organic matter and sulfide inhibit methylmercury production in sediments of New York/New Jersey Harbor [J]. Marine Chemistry, 2008, 109(1): 165-182
[44] Drott A, Lambertsson L, Björn E, et al. Importance of dissolved neutral mercury sulfides for methyl mercury production in contaminated sediments [J]. Environmental Science & Technology, 2007, 41(7): 2270-2276
[45] Li Y B, Cai Y. Progress in the study of mercury methylation and demethylation in aquatic environments [J]. Chinese Science Bulletin, 2013, 58(2): 177-185
[46] Benoit J M, Gilmour C C, Mason R P, et al. Sulfide controls on mercury speciation and bioavailability to methylating bacteria in sediment pore waters [J]. Environmental Science & Technology, 1999, 33(6): 951-957
[47] Parks J M, Johs A, Podar M, et al. The genetic basis for bacterial mercury methylation [J]. Science, 2013, 339(6125): 1332-1335
[48] Berman M, Bartha R. Levels of chemical versus biological methylation of mercury in sediments [J]. Bulletin of Environmental Contamination and Toxicology, 1986, 36(1): 401-404
[49] Celo V, Lean D R S, Scott S L. Abiotic methylation of mercury in the aquatic environment [J]. Science of the Total Environment, 2006, 368(1): 126-137
[50] Pak K R, Bartha R. Mercury methylation by interspecies hydrogen and acetate transfer between sulfidogens and methanogens [J]. Applied and Environmental Microbiology, 1998, 64(6): 1987-1990
[51] DeSimone R E, Penley M W, Charbonneau L, et al. The kinetics and mechanism of cobalamin-dependent methyl and ethyl transfer to mercuric ion [J]. Biochimica et Biophysica Acta (BBA)-General Subjects, 1973, 304(3): 851-863
[52] Brinckman F E, Bellama J M. Organometals and organometalloids: occurence and fate in the environment; based on a symposium sponsored by the Division of Inorganic Chemistry at the 175th meeting of the American Chemical Society [C]//American Chemical Society ACS symposium series, 1978: 13-17
[53] Chau Y K, Wong P T S, Mojesky C A, et al. Transmethylation of metals in aquatic systems [J]. Applied Organometallic Chemistry, 1987, 1(3): 235-239
[54] Weber J H. Review of possible paths for abiotic methylation of mercury (II) in the aquatic environment [J]. Chemosphere, 1993, 26(11): 2063-2077
[55] Nagase H, Ose Y, Sato T. Possible methylation of inorganic mercury by silicones in the environment [J]. Science of the Total Environment, 1988, 73(1): 29-38
[56] Hamasaki T, Nagase H, Yoshioka Y, et al. Formation, distribution, and ecotoxicity of methylmetals of tin, mercury, and arsenic in the environment [J]. Critical Reviews in Environmental Science and Technology, 1995, 25(1): 45-91
[57] Robinson J B, Tuovinen O H. Mechanisms of microbial resistance and detoxification of mercury and organomercury compounds: Physiological, biochemical, and genetic analyses [J]. Microbiological Reviews, 1984, 48(2): 95
[58] Marvin-DiPasquale, Agee J, McGowan C, et al. Methyl-mercury degradation pathways: A comparison among three mercury-impacted ecosystems [J]. Environmental Science & Technology, 1991, 57(1): 130-137
[59] Oremland R S, Miller L G, Dowdle P, et al. Methylmercury oxidative degradation potentials in contaminated and pristine sediments of the carson river, nevada [J]. Applied and Environmental Microbiology, 1995, 61(7): 2745-2753
[60] Baughman G L. Chemistry of Organomercurials in Aquatic Systems [M]. Oregon: 1973
[61] Seller P, Kelly C A, Rudd J W M, et al. Photodegradation of methylmercury in lakes [J]. Nature, 1996, 380(6576): 694-697
[62] Avramescu M L, Yumvihoze E, Hintelmann H, et al. Biogeochemical factors influencing net mercury methylation in contaminated freshwater sediments from the St. Lawrence River in Cornwall, Ontario, Canada [J]. Science of the Total Environment, 2011, 409(5): 968-978
[63] Khan M A K, Wang F. Chemical demethylation of methylmercury by selenoamino acids [J]. Chemical Research in Toxicology, 2010, 23(7): 1202-1206
[64] Schaefer J K, Rocks S S, Zheng W, et al. Active transport, substrate specificity, and methylation of Hg(II) in anaerobic bacteria [J]. Proceedings of the National Academy of Sciences, 2011, 108(21): 8714-8719
[65] Pedrero Z, Bridou R, Mounicou S, et al. Transformation, localization, and biomolecular binding of Hg species at subcellular level in methylating and nonmethylating sulfate-reducing bacteria [J]. Environmental Science & Technology, 2012, 46(21): 11744-11751
[66] Ekstrom E B, Morel F M M. Cobalt limitation of growth and mercury methylation in sulfate-reducing bacteria [J]. Environmental Science & Technology, 2007, 42(1): 93-99
[67] King J K, Kostka J E, Frischer M E, et al. Sulfate-reducing bacteria methylate mercury at variable rates in pure culture and in marine sediments [J]. Applied and Environmental Microbiology, 2000, 66(6): 2430-2437
[68] Macalady J L, Mack E E, Nelson D C, et al. Sediment microbial community structure and mercury methylation in mercury-polluted Clear Lake, California [J]. Applied and Environmental Microbiology, 2000, 66(4): 1479-1488
[69] Ramamoorthy S, Cheng T C, Kushner D J. Effect of microbial life stages on the fate of methylmercury in natural waters [J]. Bulletin of Environmental Contamination and Toxicology, 1982, 29(2): 167-173
[70] Biswas A, Brooks S C, Miller C L, et al. Bacterial growth phase influences methylmercury production by the sulfate-reducing bacterium Desulfovibrio desulfuricans ND132 [J]. Science of the Total Environment, 2011. 409(19): 3943-3948
[71] Douglas T A, Loseto L L, Macdonald R W, et al. The fate of mercury in Arctic terrestrial and aquatic ecosystems, a review [J]. Environmental Chemistry, 2012, 9(4): 321-355
[72] Han S, Obraztsova A, Pretto P, et al. Biogeochemical factors affecting mercury methylation in sediments of the Venice Lagoon, Italy [J]. Environmental Toxicology and Chemistry, 2007, 26(4): 655-663
[73] Hammerschmidt C R, Fitzgerald W F, Lamborg C H, et al. Biogeochemical cycling of methylmercury in lakes and tundra watersheds of Arctic Alaska [J]. Environmental Science & Technology, 2006, 40(4): 1204-1211
[74] Schaefer J K, Morel F M M. High methylation rates of mercury bound to cysteine by Geobacter sulfurreducens [J]. Nature Geoscience, 2009, 2(2): 123-126
[75] Hintelmann H, Keppel-Jones K, Evans R D. Constants of mercury methylation and demethylation rates in sediments and comparison of tracer and ambient mercury availability [J]. Environmental Toxicology and Chemistry, 2009, 19(9): 2204-2211
[76] Phelps T J, Conrad R, Zeikus J G. Sulfate-dependent interspecies H2 transfer between Methanosarcina barkeri and Desulfovibrio vulgaris during coculture metabolism of acetate or methanol [J]. Applied and Environmental Microbiology, 1985, 50(3): 589-594
[77] Han S, Narasingarao P, Obraztsova A, et al. Mercury speciation in marine sediments under sulfate-limited conditions [J]. Environmental Science & Technology, 2010, 44(10): 3752-3757
[78] Nogaro G, Mermillod-Blondin F. Stormwater sediment and bioturbation influences on hydraulic functioning, biogeochemical processes, and pollutant dynamics in laboratory infiltration systems [J]. Environmental Science & Technology, 2009, 43(10): 3632-3638
[79] Nogaro G, Hammerschmidt C R. Influence of benthic macrofauna on microbial production of methylmercury in sediments on the New England continental shelf [J]. Hydrobiologia, 2013, 701(1): 289-299
[80] Yu R Q, Flanders J R, Mack E E, et al. Contribution of coexisting sulfate and iron reducing bacteria to methylmercury production in freshwater river sediments [J]. Environmental Science & Technology, 2012, 46(5): 2684-2691
[81] Covelli S, Faganeli J, De Vittor C, et al. Benthic fluxes of mercury species in a lagoon environment (Grado Lagoon, Northern Adriatic Sea, Italy) [J]. Applied Geochemistry, 2008, 23(3): 529-546
[82] Hines N A, Brezonik P L, Engstrom D R. Sediment and porewater profiles and fluxes of mercury and methylmercury in a small seepage lake in northern Minnesota [J]. Environmental Science & Technology, 2004, 38(24): 6610-6617
[83] Creswell J E, Kerr S C, Meyer M H, et al. Factors controlling temporal and spatial distribution of total mercury and methylmercury in hyporheic sediments of the Allequash Creek wetland, northern Wisconsin [J]. Journal of Geophysical Research: Biogeosciences (2005-2012), 2008, 113(G2)
[84] Hammerschmidt C R, Fitzgerald W F. Geochemical controls on the production and distribution of methylmercury in near-shore marine sediments [J]. Environmental Science & Technology, 2004, 38(5): 1487-1495
[85] Marvin-DiPasquale M, Agee J L. Microbial mercury cycling in sediments of the San Francisco Bay-Delta [J]. Estuaries, 2003, 26(6): 1517-1528
[86] Harmon S M, King J K, Gladden J B, et al. Methylmercury formation in a wetland mesocosm amended with sulfate [J]. Environmental Science & Technology, 2004, 38(2): 650-656
[87] Mitchell C P J, Branfireun B A, Kolka R K. Assessing sulfate and carbon controls on net methylmercury production in peatlands: An in situ mesocosm approach [J]. Applied Geochemistry, 2008, 23(3): 503-518
[88] Hollweg T A, Gilmour C C, Mason R P. Methylmercury production in sediments of Chesapeake Bay and the mid-Atlantic continental margin [J]. Marine Chemistry, 2009, 114(3): 86-101
[89] Han S, Obraztsova A, Pretto P, et al. Sulfide and iron control on mercury speciation in anoxic estuarine sediment slurries [J]. Marine Chemistry, 2008, 111(3): 214-220
[90] Lambertsson L, Nilsson M. Organic material: the primary control on mercury methylation and ambient methyl mercury concentrations in estuarine sediments [J]. Environmental Science & Technology, 2006, 40(6): 1822-1829
[91] Gray J E, Hines M E. Biogeochemical mercury methylation influenced by reservoir eutrophication, Salmon Falls Creek Reservoir, Idaho, USA [J]. Chemical Geology, 2009, 258(3): 157-167
[92] Mitchell C P J, Gilmour C C. Methylmercury production in a Chesapeake Bay salt marsh [J]. Journal of Geophysical Research: Biogeosciences (2005-2012), 2008, 113(G2)
[93] Ravichandran M. Interactions between mercury and dissolved organic matter-a review [J]. Chemosphere, 2004, 55(3): 319-331
[94] Miller C L, Mason R P, Gilmour C C, et al. Influence of dissolved organic matter on the complexation of mercury under sulfidic conditions [J]. Environmental Toxicology and Chemistry, 2007, 26(4): 624-633
[95] DeLaune R D, Jugsujinda A, Devai I, et al. Relationship of sediment redox conditions to methyl mercury in surface sediment of Louisiana Lakes [J]. Journal of Environmental Science and Health, Part A, 2004, 39(8): 1925-1933
[96] Jara-Marini M E, Soto-Jiménez M F, Páez-Osuna F. Mercury transfer in a subtropical coastal lagoon food web (SE Gulf of California) under two contrasting climatic conditions [J]. Environmental Toxicology, 2012, 27(9): 526-536
[97] Schäfer J, Castelle S, Blanc G, et al. Mercury methylation in the sediments of a macrotidal estuary (Gironde Estuary, south-west France) [J]. Estuarine, Coastal and Shelf Science, 2010, 90(2): 80-92
[98] Bouchet S, Bridou R, Tessier E, et al. An experimental approach to investigate mercury species transformations under redox oscillations in coastal sediments [J]. Marine Environmental Research, 2011, 71(1): 1-9
[99] Canário J, Caetano M, Vale C, et al. Evidence for elevated production of methylmercury in salt marshes [J]. Environmental science & technology, 2007, 41(21): 7376-7382
[100] Acquavita A, Emili A, Covelli S, et al. The effects of resuspension on the fate of Hg in contaminated sediments (Marano and Grado Lagoon, Italy): Short-term simulation experiments [J]. Estuarine, Coastal and Shelf Science, 2012, 113: 32-40
[101] Rodríguez Martín-Doimeadios R C, Tessier E, Amouroux D, et al. Mercury methylation/demethylation and volatilization pathways in estuarine sediment slurries using species-specific enriched stable isotopes [J]. Marine Chemistry, 2004, 90(1): 107-123
[102] Heyes A, Mason R P, Kim E H, et al. Mercury methylation in estuaries: Insights from using measuring rates using stable mercury isotopes [J]. Marine Chemistry, 2006, 102(1): 134-147
[103] Compeau G C, Bartha R. Effect of salinity on mercury-methylating activity of sulfate-reducing bacteria in estuarine sediments [J]. Applied and Environmental Microbiology, 1987, 53(2): 261-265
[104] Chen B, Wang T, Yin Y, et al. Methylation of inorganic mercury by methylcobalamin in aquatic systems [J]. Applied Organometallic Chemistry, 2007, 21(6): 462-467
[105] Compeau G, Bartha R. Methylation and demethylation of mercury under controlled redox, pH and salinity conditions [J]. Applied and Environmental Microbiology, 1984, 48(6): 1203-1207
[106] Wu H, Ding Z, Liu Y, et al. Methylmercury and sulfate-reducing bacteria in mangrove sediments from Jiulong River Estuary, China [J]. Journal of Environmental Sciences, 2011, 23(1): 14-21
[107] Xun L, Campbell N E R, Rudd J W M. Measurements of specific rates of net methyl mercury production in the water column and surface sediments of acidified and circumneutral lakes [J]. Canadian Journal of Fisheries and Aquatic Sciences, 1987, 44(4): 750-757
[108] Golding G R, Sparling R, Kelly C A. Effect of pH on intracellular accumulation of trace concentrations of Hg (II) in Escherichia coli under anaerobic conditions, as measured using a mer-lux bioreporter [J]. Applied and Environmental Microbiology, 2008, 74(3): 667-675
[109] Ramial P S, Rudd J W M, Furutam A, et al. The effect of pH on methyl mercury production and decomposition in lake sediments [J]. Canadian Journal of Fisheries and Aquatic Sciences, 1985, 42(4): 685-692
[110] Steffan R J, Korthals E T, Winfrey M R. Effects of acidification on mercury methylation, demethylation, and volatilization in sediments from an acid-susceptible lake [J]. Applied and Environmental Microbiology, 1988, 54(8): 2003-2009
[111] Kelly C A, Rudd J W M, Holoka M H. Effect of pH on mercury uptake by an aquatic bacterium: Implications for Hg cycling [J]. Environmental Science & Technology, 2003, 37(13): 2941-2946
[112] Tjerngren I, Karlsson T, Björn E, et al. Potential Hg methylation and MeHg demethylation rates related to the nutrient status of different boreal wetlands [J]. Biogeochemistry, 2012, 108(1-3): 335-350
[113] Matilainen T, Verta M, Niemi M, et al. Specific rates of net methylmercury production in lake sediments [J]. Water Air & Soil Pollution, 1991, 56(1): 595-605
[114] Faganeli J, Hines M E, Covelli S, et al. Mercury in lagoons: An overview of the importance of the link between geochemistry and biology [J]. Estuarine, Coastal and Shelf Science, 2012, 113: 126-132
[115] Mehrotra A S, Horne A J, Sedlak D L. Reduction of net mercury methylation by iron in Desulfobulbus propionicus (1pr3) cultures: Implications for engineered wetlands [J]. Environmental Science & Technology, 2003, 37(13): 3018-3023
[116] Chadwick S P, Babiarz C L, Hurley J P, et al. Influences of iron, manganese, and dissolved organic carbon on the hypolimnetic cycling of amended mercury [J]. Science of the Total Environment, 2006, 368(1): 177-188
[117] Johnson N W, Reible D D, Katz L E. Biogeochemical changes and mercury methylation beneath an in-situ sediment cap [J]. Environmental Science & Technology, 2010, 44(19): 7280-7286
[118] Truong H Y T, Chen Y W, Saleh M, et al. Proteomics of Desulfovibrio desulfuricans and x-ray absorption spectroscopy to investigate mercury methylation in the presence of selenium [J]. Metallomics, 2014, 6(3): 465-475
[119] Liu Y R, Yu R Q, Zheng Y M, et al. Analysis of the microbial community structure by monitoring an hg methylation gene (hgcA) in paddy soils along an Hg gradient [J]. Applied and Environmental Microbiology, 2014, 80(9): 2874-2879
[120] Chiasson-Gould S A, Blais J M, Poulain A J. Dissolved organic matter kinetically controls mercury bioavailability to bacteria [J]. Environmental Science & Technology, 2014, 48(6): 3153-3161
[121] Liang P, Lam C L, Chen Z, et al. Formation and distribution of methylmercury in sediments at a mariculture site: A mesocosm study [J]. Journal of Soils and Sediments, 2013, 13(7): 1301-1308
◆
ResearchProgressonMercuryMethylationinSediments
Yin Jiaoyang, Yin Daqiang, Wang Rui*
College of Environmental Science and Technology, Tongji University, State Key Laboratory of Pollution Control and Resources Reuse, Shanghai 200092, China
9 May 2014accepted15 June 2014
Mercury is an important contaminant existed in the environment, and the toxicity of mercury strongly depends on its chemical species. Mercury exists in the natural environment mainly as inorganic mercury, however, inorganic mercury could be transformed to methylmercury (a more toxic form) via methylation process, thus pose higher health risk to the exposed biota and human beings. Sediments are often considered as the major sink of mercury in aquatic environment, and it is also the major site where mercury methylation occurs. Mercury methylation processes in sediments are controlled by various biotic (e.g., biological species and Hg bioavailability) and abiotic factors (e.g., temperature, sulfur compound, organic matter and redox conditions). The present article summarizes the research history and recent progresses in studying the mechanisms underlying mercury methylation in sediments and its influencing factors, and further draw some perspectives for future research.
mercury; sediments; methylation; bioavailability
国家自然科学基金青年项目(41301557);国家水体污染控制与治理科技重大专项(2012ZX07403-002)
阴皎阳(1990-),女,工学硕士,研究方向为沉积物中汞的生物可利用性,E-mail: 0419yinjiaoyang@tongji.edu.cn;
*通讯作者(Corresponding author),E-mail: wangr@tongji.edu.cn
10.7524/AJE.1673-5897-20140509002
2014-05-09录用日期:2014-06-15
1673-5897(2014)5-819-13
: X171.5
: A
王锐(1986—),女,环境生物学博士,讲师,主要研究方向为汞的生态毒理学及生物地球化学,发表学术论文10篇。
阴皎阳, 尹大强, 王 锐. 沉积物中汞的甲基化研究进展[J]. 生态毒理学报,2014, 9(5): 819-831
Yin J Y, Yin D Q, Wang R. Research progress on mercury methylation in sediments [J]. Asian Journal of Ecotoxicology, 2014, 9(5): 819-831 (in Chinese)

