从维生素K1注射液不良反应/事件分析与其工艺助溶剂吐温的相关性
马礼媛,匡丽清,王 静,杨 劲
中国药科大学,南京 210009
本研究通过查询药品生产企业ADR信息查询系统,获得包括广东省、海南省、湖南省、四川省、广西壮族自治区、福建省、贵州省、河南省、云南省、江西省等10个省区病例报告数据库2002年1月1日~2011年9月15日的维生素K1注射液不良反应/事件(ADR/ADE)病例报告,并对其进行统计和分析,探讨维生素K1注射液ADR/ADE发生的原因[1]、相关机理及后续建议,旨在为临床安全合理用药提供参考。
1 调研资料及分析
涉及维生素K1注射液ADR/ADE共4162例次,其中3687例次为单独用药引起的ADR/ADE,475例次为合并用药引起的ADR/ADE。
1.1 一般情况
ADR/ADE报告中年龄分布统计结果见表1。报告中男女比例为1∶1.3,可能是因为女性的特殊生理期决定其用药机会较多引起的。各个年龄段均有不良反应发生,小于10岁的婴儿或儿童共881例,占21.17%,构成比略高于其它各年龄段的构成比。说明婴幼儿生理发育不全、抗过敏性差。
1.2 用药剂量情况
ADR/ADE报告的用药剂量统计结果见表2。维生素K1注射液说明书中明确指出,用于低凝血酶原血症时,每次10 mg,每日1~2次,24小时内总量不超过40 mg。4162例ADR/ADE报告中,日剂量不超过40 mg的病例共3944例,占94.76%,超过40 mg的病例共175例,占4.20%。此种状况说明剂量问题不是发生ADR/ADE的主要因素,体质差异等是主要因素。

表1 4162例ADR/ADE报告的年龄分布
1.3 ADR/ADE类型
ADR/ADE报告的类型统计结果见表3,其中严重的共311例,占7.47%,其临床表现见表4。4162例ADR/ADE报告中,严重病例311例,占7.47%,从表5可以看出,严重病例的临床表现主要为过敏性休克(110例次,占26.96%)、过敏样反应(77例次,占 18.87%)、呼吸困难(51例次,占 12.50%)、紫绀(25例次,占6.13%)等,累及全身性损害、呼吸系统、循环系统等。
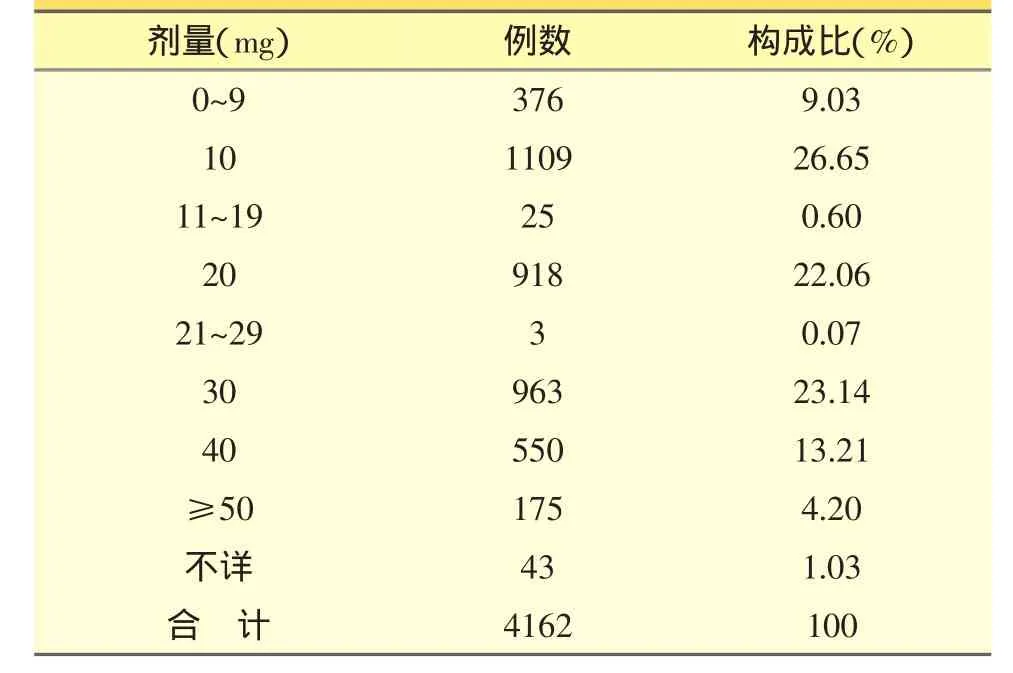
表2 4162例ADR/ADE报告的用药剂量统计
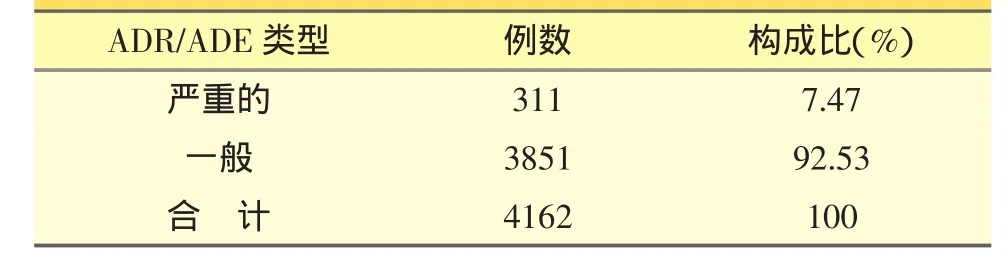
表3 4162例ADR/ADE报告的类型统计
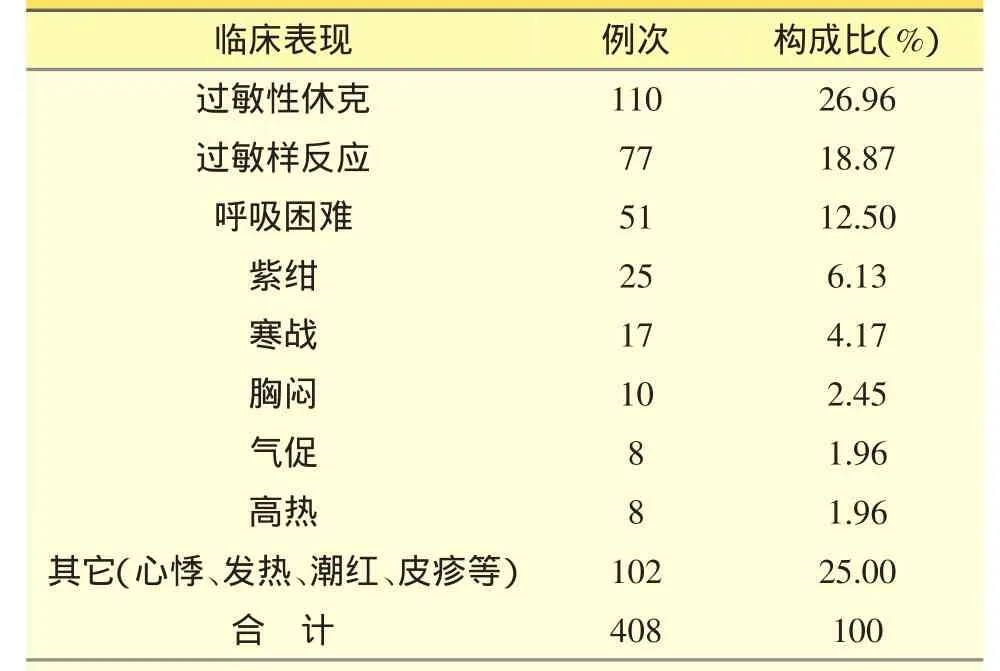
表4 311例严重ADR/ADE的临床表现
1.4 ADR/ADE累及系统/器官统计
ADR/ADE累及系统/器官统计结果见表5。
1.5 ADR/ADE转归
ADR/ADE报告的转归统计结果见表6。
2 吐温-80导致注射剂不良反应研究
由于维生素K1水溶性很弱,故在其注射剂中添加吐温-80作助溶剂。维生素K1发生ADR/ADE除与药物储存情况、遗传与患者自身体质、临床使用等因素有关,也考虑加入吐温-80所致。近年来临床上含吐温-80的制剂静脉注射易引起类过敏反应已被业界所重视[2-3],如鱼腥草注射液[4]和细辛脑注射液[5]等。相较于静脉注射的给药方式,肌内和皮下注射发生不良反应的几率低。国家食品药品监督管理总局(CFDA)发布的维生素K1注射液不良反应信息通报中显示,95.3%的严重ADR/ADE报告为静脉途径给药。故在维生素K1注射液中作为增溶剂的吐温-80,可能是引起类过敏反应的主要成分之一。

表5 4162例ADR/ADE累及系统/器官统计
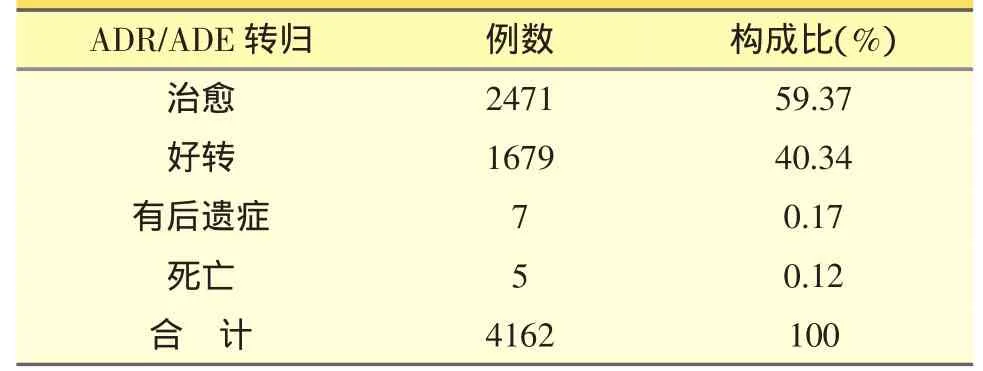
表6 4162例ADR/ADE报告的转归统计
吐温-80,又名聚山梨酯-80,化学名为聚氧乙烯-20-山梨醇酐单油酸酯,属多元醇型非离子表面活性剂,由于具有较长的碳链结构,对亲脂性药物有较好的助溶作用,可用作增溶剂、乳化剂等,为中西药注射剂的常用辅料之一。吐温-80静脉注射引起的不良反应主要为类过敏反应,不经过抗体形成过程,首次静脉注射给药即可导致Beagle犬出现明显的过敏反应症状,其发生迅速,难以预料,并可导致休克、死亡等严重后果[6]。
近年来含吐温-80的注射剂频频引发不良反应,与以下几个因素密切相关:
(1)吐温-80本身具有扩张血管、降低血压和溶血毒性。梁爱华等[7]研究结果显示,0.5%吐温-80及含0.5%吐温-80的鱼腥草注射液给Beagle犬静脉注射后,动物出现明显的血压下降,而不含吐温-80的鱼腥草蒸馏液未造成明显的血压下降。另有国外临床观察试验发现吐温-80是导致胺碘达隆临床病人血压下降的主要物质[8]。虽然吐温-80是目前吐温类增溶剂中溶血作用最轻微的,但是依然有诸多研究[9]结果表明,注射用0.5%吐温-80可导致兔细胞溶血。
(2)吐温-80用量较大。有研究表明吐温-80所致类过敏反应,反应强度与浓度成正相关。罗霞等[10]研究发现,当吐温-80的浓度范围在0.1~20 mg·mL-1时RBL-2H3细胞脱颗粒百分率以及释放β-氨基己糖苷酶和组胺的量与其浓度呈线性关系,吐温-80含量较高的注射液引起RBL-2H3细胞释放的组胺的量也较高。中药注射剂中吐温-80常用浓度多在0.1%~2%,《部颁中药标准》收载的中药注射剂制剂工艺中注明添加吐温-80者有34种,其含量超过0.5%者就有18种[9]。
(3)吐温-80含有较多的毒性杂质。我国药典对吐温-80的质量要求低于国外药典,2010版药典较2005版药典相比有所提高,增加了过氧化值、砷盐、环氧乙烷和二氧六环检测项目,但仍未明确表示其是否可用于注射剂以及注射用吐温-80的质量标准和浓度限制[10]。目前国内生产的吐温-80质量参差不齐,孙会敏等[11]采集了全国5省市7家企业的18批吐温-80进行质量分析,虽然按照2005年版药典全部产品都合格,但是按照2010年版药典检测,总体不合格率升高为62%。吐温-80生产厂家所使用的原料——油酸纯度普遍偏低,会引入脂肪酸杂质,使得成品颜色较深,为使产品颜色检查能达到药典标准,在产品中添加过氧化氢脱色。而研究发现过氧化氢是吐温-80的致敏原之一,有过氧化氢含量的吐温-80静脉注射后,Beagle犬类过敏反应高,其血液中组胺浓度也会明显升高。
(4)吐温-80本身的不稳定性。在一定条件下会发生降解,或与配伍药物发生化学反应,可能引起药物成分变化,甚至产生有毒有害的物质[12]。
而关于吐温-80导致类过敏反应发生的分子生物学基础尚不明确,目前认为主要与以下两条途径相关:一种是直接诱导肥大细胞/嗜碱粒细胞脱颗粒途径;另一种是激活补体系统途径[13]。张嘉等[14]研究表明,吐温-80直接诱导肥大细胞/嗜碱粒细胞脱颗粒作用,释放组胺和类胰蛋白酶等生物活性介质,且该作用是不依赖于细胞外游离钙离子的,该机制与经典的免疫介导的靶细胞脱颗粒作用机制不同。另有多个研究[15-16]均表明,吐温-80能通过经典补体激活途径和/或旁路补体激活途径,激活补体系统、激活人体补体系统,是导致类过敏反应的基础之一,经由级联反应生成过敏毒素后结合肥大细胞膜上的补体受体诱发肥大细胞脱颗粒。但是否出现过敏反应症状与机体补体系统对药物的敏感性、机体对过敏活性介质的敏感性等因素有关尚待研究。
3 建 议
3.1 提高吐温-80产品的质量
有报道[11]称给食蟹猴的后肢静脉注射5%的吐温-80注射液(剂量为 50 mg·kg-1),国外的和国产的吐温-80均未出现过敏反应,而猴与人的种属相近,这说明人对其的耐受性比较强,质量好的吐温-80在合理剂量下应该可以作为注射用辅料使用,并且有学者认为控制吐温-80质量,并将其浓度限定在0.25%以下,可以在保证药物增溶效果的同时避免类过敏反应的发生[17]。因此,国家相关部门应该尽早制定注射级吐温-80质量标准,限定浓度范围,达到对吐温-80的有效质控。同时,生产企业应该优化生产工艺,提高纯度,去除杂质,最大限度地提高吐温-80产品的安全性。
3.2 研发新的辅料或药物载体系统
刘倩等[18]研究发现,吐温-80作为中药注射剂的辅料,在高于0.0625%的浓度下即存在细胞毒性,故不能排除在较低浓度下,吐温-80仍可引发轻度类过敏反应的可能。另外,国内维生素K1注射液说明书提示,首选皮下或肌注,而静脉给药方式慎用。但是皮下或肌注亦会引起严重的过敏/类过敏反应和注射部位反应(包括疼痛、肿胀、触痛、红斑性疹)等[19]。皮下或肌注起效比静脉注射慢,而临床上危急重症的抢救和治疗,必须采用静脉注射,那么临床医生对病人的获益风险评估极其困难。
综上所述,提示维生素K1注射液的安全隐患,当务之急研制其他注射剂来替代含吐温-80的维生素K1注射液。一方面可以寻找更安全、适用的药用辅料,逐步取代吐温-80;另一方面还可研发新型药物传递系统,如脂质纳米粒[20]、脂肪乳等。
[1]Fiore LD,Scola MA,Cantillon CE,et al.Anaphylactoid reactions to vitamin K[J].J Thromb Thrombolysis,2001,11(2)∶175-83.
[2]Szebeni J.Complement activation-related pseudoallergy∶a new class of drug-induced acute immune toxicity[J].Toxicology,2005,216(2)∶106-21.
[3]Coors,E.A.,et al.Polysorbate 80 in medical products and nonimmunologic anaphylactoid reactions[J].Ann Allergy Asthma Immunol,2005,12,95(6)∶593-9.
[4]刘 婷,赵 雍,曹春雨,等.鱼腥草注射液致类过敏反应的物质及其作用机制研究[J].中国中药杂志,2010,35(12):1603-6.
[5]马伟从,张 青,李 慧,等.细辛脑注射液致不良反应文献回顾与原因分析 [J].中国药物警戒,2010(04):243-6.
[6]张 嘉,李贻奎,李连达,等.鱼腥草蒸馏液与3种增溶剂配伍后对Beagle犬的致敏性 [J].中国新药杂志,2008,17(17):1494-8.
[7]梁爱华,李春英,郝 然,等.用清醒Beagle犬进行中药注射液的类过敏试验方法研究 [J].中国中药杂志,2010,35(17):2328-33.
[8]Munoz A,Karila P,Gallay P,et al.A randomized hemodynamic comparison ofintravenousamiodarone with and without Tween 80[J].Eur Heart J,1988,9(2)∶142-8.
[9]李寅超,郭 琰,吴翠萍,等.6种不同来源的注射用吐温-80致敏性和溶血性实验研究 [C].首届中国药物毒理学年会(2011年)暨国际药物非临床安全性评价研究论坛论文集,2011.
[10]罗 霞,王 青,周 联,等.中药注射剂所含吐温-80与过敏反应关系的研究 [J].药物不良反应杂志,2010,(3):160-5.
[11]孙会敏,杨 锐,弈 琳,等.聚山梨酯80质量分析与致敏原探究[J]. 药物分析杂志,2011,31(10):1850-5.
[12]谭志高,巢志茂,刘海萍,等.聚山梨脂80的化学稳定性研究进展 [J].中国实验方剂学杂志,2012,18(01):251-4.
[13]Simons FE,Frew AJ,Ansotegui IJ,et al.Risk assessment in anaphylaxis∶current and future approaches[J].J Allergy Clin Immunol,2007,120(1)∶S2-S24.
[14]张 嘉,李 澎,李贻奎,等.吐温80诱导RBL-2H3细胞脱颗粒作用研究[J].现代免疫学,2009(3):240-5.
[15]Szebeni J,Baranyi L,Savay S,et al.The Interaction of Liposomes with the Complement System∶In vitro and in vivo assays[J].Methods Enzymol,2003,373∶136-54.
[16]张 嘉,李贻奎,李连达,等.补体系统激活在吐温80导致类过敏反应中的作用 [J].毒理学杂志,2009(6):457-9.
[17]孙伟伟,李贻奎,张金艳,等.吐温80及其配制的鱼腥草注射液致豚鼠过敏反应的实验研究 [J].中药新药与临床药理,2011,22(001):47-51.
[18]刘 倩,秦媛媛,张 媛,等.不同来源生脉注射液体外细胞毒性的比较及原因分析 [J].中国中药杂志,2012,37(5):643.
[19]Wong DA,Freeman S.Cutaneous allergic reaction to intramuscularvitamin K1[J].AustralasJDermatol,1999,40(3)∶147-52.
[20]Puglia C,Bonina F.Lipid nanoparticles as novel delivery systems for cosmetics and dermal pharmaceuticals[J].Expert Opinion on Drug Delivery,2012,9(4)∶429-41.

