核苷(酸)类似物联合TACE治疗中晚期原发性肝癌的效果
鞠 琪,夏月根,陆小玲,展 翔,顾亚平,宋振江,何 亮
(江苏省靖江市第二人民医院 肝病科,江苏 靖江,214500)
原发性肝癌是指来源于肝脏上皮细胞的恶性肝瘤,其中肝细胞癌最常见,约占80%~90%,且多伴有慢性肝炎病毒感染,与乙型肝炎、肝炎后肝硬化关系最密切,由于起病隐匿,患者就诊时大多已属于中、晚期。根据国际抗癌协会的TNM分期为T3或T4期。临床手术切除率较低,且大多数患者常因为肝脏储备功能差,影响经皮肝动脉栓塞化疗术(TACE)的效果[1]。因此,经核苷(酸)类似物抗病毒治疗,能有效抑制乙肝病毒复制,从而改善肝脏功能,达到Child-Pugh A或B级,为TACE创造良好条件,从而明显延长肝癌患者生存时间,提高了患者生活质量。
1 资料与方法
1.1 一般资料
所有病例均为2010年6月—2013年6月在本科住院的原发性肝癌患者,且不能行手术切除,AFP升高,血清HBV-DNA定量大于1×103copies/mL,肝功能轻-中度异常的中、晚期肝癌伴有肝硬化的患者68例,男48例,女20例,平均年龄37岁,诊断符合2001年全国肝癌会议制定肝癌分期标准[1]。纳入标准: ① 符合临床诊断为原发性肝癌中晚期(Ⅰ、Ⅱ); ② 无TACE手术禁忌证; ③ AFP均升高; ④ 血清HBV-DNA定量大于1×103copies/mL,部分患者为HBeAg阳性病随机分为2组。治疗组36例,按Child-pugh分级分为A级21例,B级14例,C级1例;对照组32例,按Child-pugh分级分为A级20例,B级11例,C级1例。2组患者年龄、性别、病情及Child-pugh分级等经比较差异无统计学意义(P>0.05),具有可比性。
1.2 治疗方法
对照组给予常规TACE治疗后,予甘草酸二胺、还原型谷胱甘肽、人血白蛋白,有腹水或感染者经对症治疗,根据肝功能情况每1~2月重复TACE治疗。治疗组在对照组基础上加用拉米夫定片(葛兰素史克)100 mg口服,1次/d(10例);阿德福韦酯(葛兰素史克)10 mg口服,1次/d (14例);替比夫定片0.6 g口服,1次/d (12例),如有耐药变异者采用拉米夫定联合阿德福韦酯治疗,或替比夫定联合阿德福韦酯治疗,疗程分6个月、第1年、第2年,观察2组治疗前后肝功能Child-Pugh评分、HBV-DNA定量、病毒变异及生存时间等情况。
经皮肝动脉化疗加栓塞术(TACE)治疗,即经皮穿刺股动脉插管至肝固有动脉,进行肝动脉造影,确定肝肿瘤供血的动脉,给予化疗药物,常用的有5-氟尿嘧啶(5-Fu)500~1 250 mg、丝裂霉素(MMC)10~20 mg、顺铂(CDDP)60~100 mg、卡铂(CBP)400~500 mg(注射卡铂需用5%葡萄糖溶解,不可用生理盐水),阿霉素(ADM)40~80 mg,表阿霉素(EPD)60~80 mg等。①FAM(5-Fu、MMC、ADM/EPD)。栓塞剂超液化碘油常用为10~30 mL,常与化疗药物混合成乳剂使用,可增加栓塞部位的药物浓度,延迟药物的释放,形成化学栓塞;②可吸收明胶海绵,但和碘油联合使用时,由于继发血栓形成,有时可致血管永久性闭塞,间隔1~2个月,予上腹部CT增强检查,根据肝功能及肿瘤情况可重复进行TACE治疗[2]。
1.3 观察指标
血常规、肝功能、肾功能用日立公司7020全自动生化分析仪测定,试剂由上海科华公司提供;凝血酶原时间、PTA检测采用普利生化仪,试剂由上海太阳生物有限公司提供;HBV-DNA定量采用德国罗氏公司荧光PCR定量仪,试剂由上海克隆生物有限公司提供;AFP采用贝克曼全自动化学发光仪,试剂由贝克曼库尔特公司提供。
2 结 果
2组治疗6个月~2年后,Child-pugh评分、HBV-DNA转阴率的比较见表1、2。治疗前,2组HBV-DNA比较无明显差异。治疗6个月所有口服核苷(酸)类抗病毒治疗患者均未出现耐药或变异。治疗1年时,有10例口服拉米夫定患者出现4例耐药,变异点为204I、180M、181T变异,HBV-DNA定量反弹,ALT升高,联合阿德福韦酯10 mg后,病情好转。14例口服阿德福韦酯患者仅3例耐药,联合拉米夫定或替比夫定患者未出现耐药。2年时共有7例耐药,及时换药或联合用药,肝功能好转,对照组未发现有病毒变异。
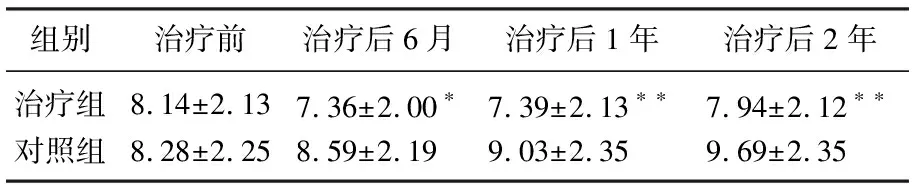
表1 2组治疗前后肝功能Child-pugh评分比较

表2 2组治疗后HBV-DNA阴转率比较 %
68例患者中,治疗2年后死亡34例。治疗组死亡13例,其中3例死于肝癌破裂出血,4例死于食道胃底静脉破裂出血,2例死于肝肾综合征,2例死于肝衰竭,1例死于肺转移呼衰,1例死于腰椎、骨盆转移、下腔静脉转移。对照组死亡21例,其中8例死于肝衰竭、肝性脑病,6例死于食道胃底静脉破裂出血,4例死于肝肾综合征感染,1例死于骨、肺转移,2例死于肝癌破裂出血。
治疗组中,有3例发现口服阿德福韦酯有轻度肌酐(cREA)升高,可能是阿德福韦酯有抑制肾细胞线粒体DNA合成的关系,从而导致近曲小管线粒体的DNA损耗,引起肾脏近曲小管功能障碍[3]。替比夫定有轻度CK升高,经休息后CK自行恢复正常。文献[4-5]报道替比夫定不良反应发生率为5%,以疲劳、血肌酸激酶(ck)升高,头晕、腹泻等多见,一般均能耐受。本研究中患者在治疗期间耐受性较好,仅1例患者出现轻度腹泻,未经处理自行恢复正常,其余未发现明显副作用。2组经治疗后第1、2年生存率比较差异均有统计学意义(P<0.05),见表3。

表3 2组患者生存率比较[n(%)]
3 讨 论
慢性乙肝病毒(HBV)感染者每年进展为肝硬化的比例为0.4%~14.2%。在HCC中,90.9%的患者有慢性乙肝病毒感染,在活动性乙肝肝硬化患者中的发生率为6%,大多数患者隐匿起病,确诊时已失去手术切除的最佳时期,即发展到原发性肝癌中、晚期。TACE是大多数不能手术切除肝癌患者的首选方法之一,但需要多次重复进行,患者常因为肝功能明显异常,或介入时化疗药物对肝脏损害,导致乙肝病毒再激活,常伴有黄疸升高,ALT、AST异常,白蛋白下降,HBV-DNA复制,发展到肝功能Child-pugh为A或B级时,甚至达C级,出现并发症,不适合进行TACE治疗,患者生存率明显下降。有研究[6]提示对HBV感染相关HCC患者,在经皮肝动脉化疗加栓塞术(TACE)治疗同时,采用核苷(酸)类似物抗病毒治疗,根据病情、乙肝病毒复制程度、经济条件等情况,在上述一般护肝、退黄疸基础上,治疗选用: ① 拉米夫定0.1 mg口服,1次/d; ② 阿德福韦酯10 mg口服,1次/d; ③ 替比夫定0.6 g口服,1次/d,减低了HBV-DNA复制水平,肝细胞坏死和炎症得到有效控制,肝功能明显好转,为反复多次采取TACE治疗创造条件,控制肝癌生长速度,延长生存时间,提高生活质量。但随着核苷(酸)类似物应用的时间延长,会导致YNDD变异发生而出现耐药情况,应及时采取联合抗病毒治疗: ① 拉米夫定联合阿德福韦酯治疗; ② 替比夫定联合阿德福韦酯治疗。后者联合用药有较好的互补性,能够有效抑制HBV-DNA的复制,减轻肝脏组织炎症程度,防止阿德福韦酯对肾损害,进而实现了肝功能的持续稳定。在治疗组中,36例患者第1年和第2年肝功能Child-pugh评分明显优于对照组。HBV-DNA定量转阴率明显高于对照组,2年生存率也是明显高于对照组。在治疗组中,口服拉米夫定抗病毒治疗的原发性肝癌患者中未见不良反应。少部分肝癌晚期患者出现肝肾综合征,是病情进展恶化的结果,有2例口服替比夫定出现一过性血清肌酸激酶(CK)轻度升高,休息后复查自行恢复正常,其他未发现明显不良反应[7-9]。
本研究结果提示,对乙肝肝硬化的患者,如果有肝癌家族史,两对半“大三阳”或“小三阳”,HBV-DNA水平较高者,肝功能持续处于炎症活动期,应首先使用核苷(酸)类似物抗病毒治疗,抑制病毒复制,减少炎症活动,降低原发性肝癌发生率,定期监测AFP、B超或上腹部CT检查,对防治或减少原发性肝癌发生率及原发性肝癌早期诊断有较大意义。对红细胞增多症、低血糖、高血钙、高纤维蛋白原血症、高胆固醇血症的肝硬化患者应引起重视,及早使用核苷(酸)类抗病毒药物治疗,稳定肝功能,为进行手术切除或TACE治疗创造条件,从而提高肝癌患者生存时间和生活质量[10]。治疗中定期监测HBV-DNA定量变化,一旦出现YMDD变异发生耐药情况,应及早联合用药或调整抗病毒药,以防止肝功能衰竭发生。
[1] 叶任高,陆在英. 内科学[M]. 北京: 人民卫生出版社,2004: 452.
[2] 徐道振. 病毒性肝炎临床实践[M]. 北京: 人民卫生出版社,2006: 393.
[3] Sun J,Liang X,Wong V W. Commentary: prognostication of chronic hepatitis B are fibrotest and fibroscan the final answers[J]. Aliment Pharmacol Ther,2013,37(11): 1113.
[4] LA I C L,GANE E,HSU C W,et al. Two-year results from the GLOBE Trial in patients with hepatitisB:greater clinical and an-tiviral efficacy for telbivuine vs lamivudine.Hepatology[J]. 2006,44(supp 11): 222.
[5] BZOWNJ N,CHAN LYH,LA I C L,et al. A randomized trial of telbivudine vs.adefovir for HBeAg-positive chronic hepatitis B:final week 52 results[J]. Hepatology,2006,44(supp 11): 563A.
[6] Shaw T,Locamini S. Entecavir for the treatment of chronic hepatitisB[J]. Expert Rev Anti Infect Ther,2004,2: 853.
[7] 刘利英,黄辰,李宗芳,等. STAT1和STAT2在磷脂酰乙醇胺诱导肝癌HepG2细胞生长抑制中的作用[J]. 南方医科大学学报,2011,31(2): 256.
[8] 林莉,林美玲. 联合检测血清中ADA、GGT和AFU对肝癌患者诊断的临床意义[J]. 海南医学院学报,2011,17(3): 328.
[9] 顾靓,张阳德,赵劲风. RNA干扰沉默mTOR基因对肝癌HepG2细胞增殖和凋亡的影响[J]. 海南医学院学报,2011,17(1): 42.
[10] 冯云,周会行,李军红,等. 肝癌缺失基因1和磷酸化粘着斑激酶蛋白在乳腺癌组织中的表达及意义[J]. 南方医科大学学报,2011,31(8): 1448.

