用基于苯并噻二唑衍生物的比率荧光化学传感器检测氟离子
喻艳华, 付 成
(江汉大学 交叉学科研究院,湖北 武汉 430056)
用基于苯并噻二唑衍生物的比率荧光化学传感器检测氟离子
喻艳华*, 付 成
(江汉大学 交叉学科研究院,湖北 武汉 430056)
研制了一种用于灵敏、快速地检测溶液中的氟离子的基于苯并噻二唑衍生物的荧光传感器. 4,7-二溴-2,1,3-苯并噻二唑与三甲基硅基乙炔通过Sonogashira偶联反应得到二取代的三甲基硅基乙炔苯并噻二唑;将该化合物用于检测氟离子,分析了检测灵敏度和选择性. 结果表明,在乙腈和水(V/V= 9∶1)混合溶液中,合成的苯并噻二唑衍生物的最大发射波长峰值为455 nm (激发波长为376 nm);就所测试的F-,Cl-,Br-, I-, ClO4-,AcO-,NO3-,H2PO3-,CN-和HSO4-等阴离子而言,仅F-可以脱除三甲基硅保护基使得该化合物荧光最大发射波长蓝移至435 nm,荧光强度降低60%,且最低检测限可达4.5×10-8mol/L. 因此,二取代的三甲基硅基乙炔苯并噻二唑应用于氟离子检测具有很好的灵敏度和选择性.
苯并噻二唑;荧光化学传感器;氟离子;检测
氟是人体所必需的微量元素之一,在形成骨骼组织、牙齿釉质以及钙磷的代谢等方面都起着无可替代的作用[1-2],但如果摄入过量的氟可导致慢性或急性中毒,例如氟斑牙,氟骨病,胃和肾功能损害等[3-4],因此发展快速、高效的氟离子检测方法在近几十年受到极大的重视[5]. 目前常用来检测氟离子的方法主要有氟离子选择电极法[6]、离子色谱法[7]、氟试剂比色法等[8]. 这些方法的优点是灵敏度高、选择性好,但是大多对样品要求高,需要用到的仪器昂贵,单个样品测定时间长,并且需要熟练的操作人员,不能满足环境监测中高效、低成本的需要.
化学荧光传感器和荧光探针以其优异的化学和生物作用性能而备受重视[9-10]. 荧光传感器法是以荧光为手段,运用受体和外来物种之间的特异结合,实现对待检测物种的定性或定量分析. 该方法具有检测限低、灵敏度高、抗干扰能力强、样本处理方便、成本低廉等优点,因而受到国内外学者的关注. 现在很多报道的检测氟离子的荧光传感器主要是将氟离子与其进行络合,使其荧光发生猝灭[11-13],利用荧光基团的强度变化和氟离子浓度之间的关系来达到检测的目的,此类方法很容易受到激发和发射光相对强度的影响. 荧光比率法是通过两个波长荧光强度的比值变化检测目标物,可以通过自我校正消除不定因素的影响,所以比率法是目前检测离子的最佳选择. 运用比率法检测氟离子的报道较少[14-17],本文作者报道了一种基于含有三甲基硅基乙炔苯并噻二唑衍生物的新型比率荧光化学传感器用来检测氟离子. 其原理是氟离子能够定量的脱除三甲基硅基保护基,使其荧光发射光谱蓝移20 nm,并且伴随荧光强度降低. 此方法可以定量、快速的检测氟离子,最低检测限达到4.8 × 10-8mol/L.
1 实验部分
1.1 仪器与试剂
LAMBDA 25型紫外-可见分光光度计(美国Pekin Elmer公司);LS55型荧光光谱仪(美国Pekin Elmer 公司);AVANCE 400型核磁共振波谱仪(瑞士Bruker公司);Bu4NHSO4(98%),Bu4NH2PO3(98%),三甲基硅基乙炔(98%)均购自上海晶纯生化科技股份有限 公司;二(三苯基膦)二氯化钯,Bu4NF(99%),Bu4NCl(99%),Bu4NBr(AR),Bu4NI(AR),Bu4NClO4(98%),Bu4NAcO(95%),Bu4NNO3(98%),Bu4NCN(99%),4,7-二溴-2,1,3-苯并噻二唑(98%),三苯基膦(CP),碘化亚铜(AR),三乙胺均购自国药集团化学试剂有限公司.
1.2 荧光化学传感器的合成
如图1所示,将4,7-二溴-2,1,3-苯并噻二唑(1.0 g,3.4 mmol),三甲基硅基乙炔(1.4 mL,10.2 mmol ),二氯三苯基膦钯(20 mg,0.03 mmol),碘化亚铜(20 mg,0.1 mmol),三苯基膦(70 mg,0.3 mmol)混合于100 mL三乙胺中,在90 ℃下搅拌4 h. 反应结束后,浓缩,硅胶柱层析(Petroleum ether/CH2Cl2=7/1,V/V)得到黄色固体1(1.0 g,95%). TLC (Petroleum ether/CH2Cl2=3/1,V/V):Rf= 0.45.1H NMR (400 MHz, CDCl3): 7.71 (s, 2H, 2×CH), 0.19 (s, 18H, 2×Si(CH3)3).13C NMR (100 MHz, CDCl3): 155.1 (Cq), 132.5 (CH), 115.0, 107.6, 95.2 (Cq); 0.0 (CH3).

图1 荧光化学传感器的合成Fig.1 Synthesis of fluorescent chemodosimeter
1.3 氟离子滴定检测
在乙腈和水(V/V= 9∶1)混合溶液中分别配制Bu4NF储备液5×10-3mol/L,化合物1储备液1×10-3mol/L. 在比色池中加入25 μL的化合物1储备液、2 475 μL乙腈和水(V/V= 9∶1)的混合溶液,滴加0.5 μL氟离子储备液,摇匀5 s后检测吸收光谱和荧光发射光谱. 重复滴加0.5 μL氟离子储备液,检测吸收光谱和荧光发射光谱,直至加入8倍量的氟离子.
1.4 氟离子选择性检测
在乙腈溶液中配制1×10-3mol/L化合物1的储备液;分别配制浓度为1×10-2mol/L的Bu4NF,Bu4NCl,Bu4NBr,Bu4NI,Bu4NClO4,Bu4NOAc,Bu4NNO3,Bu4NH2PO3,Bu4NHSO4阴离子储备液;在比色皿中加入25 mL化合物1储备液,2 475 mL乙腈和水(V/V= 9∶1)的混合溶液(最终浓度10 μmol/L),检测吸收光谱和荧光发射光谱. 然后再加入20 μL的氟离子储备液,摇匀,检测吸收光谱和荧光发射光谱. 其他阴离子(Cl-, Br-, I-, ClO4-, AcO-, NO3-, H2PO3-, HSO4-)的检测均按照此方法进行.
1.5 氟离子检测干扰实验
在比色皿中加入25 μL化合物1储备液,2 475 mL乙腈和水(9∶1,V/V)的混合溶液(最终浓度10 μmol/L),检测吸收光谱和荧光发射光谱;加入100 μL的氯离子储备液,摇匀,进行吸收光谱和荧光发射光谱检测. 然后再加入10 μL氟离子,摇匀,检测吸收光谱和荧光发射光谱. 其他阴离子(Br-, I-, ClO4-, AcO-, NO3-, H2PO3-, HSO4-)的检测均按照此方法进行.
2 结果与讨论
2.1 化合物1的紫外吸收和荧光性质
配制10 mmol/L化合物1的乙腈和水(9∶1,V/V)混合溶液,测定其紫外吸收光谱,结果如图1所示. 化合物1的最大吸收波长为376 nm, 荧光发射光谱最大波长为455 nm (激发波长为376 nm).
2.2 化合物1 紫外吸收光谱对氟离子的响应研究
图2为化合物1溶液在不同浓度的氟离子下的紫外吸收光谱.可以看到,当未加入氟离子时,化合物1的最大吸收峰为376 nm;加入氟离子后,随着氟离子浓度的增加,最大吸收峰吸光度逐渐减弱,且峰位置蓝移16 nm.

图1 化合物1在乙腈和水(9∶1, V/V)混合溶液中的紫外吸收光谱(实线)和荧光发射光谱(虚线)Fig.1 Absorption (solid) and fluorescence spectra (dash) of compound 1 in the mixture of acetonitrile and water (V/V = 9∶1)

溶剂:乙腈/水 = 9/1 (V/V)
2.3 化合物1 荧光光谱对氟离子的响应研究
图3为化合物1溶液加入不同浓度的氟离子后的荧光发射光谱,随着氟离子浓度的增加,荧光强度逐渐减弱,并且最大发射峰发生蓝移,直至加入两倍量的氟离子后荧光强度变化达到平衡,最大发射峰由455 nm蓝移至435 nm,荧光强度降低60%. 主要原因是氟离子具有强碱性,可以使硅炔键断裂,得到化合物2和三甲基氟化硅(图4). 当化合物1脱除TMS后,苯并噻二唑的电子云密度降低,导致荧光强度减弱,并且发生蓝移. 由于是定量的化学反应,所以加入两倍量的氟离子可使TMS完全脱除,继续滴加氟离子荧光则不会再发生改变. 此反应非常快速,加入氟离子后摇匀即可测定.

激发波长为376 nm,溶剂:乙腈/水= 9/1 (V/V)

图4 TBAF脱除TMS保护基Fig.4 Deprotection of TMS by TBAF
2.4 化合物1对氟离子检测限的测定
如图3所示,当氟离子的浓度范围为 0~20 μmol/L时,化合物1在不同浓度氟离子下产生荧光发射波长在402 nm处的强度值与最大发射峰455 nm峰值的比值的变化曲线线性增长并表现出较好的线性关系(R2=0.970 0,见图5).根据国际纯粹与应用化学联合会(IUPAC)对检测限的定义,可以利用“检测限= 3σ/k”这一公式来计算检测限.其中σ为空白样的标准偏差, 对化合物1空白样 (未加入氟离子)分别进行12次荧光测量,取测量结果并计算各自的标准偏差.k为线性拟合方程中拟合直线的斜率.通过公式可得,化合物1对氟离子的检测限为4.5×10-8mol/L, 表明此化合物可以作为理想的检测氟离子的荧光化学传感器.

图5 氟离子的检测限测定Fig.5 The determination of the detection limit (LOD) for F-
2.5 化合物1对氟离子选择性的响应
为了确定此方法在检测中常见的阴离子是否会对氟离子的检测造成干扰,研究了可能对氟离子检测造成干扰的阴离子对化合物1荧光强度的影响. 图6是化合物1对氟离子的选择性的研究示意图.从图6A中可以看出,在向化合物1溶液中加入不同阴离子时,只有氟离子能引发化合物1产生荧光变化,荧光强度降低60%,最大发射峰蓝移20 nm,其他离子对化合物1没有明显的响应. 这主要基于氟离子具有强碱性可以使硅炔键断裂,而其他阴离子由于碱性不足无法诱导反应发生. 通过荧光比率法I402 nm/I455 nm得到柱状图6B,从图6B可见,化合物1对氟离子具有非常好的选择性.
为了进一步测试化合物1检测体系对氟离子的检测能力,分析了化合物1检测体系在不同阴离子与氟离子共存的条件下对氟离子的检测效果,结果如图7所示. 可以看出,在与其他阴离子共存的情况下,氟离子依然可以脱除化合物1中的TMS,诱导化合物1产生荧光强度减弱且蓝移的效果. 因此可以得出结论,化合物1作为检测氟离子的荧光化学传感器具有很好的抗干扰能力,在检测过程中其他阴离子不会对检测结果带来明显的干扰.

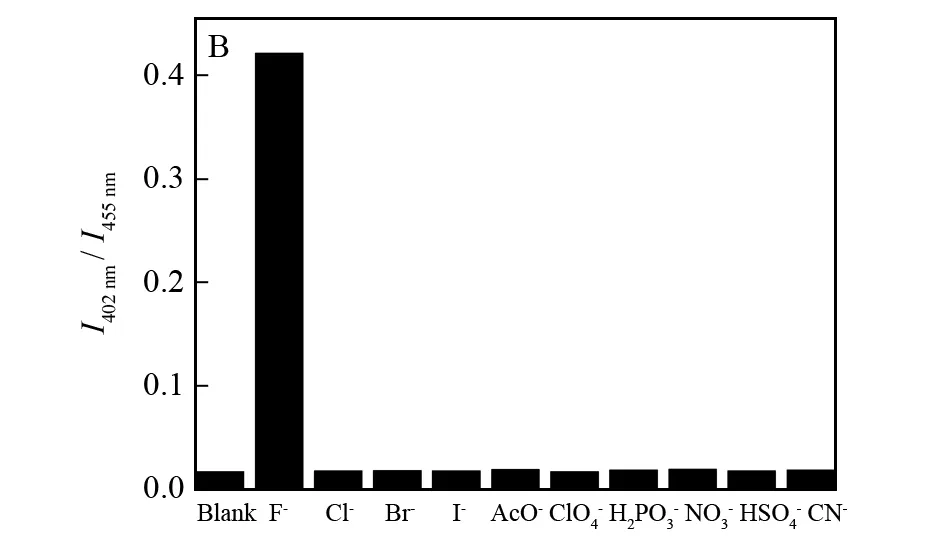
激发波长为376 nm;A:荧光光谱图;B: I402 nm / I455 nm柱状图

激发波长为376 nm
3 结论
以苯并噻二唑为荧光发色团引入TMS保护的炔基,设计、合成化合物1新型的荧光化学传感器,并考察了其对氟离子荧光检测的性能.研究结果表明,在乙腈和水(9∶1,V/V)的溶剂中氟离子可以快速脱除TMS,得到只含炔基的苯并噻二唑,同时伴随着荧光发射光谱的强度降低60%,且最大发射峰蓝移20 nm. 化合物1对氟离子的检测限为4.5×10-8mol/L,在检测过程中其他阴离子不会对检测结果带来影响.综上所述,化合物1对氟离子的检测具有简单、快速和高灵敏度等特点,在氟离子检测中具有潜在的应用价值.
[1] 郝一莼, 孙小单, 徐 桐, 等. 氟离子检测分析方法研究进展[J]. 中国地方病防治杂志, 2010, 25(6): 412-415.
[2] LI Y M, ZHANG X L, ZHU B C, et al. A highly selective colorimetric and “off-on-off” fluorescent probe for fluoride ions [J]. Anal Sci, 2010, 26 (10): 1077-1080.
[3] KLEEREKOPER M. The role of fluoride in the prevention of osteoporosis [J]. Endocrinol Metab Clin North Am, 1998, 27(2): 441-452.
[4] BARBIER O, ARREOLA-MENDOZA L, DEL RAZO L M. Molecular mechanisms of fluoride toxicity [J]. Chem Biol Interact, 2010, 188 (2): 319-333.
[5] XU Z, KIM S K, YOON J. Revisit to imidazolium receptors for the recognition of anions: highlighted research during 2006-2009 [J]. Chem Soc Rev, 2010, 39(5): 1457-1466.
[6] 俞 冰. 电极法测定水中氟离子浓度研究[J]. 东北电力技术, 2000(5):24-26.
[7] 吴伟杰. 氟离子检测方法的改进及离子色谱法的应用[J]. 广东化工, 2005(8): 69-71.
[8] 王秀珍, 王永勤, 巩丽青, 等. 双波长比色法测定饮用水中氟含量[J]. 中华预防医学杂志, 2003, 37(1): 48-49.
[9] ZHANG X J, XU Y F, GUO P, et al. A dual channel chemodosimeter for Hg2+and Ag+using a 1,3-dithiane modified BODIPY [J]. New J Chem, 2012, 36 (8): 1621-1625.
[10] ZHOU Y, LIU K, LI J Y, et al. Visualization of nitroxyl in living cells by a chelated copper(II) coumarin complex [J]. Org Lett, 2011, 13(11): 1290-1293.
[11] CHANG K J, MOON D, LAH M S, et al. Indole-based macrocycles as a class of receptors for anions [J]. Angew Chem Int Ed, 2005, 44(48): 7926-7929.
[12] BOWMAN-JAMES K. Alfred Werner revisited: the coordination chemistry of anions [J]. Acc Chem Res, 2005, 38(8): 671-678.
[13] SONG P, DING J X, CHU T S. TD-DFT study on the excited-state proton transfer in the fluoride sensing of a turn-off type fluorescent chemosensor based on anthracene derivatives [J]. Spectrochim Acta A, 2012, 97: 746-752.
[14] ZHOU Y, WANG F, KIM Y, et al. Cu2+-selective ratiometric and “off-on” sensor based on the rhodamine derivative bearing pyrene group [J]. Org Lett, 2009, 11(19): 4442-4445.
[15] ZHANG X, XIAO Y, QIAN X. A ratiometric fluorescent probe based on FRET for imaging Hg2+ions in living cells [J]. Angew Chem Int Ed, 2008, 47(42): 8025-8029.
[16] QU Y, HUA J, TIAN H. Colorimetric and ratiometric red fluorescent chemosensor for fluoride ion based on diketopyrrolopyrrole [J]. Org Lett, 2010, 12(15): 3320-3323.
[17] KAI Y M, HU Y H, WANG K, et al. A highly selective colorimetric and ratiometric fluorescent chemodosimeter for detection of fluoride ions based on 1,8-naphthalimide derivatives [J]. Spectrochim Acta A Mol Biomol Spectrosc, 2014, 118: 219-243.
[责任编辑:吴文鹏]
Detectionoffluorideionbyratiometricfluorescentchemodosimeterbasedonbenzotiadiazolederivative
YU Yanhua*, FU Cheng
(InstituteforInterdisciplinaryResearch,JianghanUniversity,Wuhan430056,Hubei,China)
A ratiometric fluorescent chemodosimeter based on benzotiadiazole derivative has been developed for detecting fluoride ion (F-) in solution sensitively and rapidly. Namely, bis-trimethylsilylalkyne benzothiadiazole was prepared by Sonogashira coupling reaction of 4,7-dibromo-2,1,3-benzothiadiazole and trimethylsilyl ethyne. As-synthesized product was used to detect F-, and the detection sensitivity and selectivity were analyzed. Results show that the emission band of the as-synthesized benzothiadiazole derivative in the mixture of acetonitrile and water (V/V= 9∶1) is centered around 455 nm (the excitation wavelength is 376 nm). Among tested anions such as F-, Cl-, Br-, I-, ClO4-, AcO-, NO3-, H2PO3-, CN-and HSO4-, only F-is able to eliminate the trimethylsilyl (TMS) protective group thereby leading to a blue shift of the maximum fluorescent emission wavelength from 455 nm to 435 nm as well as a decrease of the fluorescence intensity by 40%, with the detection 1imit being 4.5×10-8mol/L. This means that bis-trimethylsilylalkyne benzothiadiazole can be well used to detect F-with good sensitivity and selectivity.
benzotiadiazole; fluorescent chemodosimeter; fluoride ion; detection
2014-06-03.
江汉大学博士科研启动基金(2014036)
喻艳华(1985-),女,助理研究员,研究方向为有机化学.*
,E-mail:hpyyh@aliyun.com.
O 657.39
A
1008-1011(2014)05-0482-06
10.14002/j.hxya.2014.05.010

