生物活性玻璃结合浸浴治疗烧伤残余创面的疗效评价
胡 亮,孙炳伟,肖贵喜,于 冶
(1.江苏大学附属昆山医院 昆山市第一人民医院,烧伤整形外科,江苏 昆山,215300;2.江苏大学附属医院 烧伤整形科,江苏 镇江,212001)
烧伤深度创面在临床治疗过程中常常易造成残余创面,特别是大面积烧伤患者更易出现多处创面的残留。如何安全有效的促进烧伤残余创面的愈合成为临床工作中有待解决的问题。本科2011年1月—2013年2月使用生物活性玻璃结合浸浴疗法治疗烧伤残余创面,取得了较好的疗效,现报告如下。
1 资料与方法
1.1 一般资料
60例患者中男42例,女18例,年龄12~64岁。患者烧伤总面积7%~92%TBSA,深Ⅱ~Ⅲ度,残余创面面积1%~10%,创面残余时间31~42 d,单个残余创面面积3.5~21.5 cm2,位于四肢以及躯干,散在或密集分布。纳入标准:残余创面小于10% TBSA; 单个创面小于5 cm×5 cm; 残余创面形成时间大于30 d。排除标准:明显脓毒血症伴有全身严重感染患者;有严重心、肺、肝、肾以及造血系统的疾病患者;患肢有下肢静脉曲张或者皮肤病患者;糖尿病患者;女性患者处于生理期、哺乳期或妊娠期。随机分为试验组和对照组,每组30例。2组患者在年龄、性别、烧伤总面积及残余创面面积方面比较无显著差异(P>0.05),具有可比性。见表1。
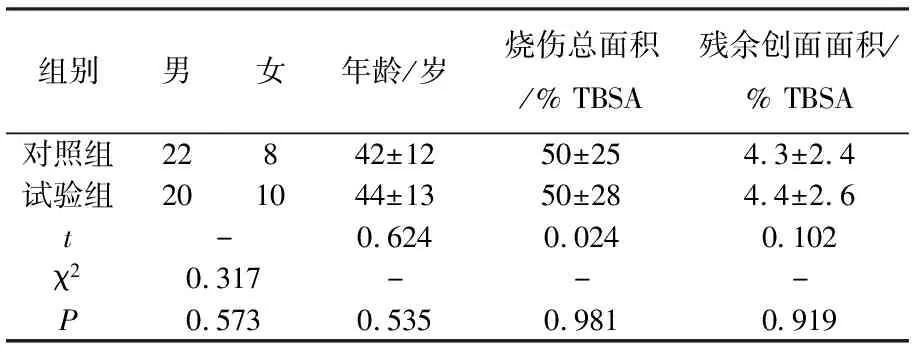
表1 2组患者年龄、性别、烧伤总面积及残余创面面积比较
1.2 治疗方法
2组患者均使用浸浴治疗机(型号HP-DC,开封康复医用设备有限公司)进行浸浴治疗。浸浴液选用0.9%氯化钠溶液,根据残余创面面积以及部位选用全身浸浴或局部浸浴。水温设置恒定于37 ℃~39 ℃,浸浴时间20~45 min。浸浴时,保持室内温度25 ℃~30 ℃,避免患者受凉,医务人员穿手术衣,带无菌手套协助患者浸浴。待创面浸渍后揭除内层敷料,用无菌纱布轻拭创面,尽量清除创面分泌物以及脱离的坏死组织。浸浴过程中可适当补充水分,同时密切观察患者反应,若患者出现面色苍白、头晕呕吐、呼吸心跳加快等现象需立即停止浸浴。浸浴结束后,予无菌纱布擦干。
浸浴结束后,试验组应用生物活性玻璃材料粉剂(商品名:肌肤生)均匀喷洒于创面,凡士林油纱布覆盖,外以干燥无菌纱布覆盖包扎,每日更换1次。对照组应用碘伏纱布后覆盖创面,外以干燥无菌纱布包扎,每日更换1次。创面愈合或用药后21 d终止本试验。
1.3 观察指标
密切观察并记录2组患者创面在用药7、14、21 d的愈合程度以及肉芽生长情况,并于用药后21 d判定疗效。判定标准[1]: 用药21 d内创面愈合或缩小2/3以上且肉芽嫩长生长情况良好为显效;用药21 d内创面缩小1/3以上为有效;用药21 d创面缩小不到1/3为可疑有效;创面延迟愈合或无明显变化为无效。肉芽组织红润,易出血即为生长良好。
分别在用药7、14、21 d后,下次浸浴前对患者采集1次创面分泌物进行细菌学检测,创面愈合后不采集。检出细菌记为阳性。用药前及用药后监测2组患者血常规以及肝肾功能情况,用药后观察患者全身以及局部不良反应。
2 结 果
试验组7 d时,24例患者创面渗出减少,肉芽生长良好; 14 d时,7例患者创面痊愈,余23例患者创面均有不同程度缩小,肉芽组织均新鲜,渗出少; 21 d时,8例患者创面痊愈,8例患者创面缩小2/3以上,5例患者创面缩小1/3以上,仅2例患者创面缩小不到1/3,但肉芽组织生长良好,渗出少。对照组7 d时,10例患者创面肉芽较前新鲜,渗出减少; 14 d时,1例患者创面痊愈,22例患者创面有不同程度缩小,肉芽组织新鲜,渗出少,7例患者创面肉芽无明显变化; 21 d时,3例患者创面痊愈,2例患者创面缩小2/3以上,12例患者创面缩小1/3以上,11例患者创面缩小不到1/3,1例患者创面无明显缩小,肉芽组织较前新鲜,渗出少。根据创面愈合疗效判定标准,试验组中显效23例,有效5例,可疑有效2例,无效0例,总有效率为93.3%;对照组中显效6例,有效11例,可疑有效12例,无效1例,总有效率为56.7%。试验组总有效率显著高于对照组,差异有统计学意义(P<0.01)。
2组患者创面分泌物培养在7、14、21 d均检出细菌,包括金黄色葡萄球菌、表皮葡萄球菌、铜绿假单胞菌、大肠埃希菌、肺炎克雷伯菌以及鲍曼不动杆菌。2组比较差异无统计学意义(P>0.05)。见表2。
试验组7、14、21 d取样创面阳性分别为12、7、4次,共取样创面68次,阳性共23次,阳性率33.8%; 对照组7、14、21 d取样创面阳性分别为13、12、8次,共取样创面85次,阳性共33次,阳性率38.8%。2组患者创面细菌检出率比较无显著差异(P>0.05)。
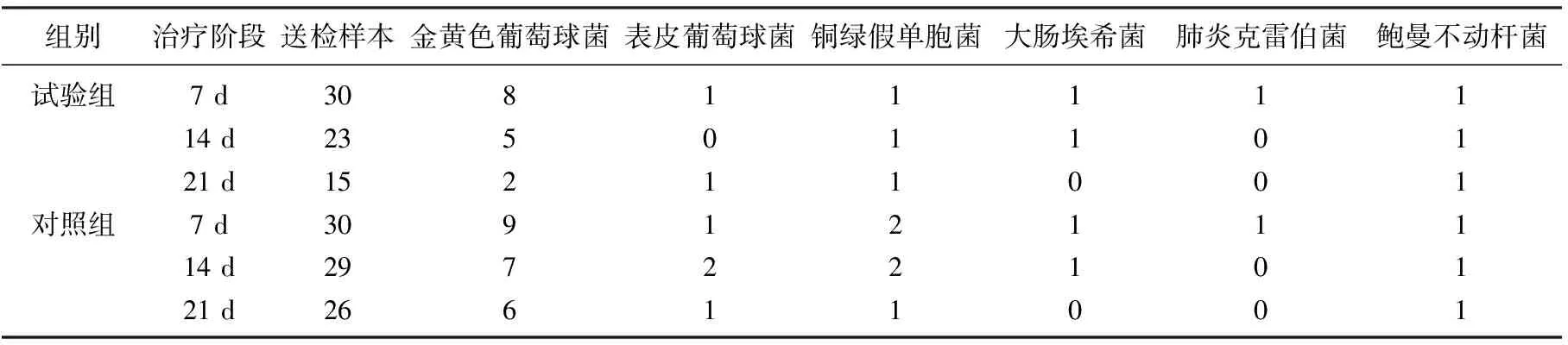
表2 2组患者各时相创面检出细菌比较 株
2组患者均未出现明确的全身或局部不良反应。用药前后试验组与对照组血常规以及肝肾功能结果比较,差异无统计学意义。试验组有2例患者在用药后出现局部刺痛,皮肤发热感,未做特殊处理,症状均在30 min内自行缓解。
3 讨 论
烧伤残余创面由多种原因引起,多见于深度烧伤的治疗后期,其形成的常见原因有: ① 大面积烧伤,多次手术修复创面,手术打击以及创面营养成分丢失,能量消耗,血红蛋白以及血浆白蛋白不足,创面愈合迟缓; ② 创面反复感染,尤其耐药菌感染; ③ 自体移植皮源不够等原因,造成植皮不及时和植皮密度不够; ④ 植皮后新生长皮耐磨性差,创面换药揭除敷料动作过大及愈合后患者功能锻炼时导致上皮破溃; ⑤ 深Ⅱ度创面和取皮较深的供皮区创面在愈合过程中,残留在真皮内的皮脂腺、汗腺分泌物阻塞形成潴留性小囊泡,继而感染破溃形成残余创面; ⑥ 早期破溃的创面未进行及时有效的处理,形成慢性溃疡[2]。由于烧伤残余创面的特点常常是散在分布,反复破溃,牵延不愈[3],因此其治疗一直是临床工作中的棘手问题。
综合治疗是治疗残余创面的关键[4],包括全身营养支持治疗、浸浴治疗、全身或局部抗感染治疗,创面应用药物治疗以及手术植皮治疗等。临床上对于面积较大的残余创面>5 cm,可以通过植皮方法修复创面,效果较好[5-6],但多个部位反复出现的小的残余创面,患者无论心理上还是经济上均难以接受手术治疗。对于面积较小,且多个部位的残余创面,浸浴治疗及创面局部用药均能促进愈合,二者有效结合后更易被患者所接受。通过浸浴治疗,能使皮肤清洁减少感染,促进坏死痂皮脱落,改善局部微循环,同时使患者全身处于放松状态,保持心情愉快,从而促进创面愈合。另外,浸浴时内层敷料浸渍后易接触,避免了换药动作过大造成的新生上皮损伤。关于创面局部用药,金属银及其各类衍生制剂被视作传统的方法用以治疗各类皮肤创面,其抵抗创面细菌感染的作用已得到肯定[7]。但银制剂没有促进创面生长的作用,难以加快创面的再上皮化。同时银制剂的局部超量可引起明显的细胞毒性,从而阻止创面的上皮化[8]。
近年来,随着医学的发展,各类创面药物以及敷料层出不穷。生物组织工程技术已经广泛应用在皮肤创伤的创面修复和上皮功能重建等方面。20世纪70年代由美国生物材料公司和弗罗里达大学研究开发的生物活性玻璃材料(BioGlass)是一种创伤主动修复的无机材料,主要成分为二氧化硅、氧化钠、氧化钙和五氧化二磷[9],颗粒直径<90 μm。作用是通过材料与机体组织的键合作用,从而对机体组织进行修复、替代与再生。生物活性玻璃材料的衍生产品DermGlas(商品名:肌肤生)主要用于各类急、慢性创面的愈合。使用生物活性玻璃材料应用于创面,可利用钙、磷等无机元素的生物诱导作用,代替生物蛋白类制剂,起到主动诱导上皮细胞增殖和分化的上皮化作用。生物活性玻璃材料的粉体与创面接触后,迅速在表面形成一个碳酸羟基磷灰石胶结层[10],能诱导创面上皮细胞合成第IV 型胶原纤维,并能持续性地诱导促创伤愈合因子如 EGF、bFGF及TGF-β等的自泌,为创面局部提供患者自身的具有完全生物功能的天然上皮生长因子[11]。这些上皮生长因子增多可以有效的改善创面营养环境以及微循环,同时刺激创面上参与愈合的细胞加速增殖与分化,并聚集于碳酸羟基磷灰石胶结层,有利于新生上皮的覆盖以及爬行,从而加速创面的愈合。
本研究结果显示,浸浴治疗后经生物活性玻璃材料处理的烧伤残余创面愈合情况明显优于浸浴后碘伏纱布处理的创面(P=0.001),故使用生物活性玻璃材料能有效的促进烧伤残余创面的愈合。2组患者创面在3个不同时相均检出金黄色葡萄球菌、表皮葡萄球菌、铜绿假单胞菌、大肠埃希菌、肺炎克雷伯菌以及鲍曼不动杆菌,检出细菌比较差异无统计学意义(P=0.790); 同时,创面细菌培养的结果显示试验组与对照组在细菌培养检出率上也没有显著差异(P=0.523)。与具有抗菌活性的碘伏纱布比较,应用生物活性玻璃材料未增加细菌感染的概率,这说明生物活性玻璃有一定的抗感染能力,其机制是粉体在创面被组织渗透液溶解后能在局部形成碱性环境,从而在早期能发挥一定的抗菌作用,这对创面愈合也是极其有利的[12]。对于生物活性玻璃材料的安全性,由于其重要的化学成分类似于人体内自然存在的无机元素,其安全性和稳定性均保证了临床使用的可行性[13]。本研究中试验组与对照组均未出现明确的局部或全身不良反应,药物安全性好,试验组有2例出现创面局部刺痛与发热感,30 min内均自行缓解,可能与剂量大小以及用药面积有关。
[1]田利剑,金森,王建亭,等.水溶性胶冻剂烧伤0号治疗深II度烧伤的临床研究[J].中华医学研究杂志,2007,7(1): 34.
[2]吕庆兵,于冶,肖贵喜,等.浸浴结合银离子敷料治疗大面积烧伤患者残余创面的疗效[J].中华烧伤杂志,2013,29(2): 203.
[3]宋知仁,何学贤,成路,等.外用新鲜冷冻血浆治疗烧伤残余创面自身对比观察[J].中国医师杂志,2010,12(7): 952.
[4]王屋金.68例烧伤残余创面综合治疗体会[J].白求恩军医学院学报,2012,10(5):385.
[5]承宇,闵文华.203例重度烧伤治疗后期残余创面的处理[J].中华烧伤杂志,2005,21(1): 71.
[6]刘郭,董乐乐,陈存富,等.58例烧伤后残余创面的综合治疗[J].实用医学杂志,2008,25(3): 294.
[7]Fuller F,Parrish M,Nance F.A review of the dosimetry of 1% silver sulfadiazine cream in burn wound treatment[J].J Burn Care Rehab,1994,15:213.
[8]周来生.生物医学工程学技术在创面修复领域的应用前景[J].中华烧伤杂志,2005,21(1): 6.
[9]姜睿又超,贵超.创面生物活性玻璃新型敷料临床应用[J].中国医药科学,2011,1(12):47.
[10]陈良,徐玲玲,张志宾.生物活性玻璃的制备、应用及活性机制[J].材料导报,2008,22(Z2):348.
[11]Hench L L,Lobel K D.In vitro adsorption and activity of enzymes reaction layers of bioactive glass substrates[J].J Biomed Mater Res,1998,39(4):575.
[12]王钰,马兵,夏照帆,等.生物活性玻璃对30例烧伤患者治疗后期创面的疗效观察[J].中华烧伤杂志,2006,22(6):474.
[13]吴燕文,王春明,寿倍明.生物活性玻璃创面敷料对深Ⅱ度烧伤创面愈合的疗效观察[J].现代医学,2012,40(1):63.

