青娥丸治疗绝经后骨质疏松症(肾虚血瘀证)的临床研究*
李 萍 沈 霖 杨艳萍 帅 波 邹小娟 柯 晖
1湖北中医药大学基础医学院,武汉 430065 2华中科技大学同济医学院附属协和医院中西医结合科,武汉 430022
绝经后骨质疏松症(postmenopausal osteoporosis,PMOP)作为原发性骨质疏松症的常见类型之一,其高发病率已经严重困扰中老年绝经女性的健康。西医防治PMOP的药物主要有二膦酸盐、降钙素、雌激素、异黄酮衍生物、德诺苏单抗,但都有一定的毒副作用和不良反应[1-2]。近10余年来,中药处方及中成药在PMOP的应用也取得一定临床效果,其中青娥丸作为传统补肾壮骨的良方,不论是以之作为中药处方加减还是使用其成药制剂均有较好临床疗效[3]。为进一步探讨青娥丸治疗PMOP的临床疗效,特研究并报道如下。
1 资料与方法
1.1 一般资料
搜集2013年8月—2013年11月华中科技大学同济医学院附属协和医院骨质疏松症专病综合门诊收治的符合纳入标准的患者72例,随机分为A、B、C组,每组24例。A组为钙剂对照组,平均年龄(58.08±3.67)岁;B组为青娥丸低剂量组,平均年龄(59.33±4.05)岁;C组为青娥丸高剂量组,平均年龄(58.57±3.93)岁。3组在人口学特征(如年龄、绝经年龄、身高等)、生命体征(如心率、血压等)、体重、体重指数以及疗效指标的基线值等方面比较,差异无统计学意义(P>0.05),具有可比性。
1.2 纳入标准
1.2.1 PMOP诊断标准 参考WHO标准,用双能X线骨密度仪(DEXA)测定骨密度(BMD),T值≤-2.5 SD[3];绝经时间2年以上,且年龄≤70岁;患者知情自愿,能接受治疗并能完成本研究者。
1.2.2 中医肾虚血瘀证诊断标准 参考《中药新药临床研究指导原则》[4]制订症状积分标准。主症:①全身骨痛或腰膝酸痛;②胸腰部椎体叩击痛;③全身酸软。次症:①下肢痿软;②心烦失眠;③耳鸣耳聋;④肢体麻木;⑤肌肤甲错;⑥舌脉:舌暗红或淡紫或见瘀点,脉沉涩或涩弱。具备主症3项,以及次症中①、②、③中的1项以上,以及④、⑤中的1项以上,结合舌脉,即为骨质疏松症肾虚血瘀证候。
1.3 排除标准
继发性骨质疏松症患者;合并糖尿病、风湿、类风湿、原发性甲亢等影响骨代谢疾病的患者;合并其他严重器质性病变或严重肝肾功能不全者;近6个月使用过对骨代谢有影响的药物者;近3个月使用过雌激素者;近期有骨折者;不能完成本研究方案者。
1.4 药物制备与方法
1.4.1 青娥丸的制备 补骨脂160 g(酒浸,炒),杜仲80 g(去皮,姜汁浸,炒),胡桃(去皮、膜)60个,上为细末,蒜(熬膏)60 g,蒜膏为丸。药物在华中科技大学同济医学院附属协和医院中药房加工制作。中药饮片均购自湖北省中药材公司。对照组制作青娥丸模拟剂,并采用与青娥丸一致的剂型、外观及规格。
1.4.2 给药方法 3组均以钙尔奇D为基础治疗,600 mg/次,1次/d,口服。B组与C组在此基础上加用青娥丸口服,B组6 g/次,3次/日;C组12 g/次,3次/日。3组均治疗24周。
1.5 观察指标
1.5.1 疼痛VAS评分 采用疼痛10 CM水平视力对照表(VAS),让患者进行自我评价。入组时作基线评定,分别于治疗8、16、24周后再次评定。
1.5.2 中医临床症状疗效判定 依据肾虚血瘀证诊断标准,将主症以及次症分为无、轻、中、重级,依次计分为0、1、2、3分。疼痛等症状基本消失,症状积分下降≥2/3为显效;症状好转,症状积分下降≥1/3并<2/3为有效;症状无好转,症状积分下降<1/3为无效。入组时作基线评分,治疗24周后再次评分并转化,记录各组显效、有效、无效例数。
1.5.3 骨代谢标志物 采用电化学发光法[5],检测各组Ⅰ型前胶原氨基端前肽(PⅠNP)、Ⅰ型胶原羧基端肽β特殊序列(β-CTX)、血清骨钙素(BGP)、25-羟维生素D3。入组时作基线检测,治疗24周后再次检测。
1.5.4 BMD测定 采用双能X线骨密度仪(GE Lunar,Madison,WI,USA)对腰椎L2~L4、股骨颈、大粗隆、Ward’s三角进行测量,腰椎L2~L4取均值,以上测量值均转化为T值。入组时作基线测定,治疗24周后再次测定。
1.5.5 安全性指标检测及不良事件 治疗期间每8周于本院检验科检测血常规、尿常规以及肝肾功能,于心电图室检测心电图,另随时记录患者所发生的不良反应。
1.6 统计学处理
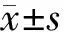
2 结果
2.1 各组治疗前后不同时间疼痛VAS评分变化比较
3组治疗前差异均无统计学意义(P>0.05)。治疗8周后C组即能有效缓解疼痛症状(P<0.05),B组为16周(P<0.05),而A组则无明显缓解疼痛(P>0.05);自16周开始,C组缓解疼痛的效果就明显优于A组(P<0.01),24周时B组缓解疼痛的效果也优于A组(P<0.01)。见表1。
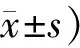
表1 各组治疗不同时间骨痛评分比较(n=24,分,
2.2 各组治疗后中医临床疗效比较
治疗24周后,A组与B组各脱落1例,C组脱落2例;经Ridit分析,B组与C组症状改善情况明显优于A组(P<0.01),B组与C组间比较,C组效果显著优于B组(P<0.05)。见表2。
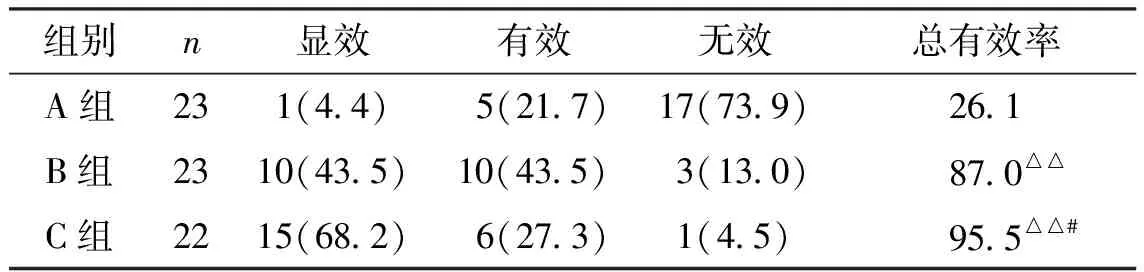
表2 各组临床疗效比较(例,%)
2.3 各组治疗前后骨代谢标志物变化情况
3组治疗前在各项目差异无统计学意义(P>0.05)。C组经24周治疗后,各项指标都有较明显的下降(P<0.05),B组仅在β-CTX的指标中有较好的治疗效果(P<0.05)。B组与C组相比较,虽然C组的相关数值较B组更理想,但差异无统计学意义(P>0.05)。A组各项指标在治疗前后差异均无统计学意义(P>0.05)。见表3。
2.4 各组治疗前后BMD T值变化比较
以转化后的T值进行统计分析。3组患者各部位T值均不相同,腰椎L2~L4以及Ward’s三角的T值最低,大粗隆的T值最高。治疗前3组各部位的BMD均无明显差异(P>0.05)。治疗24周后,B组、C组能有效提高各部位的BMD(P<0.05,P<0.01),其中C组对股骨颈及Ward’s三角的作用尤为显著(P<0.01)。A组各部位的BMD在治疗前后差异均无统计学(P>0.05)。见表4。
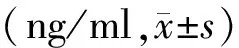
表3 各组骨代谢标志物变化比较
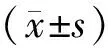
表4 各组BMD T值变化比较
2.5 不良反应事件记录
治疗期间,3组患者均未出现明显实验室指标异常或心电图异常情况。B组有1例发生口干症状,嘱增加饮水后缓解;C组在治疗初期有2例发生便秘,以五仁润肠丸口服后缓解。
3 讨论
中医认为,骨质疏松症属于中医“腰痛”、“骨痿”、“骨痹”等范畴。对于PMOP患者而言,其病机多为肾虚血瘀,肾虚为本,血瘀为标。《内经》言:“阳化气,阴成形”,肾藏全身阴精、精微物质而筑骨构形。绝经后女性“天癸竭,地道不通”,是为阴精亏虚之象,阴精既亏,时日迁延则耗损精髓,髓海空虚。《素问·生气通天论》言:“凡阴阳之要,阳密乃固”,又言:“阳强不能密,阴气乃绝”,前一句指出了人之阴阳平衡充盈,需要阳气固密的重要性,后者从阳亢的病理角度指出阳不能密的后果,即“阴气乃绝”。绝经后女性若肾阳虚衰,则阳虚气化无力,固护无权,会出现“阳虚不能密”之象,从而导致其机体“阴”的流失。人之“阴”因这两方面的原因会耗损、流失、衰竭,继而导致“不荣则痛”,出现“骨痛”之症、“骨痿”之病。另一方面,肾之阳气不足,则血行无力,血脉不温,脉寒流缓而瘀;肾之阴精不足,则精津亏少,血少而稠,血流黏滞而瘀。血瘀气不行会“不通则痛”,流通不畅供养不足会加剧“不荣则痛”。
因此针对本病本证,应该以补肾为主,兼以活血化瘀。青娥丸自古以来即为治疗肾虚腰痛的名方,由补骨脂、杜仲、胡桃仁、大蒜组方而成。补骨脂辛温,功能温肾壮阳,固精纳气;胡桃仁甘温,能补能固能温、能通润血脉;二者相合其效更著,故《本草纲目》言补骨脂:“得胡桃、胡麻良”;杜仲性甘温,入肝肾经,能补肝肾强筋骨;大蒜辛温走窜,宣通祛寒,行滞通络,《日华子本草》说大蒜:“健脾,治肾气”。青娥丸原方以大蒜蒸熟糊丸,一益脾胃一引诸药。四药合用,共达内充肾气,调达气血之功。本研究显示,高剂量青娥丸组(C组)能有效且快速地缓解患者疼痛症状和其他临床症状,其作用效果明显优于钙剂对照A组和低剂量青娥丸组(B组),此结果某种程度上证实了本病中医辨证论治思路的正确性。
近年来的研究[2]证实,PMOP患者是由于雌激素减少所致。然而单纯的补充雌激素虽然能抑制骨吸收,减少骨丢失,有效防治骨质疏松症,但其不良反应及毒副作用不容忽视。补骨脂的雌激素样作用以及青娥丸的雌激素样作用在较多文献中得到证实[6-8],在本研究中,B组和C组均能增加患者BMD(P<0.05,或P<0.01),改善患者骨质疏松症状,且C组中各骨代谢标志物都有明显降低(P<0.05),B组中仅有骨吸收标志物β-CTX有显著降低,与同类文献相似[3,9]。有学者[10]认为,雌激素在中医学范畴中具有“阴”的属性,雄激素具有“阳”的属性。青娥丸具有补益肾之阳气的功效,也应该具有提高雄激素的作用。而雄激素除通过芳香化作用转化为雌激素在骨代谢中发挥作用外[11],还能直接抑制破骨细胞吸收活性[12]。因此,考虑B组中低剂量青娥丸是否轻度提升雄激素而发挥作用,从而降低β-CTX,当然此假设还需进一步研究证实。另外,青娥丸对患者血瘀病机下微循环、骨转换标志物的影响,尚需要更多的实验与临床研究。本研究中不良反应轻微,也说明青娥丸具有较好的安全性。
综上所述,青娥丸的功效为“补益肾气,活血化瘀”,通过发挥雌激素样作用,或者还有雄激素样作用,能明显改善肾虚血瘀证PMOP患者局部疼痛等临床症状,有效提高患者BMD,降低患者骨代谢标志物,并且其效果跟用药剂量呈正相关。
[1] XU XJ,SHEN L,YANG YP,et al.Serum sclerostin levels associated with lumbar spine bone mineral density and bone turnover markers in patients with postmenopausal osteoporosis[J].Chinese Med(Engl),2013,126(13):2480-2484.
[2] 马芳远,高青房,朱秀华.原发性骨质疏松症临床药物治疗新进展[J].中国老年保健医学,2013,11(1):48-49.
[3] 赵光,沈霖,杨艳萍,等.青娥丸对绝经后骨质疏松症患者骨密度、血清MMP-2水平及骨代谢指标的影响[J].中西医结合研究,2012,4(3):113-117.
[4] 郑莜萸.中药新药临床研究指导原则[M].北京:中国医药科技出版社,2002:356-361.
[5] XU XJ,SHEN L,YANG YP,et al.Serum β-catenin levels associated with the ratio of RANKL/OPG in patients with postmenopausal osteoporosis[J].Int J Endocrinol,2013,doi:10.1155/2013/534352.
[6] 牛煜.青娥丸治疗绝经后骨质疏松症疗效观察[J].深圳中西医结合杂志,2012,22(2):101-102.
[7] 孙冠芸,王星琴,薛冰洁,等.复方青娥丸不同萃取部位雌激素样作用研究[J].重庆中草药研究,2011,64(2):37-40.
[8] 李璘,邱蓉丽,乐巍,等.补骨脂雌激素样作用实验研究[J].辽宁中医药大学学报,2012,14(4):57-58.
[9] 徐晓娟,沈霖,杨艳萍,等.青娥丸对绝经后骨质疏松症患者骨密度和骨转换标志物的影响[J].中国中医骨伤科杂志,2013,21(6):9-10.
[10] 崔晓萍,张庆文,陈玉娟,等.雌雄激素与中医阴阳及抑郁障碍的相关性研究[J].陕西中医,2007,28(7):862-864.
[11] 贾悦,孙敏,孙毓桂.雄激素对女性骨质代谢的作用[J].国外医学:计划生育分册,2005,24(6):283-286.
[12] VANDERSCHUEREN D,VANDENPUT L,BOONEN S,et al.Androgens and bone[J].Endocr Rev,2004,25(3):389-425.

