聚合物载药胶束的制剂学性质考察
杨 君,梁慧敏,丁平田,杨跃辉
0 引言
两亲性嵌段共聚物在选择性溶剂中自发形成具有核-壳结构的胶束,其疏水内核可作为难溶性药物存储,能够增大药物溶解度,而亲水外壳则形成胶束聚集体的空间屏障,保证其在水性环境中的稳定性。胶束的上述优点拓展了口服给药新途径。如果能将共聚物胶束制备成口服给药形式,就可以实现在增大药物溶解度的同时提高药物胃肠道内稳定性,从而实现方便给药与提高药物生物利用度的双重目的[1-4]。此外,口服胶束还具有减少药物对胃肠道正常细胞毒性、降低对胃肠道刺激性的优点。
硝苯地平(Nifedipine)是第一代钙拮抗剂,为抗高血压、防治心绞痛的药物,治疗效果显著。硝苯地平属于生物药剂学分类中的第二类药物,生物通透性好,但因溶解性较差(室温下溶解度约为10 μg/mL),生物利用度低,给药物临床应用带来诸多不便。本文以硝苯地平为模型药物,以自制两亲性嵌段共聚物 mPEG-b-PCL为载体,制备单甲基醚聚乙二醇-聚己内酯-硝苯地平(mPEG-b-PCL-nifedipine)口服胶束,并对胶束的外观、形态、粒径、体外释放等制剂学性质进行考察,现报道如下。
1 仪器与试药
1.1 仪器 BS 110 S型分析天平(北京赛多利斯仪器系统有限公司);KQ-50B型超声波清洗器(昆山市超声仪器有限公司);Nicomp-380 粒度测定仪(美国Particle Sizing Systems公司);JEM-I200EX 透射电镜[日本电子公司(JEOL)];透析袋(MWCO=3 500),济南西美贸易有限公司;高效液相色谱仪(日本岛津,SPD-10A VP检测器,LC10-AT VP泵)。
1.2 试药 硝苯地平原料药(自制);mPEG-b-PCL聚合物(自制);甲醇(色谱纯,江苏汉邦科技有限公司);乙腈(色谱纯,山东禹王集团);磷酸二氢钠,二水(分析纯,国药集团化学试剂有限公司);磷酸氢二钠,十二水(分析纯,国药集团化学试剂有限公司);0.05 M磷酸盐缓冲液(氯化钠 8 g,氯化钾0.2 g,磷酸氢二钠1.44 g,磷酸二氢钾0.24 g,调pH 至7.4,并定容至1 L)。
2 聚合物载药胶束的制备
称取一定量的共聚物和药物共溶于两者的良溶剂中,剧烈搅拌下缓慢滴加一定体积重蒸水,搅拌平衡2 h,然后在一定温度下挥发有机溶剂。待有机溶剂完全去除后,0.45 μm微孔滤膜过滤,即得到载药胶束样品。
3 方法与结果
3.1 外观 自制的mPEG45-b-PCL25-nifedipine 与mPEG114-b-PCL61-nifedipine聚合物胶束溶液均为无色澄清透明液体,流动性好,肉眼观察未见不溶性成分或絮状聚集物。加蒸馏水适当稀释后外观仍然无色澄清透明。
3.2 形态观察 采用透射电镜(Transmission electron microscopy,TEM)JEM-1200EX观察聚合物胶束的表面形态。试验采用磷钨酸负染色法制备样品。样品制备方法如下:取自制的胶束溶液适量滴加至覆有碳包衣的400目铜筛网上,加1%磷钨酸负染,在100 kV加速电压下,在透射电镜下观察形态。见图1。由图1可见,自制mPEG45-b-PCL25-nifedipine胶束为外观圆整的球形,粒径<50 nm。
3.3 聚合物胶束粒径 图2为mPEG45-b-PCL25-nifedipine 与mPEG114-b-PCL61-nifedipine聚合物胶束在Nicomp-380 粒度测定仪下测定的粒径与粒度分布图。图中可见,mPEG45-b-PCL25-nifedipine聚合物胶束的粒径在28.4 nm,mPEG114-b-PCL61-nifedipine聚合物胶束的粒径在34.8 nm,两者都有较窄的粒度分布。载药后聚合物胶束的粒径变化不大,该粒径测定结果和透射电镜的测定结果一致。

图1 mPEG45-b-PCL25-nifedipine聚合物胶束(a)、mPEG114-b-PCL61-nifedipine聚合物胶束(b)电镜形态
3.4 聚合物胶束的体外释放特性 聚合物胶束作为新型纳米级药物载体具有十分显著的优越性,能显著提高难溶性药物的溶解度,而聚合物胶束的释药行为,是评价制剂安全性的一项重要指标,药物的释放行为与制剂安全性、有效性密切相关,因此本研究考察了硝苯地平聚合物胶束的体外释放行为。
3.4.1 聚合物胶束释放的液相条件 ①色谱条件(前期试验所建立方法学)色谱柱:Diamonsil C18色谱柱(250 mm×4.6 mm,5μm);流动相:甲醇-水(66∶34,V/V);检测波长:235 nm;流速:1.0 mL/min;柱温:25 ℃;进样量:20 μL。②释放标准曲线的绘制:分别精密量取硝苯地平标准储备液适量,加甲醇逐步稀释分别配置0.2、0.5、1、2、5、10 μg/mL的硝苯地平溶液,HPLC法测定主峰面积,以浓度(C)和峰面积回归得标准曲线:A=26.339 C+0.129 8,r=1(见表1)。③空白干扰试验:精密吸取空白释放介质磷酸盐缓冲液(PBS)20 μL,过滤后进样,检测波长235 nm,考察有无干扰因素。见图3。

图2 mPEG45-b-PCL25-nifedipine聚合物胶束(a)、mPEG114-b-PCL61-nifedipine聚合物胶束(b)粒径

表1 硝苯地平标准曲线相关数据

图3 空白PBS色谱图
在硝苯地平的保留时间7.1 min左右未检测到色谱峰,说明释放介质中无干扰试验测定的因素存在。
3.4.2 释放试验操作 采用透析袋法考察硝苯地平胶束释放情况,即在一定操作条件下,将装有载药胶束的透析袋置于生理介质中进行透析,定时取样测定释放介质中的药物浓度。透析袋的孔径可截留聚合物胶束而允许游离药物自由通过。
精密吸取1.5 mL的载药胶束溶液置于透析袋中,并将透析袋放入50 mL的PBS缓冲液中,然后置于37 ℃的恒温空气浴振荡器中,转速150 rpm。每隔一定的时间,取0.3 mL透析袋外的释放液,过滤后进样20 μL,并同时向释放介质中补充等量新鲜的PBS缓冲液以保持恒定的体积。
3.4.3 累计释放量的计算 药物的累计释放量计算公式如下:
式中Er—— 硝苯地平累计释放量,%;
Ve—— PBS的置换体积,0.3 mL;
V0—— 释放介质PBS的体积,50 mL;
Ci—— 第i次置换取样时释放液中药的浓度,mg/L;
Cn—— 第n次置换取样时释放液中药的浓度,mg/L;
mdrug—— 用于释放的药量,mg。
3.4.4 释放情况考察 聚合物疏水性嵌段的化学组成、亲水链段和疏水链段的比例与分子量、药物的理化性质、胶束粒径大小和环境pH值等均会影响聚合物物胶束的药物释放。试验从聚合物的组成来探讨药物的释放情况。
不同材料制备胶束的药物释放情况有所差别。试验选择温度37 ℃、转速100 rpm、时间24 h,考察自制的mPEG-b-PCL-nfidipine 聚合物胶束在pH=7.4、离子强度0.05 M的磷酸盐缓冲液中的释放情况。见表2。
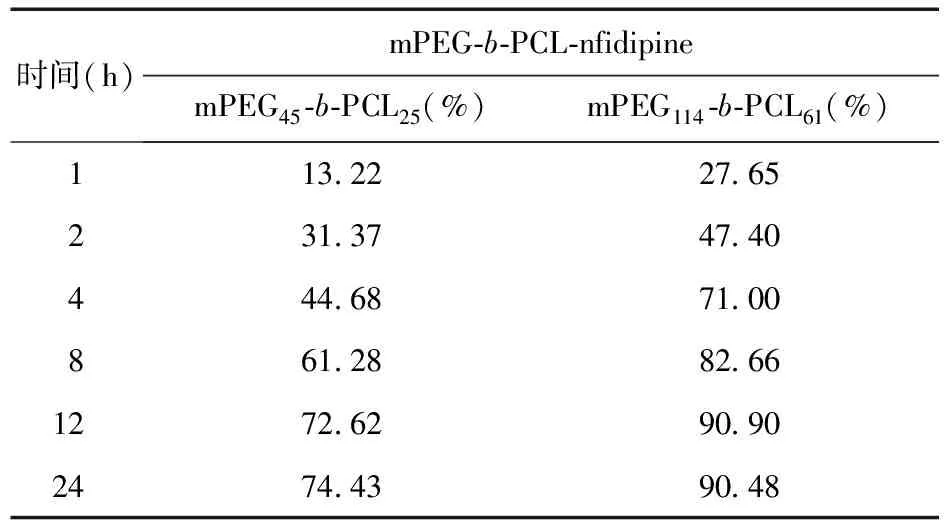
表2 mPEG-b-PCL释放情况(n=3)
结果显示:mPEG45-b-PCL25在 4 h药物累计释放百分率为44.68%,12 h药物累计释放量达到72.62%,此后药物释放极为缓慢,24 h为74.43%,释放不完全;mPEG114-b-PCL61在4 h药物累计释放百分率为71.00%,12 h药物累计释放量达到90.48%。释放速率的先后顺序mPEG114-b-PCL61> mPEG45-b-PCL25。
这2种材料的释放情况说明:当聚合物的种类一定时,疏水链越长,聚合物胶束药物释放越慢。这是由于药物与疏水链段、亲水链段的相互作用参数决定了药物在胶束内的位置,硝苯地平为疏水性药物,大部分定位在胶束的内核,所以疏水链段越长,内核越大,药物释放越慢。此外,从试验结果中还可以看出,24 h内mPEG114-b-PCL61比mPEG45-b-PCL25制备的胶束释放速度较快,且较为完全。
4 讨论
4.1 聚合物胶束常用的体外释药试验有2种,一种是本文采用的透析袋法,另一种是直接将聚合物胶束和生理介质孵化,然后通过凝胶渗透色谱法分离游离药物和包封药物[5-9]。透析袋法由于操作简单,更为常用。在试验过程中,采用MWCO=3 500的透析袋进行透析,在保证药物能自由进出透析袋的同时,有效截留聚合物大分子。
4.2 37 ℃时硝苯地平在水和 0.05、0.1、0.2 M三种不同离子强度磷酸盐缓冲液(pH 7.4)中的溶解度均为11.6 μg/mL,磷酸根离子的加入对药物无增溶作用。为了满足释放漏槽条件,用添加5%SDS的方式来增大药物的溶解度,但是试验考虑到加入表面活性剂后可能会影响胶束的结构。为了更接近体内生理环境,试验采用增大释放介质体积的方式来达到漏槽条件。
5 小结
5.1 本研究利用透射电镜和Nicomp-380 粒度测定仪考察了胶束的外观、粒度分布。结果表明此胶束为澄清透明的液体,粒径20~60 nm,呈圆整球形,粒径分布均匀。
5.2 本研究采用透析袋法考察了体外释放。结果表明药物释放与聚合物的组成有关,当聚合物的种类一定时,疏水链越长,聚合物胶束药物释放越慢。
参考文献:
[1] 赵军.两亲性核交联聚合物胶束的制备与载药应用研究[D].天津:天津科技大学,2009.
[2] 袁建军,程时远,封麟先.嵌段共聚物自组装及其在纳米材料制备中的应用[J].高分子通报,2002,1:6-13.
[3] Bader H,Ringsdorf H,Schmidt B.Water soluble polymers in medicine [J].Die Angewandte Makromolekulare Chemie,1984,123(1):457-485.
[4] George MW,Jhon PM.Molecular self-assembly and nanochemistry:a chemical strategy for the synthesis of nanostruetures[J].Maeromoleeules,1992,254:1312-1318.
[5] Gaucher G,Dufresne MH,Sant VP,et al.Block copolymer micelles:preparation,characterization and application in drug delivery[J].Journal of Controlled Release,2005,109:169-188.
[6] Aguiar J,Carpena P,Molivar JA,et al.On the determination of the critical micelle concentration by the pyrene 1∶3 ratio method [J].Journal of Colloid an Interface Science,2003,258(1):116-122.
[7] Demina T,Grozdova I,Krylova O,et al.,Relationship between the structure of amphiphilic polymers and their ability to disturb lipid bilayers[J].Biochemistry,2005,44:4042-4054.
[8] Yu C,He B,Xiong MH,et al.The effect of hydrophilic and hydrophobic structure of amphiphilic polymeric micelles on their transport in epithelial MDCK cells.[J].Biomaterials,2013,34(26):6284-E298.
[9] Kaihara S,Fisher JP,Matsumura S.Chemo-enzymatic synthesis of degradable PTMC-b-PECA-b-PTMC triblock copolymers and their micelle formation for pH-dependent controlled release.[J].Macromol Biosci,2009,9(6):613-621.

