HPLC-ELSD法同时测定复方三七漱口液中三七皂苷R1、人参皂苷Rg1、Rb1的含量
王 莹,贺文娟,顾 宜,成黎霏,王晓娟
0 引言
复方三七漱口液收载于《中国人民解放军医疗机构制剂规范》2002年版[1]。由三七和醋酸氯己定组成,具有散瘀止血、消肿定痛的功效,用于口腔炎、牙周炎、牙周肿痛、咽喉痛、牙龈出血等常见病的防治。三七中主要含三七皂苷R1、人参皂苷Rb1和人参皂苷Rg1[2],原标准只对三七中人参皂苷Rb1进行了薄层鉴别,未对三七中的专属性成分三七皂苷R1及人参皂苷Rg1进行鉴别和含量测定,不能有效控制该制剂的质量。目前文献报道中关于三七皂苷R1、人参皂苷Rb1和人参皂苷Rg1的测定多采用HPLC-UV法[3-6],亦有采用HPLC-ELSD法[7-9]。因皂苷类成分的紫外吸收均为末端吸收,使用HPLC-UV法时基线易漂移,且灵敏度低,故本试验选用HPLC-ELSD法测定复方三七漱口液中三七皂苷R1、人参皂苷Rb1和人参皂苷Rg1的含量。
1 仪器与试药
1.1 仪器 LC-2010A高效液相色谱仪(日本岛津制作所);DL-720超声仪(浙江石浦海天电子仪器厂);BT125D分析天平(北京赛多利斯科学仪器有限公司)。
1.2 试药 复方三七漱口液(200 mL/瓶,批号:130723、130804、130810,第四军医大学口腔医院药剂科);对照品三七皂苷R1(批号:110745-200617,纯度大于98%),人参皂苷Rg1(批号:110703-201027,纯度为96.3%),人参皂苷Rb1(批号:110704-201223,纯度为95.9%),均购自于中国药品生物制品检定所;乙腈、甲醇[色谱纯,购于霍尼韦尔贸易(上海)有限公司];水为实验室自制超纯水;其他试剂均为分析纯。
2 方法与结果
2.1 薄层鉴别[1-2,11-12]
2.1.1 供试品溶液 取10 mL复方三七漱口液,加10 mL饱和正丁醇萃取3次,合并正丁醇层,加3倍正丁醇饱和的水,放置分层,取正丁醇层,水浴蒸干,加2 mL甲醇溶解,作为供试品溶液。
2.1.2 对照药材溶液 取0.5 g三七粉,加水5滴,再加水饱和的正丁醇5 mL,振摇10 min,放2 h,取上清液,加3倍正丁醇饱和的水,放置分层,取正丁醇层,水浴蒸干,加1 mL甲醇溶解,作为对照药材溶液。
2.1.3 对照品溶液 称取适量三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1,分别制成0.5 mg/mL的溶液,作为对照品溶液。
2.1.4 阴性对照溶液 按处方比例,制成不含三七提取液的阴性药,按“2.1.1”项下制备,作为阴性对照溶液。
2.1.5 薄层展开 照薄层色谱法试验,吸取以上溶液各10 μL,分别点于同一硅胶G薄层板上,以氯仿-甲醇-水(13∶7∶2)置于10 ℃以下,放置12 h,取下层溶液作为层析液,展开,预饱和30 min,展距10 cm,喷以10%硫酸乙醇,105 ℃烘至斑点清晰。供试品色谱中,在与对照药材及对照品色谱相应位置上,显相同颜色的斑点。见图1。
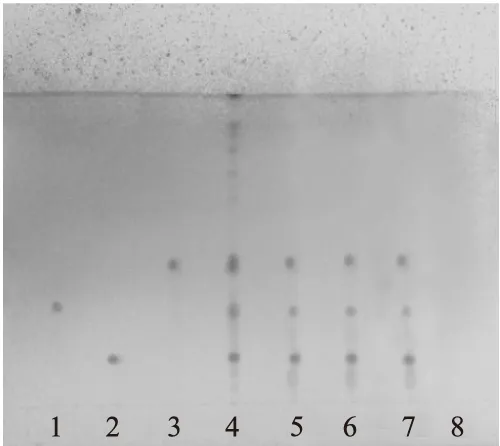
图1 复方三七漱口液薄层色谱图
2.2 含量测定
2.2.1 溶液的配制 a.混合对照品溶液:精密称取适量的三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1,分别制成每1 mL含三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1分别为0.1 mg、0.4 mg和0.4 mg的溶液,即为混合对照品溶液。b.供试品溶液:取本品一瓶超声20 min,精密量取5 mL,加甲醇稀释溶解至10 mL,即得。c.阴性样品溶液:按处方比例,制成不含三七提取液的阴性药,按“供试品溶液”制备,即得。
2.2.2 色谱条件 色谱柱:DIKMA Diamonsil C18(2)(250 mm×4.6 mm,5 μm);流动相:乙腈-水梯度洗脱;流速:1 mL/min;柱温为30 ℃;蒸发光散射检测器漂移管温度47 ℃,载气流速1.5 L/min。梯度洗脱条件见表1。
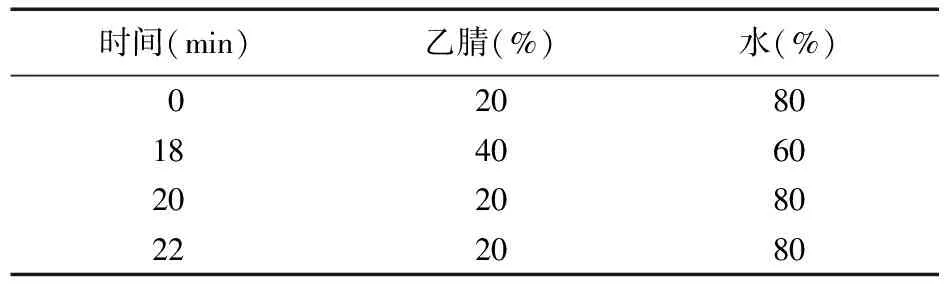
表1 梯度洗脱程序
2.2.3 方法学考察 专属性:分别精密吸取三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1标准溶液、供试品溶液、阴性对照溶液各10 μL,注入高效液相色谱仪,按“2.2.2”项下色谱条件进行测定,记录色谱图,见图2。结果显示,三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1与其他组分峰的分离度均大于1.5,阴性对照溶液在相应保留时间内未出现色谱峰,表明阴性对照溶液无干扰,专属性强。
标准曲线:精密吸取混合对照品溶液4、6、8、10、12、15 μL,注入液相色谱仪,以进样质量的对数为横坐标(X)、峰面积的对数为纵坐标(Y),进行线性回归,结果见表2。
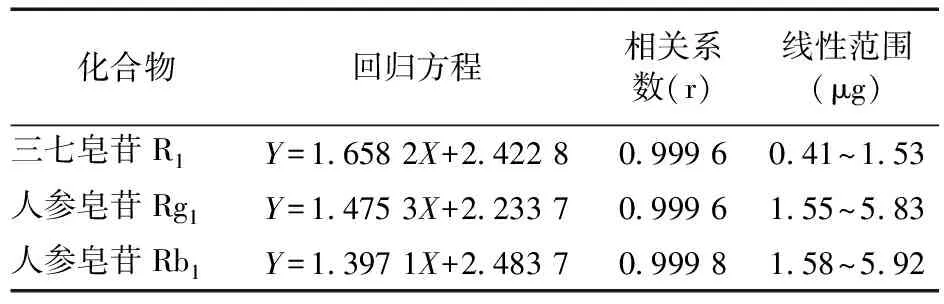
表2 三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的线性关系
稳定性:精密吸取同一供试品溶液10 μL,分别于0、2、4、6、8、12 h按“2.2.2”项下色谱条件进样测定,记录峰面积。结果三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1峰面积的RSD分别为1.96%、1.43%和1.97%,表明供试品溶液在12 h内稳定。
精密度:分别精密吸取三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的混合对照品溶液10 μL,按“2.2.2”项下色谱条件进样测定,连续测定6次。结果三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1峰面积的RSD分别为1.75%、1.83%和1.88%,表明精密度良好。
重复性:取同一批号(130723)的复方三七漱口液,按“2.2.1”项下供试品溶液的制备平行制备供试品6份,按“2.2.2”项下色谱条件进样测定,记录峰面积。结果三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的RSD分别为1.80%、1.77%和2.00%,表明该方法重复性良好。
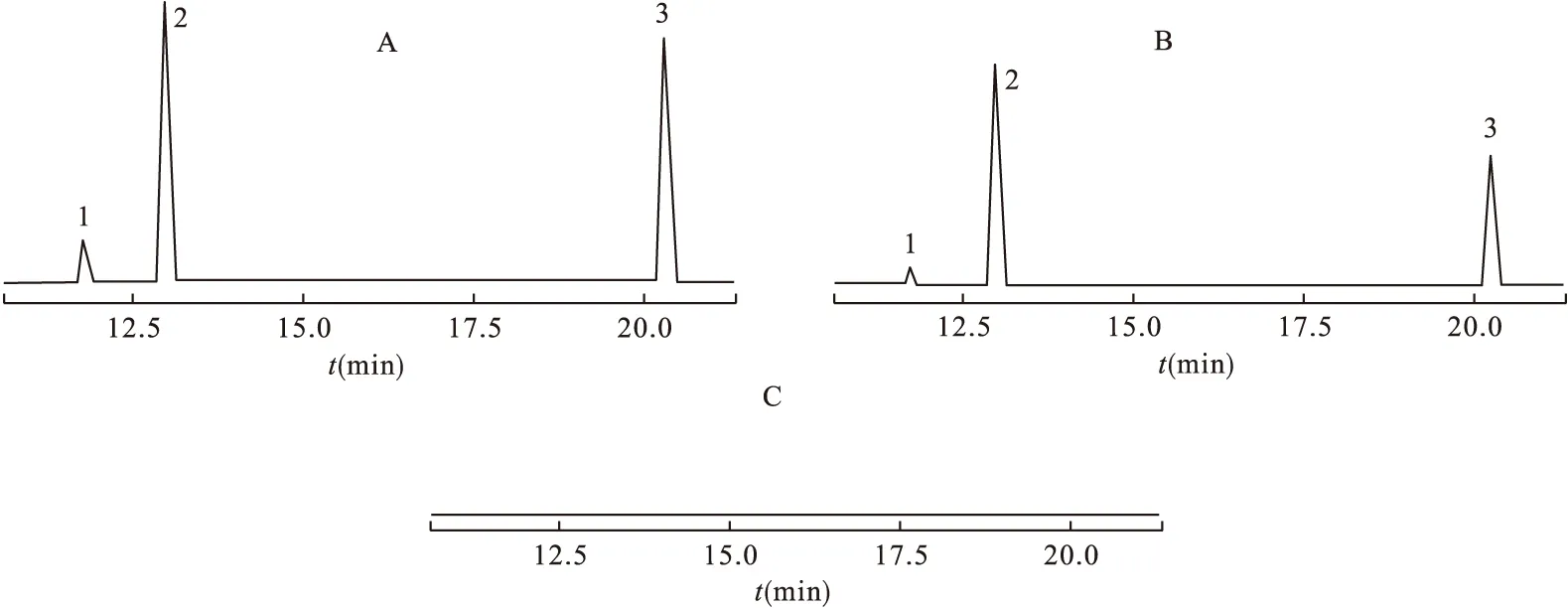
图2 高效液相色谱图
加样回收率:精密量取已知含量的样品(批号:130723,三七皂苷R10.06 mg/mL,人参皂苷Rg10.25 mg/mL,人参皂苷Rb10.20 mg/mL)5 mL,共9份,分别精密加入三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1对照品适量,按“2.2.1”项下供试品溶液的制备制成低、中、高三种浓度,每组3份,按“2.2.2”项下色谱条件进样测定,计算回收率。结果见表3。

表3 加样回收率试验结果(n=9)
2.2.4 样品含量测定 取3个批号(130723、130804、130810)的复方三七漱口液,分别按照“2.2.1”项下供试品溶液的制备方法制成供试品溶液,取供试品溶液和混合对照品溶液适量,按照“2.2.2”项下条件进样,记录峰面积,按照外标两点对数法计算三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1含量,见表4。

表4 样品含量测定结果(mg/mL)
3 讨论
在预试验阶段,参照中国药典2010版一部中三七项下皂苷类化合物的测定方法,采用HPLC-UV法对复方三七漱口液中的三七皂苷R1,人参皂苷Rg1和人参皂苷Rb1进行测定,结果发现基线漂移严重,各指标成分分离较差;而蒸发光散射检测器(ELSD)是一种质量型检测器,其响应与被测物质的质量相关而不依赖于被测物的光学性质,所以在选用ELSD作为检测器进行检测时,基线平稳,色谱峰峰形较好,分离度好。
复方三七漱口液中三七皂苷R1含量较少,参考2010版中国药典中三七药材的处理方法,对复方三七漱口液用饱和正丁醇萃取3次,使三七皂苷R1更多地被提取,使TLC鉴别现象更明显;所建立的HPLC-ELSD法避免了HPLC-UV法基线漂移、分离度差的问题,较其他的HPLC-ELSD法所用分析时间更短[8-10]。通过运用本实验建立的HPLC-ELSD法对三批制剂中三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的含量进行测定,结果表明,该方法简便、稳定、可靠,可更好地控制复方三七漱口液的质量
参考文献:
[1] 中国人民解放军总后勤部卫生部编.中国人民解放军医疗机构制剂规范(2002年版)[S].北京:人民军医出版社,2003:281-282.
[2] 国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2010:11-12.
[3] 叶厚春,李爱伟.RP-HPLC法同时测定定风止痛片中三七皂苷R1、人参皂苷Rg1、Rb1的含量[J].亚太传统医药,2013,9(4):42-44.
[4] 杨学芳,苏万福,唐晓霞,等.RP-HPLC测定药流净颗粒中三七皂苷R1与人参皂苷Rg1、Rb1的含量[J].中国民族民间医药,2013,22(9):17-18.
[5] 孙小玲.HPLC梯度法测定复方三七维康胶囊中三七皂苷R1、人参皂苷Rb1、Rg1的含量[J].中国药师,2013,16(3):349-351.
[6] 钱鑫,徐飞.HPLC法测定云南白药胶囊中三七皂苷R1和人参皂苷Rg1的含量[J].西北药学杂志,2013,28(3):263-265.
[7] 吴笛,叶秋雄,王德勤,等.HPLC-ELSD法同时测定复方丹参片中4种皂苷的含量[J].世界中医药,2013,8(2):201-204.
[8] 唐露,李希,冯建安.HPLC-ELSD法测定舒络颗粒中黄芪甲苷、三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的含量[J].实用中医药杂志,2012,28(11):964-967.
[9] 郑义,陈晓兰,丁宁.HPLC-ELSD法测定三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的含量[J].江苏农业科学,2013,41(5):297-298.
[10]徐鹏,冯素香,赵迪,等.HPLC-ELSD法测定血塞通注射液中三七皂苷R1、人参皂苷Rg1、Re、Rb1、Rd [J].中成药,2013,35(3):521-524.
[11]李霄,万丹丹,郭洛红.薄层色谱法对复方丹参片中三七皂苷R1和人参皂苷Re的鉴别[J].中成药,2009,31(9):1470-1472.
[12]李顺龙,郭建明.复方血栓通滴丸的TLC鉴别[J].中国药师,2008,11(8):925-926.

