快堆MOX燃料氧与金属原子比控制原理
屈哲昊,尹邦跃,杨启法,梁雪元
(1.中国原子能科学研究院 反应堆工程研究设计所,北京 102413;
2.核工业标准化研究所,北京 100091)
氧与金属原子比(O/M比,余同)指MOX燃料即(U1-yPuy)O2±x混合氧化物燃料晶格中氧原子与金属原子个数的比值,即O/M比=2±x。O/M比是MOX燃料最重要的性能指标之一,对MOX燃料的熔点、晶格常数、理论密度、热物性、扩散系数、氧在燃料中的化学位即氧势以及堆内辐照性能均有很大影响。而PuO2含量、Pu分布均匀性、烧结温度、烧结气氛氧分压、粘接剂种类和添加量、批次质量等因素均对O/M比有影响。Toci等[1]指出,富钚颗粒的氧势一般要高于钚均匀分布的MOX固溶体的氧势。中国实验快堆MOX燃料的PuO2质量分数为25%,O/M比为1.96~1.99,如何从理论计算和工艺控制方面达到所要求的O/M比是一个重要的研究课题。
国外从20世纪50年代开始研究核燃料的氧势和O/M比,现已得到数千个数据,但这些数据通常是在有限的“氧势-温度-成分”范围内重复进行,由于实验测量条件不同,数据分散性较大。各国也提出了很多氧势理论模型,但由于采用不同的离子平衡假设和不同的热力学数据,计算结果与实验数据存在较大差异,至今没有一个普遍公认的氧势模型[2-7]。根据经验,在MOX燃料芯块生产过程中,一般通过控制烧结气氛的氧分压即气体氧势来调整固体芯块的氧势和O/M比。显然,了解MOX燃料的O/M比控制原理将有利于优化MOX燃料芯块的烧结工艺参数,本文将进行MOX燃料的O/M比控制原理的研究。
1 氧势模型
氧化物陶瓷芯块在保温烧结过程中,固体芯块内的氧势与烧结气氛的氧势存在平衡,根据热力学定律,氧化学位为:
(1)


(2)

MOX芯块的O/M比是固体内的化学位即氧势、温度和Pu含量的函数,为建立O/M比与MOX燃料芯块烧结工艺(烧结温度、氧分压和PuO2含量)之间的关系,需通过热力学参数或离子反应平衡常数精确计算氧势,并建立O/M比与氧势之间的关系式。国外早在20世纪50年代就已开始进行核燃料的氧势研究,从晶体结构缺陷、热力学行为角度出发,发展了燃料的多种氧势热力学理论和数学模型[8]。公认的氧势模型主要有Rand-Markin模型、Blackburn模型、相平衡模型、点缺陷模型。这些理论模型采用了一些假设和有差异的热力学数据,测量数据由于原理或技术的原因存在误差,使氧势模型的应用有限。
1) Rand-Markin价态模型
Rand-Markin模型是基于实验结果的经验模型,它把MOX视为UO2+x与PuO2-x形成的理想固溶体(U1-yPuy)O2±x。该模型假设:当MOX芯块为超化学计量时,即(U1-yPuy)-O2+x的O/M比大于2.00时,氧势为铀平均价态的函数;当其为亚化学计量时,即(U1-yPuy)-O2-x的O/M比小于2.00时,氧势为钚平均价态的函数,且不受温度和Pu/U比的影响[9]。
对于亚化学计量(U1-yPuy)O2-x而言,U离子的价态VU是+4,但Pu离子的平均价态VPu不是整数。
VPu=4-2x/y
(3)
对于超化学计量(U1-yPuy)O2+x而言,Pu离子的价态为+4,但U离子的平均价态不是整数:
VU=4+2x/(1-y)
(4)

2) Blackburn离子平衡模型
Blackburn模型[12]可认为是半经验性模型,它认为MOX固溶体中存在确定的U、Pu离子价态,各价态离子相互平衡,构成一系列平衡方程。MOX燃料通常在强还原性气氛中进行烧结,离子平衡反应要考虑U2+-U4+、U4+-U6+、Pu3+-Pu4+、Pu2+-Pu3+等反应体系,其对应的反应平衡常数分别为:
(5)
(6)
(7)
(8)
式中,[U2+]、[U4+]、[U6+]、[Pu2+]、[Pu3+]、[Pu4+]、[O2-]分别为U2+、U4+、U6+、Pu2+、Pu3+、Pu4+、O2-的浓度,余同。
对于确定成分与O/M比的(U1-yPuy)O2±x燃料,x和y是已知量,有:
[U2+]+[U4+]+[U6+]=1-y
(9)
[Pu2+]+[Pu3+]+[Pu4+]=y
(10)
2[U2+]+4[U4+]+6[U6+]+2[Pu2+]+
3[Pu3+]+4[Pu4+]=2±x=2[O2-]
(11)
当反应平衡常数已知,联立解上述7个公式即可求得pO2;或当pO2和y已知,同样可根据式(5)~(8)求解x,从而得到混合氧化物燃料的O/M比。图1为利用Blackburn模型计算得到的MOX燃料氧势与O/M比的关系[13]。
Blackburn模型计算过程较简单,方法易掌握,计算量少,精确度受反应平衡常数的影响较大。Blackburn发布模型时,利用相图中UO2/U4O9、UO2-x/U(l)平衡数据分别计算得到了KU24、KU46。也可利用已知的pO2、x、y等数据,拟合得到平衡常数。受Stan等[11,14]的启发,若结合量子力学理论与分子动力学计算技术进行反应平衡常数的理论估算,再利用实验数据进行修正,可得到更准确的反应平衡常数,从而提高Blackburn模型的计算准确度。

图1 Blackburn模型计算得到的MOX燃料的氧势与O/M比的关系[13]
3) 相平衡模型
相平衡模型假定MOX燃料中U4O9与UO2、Pu2O3与PuO2之间存在相互平衡,且U4O9、Pu2O3这两种含非化学计量缺陷的化合物可对应地溶解于无缺陷的化学计量比化合物UO2、PuO2中。
8UO2+O2(g)=2U4O9
2Pu2O3+O2(g)=4PuO2
形成(U1-yPuy)Ox固溶体的标准吉布斯自由能为:
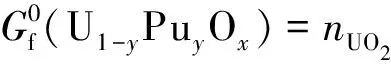


(12)

相平衡模型是Hoch等[15]在锕系氧化物中采用的模型,Besmann等[16-17]和Krishnaiah[18]将其应用于MOX燃料。目前很少采用该方法计算MOX燃料的氧势,仅Varamban等[19]利用此方法预测MOX燃料的氧势。
4) 点缺陷模型
由于非化学计量化学物中必然存在间隙离子、空位、自由电子、电子空隙等结构缺陷,它们之间也会构成平衡,因此点缺陷模型认为可通过计算缺陷平衡反应来得到固溶体的氧势。
MOX燃料可能存在以下缺陷反应(使用Kroger-Vink符号表示缺陷):







假设上述6个反应平衡常数已知,则可通过计算MOX固溶体的氧空位与氧间隙原子浓度计算O/M比:

(13)
利用点缺陷模型求解MOX燃料氧势的计算结果与实验结果符合较好,此方法被Kato等[20-21]广泛应用于MOX燃料和嬗变燃料的研究中。但目前尚无文献报道如何通过理论计算得到平衡常数。Kato等[22]利用实际测量的氧势拟合计算得到U0.8Pu0.2O2±x的各平衡常数如下:

(14)

(15)

(16)

(17)

(18)

(19)
Blackburn模型和点缺陷模型是目前应用最多的两种理论模型,并已积累了大量实验数据。利用国外现有离子反应平衡常数和热力学数据,采用Blackburn模型可精确研究MOX燃料的氧势,但目前这些数据较少,今后应开展更为精确的点缺陷模型计算研究。
2 MOX燃料O/M比控制工艺计算
2.1 氧分压计算
为使MOX燃料的O/M比达到指标设计要求,要根据氧势模型计算出氧势的控制范围,再根据氧势精确计算结果计算在某烧结温度下的氧分压,最后根据氧分压控制气体露点。
假设快堆MOX燃料芯块的设计成分分别为(U0.7Pu0.3)O2-x、(U0.75Pu0.25)O2-x、(U0.8Pu0.2)O2-x,分别利用Blackburn模型和点缺陷模型计算得到不同O/M比对应的氧分压,结果分别列于表1和2。采用Blackburn模型进行计算,对于(U0.7Pu0.3)O2-x燃料,当设计O/M比为1.97时,若在1 700 ℃、Ar-5%H2气中烧结,则要求将氧分压控制为7.70×10-6Pa,或将氧势控制为-381.98 kJ/mol。对于(U0.75Pu0.25)O2-x燃料,当设计O/M比为1.97时,若在1 700 ℃、Ar-5%H2气中烧结,则要求将氧分压控制为3.05×10-6Pa,或将氧势控制为-397.18 kJ/mol。可见,要达到相同的亚化学计量O/M比,PuO2含量高则对烧结气氛的氧分压控制要求可适当放松。
采用点缺陷模型计算得到了MOX燃料的烧结气氛氧分压,对于(U0.7Pu0.3)O2-x燃料,当设计O/M比为1.97时,如果在1 700 ℃、Ar-5%H2气中烧结,则要求将氧分压控制在3.52×10-6Pa(而Blackburn模型计算值为7.70×10-6Pa),或将氧势控制在-394.87 kJ/mol。对于(U0.75Pu0.25)O2-x燃料,当设计O/M比为1.97时,如果在1 700 ℃、Ar-5%H2气中烧结,则要求将氧分压控制在1.23×10-6Pa(而Blackburn模型计算值为3.05×10-6Pa),或将氧势控制在-412.11 kJ/mol。

表1 Blackburn模型计算得到的烧结气氛的氧分压和氧势

表2 点缺陷模型计算得到的烧结气氛的氧分压和氧势

续表2
比较Blackburn模型与点缺陷模型的计算结果可发现,两种模型的计算结果变化规律基本一致(图2),但Blackburn模型的氧势和氧分压随O/M比增大而增大的速度较快。图2显示,当O/M比≤1.96时,Blackburn模型的氧势和氧分压计算结果均相应地低于点缺陷模型的;而当O/M比>1.96时,Blackburn模型的氧势和氧分压计算结果均相应地高于点缺陷模型的。今后应根据自有实验数据选择合适模型以用于理论预测我国MOX芯块烧结气氛氧分压。由于目前文献报道的点缺陷模型平衡常数有限,尽管国外研究者认为其与实验符合较好,但在本文后续计算中仍选用Blackburn模型计算数据。

图2 Blackburn模型与点缺陷模型计算结果的比较
2.2 露点计算
如果烧结气氛中存在水,存在2H2+O2→2H2O反应,则:
(20)
式中:p为各气态物质的分压;Keq为该反应平衡常数,有:
(21)
ΔG0=ΔH0-TΔS0=-492 880+109.6T
(22)
pH2/pH2O=
(23)
根据Blackburn模型计算结果,以(U0.75-Pu0.25)O1.97为例进行计算分析,1 700 ℃烧结时要求将氧分压控制在3.05×10-6Pa,于是计算得到:
pH2/pH2O=

若pH2=0.1 MPa,则pH2O=2 529.08 Pa。实际MOX芯块烧结气氛为Ar-5%H2混合气体,若混合气体的压力为0.1 MPa,pH2=5 kPa,则pH2O=126.45 Pa,即混合气体中的水分含量应控制为1 264.5 ppm。
通过冷凝器冰浴[23]可调节气体pH2/pH2O,对于冰面体系,饱和水蒸气压与温度的关系可通过以下方程计算:
lnpH2O=-6 024.528 2T-1+29.327 07+
1.061 386 8×10-2T-1.319 882 5×
10-5T2-0.493 825 77lnT
(24)
通过式(23)计算得到pH2O后,求解式(24)即可得到冷凝器的工作温度即露点T为291.58 K(18.58 ℃)。可见,将露点为18.58 ℃的0.1 MPa纯H2气或水分含量为1 264.5 ppm、露点为255.28 K(-17.72 ℃)的0.1 MPa Ar-5%H2混合气通过冷凝器冰浴脱水后,再通入烧结炉内在1 700 ℃烧结,理论上可得到成分为(U0.75Pu0.25)O1.97的MOX芯块。若烧结温度提高至1 750 ℃,要使(U0.75Pu0.25)O2-x的O/M比控制在1.97,则要求将0.1 MPa Ar-5%H2气体的水分含量控制在1 633.7 ppm、露点控制在258.02 K(-14.98 ℃)。
采用上述同样方法可计算得到1 750 ℃烧结具有不同成分和O/M比的(U0.75Pu0.25)O1.95、(U0.75Pu0.25)O1.96、(U0.75Pu0.25)O1.98、(U0.75Pu0.25)-O1.99、(U0.75Pu0.25)O1.995芯块时,必须将0.1 MPa Ar-5%H2气体的水分含量分别控制在370.4、739.8、4 403.6、17 855.4、43 064.8 ppm,露点分别控制在-30.10、-23.27、-3.77、13.83、26.16 ℃(图3)。其他成分MOX燃料的烧结气体水分含量和露点计算结果列于表3。

表3 MOX芯块烧结气氛中水分含量及露点

图3 (U0.75Pu0.25)O2-x的O/M比与烧结气体水分含量和露点的关系

图4 氧势、烧结温度、气体水分含量和露点对(U0.8Pu0.2)O2-x燃料O/M比的影响[24]
图4所示为美国阿贡国家实验室的(U0.8Pu0.2)O2-x燃料的O/M比与氧势、温度和气体露点的关系[24]。可见,若要求O/M=1.97,在1 700 ℃烧结时气体的氧势应控制在约-420 kJ/mol,较本文计算的氧势偏低(Blackburn模型计算的氧势为-397.18 kJ/mol,点缺陷模型的为-412.11 kJ/mol),露点约为-20 ℃。本文计算得到(U0.8Pu0.2)O1.97燃料在1 700 ℃烧结时,要求控制气体水分含量为690.2 ppm、露点为-23.98 ℃;在1 750 ℃烧结时,要求控制气体水分含量为893.4 ppm、露点为-21.35 ℃,这与文献[24]的结论基本一致。俄罗斯专家指出快堆MOX芯块在1 750 ℃、Ar-8%H2气中烧结,当H2气中H2O含量分别为0.03%、0.3%时,即气体露点分别为-40、-16 ℃时,对应O/M比可分别达到1.95、1.98,但其MOX燃料的PuO2含量未知。本文计算得到(U0.75Pu0.25)O1.95、(U0.75Pu0.25)O1.98燃料分别在1 750 ℃、Ar-8%H2气中烧结时,要求控制气体露点分别为-32.34、-6.5 ℃,比俄罗斯专家提出的露点均高约8 ℃。
3 结论
1) Blackburn模型和点缺陷模型是两种常用的核燃料氧势模型,离子反应平衡常数和热力学数据是影响氧势模型精确度的主要因素。采用精确的平衡常数和热力学数据,以及大量实测数据对氧势模型进行修正,可提高氧势计算和O/M比预测的精确度。
2) 在PuO2含量和烧结温度一定的情况下,MOX芯块的O/M比可通过控制气相中氧分压或露点来调整。将保护气体通过冷凝器冰浴脱水后再进入烧结炉内,可定量调节气体氧势和精确控制芯块的O/M比。
3) 当要求(U0.75Pu0.25)O2-x燃料的O/M比为1.97时,若在1 750 ℃、0.1 MPa Ar-5%H2气中烧结,采用Blackburn模型进行计算,则理论上要求将氧分压控制在1.07×10-5Pa,或将氧势控制在-386.15 kJ/mol。采用点缺陷模型计算,要求将氧分压控制在0.7×10-5Pa,或将氧势控制在-393.22 kJ/mol。
4) (U0.75Pu0.25)O2-x燃料在1 750 ℃、0.1 MPa Ar-5%H2气中烧结,当要求O/M比分别为1.95、1.96、1.97、1.98、1.99、1.995时,理论上应将气体中的水分含量分别控制在370.4、739.8、16 33.7、4 403.6、17 855.4、43 064.8 ppm,或将气体露点分别控制在-30.10、-23.27、-14.98、-3.77、13.83、26.16 ℃。
参考文献:
[1] TOCI F, MANES L, EWART F T, et al. On the determination of oxygen potentials and O/M ratios in mixed U-Pu oxides by means of solid state galvanic cells[J]. Journal of Applied Electrochemistry, 1979, 9(3): 399-401.
[2] KUTTY T R G, HEGDE P V, KAHN K B, et al. Densification behavior of UO2in six different atmospheres[J]. Journal of Nuclear Materials, 2002, 305(2-3): 159-168.
[3] LAY K W, CARTER B E. Role of the O/U ratio on the sintering of UO2[J]. Journal of Nuclear Materials, 1969, 30(1-2): 74-87.
[4] HARADA Y. UO2sintering in controlled oxygen atmospheres of three-stage process[J]. Journal of Nuclear Materials, 1997, 245(2-3): 217-223.
[5] CHEVREL H, DEHAUDT P, FRANCOIS B, et al. Influence of surface phenomena during sintering of over stoichiometric uranium dioxide UO2+x[J]. Journal of Nuclear Materials, 1992, 189(2): 175-182.
[6] ASSMANN H, DOERR W, PEEHS M. Oxide fuels with controlled microstructure[J]. Journal of the American Ceramic Society, 1984, 67(9): 631-636.
[7] FUHRMAN N, HOWER L D, HOLDEN R B. Low-temperature sintering of uranium dioxide[J]. Journal of the American Ceramic Society, 1963, 46(3): 114-121.
[8] 唐纳德·奥兰德. 核反应堆燃料元件基本问题[M]. 北京:原子能出版社,1983:231.
[9] RAND M H, MARKIN T L. Some thermodynamic aspects of (U, Pu)O2solid solutions and their use as nuclear fuels[C]∥Thermodynamics of Nuclear Materials 1967 Symposium Proceedings. Vienna: [s. n.], 1968: 637-650.
[10] FUJINO T, SATO N, YAMADA K. A refined analysis of oxygen potential of MyU1-yO2+x(M=M3+and M2+) by lattice statistics based on the grand partition function and the Flory methods[J]. Journal of Nuclear Materials, 1995, 223(1): 6-19.
[11] STAN M, CRISTEA P, Sr WALLACE T C. Thermochemistry of defects and oxygen diffusion in PuO2-x[C]∥Proceedings of 11th Symposium on Thermodynamics of Nuclear Materials. Karlsruhe, Germany: [s. n.], 2004.
[12] BLACKBURN P E, JOHNSON C E. Oxygen pressures over fast breeder reactor fuel (Ⅰ): A model for UO2±x[J]. Journal of Nuclear Materials, 1973, 46(3): 244-252.
[13] 梁雪元. MOX燃料混合工艺及热力学分析[D]. 北京:中国原子能科学研究院,2006.
[14] STAN M. Theory-based models and simulations of materials for fusion[C]∥Fusion Power Renew Workshop. US: University of California, 2009.
[15] HOCH M, FURMAN F J. Non-stoichiometry of UO2-CeO2: The system UO2-CeO2-CeO1.5at 900 to 1 200 ℃[C]∥Thermodynamics Proceedings of the Symposiumn on Thermodynamics With Emphasis on Nuclear Materials and Atomic Transport in Solids. Vienna: IAEA, 1966: 517-532.
[16] BESMANN T M, LINDEMER T B. Chemical thermodynamic representation of UO2±x[C]∥ Proceedings of Conference on Thermodynamics. Hamilton, Canada: [s. n.], 1984.
[17] BESMANN T M, LINDEMER T B. Chemical thermodynamic representation of PuO2-xand U1-zPuzOw[C]∥ Proceedings of Conference on Chemical Thermodynamics and 39 Calorimetry Conference. Hamilton, Canada: [s. n.], 1984.
[18] KRISHINAIAH M V, SRIRAMAMURTI P. Computational model for the oxygen potentials of mixed uranium-plutonium oxide[J]. Journal of the American Ceramic Society, 1984, 67(8): 568-571.
[19] VANA VARAMBAN S, GANESAN V, VASUDEVA RAO P R. Estimation of oxygen potential for U-Pu-O mixed oxide fuel[J]. Journal of Nuclear Materials, 2009, 389(1): 72-77.
[20] KATO M, NAKAMICHI S, TAKEUCHI K, et al. Measurement of oxygen potential of (U0.8-Pu0.2)O2±xat 1 773 and 1 873 K, and its analysis based on point defect chemistry[J]. CALPHAD, 2011, 35(4): 623-626.
[21] KATO M, KONASHI K, NAKAE N. Analysis of oxygen potential of (U0.7Pu0.3)O2±xand (U0.8-Pu0.2)O2±xbased on point defect chemistry[J]. Journal of Nuclear Materials, 2009, 389(1): 164-169.
[22] KATO M. Oxygen potentials and defect chemistry in nonstoichiometric (U, Pu)O2[R]∥Stoichiometry and Materials Science: When Numbers Matter. [S. l.]: [s. n.], 2012: 203-218.
[23] RASMUSSEN D E, BENECKE M W, JENTZEN W R, et al. Oxygen to metal ratio control during fabrication of mixed oxide fast breeder reactor fuel pellets, HEDL-SA-1763FP[R]. Atlanta: Hanford Engineering Development Laboratory, 1979.
[24] JAVED N A. Thermodynamic behavior of (U, Pu) mixed-oxide fuels[J]. Journal of Nuclear Materials, 1973, 47(3): 336-344.

