浊点萃取-紫外分光光度法同时测定厚朴酚与和厚朴酚的含量
刘超美, 仲淑贤, 杨利宁,邬梦璐, 叶建萍, 陈建荣,
(1.浙江师范大学 化学与生命科学学院,浙江 金华 321004;2.浙江师范大学 地理与环境科学学院,浙江 金华 321004)
厚朴酚与和厚朴酚互为同分异构体,是我国传统中药厚朴的主要活性成分,广泛用于临床治疗,具有抗炎、抗菌、抗肿瘤、抑制血小板聚集等药理作用[1].因此,建立一种灵敏简便的分析方法用于活性成分的质量控制非常有必要.目前,用于定量测定厚朴酚与和厚朴酚含量的方法有高效液相色谱法、毛细管电泳法、气相色谱法、薄层扫描法和紫外分光光度法等[2-5].
浊点萃取技术(CPE)是近年来出现的一种液-液萃取新技术,它是一种利用表面活性剂的增溶和浊点现象,将体系分为两相,使目标物进入表面活性剂富集相,从而进行分离与浓缩的萃取技术.该技术具有绿色环保、操作简便等优点.浊点萃取技术已成功用于金属离子和有机物的测定[6-10].本文以Triton X-114为表面活性剂,将体系分为上层水相和下层表面活性剂富集相,采用浊点萃取-紫外分光光度法联用技术,成功实现了对药材中厚朴酚与和厚朴酚含量的测定.
1 实验部分
1.1 仪器
Lambda 25紫外分光光度计(美国Perkin Elmer公司),PDC-2010低温恒温槽(宁波莱福科技有限公司),PP-50型精密pH计(德国赛多利斯科学仪器有限公司),DK-8D型电热恒温水槽(上海一恒科技有限公司),Hettich Rotanto460型高速离心机(德国),AL204型电子分析天平(梅特勒-托利多仪器(上海)有限公司),Milli-Q 超纯水系统(Millipore公司).
1.2 试剂
厚朴酚与和厚朴酚的标准品(阿拉丁试剂有限公司,AR,纯度>99.7%):取0.20 g标准品于100 mL容量瓶中,用甲醇稀释至刻度,即得2 g/L的标准品储备液,临用时用甲醇稀释至所需的浓度.配制不同pH值的B-R(Britton-Robinson)缓冲溶液及其他缓冲溶液所需要的KH2PO4,NH4Cl,NaOH,Na2B4O7·10H2O等试剂均为分析纯试剂.所有标准溶液在黑暗处4 ℃保存.
非离子型表面活性剂Triton X-114(Sigma-Aldrich,Germany):称取25 g于500 mL容量瓶中,用二次水配制成50 g/L的Triton X-114溶液.
1.3 实验过程
1.3.1 浊点萃取过程
准确移取2.50 mL厚朴酚(10 mg/L)标准溶液与1.25 mL和厚朴酚(10 mg/L)标准溶液于50.0 mL
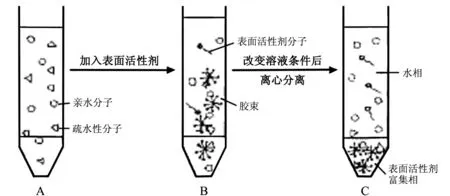
A:含有萃取物的初始溶液;B:加入表面活性剂后萃取物与胶束结合;C:发生浊点相分离,离心后萃取物富集在胶束相图1 浊点萃取过程
离心管中,分别加入0.6 mL 5%的Triton X-114溶液,用5 mL B-R缓冲溶液调节pH值为6,用二次水定容至50 mL,充分振荡混匀后,置于45 ℃恒温水浴中平衡15 min.为促进两相快速分离,以4 000 r/min离心 10 min,离心后表面活性剂相在下层,冰水浴冷冻后弃去上层液,试管底部得到300 μL表面活性剂富集相(见图1).
1.3.2 检测方法
单组分的检测:按照上述方法进行浊点萃取,得到表面活性剂富集相,用甲醇稀释到1.0 mL,在最大吸收波长290 nm处测定厚朴酚与和厚朴酚的吸光度.
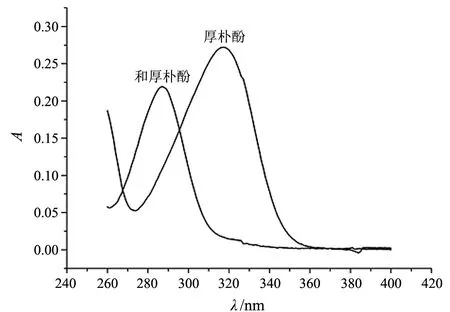
图2 厚朴酚与和厚朴酚的最大吸收峰
混合样的同时测定:按照上述方法萃取到的表面活性剂富集相用甲醇稀释至1 mL,再加入pH=9的KH2PO4-NaOH缓冲溶液1 mL,然后移入1 mL微量比色皿中,测定在290 nm和320 nm处样品的吸光度,分别记作A290和A320,未加厚朴酚与和厚朴酚的空白溶液作为对照.
1.3.3 测定原理
在中性溶液中,厚朴酚与和厚朴酚的最大吸收波长几乎重叠.利用两者羟基质子离解性的差异,在它们的混合液中加入缓冲溶液,厚朴酚解离而和厚朴酚不解离,使厚朴酚的最大吸收峰红移,这样两者的吸收峰不再重叠.吸收波长的选择如图2所示.根据吸光度的加和性,可以计算出厚朴酚与和厚朴酚的含量.
A320(总)=ε320(厚朴酚)·C(厚朴酚)+ε320(和厚朴酚)·C(和厚朴酚);
A290(总)=ε290(厚朴酚)·C(厚朴酚)+ε290(和厚朴酚)·C(和厚朴酚).
2 结果与讨论
2.1 浊点萃取条件的选择
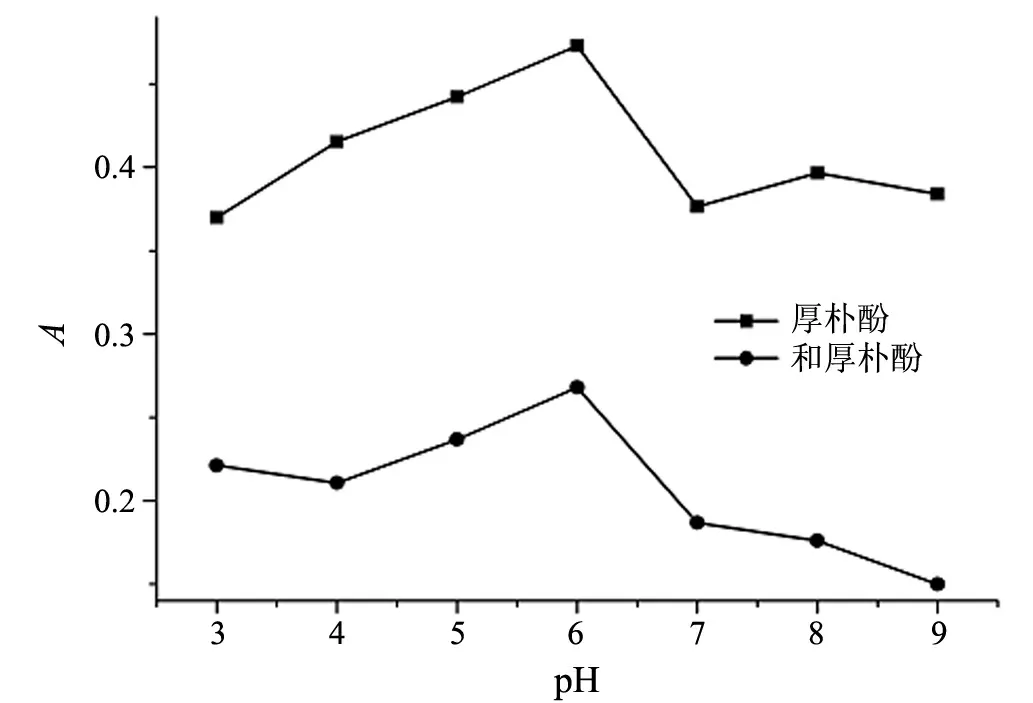
图3 pH对浊点萃取的影响
2.1.1pH对萃取效率的影响
萃取效率取决于待测化合物的性质和表面活性剂的性质.厚朴酚与和厚朴酚均是弱酸性化合物,厚朴酚的解离常数pKa1和pKa2分别是7.54和14.38[11],溶液pH影响着分析物的存在形式.浊点萃取的其他条件如上所述,为了提高萃取效率,考察了pH 3~10范围内溶液的酸度对待测物萃取效果的影响.图3表明,在pH值为6时目标物的萃取量最大.因此,选择萃取体系的最佳pH值为6.
2.1.2 Triton X-114浓度的影响
Triton X-114具有较低的浊点温度(23~26 ℃)和较高的密度,可有助于相分离,在浊点萃取技术中常用作萃取剂.同时,Triton X-114的用量会影响富集相的体积,从而影响萃取率.在保证完全萃取的前提下,应减小表面活性剂的体积以提高相比.本实验研究了0.03%~0.09%的Triton X-114溶液对萃取的影响.从图4可知,选择体积分数为0.06%的Triton X-114溶液可以达到最高的萃取效率.
2.1.3 水浴温度和平衡时间的影响
平衡温度高于表面活性剂的浊点温度时才会引发相分离,提高温度,缩短萃取时间,对浊点萃取起着至关重要的作用.本实验考察了25~60 ℃范围内温度对萃取率的影响.图5中达到最高萃取率的温度为45 ℃.
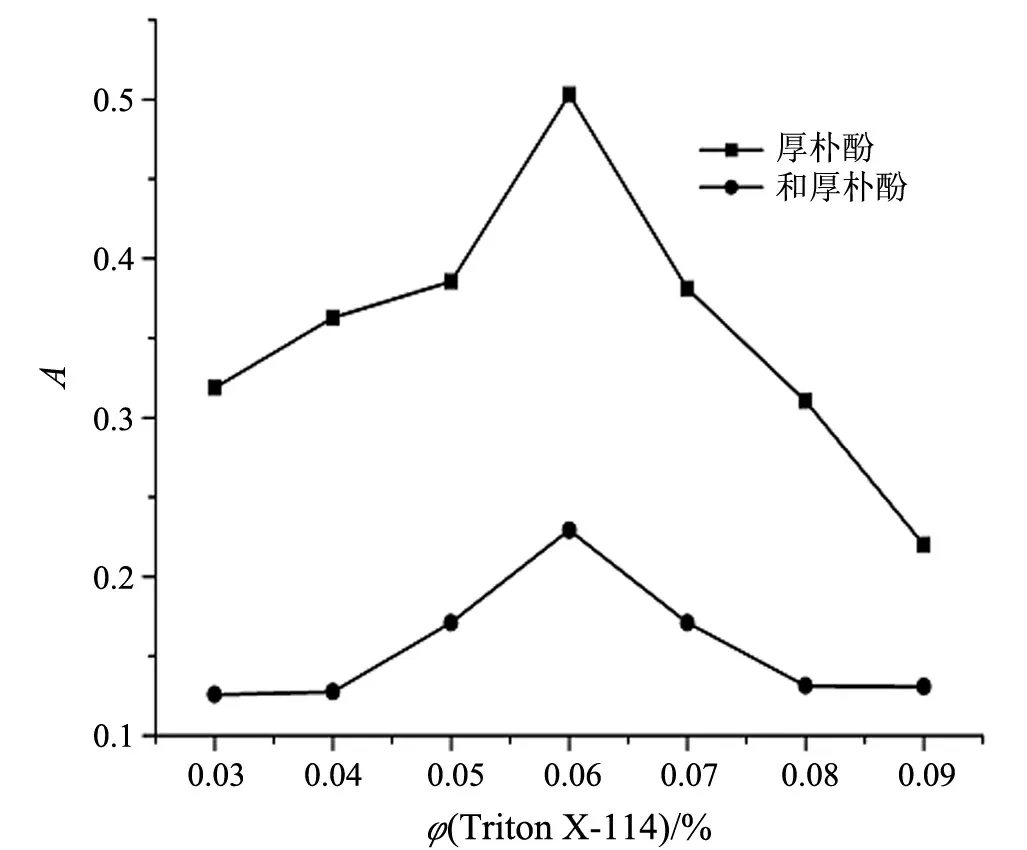
图4 Triton X-114浓度对浊点萃取的影响
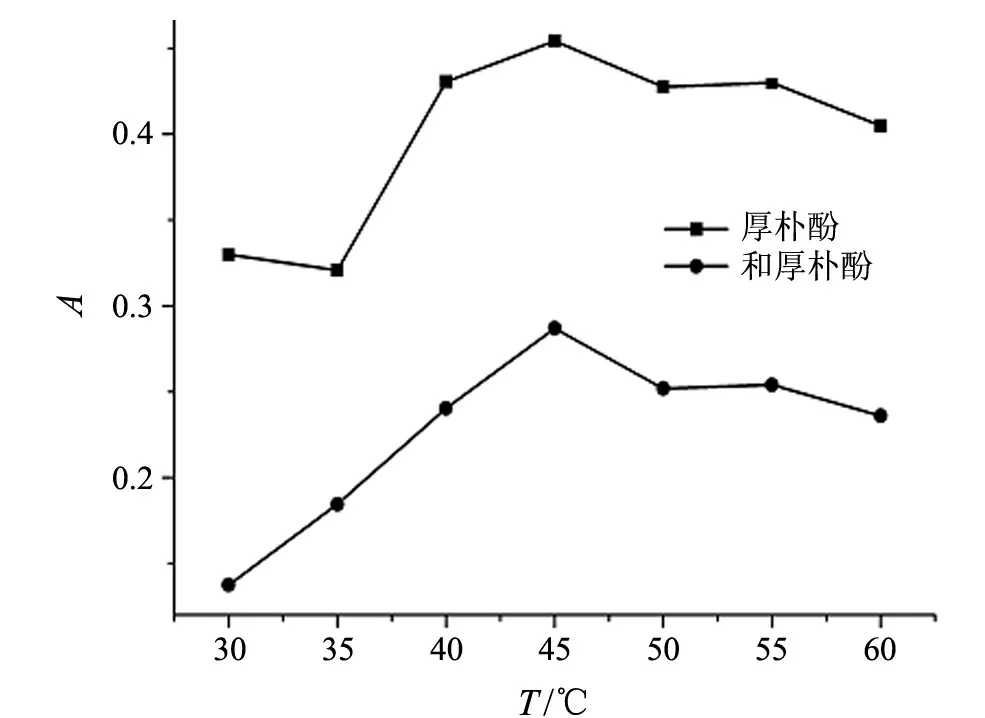
图5 平衡温度对浊点萃取的影响
平衡时间的延长有利于增加分配比,但同时会影响实验周期.本实验研究了5~35 min的平衡时间对萃取率的影响,最终选择15 min作为平衡时间.
2.2 检测条件的选择
2.2.1 稀释剂用量的选择
浊点萃取后待测物进入富集相,为保证比色皿中相的均一性,需要对表面活性剂相进行稀释,降低样液的黏度.甲醇可以较好地溶解Triton X-114,故本实验选择甲醇作为稀释剂.本实验对不同的甲醇用量进行了考察.当甲醇稀释后样液的体积小于1 mL时,Triton X-114对待测物峰形的干扰较大,所以稀释剂甲醇的用量为1 mL.
2.2.2 缓冲体系及其pH的选择
配制不同pH值的KH2PO4-NaOH,Na2B4O7-HCl和NH4Cl-NH3·H2O缓冲溶液,分别按照上述方法萃取和测定.由于KH2PO4-NaOH体系的干扰相对最小,样品的峰形好,所以本实验选择该体系.在其他条件不变时改变缓冲溶液的用量,发现其用量为1 mL时可以得到较好的峰形.体系pH值为8.5~9.0时,厚朴酚已经解离,其最大吸收峰红移到320 nm处;而和厚朴酚未解离,其最大吸收峰还在290 nm处.故本实验选择pH=9的KH2PO4-NaOH缓冲溶液.
2.3 分析特性
在已确定的最佳条件下,分别对方法的线性方程、线性范围、相关系数、相对标准偏差、检测限和富集倍数进行了研究.建立了吸光度与对应质量浓度的线性回归方程,结果见表1,其中5次测定厚朴酚、和厚朴酚的相对标准偏差分别为1.75%和1.49%.厚朴酚、和厚朴酚的检测限分别为2.5和1.0 μg/L,富集倍数为25,表明在最佳条件下能定量萃取.其他数据如表1所示.
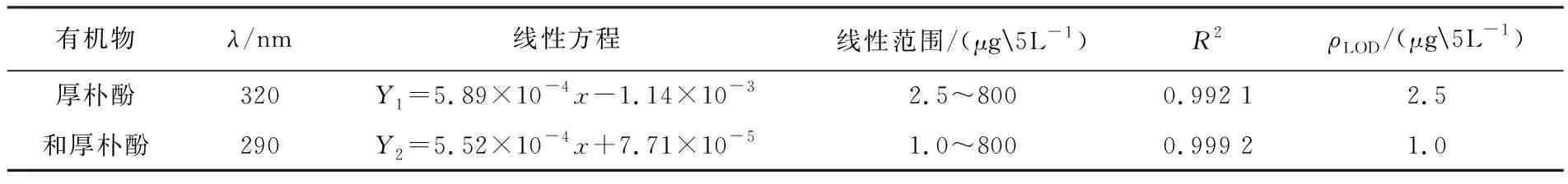
表1 线性回归方程和检测限(n=5)
2.4 样品分析及回收率实验
准确称取0.20 g厚朴药材(产地:浙江),加入1 L水于烧杯中,电炉煮沸40 min,冷却后用定性滤纸过滤以除去悬浮在水中的微粒.取50 mL样品溶液于50 mL离心管中,按照上述浊点萃取和检测方法处理,测得厚朴药材中厚朴酚与和厚朴酚的含量见表2.采用加标回收率法验证方法的准确性和可行性,实验结果见表2,厚朴酚的加标回收率为102.0%~104.3%,和厚朴酚的加标回收率为98.37%~104.3%.

表2 样品测定结果和加标回收率
3 结 论
本文建立了一种浊点萃取-分光光度法同时测定厚朴酚与和厚朴酚的新方法,以Triton X-114为表面活性剂对厚朴酚与和厚朴酚同时浊点萃取,提高了方法的选择性和灵敏度,同时利用二者pKa的差异,调节测定液pH使二者的紫外光谱出现不同,利用同一波长下吸光度的加和性,从而同时测得厚朴酚及和厚朴酚的含量.与其他文献方法相比,本方法具有操作快速、简便及成本低廉等优点.
[1]刘可云,董志,朱毅.厚朴酚与和厚朴酚的药理学研究现状[J].中成药,2006,28(5):716-718.
[2]苏健,王宝琴.厚朴及其制剂中厚朴酚、和厚朴酚含量测定方法研究综述[J].中国中医药信息杂志,2002,9(9):35-37.
[3]刘西茜,董慧茹,傅海珍.溶剂浮选分离-紫外分光光度法测定环境水样中罗红霉素残留量[J].理化检验:化学分册,2008,27(10):96-98.
[4]张海江,郭怀忠,杨晓萍,等.固相萃取-高效液相色谱法测定藿香正气口服液中厚朴酚与和厚朴酚的含量[J].药物分析杂志,2009,29(2):316-319.
[5]陈颖,段建平,陈红青,等.毛细管电泳安培检测法同时测定厚朴酚与和厚朴酚[J].福州大学学报:自然科学版,2007,35(4):612-615.
[6]肖珊美,陈建荣,沈玉勤.双硫腙浊点萃取-石墨炉原子吸收光谱法测定环境水样中痕量铅的研究[J].光谱学与光谱分析,2006,26(5):955.
[7]杨利宁,赵玲玲,陈建荣.浊点萃取-原子光谱法在金属离子形态分析中的应用[J].浙江师范大学学报:自然科学版,2012,35(4):426-431.
[8]Chen Jianrong,Teo K C.Determination of cadmium,copper,lead and zinc in water samples by flame atomic absorption spectrometry after cloud point extraction[J].Analytica Chimica Acta,2001,450(1):215-222.
[9]孙博思,任婷,赵丽娇,等.浊点萃取-高分辨连续光源石墨炉原子吸收光谱法测定环境水样中的痕量铅[J].光谱学与光谱分析,2012,32(10):2847-2852.
[10]Zhong Shuxian,Tan S N,Ge Liya,et al.Determination of bisphenol A and naphthols in river water samples by capillary zone electrophoresis after cloud point extraction[J].Talanta,2011,85(1):488-492.
[11]保志娟,杨雪琼,邹永明,等.厚朴酚与和厚朴酚清除DPPH·的作用[J].云南大学学报:自然科学版,2005,27(1):60-63.

