RRLC-Q-TOF MS/MS法分析生晒参和大力参中的皂苷类成分
郝 颖,于珊珊,戴雨霖,张 颖,钟 薇,刘淑莹,越 皓
(长春中医药大学,吉林省人参科学研究院,吉林 长春 130117)
人参为五加科人参属植物人参(panaxginsengC. A. Meyer)的干燥根,是我国名贵的中药材之一,具有安神益智、抗肿瘤、调节免疫系统、心血管系统等功效[1-2],而人参皂苷是人参中的主要活性成分[3]。人参皂苷属三萜类化合物,按照其皂苷元结构的不同,可大致分为3类,分别是原人参二醇型皂苷(Protopanaxadiol,PPD),原人参三醇型皂苷(Protopanaxatriol,PPT)和齐墩果烷型人参皂苷(Oleanolic acid)。同时,按其C-20位结构的不同,又可分为20(S)-和20(R)-型,其中20(S)-构型为人参中天然的人参皂苷构型。大力参是将新鲜的人参经沸水浸煮或汽烫后晒干而成,又称为烫通参或烫参[4]。据研究表明,大力参具有降血脂和肝糖原等作用,其药效“中和平稳”,介于生晒参和红参之间,但加工大力参对原料要求较高。目前,仅有少量研究[4-5]对大力参中的人参皂苷成分进行分析。本实验利用高分离度快速液相色谱与四极杆-飞行时间质谱(RRLC-Q-TOF MS/MS)联用技术对生晒参和大力参中的人参皂苷类成分进行鉴别和对比分析,从化学角度阐释了大力参区别于生晒参的物质基础,为探索大力参的质量评价和临床安全有效地使用提供一定的科学依据。
1 实验部分
1.1 主要仪器与试剂
Agilent 1200型快速分离液相色谱系统,Agilent 6520 Q-TOF质谱仪:美国Agilent公司产品。
人参皂苷Rg1、Rg2、Rb1、Rb2、Re和Rd等对照品(纯度大于98%):购自南京泽朗医药科技有限公司;乙腈为色谱纯;其他试剂为分析纯。
1.2 样品溶液的制备
分别精密称取1 g生晒参和大力参粉末,置于索氏提取器中,乙醚提取2 h,弃去乙醚液,再用甲醇浸泡过夜,提取3 h,蒸发皿中蒸干甲醇提取液,再用少量蒸馏水溶解后,用水饱和的正丁醇萃取4次,合并浓缩水饱和正丁醇层溶液,用色谱甲醇定容至10 mL,待测。
1.3 实验条件
1.3.1液相色谱条件 色谱柱:Agilent Eclipse Plus C18柱(2.1 mm×100 mm×3.5 μm);梯度洗脱;流动相: 0.1%甲酸水溶液(A),乙腈(B); 流动相梯度:0~3 min、25%~30%(B),3~6 min、30%~32%(B),6~7 min、32%~35%(B),7~13 min、35%~37%(B),13~19 min、37%~48%(B),19~22 min、48%~90%(B),22~25 min、90%(B),30 min、25%B;柱温30 ℃;流速0.3 mL/min;进样量5 μL。
1.3.2质谱条件 采用电喷雾负离子扫描模式(ESI-),干燥气(N2)流速9 L/min,干燥气温度 300 ℃,雾化气压力 2.41×105Pa,毛细管电压为3.5 kV,碎裂电压175 V,锥孔电压65 V,质量扫描范围m/z100~2 000。实验数据采用Masshunter Qualitative Analysis(B.03.01)软件分析处理。
2 结果与分析
由于ESI是一种软电离技术,在负离子模式下的一级质谱图中,其准分子离子主要以[M-H]-和[M+HCOOH-H]-的形式存在[6-7]。通过ESI和飞行时间质谱分析可获得皂苷类化合物的精确分子质量信息。为了获得更多的碎片离子结构信息,需进行串联分析,得到二级质谱数据。实验数据采用提取离子流(EIC)方法进行分析。
分别对人参皂苷Rd、Re标准对照品进行质谱分析,人参皂苷Rd和Re的理论分子质量均为946.550 1,且元素组成一致,二者在一级质谱图中产生[M+HCOOH-H]-离子(理论值m/z991.548 3),其准分子离子峰的质量数均为991,很难对两者进行辨认和区分。但人参皂苷Rd和Re分别属于二醇型人参皂苷和三醇型人参皂苷,分别对m/z991的分子离子进行串联分析。人参皂苷Rd和Re在二级串联质谱条件下得到的质谱图示于图1。
在图1a中,观察到分别丢失1-3分子中性葡萄糖(162 u)得到的碎片离子(Y0α/Y1β)m/z783、(Y1β)m/z621和(Y0β)m/z459,其中m/z459离子为二醇型人参皂苷的特征碎片离子[8]。在图1b中,可以观察到m/z945、799、783、637、475等碎片离子,推测分子离子m/z991连续脱去一分子甲酸、一分子146 u的脱氧六碳糖(鼠里糖 Rha)以及两分子中性葡萄糖(162 u),而m/z475离子是三醇型人参皂苷的特征碎片离子。
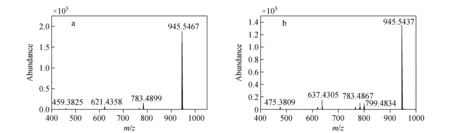
图1 负离子模式下,人参皂苷Rd (a)和人参皂苷Re (b) 的MS/MS质谱图Fig.1 The MS/MS spectrum of ginsenoside Rd (a) and ginsenoside Re (b) in negative ion mode
丙二酰基人参皂苷Rd(mRd)为二醇型人参皂苷,其C-3位取代为一分子丙二酰基和两分子葡萄糖所形成的侧链,C-20位为一分子葡萄糖。丙二酰基人参皂苷mRd的二级串联质谱示于图2。mRd理论分子质量为1 032.550 5,在Q-TOF-MS一级谱图中主要以[M-H]-离子的形式存在,[M-H]-理论值为1 031.543 2,测得值为1 031.543 8,误差为0.58×10-6。从图2中可以观察到m/z945、927、783、765、621、459等碎片离子。其中,m/z1 031离子脱去丙二酰基(86 u)产生了m/z945[M-malonyl-H]-特征碎片离子;脱去丙二酰基和水形成了m/z927离子;脱去1-3分子葡萄糖残基以及水分子产生了m/z765、783、621、459碎片离子。

图2 人参皂苷mRd的MS/MS质谱图Fig.2 The MS/MS spectrum of ginsenoside mRd
人参皂苷Rf和Rg1的理论分子质量数均为800.492 2,在一级质谱图中均产生[M+HCOOH-H]-离子(理论值m/z845.490 4)。人参皂苷Rf和Rg1均为三醇型人参皂苷,其区别主要是C-6和C-20位取代的糖基侧链不同。人参皂苷Rf的C-6位为两分子葡萄糖残基形成的糖基侧链,而人参皂苷Rg1的C-6位和C-20位各有一分子葡萄糖残基取代。人参皂苷Rg1(a)和人参皂苷Rf(b)的二级串联质谱图示于图3。从图3a、3b中均可观察到碎片离子m/z799、637、475。m/z799离子为人参皂苷Rf和Rg1的脱氢离子[M-H]-,随即连续脱去两分子葡萄糖生成碎片离子m/z637、475。但是,在图3a中,碎片离子m/z637的相对丰度要明显高于m/z475,而在图3b中却呈现出相反的现象。其原因可能是,由于人参皂苷Rg1的2个葡萄糖残基分别连在不同的碳位上,即C-6和C-20,因此较易形成脱去一分子中性葡萄糖的m/z637离子。而人参皂苷Rf的两分子葡萄糖残基连在了同一个碳链上(C-6位),因此更易形成脱去两分子中性葡萄糖的m/z475碎片离子。

图3 人参皂苷Rg1 (a)和人参皂苷Rf (b)的MS/MS质谱图Fig.3 The MS/MS spectrum of ginsenoside Rg1 (a) and ginsenoside Rf (b)
人参皂苷Rk3和Rh4的理论分子质量为620.428 8,在质谱中以[M+HCOOH-H]-形式存在,其理论值为665.427 0。大力参的提取离子流图示于图 4,可以观察到,在17~19 min出现了人参皂苷Rk3和Rh4,而在生晒参的提取离子流图中该保留时间并未出现化合物。

图4 大力参的提取离子流图 (m/z 665.427 0)Fig.4 The EIC spectrum of dali ginseng at m/z 665.427 0
通过与文献数据[9-14]、标准对照品的比较,并根据高分辨Q-TOF-MS 获得的精确分子质量、MS/MS质谱数据,对大力参和生晒参中的人参皂苷进行鉴定和分析,根据峰面积来比较各人参皂苷的含量,结果列于表1。
从表1可以观察到,在生晒参和大力参中,大多数的人参皂苷在含量上并无非常大的差异,尤其是mRb1、mRd等丙二酰基人参皂苷。由于大力参的炮制过程中未经过煎煮,因此大力参的皂苷类成分中还存在着天然的丙二酰基类人参皂苷。但是,大力参在炮制过程中仍会有一部分丙二酰基类人参皂苷水解脱去了丙二酰基,生成了相应的人参皂苷,如 mRb2经水解生成了Rb2,因此在大力参中像Rb2这样相应生成的人参皂苷的含量会有明显的增加。此外,丙二酰基类人参皂苷在串联质谱中会产生脱去丙二酰基(86 u)的特征碎片离子[M-malonyl-H]-[15]。可以看出,只有少数的人参皂苷在含量上具有较大差异,如人参皂苷Rg3、Ro,并且在大力参中存在着一些生晒参中未检测出的皂苷类成分,例如 F4、Rg6、Rg5、Rk1等。这是由于人参皂苷Re的C-20位糖基不稳定,水解后生成了人参皂苷Rg2[16],其C-20又进一步发生了脱水,生成了不饱和的人参皂苷F4与Rg6;人参皂苷Rb1、Rc、Rd、Rb2的C-20位糖基水解丢失生成了Rg3,同时Rg3又脱去了C-20位的羟基形成双键,从而生成了人参皂苷Rk1与Rg5。而与生晒参相比较,存在于大力参中的这些含量、成分不同的人参皂苷,有些在红参中也存在着相应的变化[17-18],如Rg3、Rg6、Ro。

表1 负离子模式下,35种人参皂苷的MS/MS数据Table 1 The MS/MS data of 35 kinds of ginsenosides in negative ion mode
续表

序号人参皂苷分子式WGDG[M-H]-/[M+HCOOH-H]-(m/z)质量精确度<10-5MS/MS质谱特征(m/z)17mRcC56H92O25+++++1163.5855/-1077,915,783,621,45918mRdC51H84O21++++++1031.5432/-945,783,765,621,45919Rg1C42H72O14++++++-/845.4904637,47520RfC42H72O14++++++799.4849/845.4904637,47521Rg2C42H72O13++++++783.49/829.4955637,47522ReC48H82O18++++++945.5428/-799,783,637,47523NotoR1C47H80O18+++++931.5272/977.5327799,637,47524NotoR2C41H70O13++++++769.4744/815.4798637,47525mRg1C45H74O17++++++885.4853/-781,637,47526mRfC45H74O17++++++885.4853/-781,619,47527mReC51H84O21++1031.5432/-945,799,637,4752820⁃Glc⁃RfC48H82O19++++++961.5378/1007.5432799,637,47529RoC48H76O19+++++955.4908/-793,613,569,45330F4/Rg6C42H70O12-+765.4795/811.4849619,45731F4/Rg6C42H70O12-+765.4795/811.4849619,45732Rg5/Rk1C42H70O12-+765.4795/811.4849603,44133Rg5/Rk1C42H70O12-+765.4795/811.4849603,44134RH4/Rk3C36H60O8-+-/665.42745735Rh4/Rk3C36H60O8-+-/665.427457
注:1.WG=White ginseng,DG=Dali ginseng;2.编号1~18为二醇型人参皂苷,编号19~28为三醇型人参皂苷,编号29为齐墩果烷型人参皂苷,编号30~35为其他类型人参皂苷;3.“-”代表未检测到, “+”代表峰面积为 (0~3)×105, “++”代表峰面积为(3~10)×105, “+++”代表峰面积大于10×105
3 结论
本实验利用LC-ESI-MSn技术对生晒参和大力参中的人参皂苷类成分进行了比较分析。研究表明,生晒参中主要的人参皂苷在大力参中均可找到,且多数人参皂苷含量相差不大,但大力参中含有一些在生晒参中未检测到的人参皂苷,如人参皂苷F4、Rg6、Rg5、Rk1等。本工作建立了大力参中皂苷类成分的快速分析方法,为探索大力参的质量评价和药效物质基础提供了一定的科学依据。
参考文献:
[1] 王悦虹, 娄大伟, 于晓洋, 等. 人参的药理学作用研究进展[J]. 吉林化工学院学报, 2010, 27(2): 38-41.
WANG Yuehong, LOU Dawei, YU Xiaoyang, et al. Recent adwances in pharmacological effects of ginseng[J].Journal of Jilin Institute of Chemical Technology, 2010, 27(2): 38-41(in Chinese).
[2] 曹 智, 张燕娣, 许永华, 等. 人参有效成分及其药理作用研究新进展[J]. 人参研究, 2012, (2): 39-43.
CAO Zhi, ZHANG Yandi, XU Yonghua, et al. Active ingredients and pharmacological activities of ginseng new progress [J]. Ginseng Research, 2012, (2): 39-43(in Chinese).
[3] 张 萍,张南平,肖新月, 等. 人参皂苷类成分的化学分析[J]. 药物分析杂志,2004, 24(3): 229-237.
ZHANG Ping , ZHANG Nanping, XIAO Xinyue, et al. Chemical Analysis of Saponins inPanaxginseng[J]. Chin J Pharm Anal, 2004, 24(3): 229-237(in Chinese).
[4] 李树殿, 张永强, 鲁 岐, 等. 中国、高丽、日本大力参化学成分的比较研究[J]. 人参研究, 1989, (8): 21-22.
LI Shudian, ZHANG Yongqiang, LU Qi, et al. Study chemical composition of Dali ginseng in China, Korea and Japan[J]. Ginseng Research, 1989, (8): 21-22(in Chinese).
[5] CHU C, XU S J, LI X N, et al. Profiling the ginsenosides of three ginseng products by LC-Q-TOF/MS[J]. J Food Sci, 2013, 78(5): 653-659.
[6] 李 丽, 刘春明, 吴 巍, 等. 高效液相色谱-电喷雾质谱联用法测定人参和西洋参的皂苷类成分[J]. 分析化学, 2005, 33(8): 1 087-1 090.
LI Li, LIU Chunming, WU Wei, et al. Analysis of saponins in extract ofPanaxginsengandPanaxquinquofoliumby liquid chromatography-electrospray ionization mass spectrometry[J]. Chinese J Anal Chem, 2005, 33(8): 1 087-1 090(in Chinese).
[7] 张语迟, 刘志强, 宋凤瑞, 等. 利用高效液相色谱和电喷雾质谱指纹图谱鉴别人参与桔梗[J]. 质谱学报, 2008,29(4): 203-208.
ZHANG yuchi, LIU Zhiqiang, SONG Fengrui, et al. Identification ofPanaxginsengandPlatycodongrandiflorumby the fingerprint of HPLC and ESI-MS [J]. Journal of Chinese Mass Spectrometry Society, 2008,29(4): 203-208 (in Chinese).
[8] 吴 巍, 王道武, 刘志强, 等. 人参皂苷的电喷雾负离子多级串联质谱研究[J]. 质谱学报,2003,24(增刊): 43-44.
WU Wei, WANG Daowu, LIU Zhiqiang, et al. Studies on saponins using negative electropray ionization multi-stage tandem mass spectrometry[J]. Journal of Chinese Mass Spectrometry Society, 2003, 24(Suppl): 43-44 (in Chinese).
[9] 李 丽, 刘志强, 许庆轩, 等. 人参中皂苷类化合物的HPLC-ESI MS研究[J]. 分析测试学报,2006,26(1):45-48.
LI Li, LIU Zhiqiang, XU Qingxuan, et al. Determination of ginsenosides in extract ofPanaxginsengby liquid chromatography-electrospray ionization mass spectrometry[J].Journal of Instrumental Analysis, 2006,26(1):45-48(in Chinese).
[10] 张海江, 蔡小军, 程翼宇. 高效液相色谱-电喷雾质谱法鉴别人参、西洋参和三七的皂苷提取物[J]. 中国药学杂志, 2006, 41(5): 391-394.
ZHANG Haijiang, CAI Xiaojun, CHENG Yiyu. Differentiation and authentication of saponin extracts fromPanaxginseng,PanaxquinquefoliusandPanaxnotoginsengby HPLC/ESI-MSn[J].Chinese Pharmaceutical Journal, 2006, 41(5): 391-394(in Chinese).
[11] 郭继芬, 钟大放, 乔善义, 等.液相色谱-电喷雾质谱联用技术分析人参皂苷[J]. 质谱学报, 2003,24(4): 477-481.
GUO Jifen, ZHONG Dafang, QIAO Shanyi, et al. Analysis of ginsenosides by liquid chromatography-electrospray mass spectrometry[J]. Journal of Chinese Mass Spectrometry Society, 2003,24(4): 477-481(in Chinese).
[12] WANG Y, PAN J Y, XIAO X Y, et al. Simultaneous determination of ginsenosides inPanaxginsengwith different growth ages using high-performance liquid chromatography-mass spectrometry[J]. Phytochem Anal, 2006, 17(6): 424-430.
[13] CUI M, SONG F R, ZHOU Y, et al. Rapid
identification of saponins in plant extracts by electrospray ionization multi-stage tandem mass spectrometry and liquid chromatography/tandem mass spectrometry[J]. Rapid Commun Mass Spectrom , 2000, 14(14): 1 280-1 286.
[14] 徐智秀, 肖红斌, 王加宁, 等. 高效液相色谱-质谱-质谱法分析人参皂苷[J]. 色谱,2000, 18(6): 521-524.
XU Zhixiu, XIAO Hongbin, WANG Jianing, et al. Analysis of ginsenosides by high perfomance liquid chromatography/mass spectrometry/mass spectrometry(LC/MS/MS)[J].Chinese Journal of Chromatography, 2000, 18(6): 521-524(in Chinese).
[15] 孙靖辉, 米 钧, 秦秋杰, 等. RRLC-Q-TOF MS
法鉴别分析人参皂苷Rd和Re及其丙酰化产物[J].质谱学报, 2011, 32(2): 112-113.
SUN Jinghui, MI Jun, QIN Qiujie, et al. Differentiation and identification of ginsenosides Rd, Re and related malonyl-ginsenosides by RRLC-Q-TOF-MS[J]. Journal of Chinese Mass Spectrometry Society, 2011, 32(2): 112-113(in Chinese).
[16] 郑 重, 宋凤瑞, 刘淑莹, 等. 人参、红参皂苷类成分指纹图谱研究[J]. 质谱学报, 2012, 33(6): 327-333.
ZHENG Zhong, SONG Fengrui, LIU Shuying, et al. Fingerprint study on ginsenoside in ginseng and red ginseng[J]. Journal of Chinese Mass Spectrometry Society, 2012, 33(6): 327-333(in Chinese).
[17] 刘 丹, 濮社班, 钱士辉, 等. 中国红参化学成分的研究[J]. 中国中药杂志, 2011, 36(4): 462-464.
LIU Dan, PU Sheban, QIAN Shihui, et al. Chemical constituents of Chinese red ginseng[J].China Journal of Chinese Materia Medica, 2011, 36(4): 462-464(in Chinese).
[18] XIE Y Y, LUO D, CHENG Y J, et al. Steaming-induced chemical transformations and holistic quality assessment of red ginseng derived fromPanaxginsengby means of HPLC-ESI-MS/MSn-based multicomponent quantification fingerprint[J]. J Agr Food Chem, 2012, 60(33): 8 213-8 224.

