五味子多糖胶囊的质量标准和稳定性研究
闫 舒 ,仰榴青 ,赵 婷
(1.江苏省镇江市药品检验所,江苏 镇江 212003; 2.江苏大学药学院,江苏 镇江 212013)
五味子多糖胶囊以木兰科植物五味子醇提后的药渣为生产原料,经提取加工制得,具有提高免疫力、抗癌、抗氧化、调血脂等功效[1-4]。本课题组前期对五味子多糖胶囊的制备工艺进行了优化选择[5]。为有效控制制剂质量,保证临床疗效,本试验中制订了五味子多糖的鉴别和含量测定方法,并对样品的稳定性进行了初步考察,以期为五味子多糖胶囊的质量控制、生产包装、贮存及临床应用提供科学依据。
1 仪器与试药
UV-7502 PC型紫外-可见分光光度计(上海欣茂仪器有限公司);人工气候箱(上海一恒科技有限公司);101-3-S型数字控温烘箱(上海跃进医疗器械厂)。五味子多糖胶囊(实验室自制,批号为 090312,090324,090408);葡萄糖对照品(中国药品生物制品检定所,批号为145322-200508);鼠李糖、阿拉伯糖、甘露糖、半乳糖、木糖、半乳糖醛酸对照品(中国药品生物制品检定所,含量均大于95%);5%苯酚溶液(配制方法[6]为取苯酚100 g加铝片0.1 g和碳酸氢钠0.1 g蒸馏,收集182℃馏分,称取次馏分5 g加95 mL蒸馏水,置棕色瓶中,得浓度为5%的苯酚试液);95%乙醇、苯酚、浓硫酸等均为市售分析纯(江苏省镇江市华东化玻有限公司)。
2 方法与结果
2.1 理化鉴别[7]
2.1.1 碱性酒石酸铜
取本品10 mg,研细,置试管中,加碱性酒石酸铜试液2 mL,置沸水浴中加热10 min,滤过,取滤液加6 mol/L盐酸2 mL,置沸水浴中加热20 min,冷却,加10%氢氧化钠溶液调至pH=7,加碱性酒石酸铜试液2 mL,置沸水浴中加热,有棕红色沉淀生成。
2.1.2 Molish 反应
取本品 10 mg,研细,置试管中,加入2滴 Molish试剂,摇匀,将试管倾斜,沿试管壁慢慢加入1 mL浓硫酸,竖直试管,浓硫酸和糖交界面有紫色环生成,以蒸馏水为阴性对照,淀粉为阳性对照,结果阴性无干扰。
2.2 薄层色谱(TLC)鉴别
精密称定鼠李糖、阿拉伯糖、甘露糖、葡萄糖、半乳糖、木糖、半乳糖醛酸对照品各1 mg,溶于1 mL蒸馏水中,得1 g/L的各单糖对照品溶液。分别称取鼠李糖、阿拉伯糖、甘露糖、葡萄糖、半乳糖、木糖、半乳糖醛酸对照品各0.5 mg,共溶于2 mL蒸馏水,制得混合单糖对照品溶液。取五味子多糖及辅料糊精各10 mg,加入2.0 mol/L的硫酸溶液 6 mL,酒精喷灯封管,100℃水解 8 h,取出,加入碳酸钡中和,以3 000 r/min的速率离心,除去硫酸钡沉淀,冷冻干燥上清液即得各多糖的水解溶液(供试品溶液)。
取已配好的单糖对照品溶液、混合单糖对照品溶液及供试品溶液,分别点于含0.3 moL/L磷酸二氢钠的硅胶G板上,以正丁醇 -丙酮 -水(4∶3∶1)为展开剂展开,展距 15 cm,取出,晾干后,以苯胺-邻苯二甲酸显色[将邻苯二甲酸1.6 g溶于水饱和正丁醇溶液 100 mL,加苯胺 0.93 g(相当于 0.9 mL)]。按公式计算 Rf值(Rf=起始线到斑点的距离/起始线到溶剂前沿的距离)。
由图1薄层板和各样品薄层色谱的 Rf值(见表1)可见,样品多糖溶液色谱中斑点颜色、位置与标准混合单糖中半乳糖、葡萄糖和甘露糖斑点一致;糊精样品溶液色谱中斑点颜色、位置与标准混合单糖中葡萄糖斑点一致。因此,五味子多糖胶囊内容物中可见半乳糖、葡萄糖和甘露糖斑点。

图1 薄层色谱图
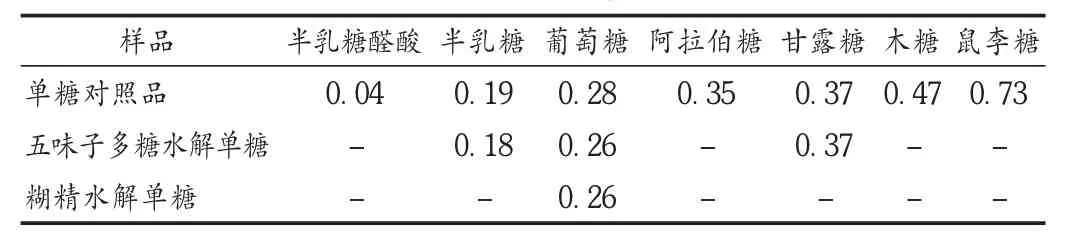
表1 各标准单糖和样品薄层色谱的 Rf值
2.3 含量测定
2.3.1 测定条件
样品处方中,五味子多糖为主要有效成分,故本试验重点应用苯酚-硫酸法建立适合本品的专属、可靠的测定方法,监测胶囊中多糖的含量,以控制药品质量。显色条件为供试品溶液加5%苯酚溶液混合后再加浓硫酸,混匀,30℃水浴中显色30 min,即可测定,测定波长为490 nm。
2.3.2 溶液制备
精密称取五味子多糖胶囊内容物5.0 mg,蒸馏水定容至25 mL,分别吸取0.6 mL稀释糖液,加入5%苯酚溶液1.2 mL混合后加入浓硫酸6.0 mL,充分混匀后,30℃水浴下放置 30 min,即得供试品溶液。
2.3.3 方法学考察
标准曲线绘制[8]:精密称取干燥的葡萄糖20 mg,置100 mL容量瓶中,用蒸馏水稀释至刻度(每1 mL溶液中含葡萄糖0.2 mg)。分别精密吸取葡萄糖标准溶液 7.5,10.0,12.5,15.0,20.0 mL 置25 mL容量瓶中,蒸馏水定容。吸取0.6 mL稀释糖液,分别加入5%苯酚溶液1.2 mL和浓硫酸6.0 mL。将充分混匀的各溶液置30℃水浴中放置30 min,另以蒸馏水同法操作制备空白对照溶液,按分光光度法于490 nm波长处测定各溶液的吸光度。以各溶液的吸光度(A)为纵坐标、葡萄糖质量浓度(C)为横坐标绘制标准曲线,得线性回归方程 A=55.785 C +0.053 5(r=0.999 8)。结果表明,葡萄糖质量浓度在0.004 6~0.012 3 g/L范围内与峰面积呈良好线性关系。
精密度试验:精密吸取葡萄糖对照品溶液(质量浓度为0.2 g/L)15 mL,置25 mL容量瓶中,加蒸馏水定容。分别吸取0.6 mL稀释糖液,加入5%苯酚溶液1.2 mL混合后加入浓硫酸6.0 mL,充分混匀后,30℃水浴下放置30 min。另以蒸馏水同上操作为空白对照溶液,在490 nm波长处测定吸光度,重复测定5次。结果葡萄糖吸光度的 RSD为0.20%,表明仪器精密度良好。
稳定性试验:精密称定五味子多糖胶囊(批号为090324)内容物5 mg,蒸馏水定容至25 mL,配制成供试品溶液。分别于配制后每20 min吸取0.6 mL稀释糖液,按拟订方法进行测定。结果葡萄糖吸光度的 RSD为0.15%,表明供试品溶液在2 h内基本稳定。
重复性试验:精密称定五味子多糖胶囊(批号为090324)内容物5份,依法制备供试品溶液,显色,在490 nm波长处测定吸光度。结果葡萄糖吸光度的 RSD为0.43%,表明方法重复性良好。
加样回收试验:精密称取已知含量的同一批(批号为090324,含量为每粒171.4 mg)样品20 mg,用蒸馏水溶解并定容至100 mL制备供试品溶液。分别精密加入葡萄糖对照品溶液(质量浓度为 0.2 g /L)10,15,20 mL,各平行加入 3 次,按拟订方法进行测定,计算回收率。结果见表2。
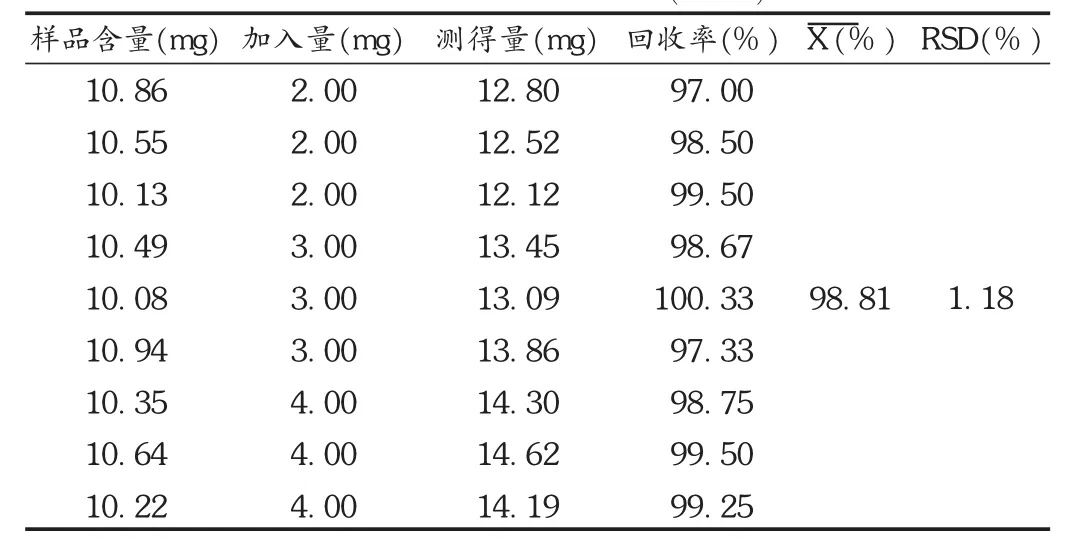
表2 加样回收试验结果(n=9)
2.3.4 样品含量测定
精密称取不同批号的样品,依法制备供试品溶液,测定3批样品中多糖的含量。结果批号为090312,090324,090408的3批样品中多糖平均含量分别为每粒 182.8,171.4,186.4 mg,RSD 分别为 1.05% ,0.72% ,1.04% 。
2.4 稳定性研究
2.4.1 影响因素试验[9]
光照试验:取五味子多糖胶囊(批号为090324)20粒,倾出内容物,平摊于称量瓶中,精密称定后开口置顶部装有20 W节能灯的木箱中,距灯底部约15 cm,经自动换档数字式照度计测得称量瓶处照度为4 500 Lx。于第0,5,10天取样考察内容物的外观、水分含量和总糖含量,结果见表3。可见,在强光照射下五味子多糖胶囊的内容物水分增加不明显,总糖含量至第10天下降了9.21%,表明光照对五味子多糖胶囊质量无明显影响。

表3 光照对胶囊剂稳定性的影响
高温试验:取五味子多糖胶囊(批号为090324)20粒,倾出内容物,平摊于称量瓶中,密塞。精密称定后置60℃恒温人工气候箱中放置,于第0,5,10天取样考察外观、水分含量和总糖含量,结果见表4。可见,五味子多糖胶囊内容物在60℃放置,水分基本无变化,而总糖含量在第10天下降了15.47%,表明温度对五味子多糖胶囊质量有一定影响。
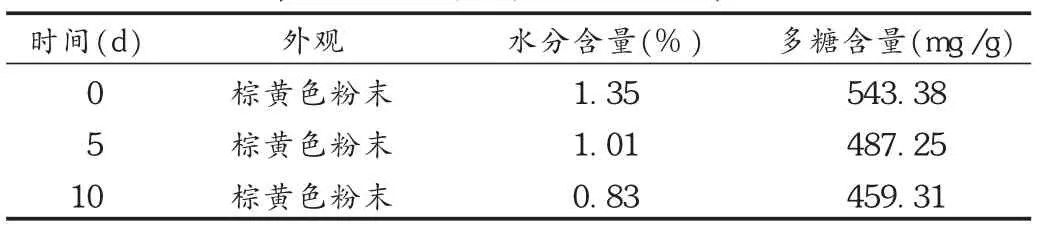
表4 温度对胶囊剂的稳定性影响
高湿试验:取五味子多糖胶囊(批号为090324)20粒,倾出内容物,平摊于称量瓶中,精密称定后置预先恒温(25℃)状态下盛有的氯化钠饱和水溶液(RH 75%)的干燥器中,分别于第0,5,10天后取样考察颜色、性状、水分含量和总糖含量,结果见表5。可见,五味子多糖胶囊内容物在RH 75%环境下放置3 d就有轻微的结块现象,至第10天结块现象严重,水分增加至4.97%,总糖含量下降了25.49%,表明湿度对五味子多糖胶囊的稳定性有明显的影响。
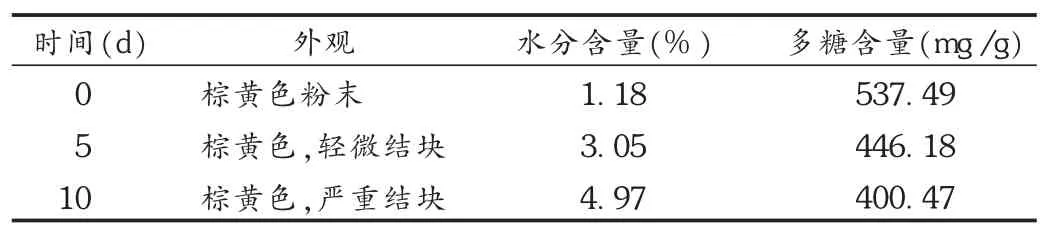
表5 湿度对胶囊剂稳定性的影响
各项影响因素试验表明,本品对高湿和高温不稳定。因此本品贮藏条件规定为“密封,阴凉干燥处保存”。
2.4.2 加速试验[10]
模拟上市包装试制3批(批号为090312,090324,090408)五味子多糖胶囊。将供试品在温度(40±2)℃、相对湿度(75±5)%的条件下放置6个月。在试验期间第1,2,3,6个月末分别取样1次,按稳定性重点考察项目检测。结果见表6。可见,本品加速试验6个月,各项指标均符合规定,故认为本品包装基本能保证药品的质量,暂订该胶囊的有效期为2年[11]。

表6 样品加速试验结果
3 讨论
目前,国内外对五味子多糖的研究大多集中在粗多糖的提取及定量测定方面[12-13],而对其单一多糖组分纯化及鉴定的研究还很少。TLC法设备简单、操作方便,是一种快速、微量的分离技术,实验室较常用。由于糖是多羟基化合物,极性强容易吸附,多采用含有无机盐水溶液制备硅胶薄层板,本试验中采用加入磷酸二氢钠以增加多糖在固定相中的溶解度。定性鉴别结果显示,五味子多糖胶囊内容物中可见半乳糖、葡萄糖和甘露糖斑点,而据文献报道,五味子纯化多糖SCP-BⅡ由鼠李糖、阿拉伯糖、甘露糖、半乳糖、葡萄糖、半乳糖醛酸组成,其摩尔比为鼠李糖 ∶阿拉伯糖 ∶甘露糖 ∶半乳糖 ∶葡萄糖 ∶半乳糖醛酸 =4.7 ∶2.6 ∶0.8 ∶5.6 ∶1 ∶5.6[14]。由于薄层色谱的灵敏度有限,水解后的单糖在总糖中所占比例较小的单糖在薄层中往往不能显出斑点,要进一步获得单糖的组成及比例,应通过气相色谱或气相色谱-质谱联用分析。
五味子多糖胶囊以五味子多糖为主要有效成分,故本试验重点运用目前常用的苯酚-硫酸法建立适合本品的专属、可靠的含量测定方法,监测胶囊中多糖的含量,以达到控制药品质量的目的。
五味子多糖胶囊的稳定性试验方法,是根据2010年版《中国药典(二部)》附录ⅪⅩC原料药与药物制剂稳定性试验指导原则中有关内容制订的。各项影响因素试验表明,本品对高湿和高温不稳定,因此本品贮藏条件规定为“密封,阴凉干燥处保存”。
[1]王艳杰,孙 阳,李明珠,等.五味子多糖对S180荷瘤小鼠红细胞免疫抗肿瘤的作用[J].天津医药,2011,39(9):824-827.
[2]Yu S,Yang L,Huang XD,et al.Purification,chemical characterization and in vitro antioxidant activities of alkali-extracted polysaccharide fractions isolated from the fruits of Schisandra chinensis[J].Journal of Medicinal Plants Research,2011,5(24):5 881-5 888.
[3]王会堂,侯 影,叶立娜,等.五味子多糖提取物的降血脂功能试验[J].长春理工大学学报:自然科学版,2009,32(4):622-624.
[4]闫 舒,仰榴青,赵 婷,等.五味子多糖的最新研究进展[J].江苏大学学报:医学版,2009,32(4):366.
[5]闫 舒,仰榴青,赵 婷,等.五味子多糖胶囊的制备工艺研究[J].中成药,2010,32(9):1 617-1 619.
[6]汪显阳,姚春艳,张佩文.六味地黄丸中多糖含量测定研究[J].中医药研究,2000,16(4):42-44.
[7]伍 艳,田淑琴,朱俊安.藏药灰兜巴化学成分的系统预实验[J].西南民族大学学报:自然科学版,2009,35(5):1 017-1 019.
[8]赵 婷,仰榴青,笪祖林,等.五味子醇提残渣中多糖的提取工艺研究[J].食品研究与开发,2008,29(8):70-73.
[9]吴晓宁,熊耀康.金耳多糖胶囊稳定性的研究[J].中华中医药学刊,2008,26(4):719-720.
[10]王 黎,马远涛,冯锁民.醋酸溴茶碱胶囊的稳定性研究[J].现代医药卫生,2011,27(15):2 298-2 300.
[11]李计萍.中药新药稳定性研究的现状与思考[J].世界科学技术,2004,6(5):26.
[12]谭小虹,王治宝,李如章.北五味子粗多糖的提取和含量测定[J].时珍国医国药,2007,18(6):1 463-1 464.
[13]安秀吉,景 旭,纪文泽,等.五味子粗多糖提取工艺及含量测定研究[J].黑龙江科技信息,2007,11(3):7-10.
[14]Gao XX, Meng XJ, Li JH, et al.Isolation, Characterization and hypoglycemic activity of an acid polysaccharide isolated from Schisandra chinensis(Turcz.)Baill[J].Letters in Organic Chemistry,2009,6(5):428-433.

